文档内容
第 5 讲 以物质的量为中心的计算
复习目标 1.掌握物质的量浓度的有关计算。2.学会常用的化学计算方法与技巧。3.能熟练
运用物质的量与相关物理量的关系进行有关计算。
考点一 有关物质的量浓度的综合计算
1.物质的量浓度、质量分数、溶解度间的换算
由定义出发,运用公式:c=、质量分数=×100%进行推理,注意密度的桥梁作用,不要死
记公式。
(1)物质的量浓度(c)与溶质质量分数(w)的换算
体积为V,密度为ρ g·cm-3的溶液,含有摩尔质量为M g·mol-1的溶质m g,溶质的质量分
数为w,则溶质的物质的量浓度c与溶质的质量分数w的关系是:c=====,反之,w
=。
(2)物质的量浓度(c)与溶解度(S)的换算
若某饱和溶液的密度为ρ g·cm-3,溶质的摩尔质量为M g·mol-1,溶解度为S g,则溶解度
与物质的量浓度的表达式分别为:S=,c===。
2.溶液稀释和混合的计算
(1)溶液稀释定律(守恒观点)
①溶质的质量在稀释前后保持不变,即mw=mw。
1 1 2 2
②溶质的物质的量在稀释前后保持不变,即cV=cV。
1 1 2 2
③溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
(2)同溶质不同物质的量浓度的溶液的混合计算
①混合后溶液体积保持不变时,cV+cV=c ×(V+V)。
1 1 2 2 混 1 2
②混合后溶液体积发生改变时,cV+cV=c V ,其中V =。
1 2 2 2 混 混 混
(3)溶质相同、质量分数不同的两溶液混合定律(教师用书独具)
①等质量混合
两溶液等质量混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),混合后溶液中溶质的质量分数w
=(a%+b%)。
②等体积混合
a.当溶液密度大于 1 g·cm-3时,必然是溶液浓度越大,密度越大,如 HSO 、HNO 、
2 4 3
HCl、NaOH等多数溶液等体积混合后,质量分数w>(a%+b%)。b.当溶液密度小于1 g·cm-3时,必然是溶液浓度越大,密度越小,如酒精、氨水等少数溶
液等体积混合后,质量分数w<(a%+b%)。
题组一 有关物质的量浓度、溶质质量分数、溶解度的换算
1.[2016·全国卷Ⅱ,36(5)节选]一种双氧水的质量分数为27.5%(密度为1.10 g·cm-3),其浓
度为________mol·L-1。
答案 8.9
解析 假设溶液的体积为1 L,则1 L溶液中含HO 的质量:
2 2
m=1 000 mL×1.10 g·cm-3×27.5%=1.10×275 g,
c(H O)==≈8.9 mol·L-1。
2 2
2.已知某饱和NaCl溶液的体积为V mL,密度为ρ g·cm-3,质量分数为w,物质的量浓度
为c mol·L-1,溶液中含NaCl的质量为m g。
(1) 用 m 、 V 表 示 溶 液 的 物 质 的 量 浓 度 :
_______________________________________________。
(2)用w、ρ表示溶液的物质的量浓度:______________________________________________。
(3)用c、ρ表示溶质的质量分数:__________________________________________________。
(4)用w表示该温度下NaCl的溶解度:______________________________________________。
答案 (1) mol·L-1 (2) mol·L-1 (3)×100% (4) g
解析 (1)c= mol·L-1= mol·L-1。
(2)c== mol·L-1。
(3)w=×100%=×100%。
(4)=,S= g。
题组二 溶液的稀释与混合
3.V mL Al (SO ) 溶液中含有Al3+m g,取 mL该溶液用水稀释至4V mL,则SO物质的量
2 4 3
浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
答案 A
解析 mL溶液中Al3+的物质的量为= mol,
稀释后溶液中Al3+的物质的量浓度为c(Al3+)== mol·L-1,
c(SO)=c(Al3+)=× mol·L-1= mol·L-1。
4.现有V L 0.5 mol·L-1的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是( )
A.加热浓缩到原来体积的一半
B.加入5 mol·L-1的盐酸0.125V LC.加入10 mol·L-1的盐酸0.1V L,再稀释至1.5V L
D.标准状况下通入11.2 L氯化氢气体
答案 C
5.下图是某学校实验室从市场买回的试剂标签上的部分内容。
硫酸 化学纯 CP
500 mL
品名:硫酸
化学式:HSO
2 4
相对分子质量:98
密度:1.84 g·cm-3
质量分数:98%
氨水 化学纯 CP
500 mL
品名:氨水
化学式:NH
3
相对分子质量:17
密度:0.88 g·cm-3
质量分数:25%
按要求回答下列问题:
(1)硫酸的物质的量浓度为________,氨水的物质的量浓度为________。
(2)各取5 mL与等质量的水混合后,c(H SO )_______9.2 mol·L-1,c(NH )_____6.45 mol·L-1
2 4 3
(填“>”“<”或“=”,下同)。
(3)各取5 mL与等体积水混合后,w(H SO )________49%,w(NH )________12.5%。
2 4 3
答案 (1)18.4 mol·L-1 12.9 mol·L-1
(2)< >
(3)> <
解析 (1)利用c=计算:c(H SO )= mol·L-1=18.4 mol·L-1,c(NH )= mol·L-1≈12.9 mol·L
2 4 3
-1。
(2)硫酸的密度大于水,氨水的密度小于水,各取5 mL与等质量的水混合后,所得稀硫酸的
体积大于10 mL,稀氨水的体积小于10 mL,故有c(H SO )<9.2 mol·L-1,c(NH )>6.45 mol·L
2 4 3
-1。
(3)5 mL浓硫酸和5 mL浓氨水的质量分别为1.84 g·cm-3×5 mL=9.2 g、0.88 g·cm-3×5 mL
=4.4 g,而5 mL水的质量约为5 g,故各取5 mL与等体积的水混合后,w(H SO )>49%,
2 4
w(NH )<12.5%。
3考点二 以“物质的量”为中心的计算
明确以物质的量为核心的各个化学计量之间的关系
1.将标准状况下的某气体(摩尔质量为M g·mol-1)溶于a g水中,所得溶液的密度为b g·cm-
3,溶质的物质的量浓度为c mol·L-1,则该气体溶入水中的体积是( )
A. L B. L
C. L D. L
答案 C
2.N 表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于冶金染料、皮革、电
A
镀等工业。硫化钠的一种制备方法是 NaSO +2C=====NaS+2CO↑。下列有关说法正确
2 4 2 2
的是( )
A.1 mol·L-1 Na SO 溶液中含氧原子的数目一定大于4N
2 4 A
B.1 L 0.1 mol·L-1 Na S溶液中含阴离子的数目小于0.1N
2 A
C.生成1 mol氧化产物时转移电子数为4N
A
D.通常状况下11.2 L CO 中含质子的数目为11N
2 A
答案 C
3.某液体化合物XY 常用作火箭燃料。16 g X Y 在一定量的O 中恰好完全燃烧,反应的
2 4 2 4 2
化学方程式为XY(l)+O(g)===X(g)+2YO(l)。冷却后标准状况下测得生成物的体积为11.2
2 4 2 2 2
L,其密度为1.25 g·L-1,则:
(1)反应前O 的体积V(O )为________。
2 2
(2)X 的摩尔质量为________;Y元素的名称是______________。
2
(3)若反应生成0.1 mol X,则转移电子的物质的量为________mol。
2
答案 (1)11.2 L (2)28 g·mol-1 氢 (3)0.41.[2020·北京,17(4)]从旧CPU中回收金部分流程如下
―――――→――――→
若用 Zn 粉将溶液中的 1 mol HAuCl 完全还原,则参加反应的 Zn 的物质的量是
4
________mol。
答案 1.5
解析 1 mol HAuCl 完全被还原,HAuCl 得到3 mol e-,锌的化合价从0价升高到+2价,
4 4
设参加反应的Zn的物质的量为x,根据得失电子守恒可知:2x=3 mol,x=1.5 mol,则参加
反应的Zn的物质的量是1.5 mol。
2.[2020·天津,15(4)(8)]为测定CuSO 溶液的浓度,甲、乙两同学设计了两个方案。回答下
4
列问题:
(4)甲方案
实验原理:CuSO +BaCl ===BaSO↓+CuCl
4 2 4 2
实验步骤:
固体质量为w g,则c(CuSO )=__________________ mol·L-1。
4
(8)乙方案,实验装置如图:
Zn粉质量为a g,若测得H 体积为b mL,已知实验条件下ρ(H )=d g·L-1,则c(CuSO )=
2 2 4
________ mol·L-1(列出计算表达式)。
答案 (4) (8)
解析 (4)w g为BaSO 的质量,BaSO 的物质的量为 mol,由化学方程式:CuSO +BaCl
4 4 4 2
===BaSO↓+CuCl 可知,CuSO 的物质的量等于BaSO 的物质的量,所以CuSO 溶液的浓
4 2 4 4 4
度为c(CuSO )== mol·L-1。
4
(8)Zn粉的物质的量为 mol,反应产生H 的物质的量为= mol,由Zn+HSO ===ZnSO +
2 2 4 4
H↑知,与HSO 反应的Zn的物质的量等于产生H 的物质的量,为 mol,与CuSO 反应消
2 2 4 2 4
耗Zn的物质的量为(-)mol。由化学方程式Zn+CuSO ===ZnSO +Cu可知,与CuSO 反应
4 4 4消耗的Zn的物质的量等于CuSO 的物质的量,所以c(CuSO )= mol·L-1。
4 4
3.[2014·江苏,18(2)(3)]碱式碳酸铝镁[Mg Al (OH)(CO)·xHO]常用作塑料阻燃剂。
a b c 3 d 2
(2)Mg Al (OH)(CO)·xHO中a、b、c、d的代数关系式为___________________________。
a b c 3 d 2
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO 0.560 L(已换算成标准状况下)。
2
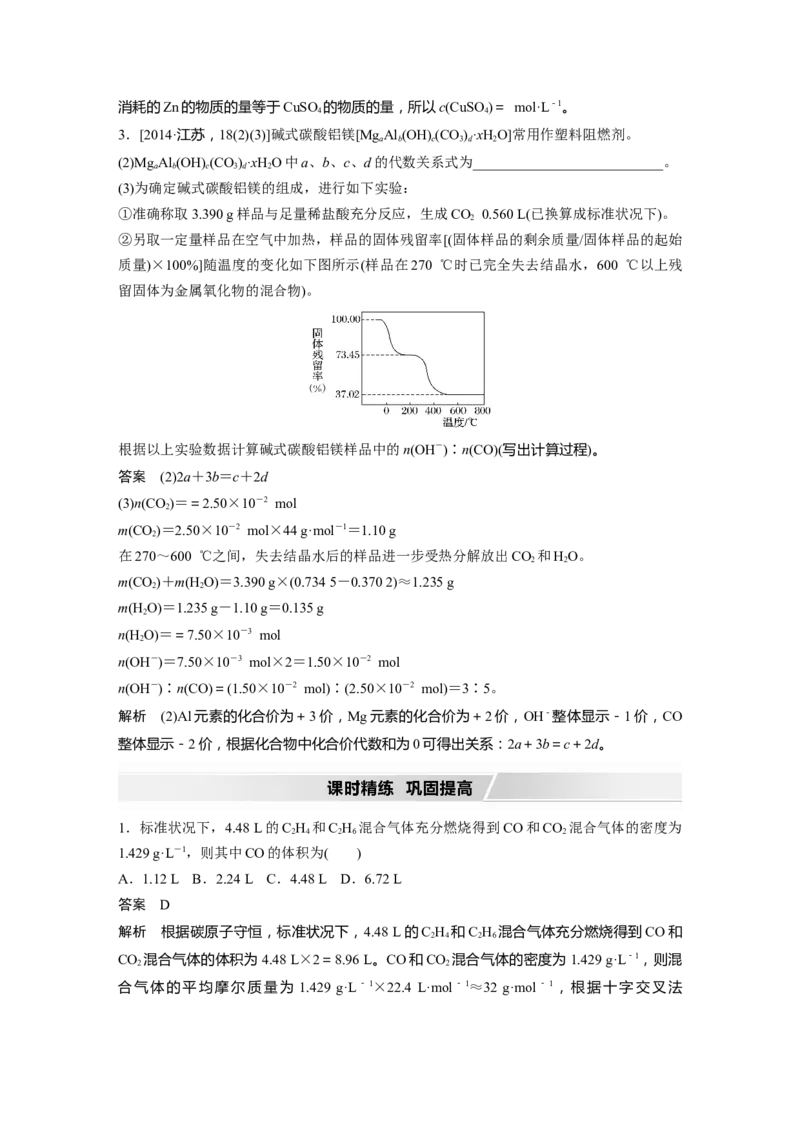
②另取一定量样品在空气中加热,样品的固体残留率[(固体样品的剩余质量/固体样品的起始
质量)×100%]随温度的变化如下图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残
留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO)(写出计算过程)。
答案 (2)2a+3b=c+2d
(3)n(CO)==2.50×10-2 mol
2
m(CO)=2.50×10-2 mol×44 g·mol-1=1.10 g
2
在270~600 ℃之间,失去结晶水后的样品进一步受热分解放出CO 和HO。
2 2
m(CO)+m(H O)=3.390 g×(0.734 5-0.370 2)≈1.235 g
2 2
m(H O)=1.235 g-1.10 g=0.135 g
2
n(H O)==7.50×10-3 mol
2
n(OH-)=7.50×10-3 mol×2=1.50×10-2 mol
n(OH-)∶n(CO)=(1.50×10-2 mol)∶(2.50×10-2 mol)=3∶5。
解析 (2)Al元素的化合价为+3价,Mg元素的化合价为+2价,OH-整体显示-1价,CO
整体显示-2价,根据化合物中化合价代数和为0可得出关系:2a+3b=c+2d。
1.标准状况下,4.48 L的C H 和C H 混合气体充分燃烧得到CO和CO 混合气体的密度为
2 4 2 6 2
1.429 g·L-1,则其中CO的体积为( )
A.1.12 L B.2.24 L C.4.48 L D.6.72 L
答案 D
解析 根据碳原子守恒,标准状况下,4.48 L的C H 和C H 混合气体充分燃烧得到CO和
2 4 2 6
CO 混合气体的体积为4.48 L×2=8.96 L。CO和CO 混合气体的密度为1.429 g·L-1,则混
2 2
合气体的平均摩尔质量为 1.429 g·L-1×22.4 L·mol-1≈32 g·mol-1,根据十字交叉法,==,因此CO的体积为8.96 L×=6.72 L。
2.V L Fe (SO ) 溶液中含有a g SO,取此溶液0.5V L,用水稀释至2V L,则稀释后溶液
2 4 3
中Fe3+的物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
答案 A
解析 a g SO的物质的量为mol,因此V L Fe (SO ) 溶液中Fe3+的物质的量为× mol=
2 4 3
mol,从中取出0.5V L后n(Fe3+)= mol×= mol,即稀释到2V L后溶液中Fe3+的物质的量
浓度为= mol·L-1。
3.相对分子质量为M的气态化合物V L(标准状况),溶于m g水中,得到质量分数为w的
溶液,物质的量浓度为c mol·L-1,密度为ρ g·cm-3。则下列说法不正确的是( )
A.相对分子质量M=
B.物质的量浓度c=
C.溶液的质量分数w=
D.溶液密度ρ=
答案 C
解析 由c=知D项正确;由c==,知B项正确;由w==,知C项错误,将此式变形后
即可得到A项中的式子。
4.(2021·广东省云浮市蔡朝焜纪念中学月考)在a L Al (SO ) 和(NH )SO 的混合溶液中加入
2 4 3 4 2 4
b mol BaCl ,恰好使溶液中的SO完全沉淀;如加入足量强碱并加热可得到c mol NH ,则
2 3
原溶液中的Al3+浓度(mol·L-1)为( )
A. B.
C. D.
答案 C
解析 由混合溶液中加入b mol BaCl ,恰好使溶液中的SO完全沉淀,则根据SO+Ba2+
2
===BaSO↓可知n(SO)=b mol;由加入足量强碱并加热可得到c mol NH ,根据NH+OH-
4 3
=====NH ↑+HO可知n(NH )=c mol,由于溶液不显电性,设原溶液中的Al3+的物质的量
3 2 3
为x mol,由电荷守恒可知,3x+c=2b,所以x=,由于溶液的体积是a L,所以原溶液中
Al3+的物质的量浓度c(Al3+)== mol·L-1。
5.某同学购买了一瓶“84”消毒液,包装说明如下:
主要成分:25%NaClO、1 000 mL、密度1.19 g·cm-3
使用方法:稀释100倍(体积比)后使用
注意事项:密封保存,易吸收空气中的CO 变质
2请根据以上信息和相关知识判断,下列分析不正确的是( )
A.该“84”消毒液的物质的量浓度约为4.0 mol·L-1
B.一瓶该“84”消毒液敞口放置一段时间后浓度会变小
C.取100 mL该“84”消毒液稀释100倍后用于消毒,稀释后的溶液中c(Na+)约为0.04 mol·L
-1
D.参阅该“84”消毒液的配方,欲用NaClO固体配制含25%NaClO的消毒液480 mL,需
要称量的NaClO固体质量为143 g
答案 D
解析 选项A,根据c=得,c(NaClO)=≈4.0 mol·L-1;选项B,一瓶该“84”消毒液敞口放
置一段时间后,由于其易吸收空气中的二氧化碳变质而会使浓度变小;选项 C,根据稀释前
后溶质的物质的量不变有100 mL×4.0 mol·L-1=100 mL×
100×c(NaClO),解得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1;
选项D,应选取500 mL规格的容量瓶进行配制,然后取出480 mL,所以需要NaClO的质
量为0.5 L×4.0 mol·L-1×74.5 g·mol-1=149 g。
6.(2020·山东省聊城第一中学期中)一定量的某磁黄铁矿(主要成分FeS,S为-2价)与100
x
mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成2.4 g硫单质、0.425 mol FeCl
2
和一定量HS气体,且溶液中无Fe3+。则下列说法正确的是( )
2
A.该盐酸的物质的量浓度为4.25 mol·L-1
B.该磁黄铁矿FeS中,Fe2+与Fe3+的物质的量之比为3∶1
x
C.生成的HS气体在标准状况下的体积为2.24 L
2
D.该磁黄铁矿中FeS的x=0.85
x
答案 D
解析 盐酸恰好反应生成FeCl 0.425 mol,
2
根据氯原子守恒得c(HCl)==8.5 mol·L-1,故A错误;
n(S)==0.075 mol,根据转移电子守恒得n(Fe3+)==0.15 mol,则n(Fe2+)=0.425 mol-0.15
mol=0.275 mol,
所以Fe2+与Fe3+的物质的量之比为0.275 mol∶0.15 mol=11∶6,故B错误;
根据氢原子、氯原子守恒得n(H S)=n(HCl)=n(FeCl )=0.425 mol,
2 2
V(H S)=0.425 mol×22.4 L·mol-1=9.52 L,故C错误;
2
FeS中n(S)=0.075 mol+0.425 mol=0.5 mol,n(Fe)=0.425 mol,
x
所以n(Fe)∶n(S)=0.425 mol∶0.5 mol=0.85,所以x=0.85,故D正确。
7.按要求回答问题。
(1)将19.4 g CO 和水蒸气的混合气体,与足量的NaO 反应,收集到标准状况下5.6 L的气
2 2 2
体,试确定混合气体的平均相对分子质量为________,CO 与水蒸气的物质的量之比为
2
________。(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应
器中,通入4.032 L(标准状况下的)O ,在高温下充分反应后测得气体的密度为1.34 g·L-1(已
2
折算成标准状况,AlN不跟O 反应),则所得气体的摩尔质量为________g·mol-1,该气体的
2
成分是________________________(写化学式),该样品中含杂质碳________g。
(3)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧
化物的重要原料。如图为二水合草酸钴(CoC O·2H O)在空气中受热的质量变化曲线,曲线
2 4 2
中300 ℃及以上所得固体均为钴氧化物。
①通过计算确定C点剩余固体的化学成分为_______________________________________
(填化学式)。试写出B点对应的物质与O 在225~300 ℃发生反应的化学方程式:
2
________________________________________________________________________。
②取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480
mL 5 mol·L-1盐酸恰好完全溶解固体,得到CoCl 溶液和4.48 L(标准状况)黄绿色气体。试
2
确定该钴氧化物中Co、O的物质的量之比。
答案 (1)38.8 4∶1
(2)30 CO 和CO 3.84
2
(3)①Co O 3CoC O+2O========Co O+6CO
3 4 2 4 2 3 4 2
②由得失电子守恒有n(Co3+)=2n(Cl )=2×=0.4 mol,
2
由电荷守恒有n(Co) =n(Co2+) =0.5n(Cl-)=0.5×(0.480×5-0.2×2)mol=1 mol,
总 溶液
所以固体中n(Co2+)=1 mol-0.4 mol=0.6 mol,
n(O)= mol=1.2 mol,
故n(Co)∶n(O)=1∶1.2=5∶6。
解析 (1)根据化学方程式 2NaO +2CO===2NaCO +O 、2NaO +2HO(g)===4NaOH+
2 2 2 2 3 2 2 2 2
O ,得关系式2CO ~O 和2H O(g)~O ,所以n(混)=0.5 mol,M(混)=38.8 g·mol-1,有
2 2 2 2 2
44 g·mol-1×n(CO)+18 g·mol-1×n(H O)=19.4 g,得n(CO)=0.4 mol,n(H O)=0.1 mol,
2 2 2 2
即n(CO)∶n(H O)=4∶1。
2 2
(2)在高温下充分反应后测得气体的密度为1.34 g·L-1,则M=1.34 g·L-1×22.4 L·mol-1≈
30 g·mol-1,所以生成气体必定是CO 和CO的混合气体。设混合气体中含有n(CO)=x,
2 2
n(CO)=y,根据氧原子守恒有2x+y=×2=0.36 mol①,根据平均相对分子质量有44x+28y
=30(x+y)②,联立方程解得:x=0.04 mol,y=0.28 mol,所以样品中C的质量为:m(C)=(0.04 mol+0.28 mol)×12 g·mol-1=3.84 g。
(3)①由图可知,CoC O·2H O的起始质量为18.3 g,其物质的量为0.1 mol,Co元素质量为
2 4 2
5.9 g,C点钴氧化物的质量为8.03 g,氧化物中氧元素质量为8.03 g-5.9 g=2.13 g,则氧化
物中Co原子与O原子物质的量之比为0.1 mol∶≈3∶4,故C点为Co O ;B点对应物质的
3 4
质量为14.7 g,与其起始物质的质量相比减少18.3 g-14.7 g=3.6 g,为结晶水的质量,故B
点物质为CoC O ,与氧气反应生成 Co O 与二氧化碳,反应的化学方程式为 3CoC O +
2 4 3 4 2 4
2O========Co O+6CO。
2 3 4 2
②黄绿色气体为Cl,其物质的量为0.2 mol,根据Cl元素守恒可知,溶液中2n(Co)=n(HCl)
2
-2n(Cl ),故n(Co)=1 mol,根据得失电子守恒n(Co3+)=2n(Cl )=0.4 mol,则n(Co2+)=
2 2
0.6 mol,根据电荷守恒可知,2n(O)=3n(Co3+)+2n(Co2+),n(O)=1.2 mol,故n(Co)∶n(O)
=1∶1.2=5∶6。
8.(2020·宜昌部分示范高中月考)Ba2+是一种重金属离子,有一环境监测小组欲利用
NaSO、KCr O 等试剂测定某工厂废水中Ba2+的物质的量浓度。
2 2 3 2 2 7
(1)现需配制250 mL 0.100 0 mol·L-1的标准NaSO 溶液,所需要的玻璃仪器除量筒、玻璃
2 2 3
棒、烧杯外,还需要________。
(2)需准确称取NaSO 固体的质量为________g。
2 2 3
(3)另取50.00 mL废水,控制适当的酸度,加入足量的KCr O 溶液,得到BaCrO 沉淀;沉
2 2 7 4
淀经洗涤、过滤后,用适量的稀盐酸溶解,此时 CrO全部转化为Cr O,再向其中滴加上述
2
标准NaSO 溶液,反应完全时,消耗NaSO 溶液36.00 mL。已知有关反应的离子方程式
2 2 3 2 2 3
为Cr O+6SO+14H+===2Cr3++3SO+7HO。则该工厂废水中Ba2+的物质的量浓度为
2 2 4 2
________。
答案 (1)250 mL容量瓶、胶头滴管 (2)4.0 (3)0.024 mol·L-1
解析 (2)Na SO 的物质的量为0.25 L×0.100 0 mol·L-1=0.025 mol,
2 2 3
其质量为0.025 mol×158 g·mol-1=3.95 g,托盘天平精确度为0.1 g,
需称量NaSO 的质量为4.0 g。
2 2 3
(3)设该工厂废水中Ba2+的物质的量为x,
由Ba2+转化为BaCrO 沉淀,CrO全部转化为Cr O,Cr O+6SO+14H+===2Cr3++3SO+
4 2 2 2 4
7HO,
2
则2Ba2+~2BaCrO~Cr O~6SO,
4 2 2
2 6
x 36.00×10-3L×0.100 0 mol·L-1
=
解得x=1.2×10-3 mol,
则c(Ba2+)==0.024 mol·L-1。