文档内容
(一)反应历程
1.化学动力学与反应历程
化学动力学是研究化学反应进行的速率和反应历程(即机理)的科学。所谓反应历程就是反应
物按什么途径,经过哪些步骤,才能转化为最终产物。选择适当的反应途径,可以使热力学
由预期转变为现实。
2.基元反应与非基元反应
例如 H++OH-===HO,反应几乎没有过程,瞬间平衡一步到位,称为简单反应;而
2
2HI===H +I 的实际机理是分两步进行的,每一步都是一个基元反应:2HI―→H +2I·、
2 2 2
2I·―→I ,存在未成对电子的微粒称为自由基,反应活性高, 寿命短,2HI===H +I 称为
2 2 2
非基元反应。
(二)有效碰撞理论与活化能
活化能 活化分子数 单位体积内活化分子数 有效碰撞
增大浓度/压强 不变 不变 增多 增加
升高温度 不变 增多 增多 增加
催化剂 下降 增多 增多 增加
备注:速率常数k= (阿伦尼乌斯公式)
A—比例系数,E—活化能,R—常数,T—开氏温度。从公式可以判断出,T越高,速率常
a
数越大,反应速率越大。E 越小,速率常数越大,反应速率越大。
a
(三)过渡态与中间体
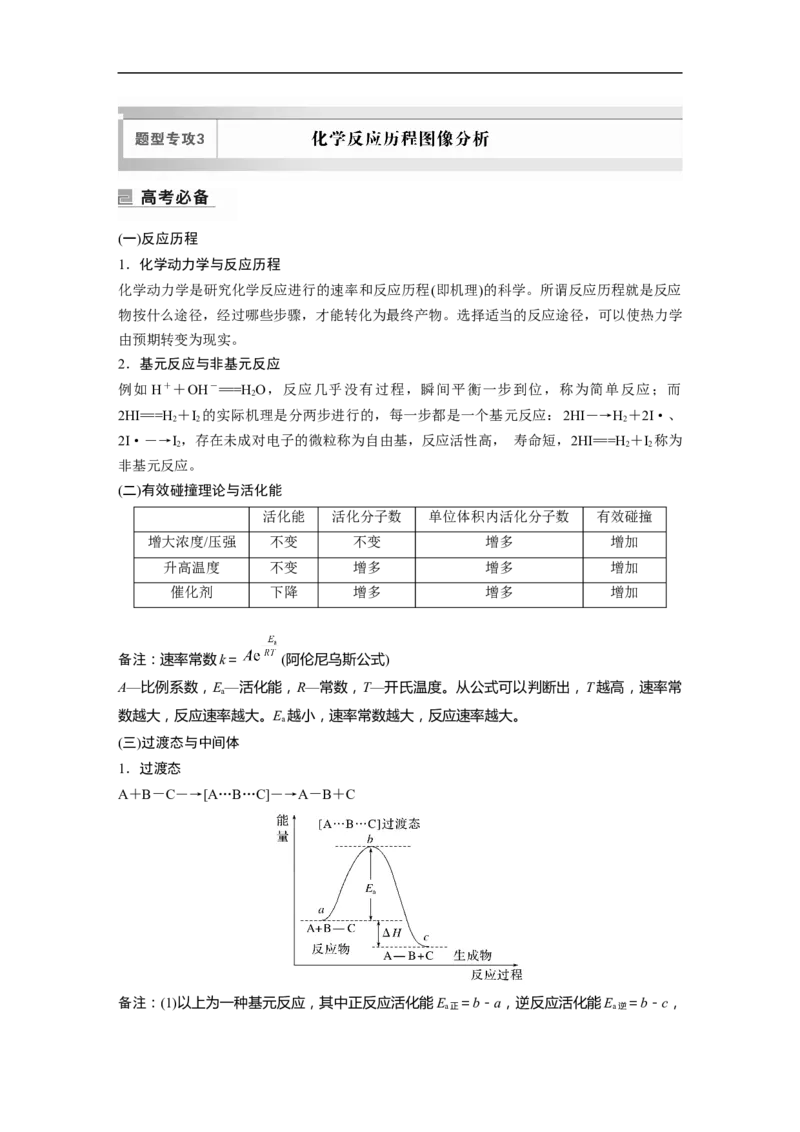
1.过渡态
A+B-C―→[A…B…C]―→A-B+C
备注:(1)以上为一种基元反应,其中正反应活化能E =b-a,逆反应活化能E =b-c,
a正 a逆ΔH=E -E 。(2)过渡态(A…B…C)不稳定。
a正 a逆
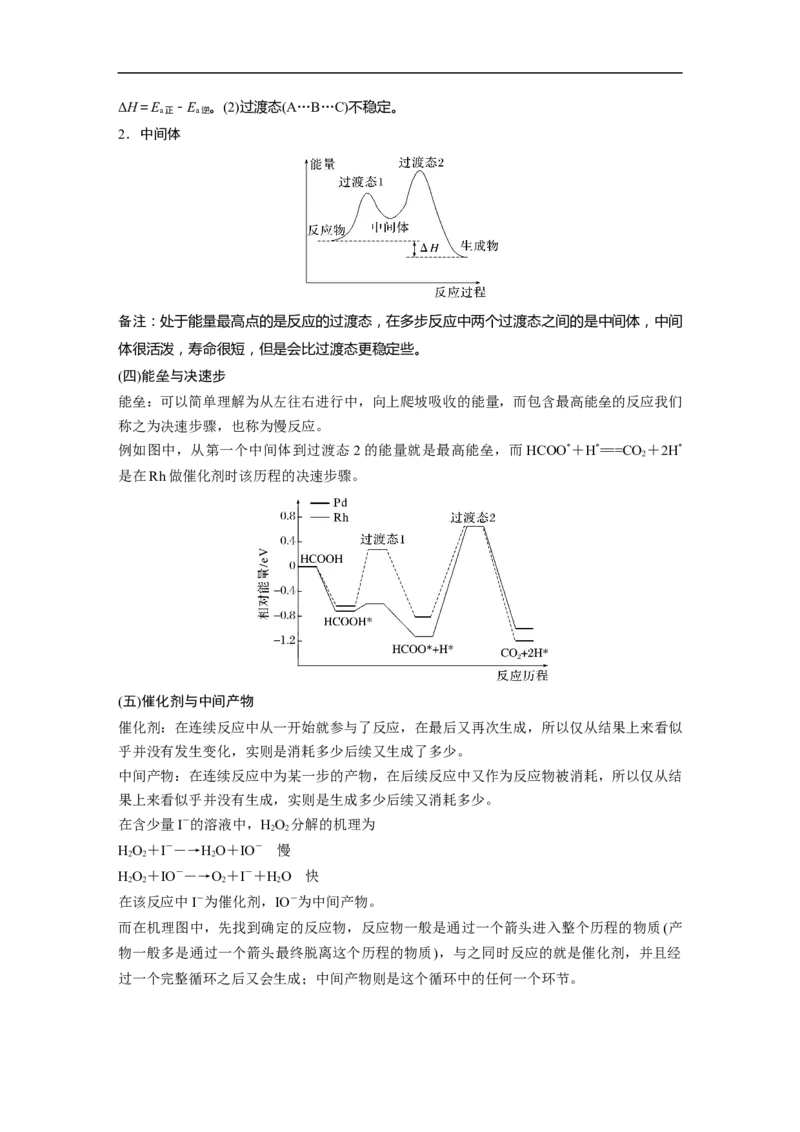
2.中间体
备注:处于能量最高点的是反应的过渡态,在多步反应中两个过渡态之间的是中间体,中间
体很活泼,寿命很短,但是会比过渡态更稳定些。
(四)能垒与决速步
能垒:可以简单理解为从左往右进行中,向上爬坡吸收的能量,而包含最高能垒的反应我们
称之为决速步骤,也称为慢反应。
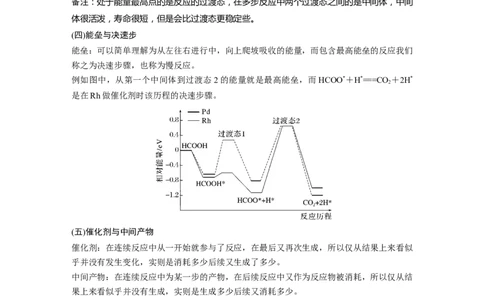
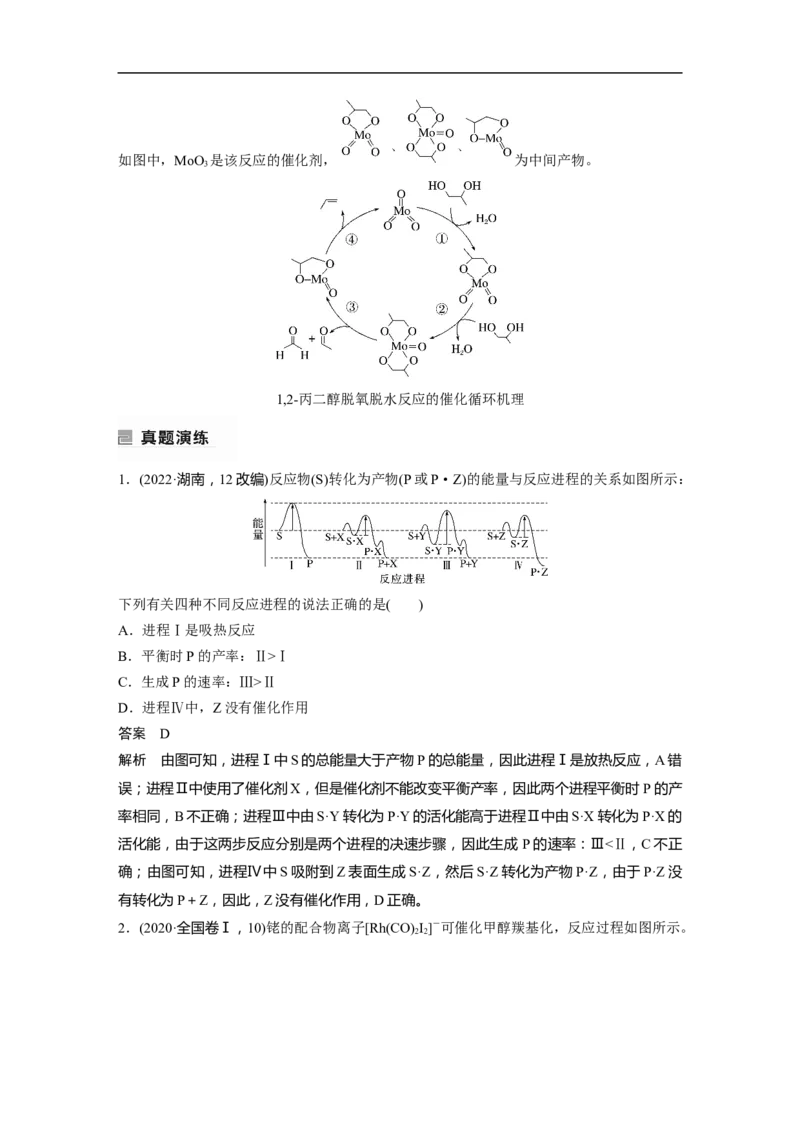
例如图中,从第一个中间体到过渡态2的能量就是最高能垒,而HCOO*+H*===CO +2H*
2
是在Rh做催化剂时该历程的决速步骤。
(五)催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似
乎并没有发生变化,实则是消耗多少后续又生成了多少。
中间产物:在连续反应中为某一步的产物,在后续反应中又作为反应物被消耗,所以仅从结
果上来看似乎并没有生成,实则是生成多少后续又消耗多少。
在含少量I-的溶液中,HO 分解的机理为
2 2
HO+I-―→HO+IO- 慢
2 2 2
HO+IO-―→O+I-+HO 快
2 2 2 2
在该反应中I-为催化剂,IO-为中间产物。
而在机理图中,先找到确定的反应物,反应物一般是通过一个箭头进入整个历程的物质(产
物一般多是通过一个箭头最终脱离这个历程的物质),与之同时反应的就是催化剂,并且经
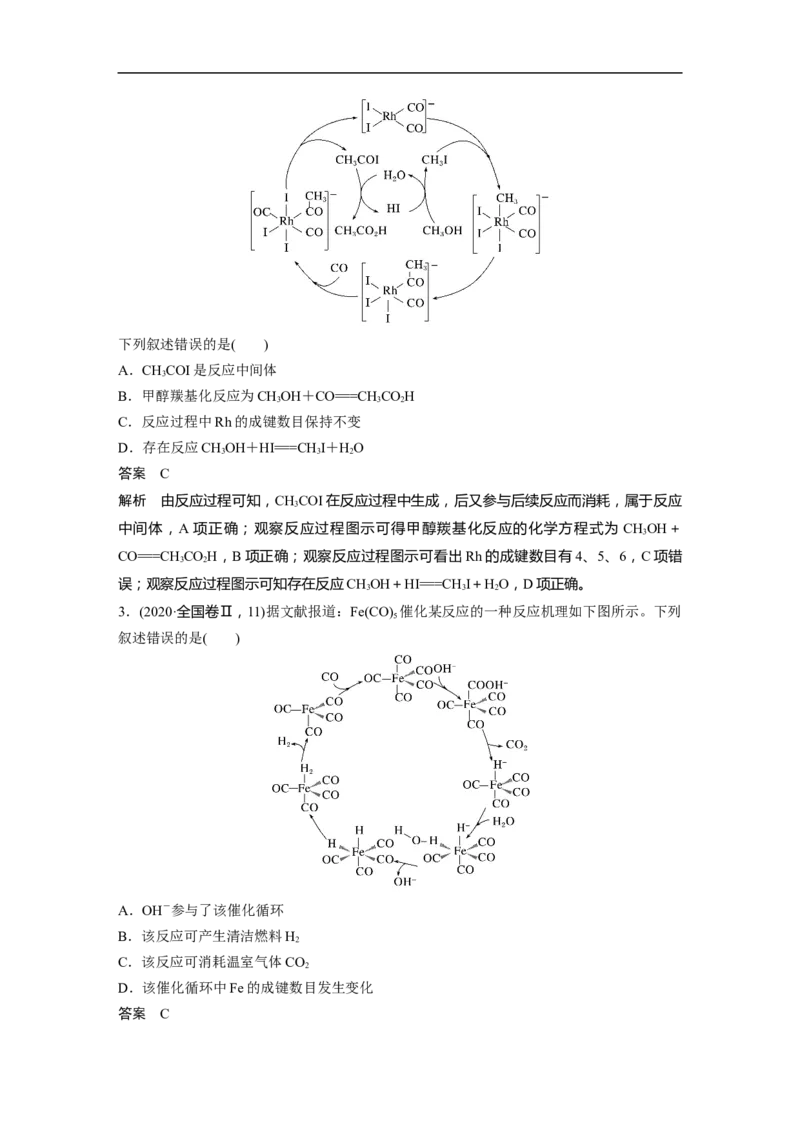
过一个完整循环之后又会生成;中间产物则是这个循环中的任何一个环节。如图中,MoO 是该反应的催化剂, 为中间产物。
3
1,2-丙二醇脱氧脱水反应的催化循环机理
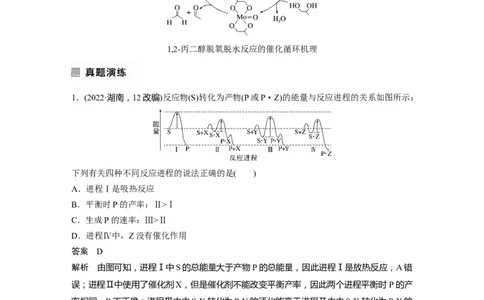
1.(2022·湖南,12改编)反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如图所示:
下列有关四种不同反应进程的说法正确的是( )
A.进程Ⅰ是吸热反应
B.平衡时P的产率:Ⅱ>Ⅰ
C.生成P的速率:Ⅲ>Ⅱ
D.进程Ⅳ中,Z没有催化作用
答案 D
解析 由图可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程Ⅰ是放热反应,A错
误;进程Ⅱ中使用了催化剂X,但是催化剂不能改变平衡产率,因此两个进程平衡时P的产
率相同,B不正确;进程Ⅲ中由S·Y转化为P·Y的活化能高于进程Ⅱ中由S·X转化为P·X的
活化能,由于这两步反应分别是两个进程的决速步骤,因此生成 P的速率:Ⅲ<Ⅱ,C不正
确;由图可知,进程Ⅳ中S吸附到Z表面生成S·Z,然后S·Z转化为产物P·Z,由于P·Z没
有转化为P+Z,因此,Z没有催化作用,D正确。
2.(2020·全国卷Ⅰ,10)铑的配合物离子[Rh(CO) I]-可催化甲醇羰基化,反应过程如图所示。
2 2下列叙述错误的是( )
A.CHCOI是反应中间体
3
B.甲醇羰基化反应为CHOH+CO===CHCOH
3 3 2
C.反应过程中Rh的成键数目保持不变
D.存在反应CHOH+HI===CHI+HO
3 3 2
答案 C
解析 由反应过程可知,CHCOI在反应过程中生成,后又参与后续反应而消耗,属于反应
3
中间体,A项正确;观察反应过程图示可得甲醇羰基化反应的化学方程式为 CHOH+
3
CO===CHCOH,B项正确;观察反应过程图示可看出Rh的成键数目有4、5、6,C项错
3 2
误;观察反应过程图示可知存在反应CHOH+HI===CHI+HO,D项正确。
3 3 2
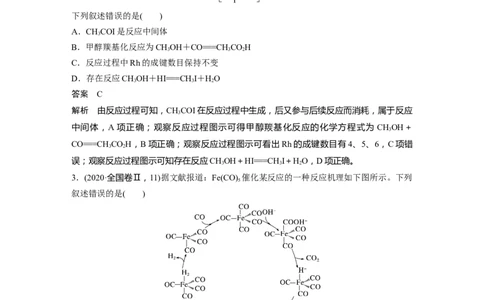
3.(2020·全国卷Ⅱ,11)据文献报道:Fe(CO) 催化某反应的一种反应机理如下图所示。下列
5
叙述错误的是( )
A.OH-参与了该催化循环
B.该反应可产生清洁燃料H
2
C.该反应可消耗温室气体CO
2
D.该催化循环中Fe的成键数目发生变化
答案 C解析 从反应机理图可知,OH-有进入的箭头也有出去的箭头,说明OH-参与了该催化循
环,故A项正确;从反应机理图可知,该反应的反应物为 CO和HO,产物为H 和CO ,
2 2 2
Fe(CO) 作为整个反应的催化剂,而OH-仅仅在个别步骤中辅助催化剂完成反应,说明该反
5
应方程式为CO+HO=====CO+H,故有清洁燃料H 生成,故B项正确;由B项分析可知,
2 2 2 2
该反应不消耗温室气体CO ,反而是生成了CO ,故C项不正确;从反应机理图可知,Fe
2 2
的成键数目在该循环过程中发生了变化,故 D项正确。
4.[2019·全国卷Ⅰ,28(3)]我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上
水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”)。该历程中最大能垒(活
化能)E =________eV,写出该步骤的化学方程式:_______________________________。
正
答案 小于 2.02 COOH +H +HO ===COOH +2H +OH (或HO ===H +OH )
2 2
解析 观察始态物质的相对能量与终态物质的相对能量知,终态物质相对能量低于始态物质
相对能量,说明该反应是放热反应,ΔH小于0。过渡态物质相对能量与始态物质相对能量
相差越大,活化能越大,由题图知,最大活化能E =1.86 eV-(-0.16 eV)=2.02 eV,该步
正
起始物质为COOH +H +HO ,产物为COOH +2H +OH 。
2
考向一 能量反应过程图分析
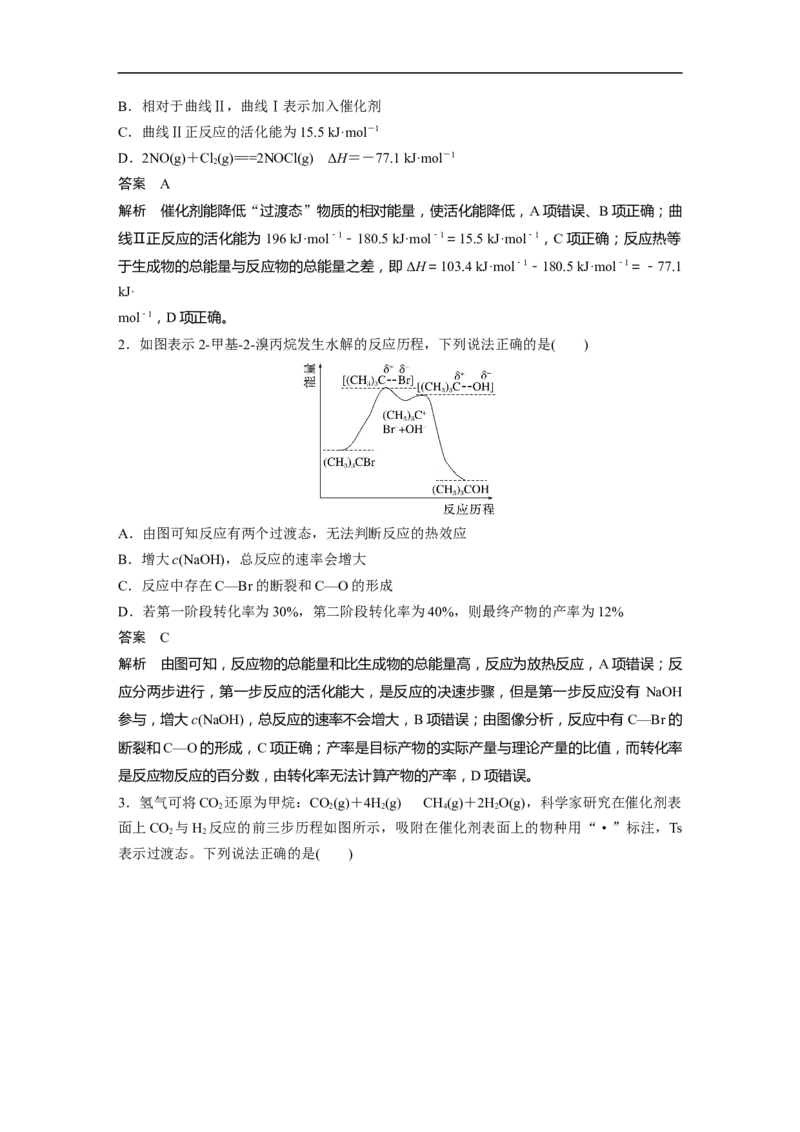
1.亚硝酰氯在有机合成中有重要应用。2NO(g)+Cl(g)===2NOCl(g)的反应历程如图所示。
2
下列说法错误的是( )
A.催化剂能提高反应物的相对能量B.相对于曲线Ⅱ,曲线Ⅰ表示加入催化剂
C.曲线Ⅱ正反应的活化能为15.5 kJ·mol-1
D.2NO(g)+Cl(g)===2NOCl(g) ΔH=-77.1 kJ·mol-1
2
答案 A
解析 催化剂能降低“过渡态”物质的相对能量,使活化能降低,A项错误、B项正确;曲
线Ⅱ正反应的活化能为196 kJ·mol-1-180.5 kJ·mol-1=15.5 kJ·mol-1,C项正确;反应热等
于生成物的总能量与反应物的总能量之差,即ΔH=103.4 kJ·mol-1-180.5 kJ·mol-1=-77.1
kJ·
mol-1,D项正确。
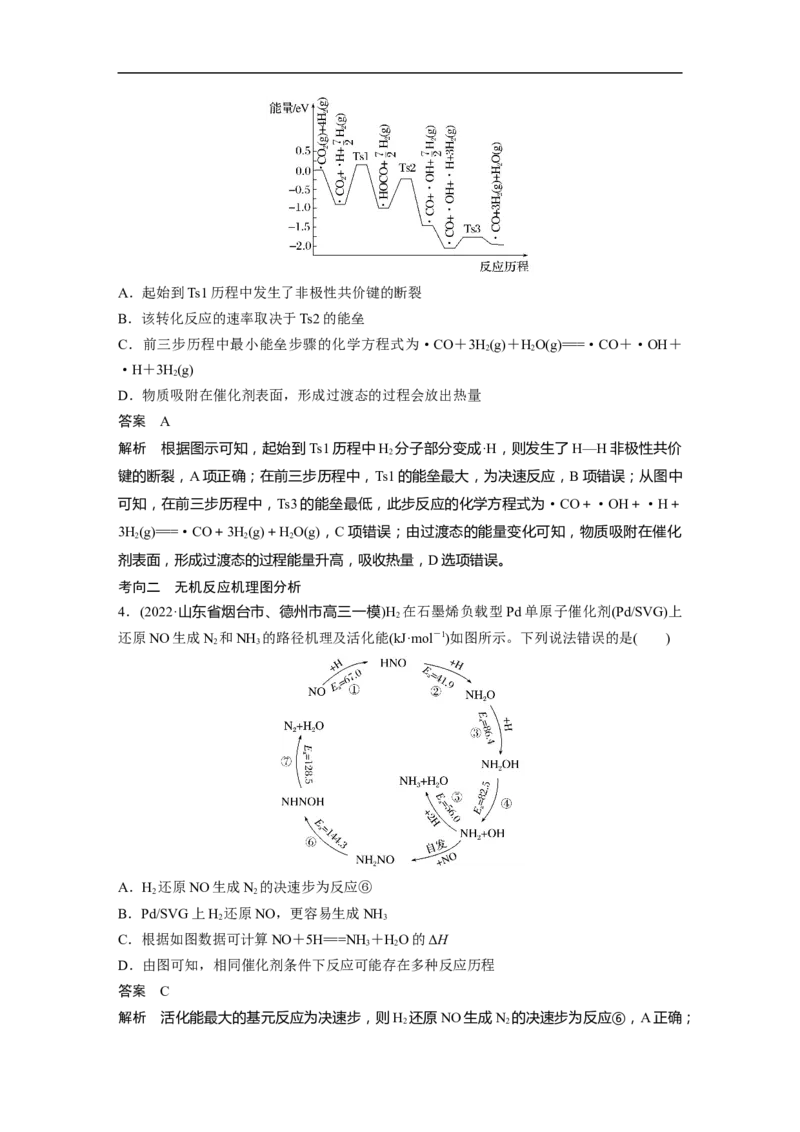
2.如图表示2-甲基-2-溴丙烷发生水解的反应历程,下列说法正确的是( )
A.由图可知反应有两个过渡态,无法判断反应的热效应
B.增大c(NaOH),总反应的速率会增大
C.反应中存在C—Br的断裂和C—O的形成
D.若第一阶段转化率为30%,第二阶段转化率为40%,则最终产物的产率为12%
答案 C
解析 由图可知,反应物的总能量和比生成物的总能量高,反应为放热反应,A项错误;反
应分两步进行,第一步反应的活化能大,是反应的决速步骤,但是第一步反应没有 NaOH
参与,增大c(NaOH),总反应的速率不会增大,B项错误;由图像分析,反应中有C—Br的
断裂和C—O的形成,C项正确;产率是目标产物的实际产量与理论产量的比值,而转化率
是反应物反应的百分数,由转化率无法计算产物的产率,D项错误。
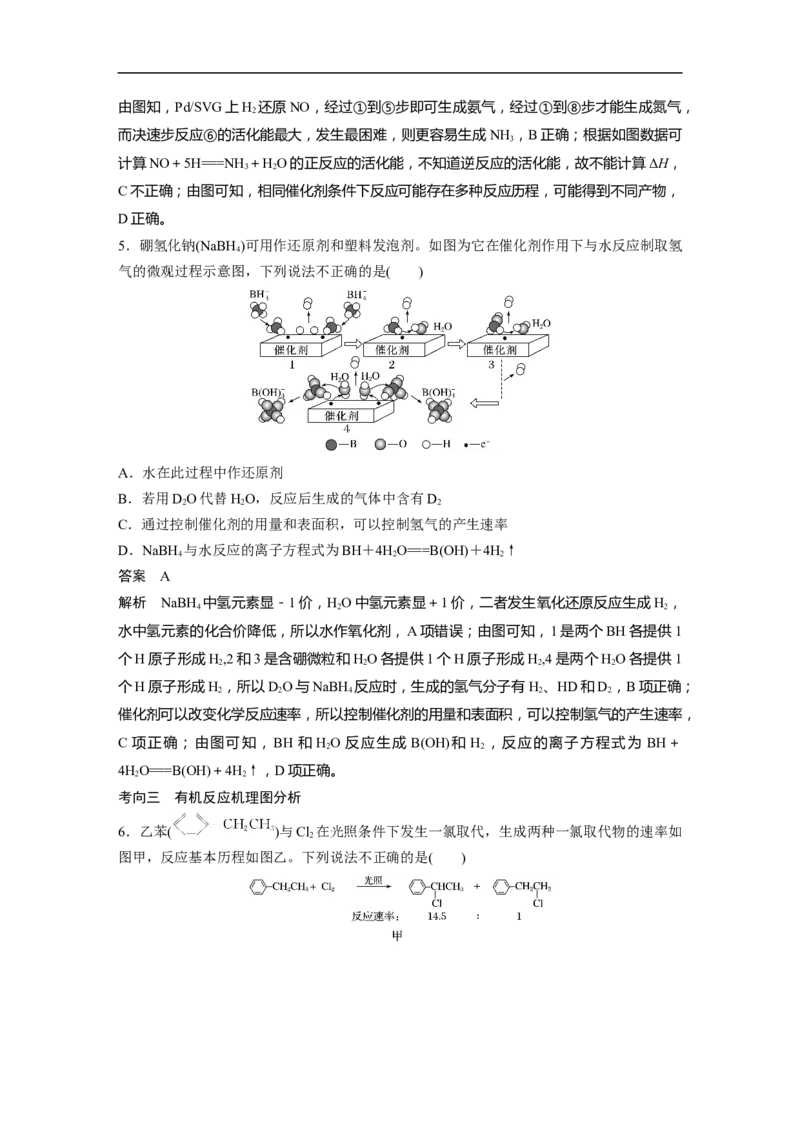
3.氢气可将CO 还原为甲烷:CO(g)+4H(g)CH(g)+2HO(g),科学家研究在催化剂表
2 2 2 4 2
面上CO 与H 反应的前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts
2 2
表示过渡态。下列说法正确的是( )A.起始到Ts1历程中发生了非极性共价键的断裂
B.该转化反应的速率取决于Ts2的能垒
C.前三步历程中最小能垒步骤的化学方程式为·CO+3H(g)+HO(g)===·CO+·OH+
2 2
·H+3H(g)
2
D.物质吸附在催化剂表面,形成过渡态的过程会放出热量
答案 A
解析 根据图示可知,起始到Ts1历程中H 分子部分变成·H,则发生了H—H非极性共价
2
键的断裂,A项正确;在前三步历程中,Ts1的能垒最大,为决速反应,B项错误;从图中
可知,在前三步历程中,Ts3的能垒最低,此步反应的化学方程式为·CO+·OH+·H+
3H(g)===·CO+3H(g)+HO(g),C项错误;由过渡态的能量变化可知,物质吸附在催化
2 2 2
剂表面,形成过渡态的过程能量升高,吸收热量,D选项错误。
考向二 无机反应机理图分析
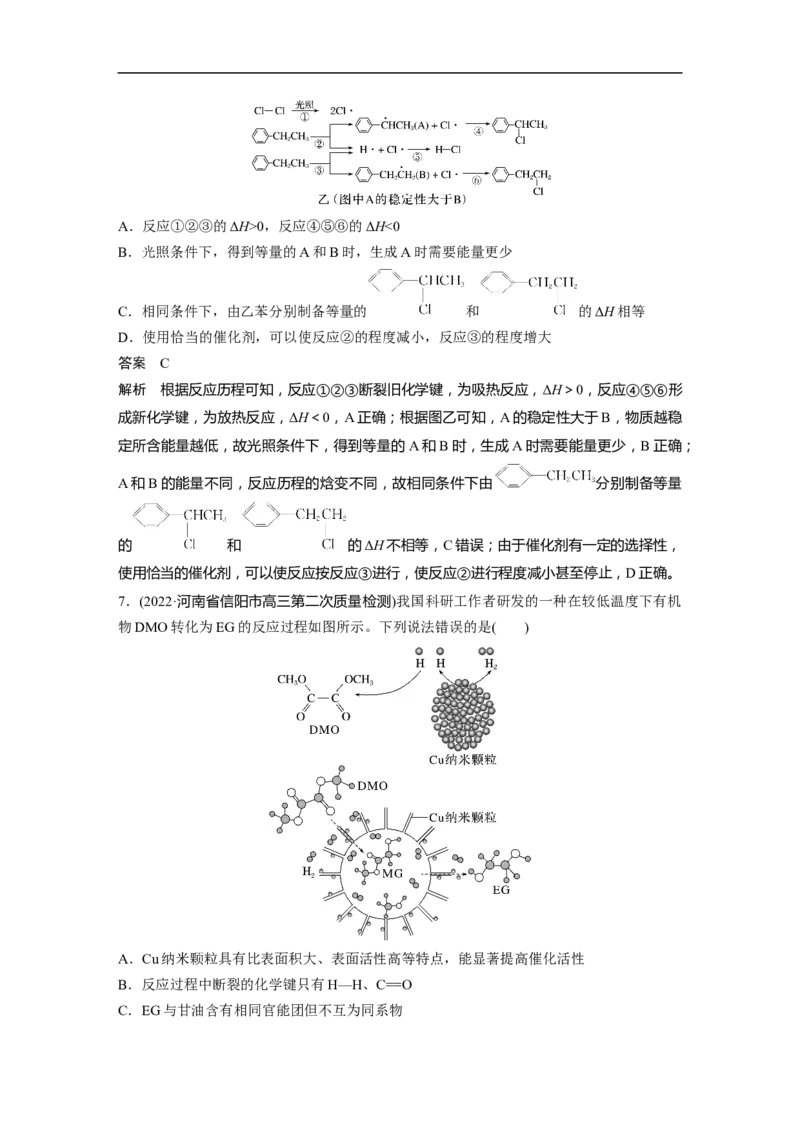
4.(2022·山东省烟台市、德州市高三一模)H 在石墨烯负载型Pd单原子催化剂(Pd/SVG)上
2
还原NO生成N 和NH 的路径机理及活化能(kJ·mol-1)如图所示。下列说法错误的是( )
2 3
A.H 还原NO生成N 的决速步为反应⑥
2 2
B.Pd/SVG上H 还原NO,更容易生成NH
2 3
C.根据如图数据可计算NO+5H===NH +HO的ΔH
3 2
D.由图可知,相同催化剂条件下反应可能存在多种反应历程
答案 C
解析 活化能最大的基元反应为决速步,则H 还原NO生成N 的决速步为反应⑥,A正确;
2 2由图知,Pd/SVG上H 还原NO,经过①到⑤步即可生成氨气,经过①到⑧步才能生成氮气,
2
而决速步反应⑥的活化能最大,发生最困难,则更容易生成NH ,B正确;根据如图数据可
3
计算NO+5H===NH +HO的正反应的活化能,不知道逆反应的活化能,故不能计算ΔH,
3 2
C不正确;由图可知,相同催化剂条件下反应可能存在多种反应历程,可能得到不同产物,
D正确。
5.硼氢化钠(NaBH )可用作还原剂和塑料发泡剂。如图为它在催化剂作用下与水反应制取氢
4
气的微观过程示意图,下列说法不正确的是( )
A.水在此过程中作还原剂
B.若用DO代替HO,反应后生成的气体中含有D
2 2 2
C.通过控制催化剂的用量和表面积,可以控制氢气的产生速率
D.NaBH 与水反应的离子方程式为BH+4HO===B(OH)+4H↑
4 2 2
答案 A
解析 NaBH 中氢元素显-1价,HO中氢元素显+1价,二者发生氧化还原反应生成H ,
4 2 2
水中氢元素的化合价降低,所以水作氧化剂,A项错误;由图可知,1是两个BH各提供1
个H原子形成H,2和3是含硼微粒和HO各提供1个H原子形成H,4是两个HO各提供1
2 2 2 2
个H原子形成H ,所以DO与NaBH 反应时,生成的氢气分子有H 、HD和D ,B项正确;
2 2 4 2 2
催化剂可以改变化学反应速率,所以控制催化剂的用量和表面积,可以控制氢气的产生速率,
C 项正确;由图可知,BH 和 HO 反应生成 B(OH)和 H ,反应的离子方程式为 BH+
2 2
4HO===B(OH)+4H↑,D项正确。
2 2
考向三 有机反应机理图分析
6.乙苯( )与Cl 在光照条件下发生一氯取代,生成两种一氯取代物的速率如
2
图甲,反应基本历程如图乙。下列说法不正确的是( )A.反应①②③的ΔH>0,反应④⑤⑥的ΔH<0
B.光照条件下,得到等量的A和B时,生成A时需要能量更少
C.相同条件下,由乙苯分别制备等量的 和 的ΔH相等
D.使用恰当的催化剂,可以使反应②的程度减小,反应③的程度增大
答案 C
解析 根据反应历程可知,反应①②③断裂旧化学键,为吸热反应,ΔH>0,反应④⑤⑥形
成新化学键,为放热反应,ΔH<0,A正确;根据图乙可知,A的稳定性大于B,物质越稳
定所含能量越低,故光照条件下,得到等量的A和B时,生成A时需要能量更少,B正确;
A和B的能量不同,反应历程的焓变不同,故相同条件下由 分别制备等量
的 和 的ΔH不相等,C错误;由于催化剂有一定的选择性,
使用恰当的催化剂,可以使反应按反应③进行,使反应②进行程度减小甚至停止,D正确。
7.(2022·河南省信阳市高三第二次质量检测)我国科研工作者研发的一种在较低温度下有机
物DMO转化为EG的反应过程如图所示。下列说法错误的是( )
A.Cu纳米颗粒具有比表面积大、表面活性高等特点,能显著提高催化活性
B.反应过程中断裂的化学键只有H—H、C==O
C.EG与甘油含有相同官能团但不互为同系物D.可用金属钠区别EG与DMO
答案 B
解析 Cu纳米颗粒具有比表面积大、表面活性高等特点,能增加反应物接触面积,显著提
高催化活性,A正确;由图可知,反应过程中断裂的化学键有H—H、C==O、C—O等,B
错误;EG是乙二醇(HOCHCHOH),与甘油含有相同官能团(—OH),但羟基数目不同,不
2 2
互为同系物,C正确;EG(乙二醇)与金属钠反应生成氢气,DMO(草酸二甲酯)与金属钠不反
应,故可用金属钠区别EG(乙二醇)与DMO(草酸二甲酯),D正确。