文档内容
第 10 讲 仪器的组合与创新使用
[复习目标] 1.了解同一仪器在不同组合中的用途及不同仪器组合的同一用途。2.了解仪器
的创新使用。
考点一 一器多用与多器一用
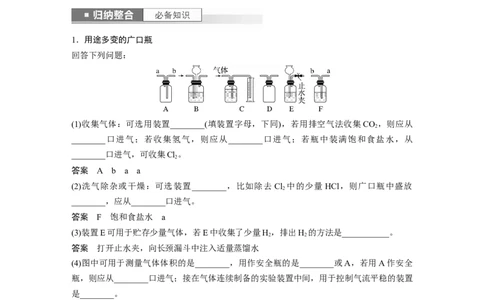
1.用途多变的广口瓶
回答下列问题:
(1)收集气体:可选用装置________(填装置字母,下同),若用排空气法收集CO ,则应从
2
________口进气;若收集氢气,则应从________口进气;若瓶中装满饱和食盐水,从
________口进气,可收集Cl。
2
答案 A b a a
(2)洗气除杂或干燥:可选装置________,比如除去 Cl 中的少量 HCl,则广口瓶中盛放
2
________,应从________口进气。
答案 F 饱和食盐水 a
(3)装置E可用于贮存少量气体,若E中收集了少量H,排出H 的方法是___________。
2 2
答案 打开止水夹,向长颈漏斗中注入适量蒸馏水
(4)图中可用于测量气体体积的是________,用作安全瓶的是________或A,若用A作安全
瓶,则应从________口进气;接在气体连续制备的实验装置中间,用于控制气流平稳的装置
是________。
答案 C D a B
(5)用于监控气体流速(如图F),广口瓶中盛有液体,从________端通入气体,根据液体中产
生气泡的速率来监控通入气体的流速。
答案 a
2.多用途的球形干燥管
位置不同,作用不同
(1)在整套实验装置的中间横放——干燥、吸收及检验装置①干燥管内装有固体干燥剂,可用于干燥气体。无机实验中常用的固体干燥剂有碱石灰、无
水氯化钙、五氧化二磷。
②干燥管内盛有无水硫酸铜(填写试剂名称)时,可用于水蒸气的检验。
③可用于定量测定气体的质量。
(2)在整套实验装置的最后横放——“左吸右挡”:既可以吸收多余的尾气,防止污染空气,
又可以阻挡外界空气中的干扰气体(如CO、水蒸气等)进入装置中。
2
3.实验仪器的“多器一用”
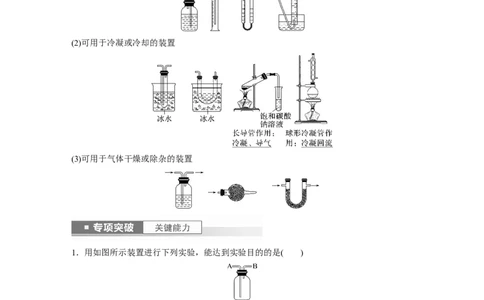
(1)可以测量气体体积的装置
(2)可用于冷凝或冷却的装置
(3)可用于气体干燥或除杂的装置
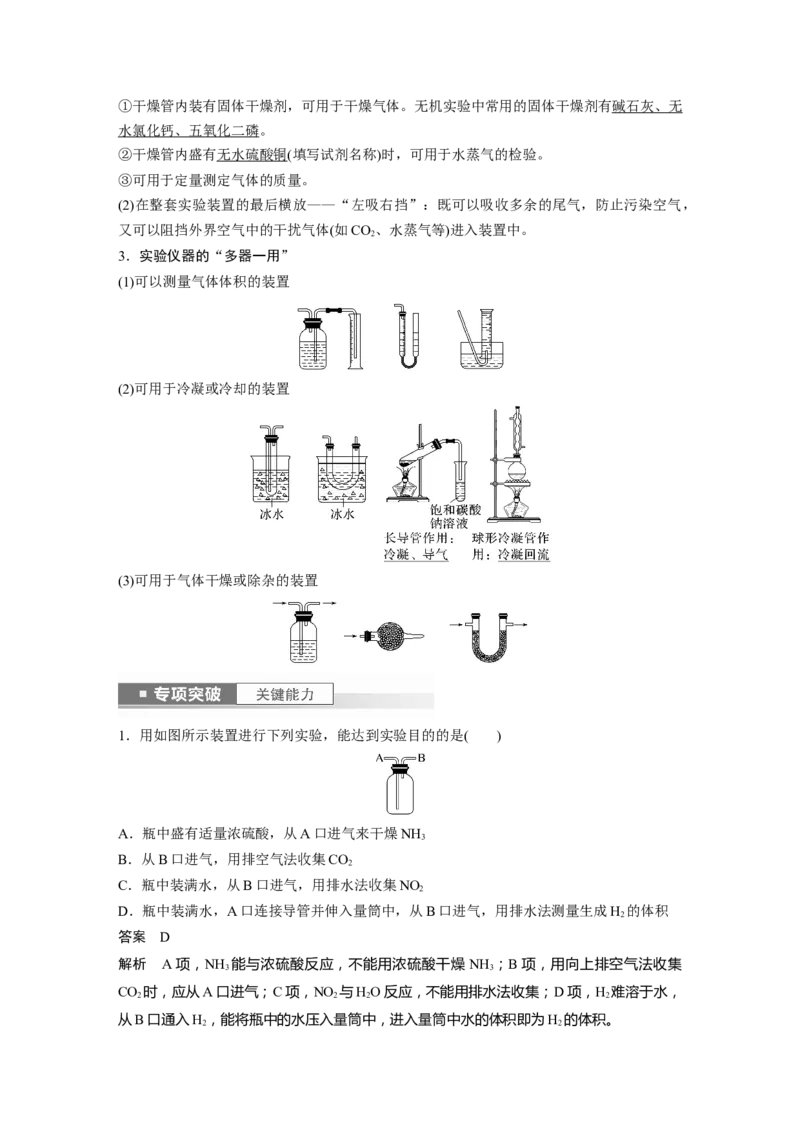
1.用如图所示装置进行下列实验,能达到实验目的的是( )
A.瓶中盛有适量浓硫酸,从A口进气来干燥NH
3
B.从B口进气,用排空气法收集CO
2
C.瓶中装满水,从B口进气,用排水法收集NO
2
D.瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H 的体积
2
答案 D
解析 A项,NH 能与浓硫酸反应,不能用浓硫酸干燥 NH ;B项,用向上排空气法收集
3 3
CO 时,应从A口进气;C项,NO 与HO反应,不能用排水法收集;D项,H 难溶于水,
2 2 2 2
从B口通入H,能将瓶中的水压入量筒中,进入量筒中水的体积即为H 的体积。
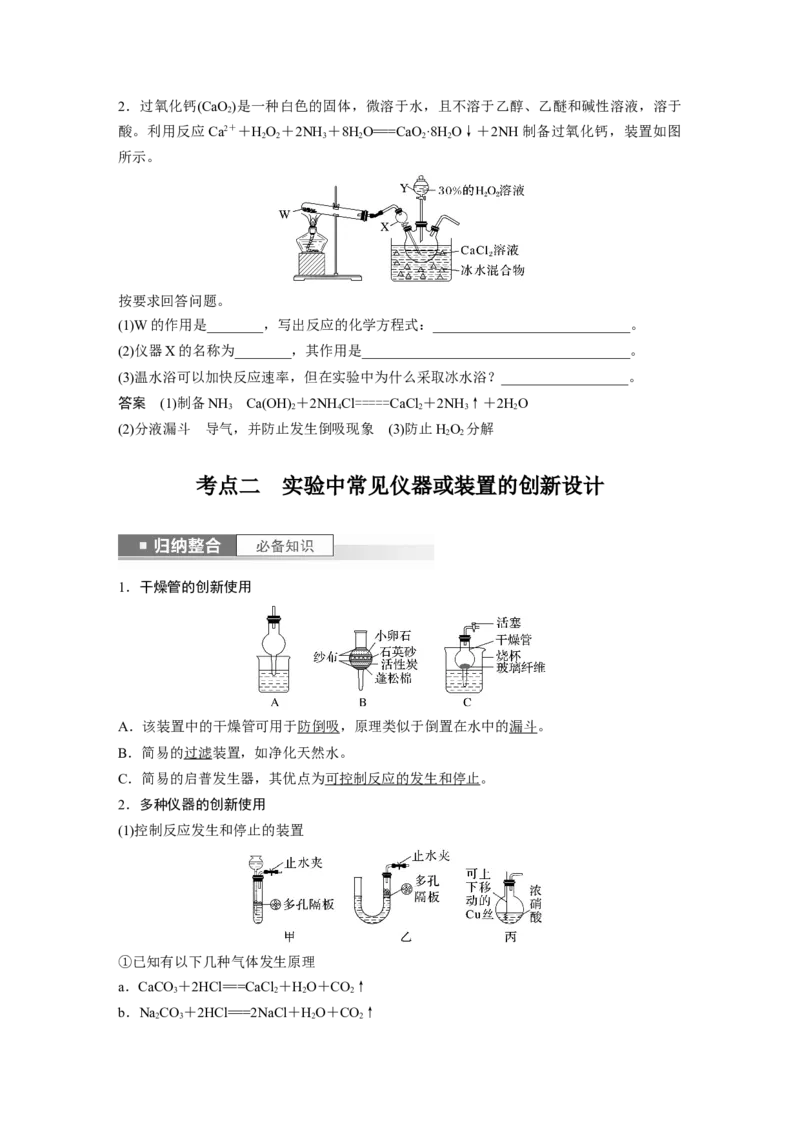
2 22.过氧化钙(CaO)是一种白色的固体,微溶于水,且不溶于乙醇、乙醚和碱性溶液,溶于
2
酸。利用反应Ca2++HO +2NH +8HO===CaO·8H O↓+2NH制备过氧化钙,装置如图
2 2 3 2 2 2
所示。
按要求回答问题。
(1)W的作用是________,写出反应的化学方程式:____________________________。
(2)仪器X的名称为________,其作用是______________________________________。
(3)温水浴可以加快反应速率,但在实验中为什么采取冰水浴?__________________。
答案 (1)制备NH Ca(OH) +2NH Cl=====CaCl +2NH ↑+2HO
3 2 4 2 3 2
(2)分液漏斗 导气,并防止发生倒吸现象 (3)防止HO 分解
2 2
考点二 实验中常见仪器或装置的创新设计
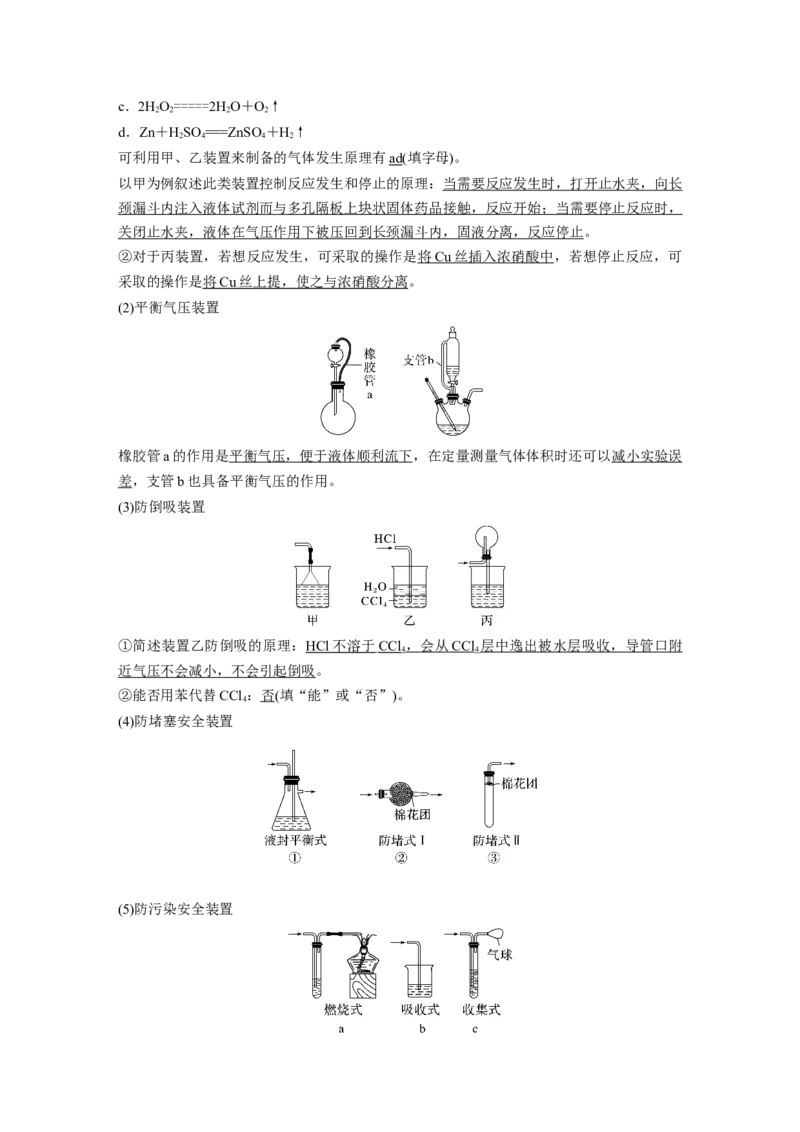
1.干燥管的创新使用
A.该装置中的干燥管可用于防倒吸,原理类似于倒置在水中的漏斗。
B.简易的过滤装置,如净化天然水。
C.简易的启普发生器,其优点为可控制反应的发生和停止。
2.多种仪器的创新使用
(1)控制反应发生和停止的装置
①已知有以下几种气体发生原理
a.CaCO +2HCl===CaCl +HO+CO↑
3 2 2 2
b.NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2c.2HO=====2HO+O↑
2 2 2 2
d.Zn+HSO ===ZnSO+H↑
2 4 4 2
可利用甲、乙装置来制备的气体发生原理有ad(填字母)。
以甲为例叙述此类装置控制反应发生和停止的原理:当需要反应发生时,打开止水夹,向长
颈漏斗内注入液体试剂而与多孔隔板上块状固体药品接触,反应开始;当需要停止反应时,
关闭止水夹,液体在气压作用下被压回到长颈漏斗内,固液分离,反应停止。
②对于丙装置,若想反应发生,可采取的操作是 将 C u 丝插入浓硝酸中 ,若想停止反应,可
采取的操作是 将 C u 丝上提,使之与浓硝酸分离 。
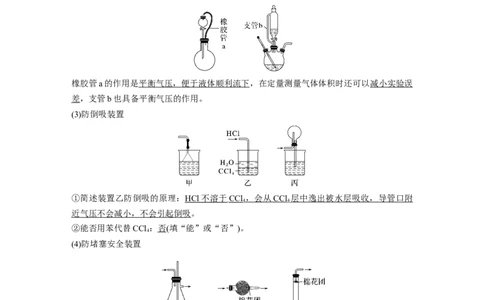
(2)平衡气压装置
橡胶管a的作用是平衡气压,便于液体顺利流下,在定量测量气体体积时还可以减小实验误
差,支管b也具备平衡气压的作用。
(3)防倒吸装置
①简述装置乙防倒吸的原理: HCl 不溶于 CCl ,会从 CC l 层中逸出被水层吸收,导管口附
4 4
近气压不会减小,不会引起倒吸。
②能否用苯代替CCl :否(填“能”或“否”)。
4
(4)防堵塞安全装置
(5)防污染安全装置①实验室制取Cl 时,尾气的处理可采用b装置。
2
②制取CO时,尾气处理可采用a、c装置。
③制取H 时,尾气处理可采用a、c装置。
2
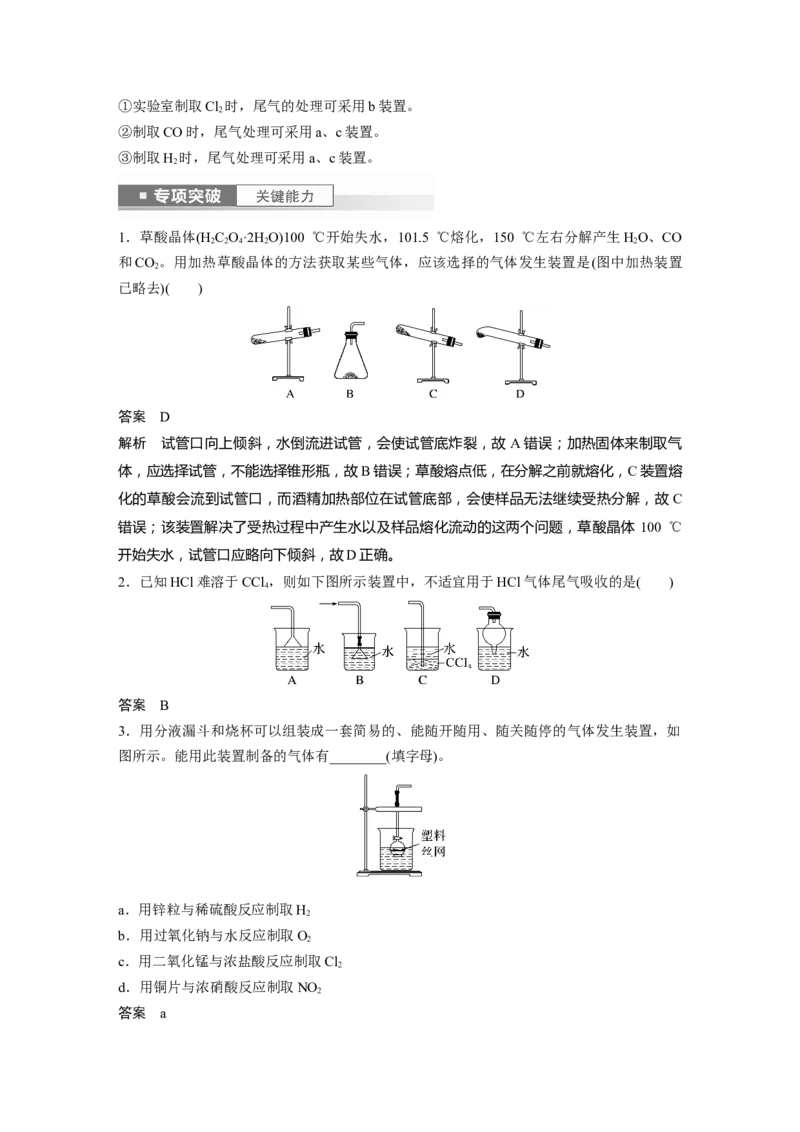
1.草酸晶体(H C O·2H O)100 ℃开始失水,101.5 ℃熔化,150 ℃左右分解产生HO、CO
2 2 4 2 2
和CO 。用加热草酸晶体的方法获取某些气体,应该选择的气体发生装置是(图中加热装置
2
已略去)( )
答案 D
解析 试管口向上倾斜,水倒流进试管,会使试管底炸裂,故 A错误;加热固体来制取气
体,应选择试管,不能选择锥形瓶,故B错误;草酸熔点低,在分解之前就熔化,C装置熔
化的草酸会流到试管口,而酒精加热部位在试管底部,会使样品无法继续受热分解,故 C
错误;该装置解决了受热过程中产生水以及样品熔化流动的这两个问题,草酸晶体 100 ℃
开始失水,试管口应略向下倾斜,故D正确。
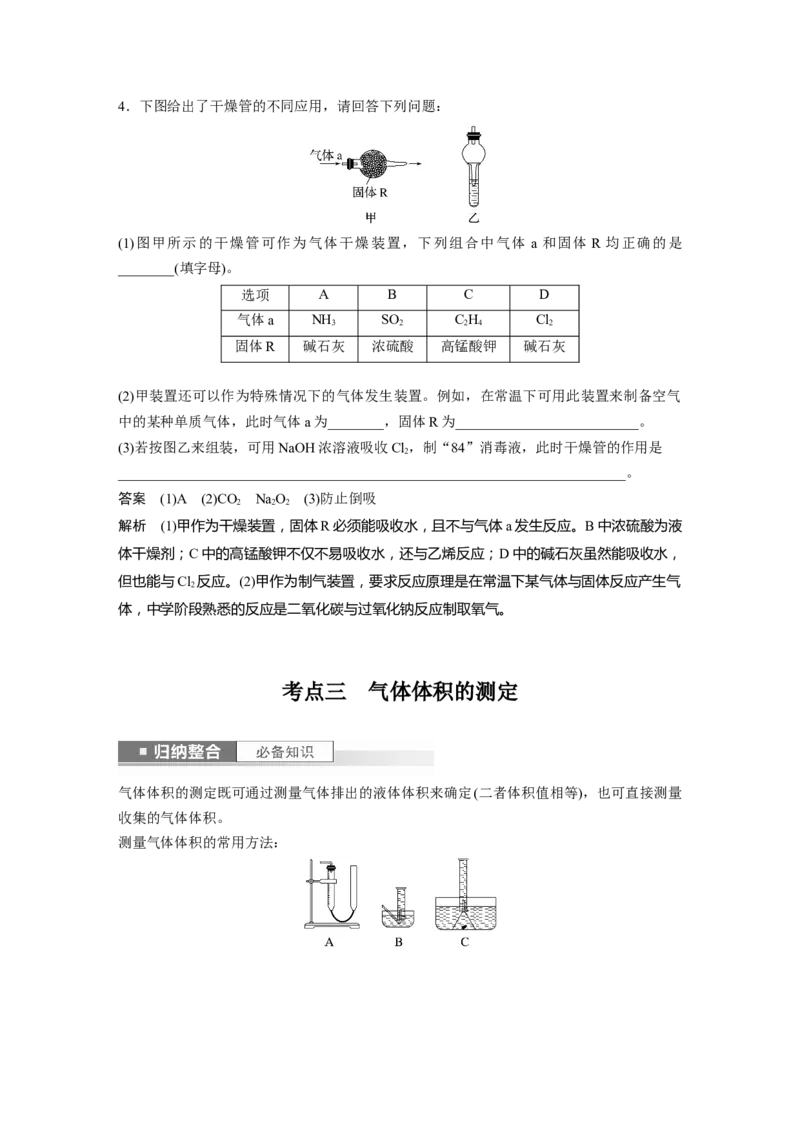
2.已知HCl难溶于CCl ,则如下图所示装置中,不适宜用于HCl气体尾气吸收的是( )
4
答案 B
3.用分液漏斗和烧杯可以组装成一套简易的、能随开随用、随关随停的气体发生装置,如
图所示。能用此装置制备的气体有________(填字母)。
a.用锌粒与稀硫酸反应制取H
2
b.用过氧化钠与水反应制取O
2
c.用二氧化锰与浓盐酸反应制取Cl
2
d.用铜片与浓硝酸反应制取NO
2
答案 a4.下图给出了干燥管的不同应用,请回答下列问题:
(1)图甲所示的干燥管可作为气体干燥装置,下列组合中气体 a 和固体 R 均正确的是
________(填字母)。
选项 A B C D
气体a NH SO C H Cl
3 2 2 4 2
固体R 碱石灰 浓硫酸 高锰酸钾 碱石灰
(2)甲装置还可以作为特殊情况下的气体发生装置。例如,在常温下可用此装置来制备空气
中的某种单质气体,此时气体a为________,固体R为__________________________。
(3)若按图乙来组装,可用NaOH浓溶液吸收Cl,制“84”消毒液,此时干燥管的作用是
2
________________________________________________________________________。
答案 (1)A (2)CO NaO (3)防止倒吸
2 2 2
解析 (1)甲作为干燥装置,固体R必须能吸收水,且不与气体a发生反应。B中浓硫酸为液
体干燥剂;C中的高锰酸钾不仅不易吸收水,还与乙烯反应;D中的碱石灰虽然能吸收水,
但也能与Cl 反应。(2)甲作为制气装置,要求反应原理是在常温下某气体与固体反应产生气
2
体,中学阶段熟悉的反应是二氧化碳与过氧化钠反应制取氧气。
考点三 气体体积的测定
气体体积的测定既可通过测量气体排出的液体体积来确定(二者体积值相等),也可直接测量
收集的气体体积。
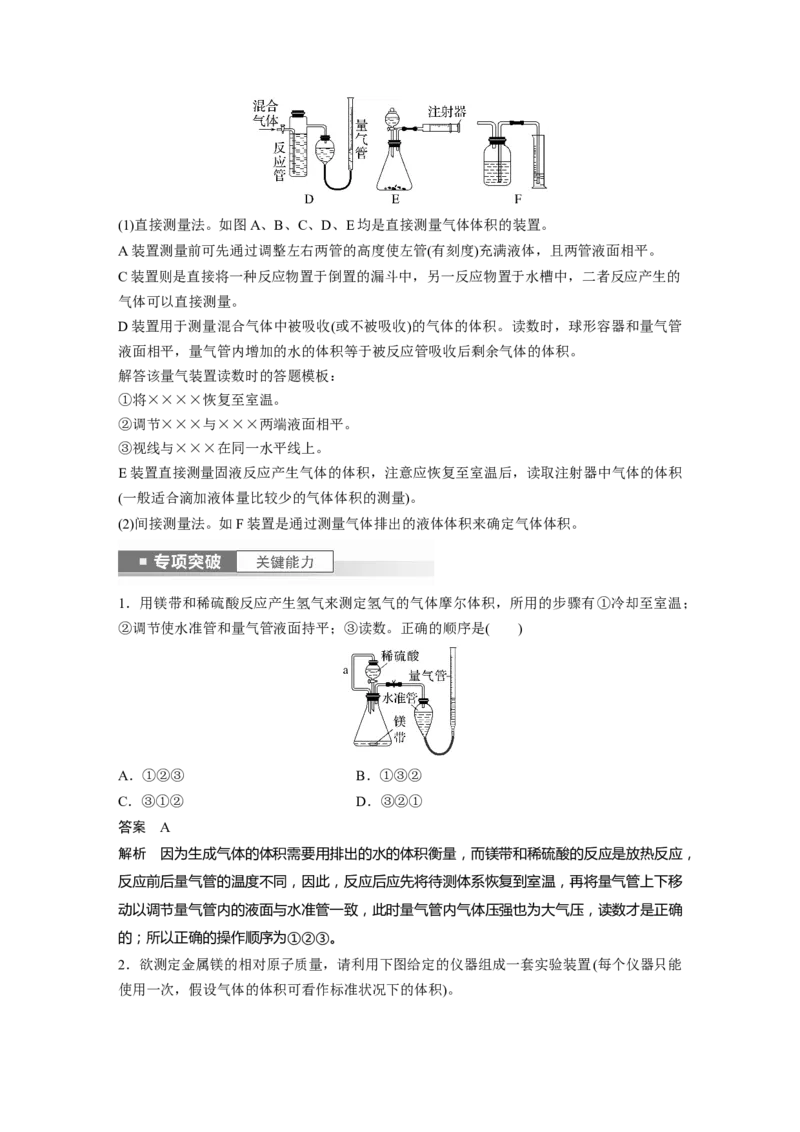
测量气体体积的常用方法:(1)直接测量法。如图A、B、C、D、E均是直接测量气体体积的装置。
A装置测量前可先通过调整左右两管的高度使左管(有刻度)充满液体,且两管液面相平。
C装置则是直接将一种反应物置于倒置的漏斗中,另一反应物置于水槽中,二者反应产生的
气体可以直接测量。
D装置用于测量混合气体中被吸收(或不被吸收)的气体的体积。读数时,球形容器和量气管
液面相平,量气管内增加的水的体积等于被反应管吸收后剩余气体的体积。
解答该量气装置读数时的答题模板:
①将××××恢复至室温。
②调节×××与×××两端液面相平。
③视线与×××在同一水平线上。
E装置直接测量固液反应产生气体的体积,注意应恢复至室温后,读取注射器中气体的体积
(一般适合滴加液体量比较少的气体体积的测量)。
(2)间接测量法。如F装置是通过测量气体排出的液体体积来确定气体体积。
1.用镁带和稀硫酸反应产生氢气来测定氢气的气体摩尔体积,所用的步骤有①冷却至室温;
②调节使水准管和量气管液面持平;③读数。正确的顺序是( )
A.①②③ B.①③②
C.③①② D.③②①
答案 A
解析 因为生成气体的体积需要用排出的水的体积衡量,而镁带和稀硫酸的反应是放热反应,
反应前后量气管的温度不同,因此,反应后应先将待测体系恢复到室温,再将量气管上下移
动以调节量气管内的液面与水准管一致,此时量气管内气体压强也为大气压,读数才是正确
的;所以正确的操作顺序为①②③。
2.欲测定金属镁的相对原子质量,请利用下图给定的仪器组成一套实验装置(每个仪器只能
使用一次,假设气体的体积可看作标准状况下的体积)。回答下列问题(气流从左到右):
(1)各种仪器连接的先后顺序是______接______、________接______、______接______、
________接________(用小写字母表示)。
(2)连接好仪器后,要进行的操作有以下几步,其先后顺序是_______________(填序号)。
①待仪器B中的温度恢复至室温时,测得量筒C中水的体积为V mL;
a
②擦掉镁条表面的氧化膜,将其置于天平上称量,得质量为m g,并将其投入试管B中的多
孔塑料板上;
③检查装置的气密性;
④旋开装置A上分液漏斗的活塞,使其中的水顺利流下,当镁完全溶解时再关闭这个活塞,
这时A中共放入水 V mL。
b
(3)根据实验数据可算出金属镁的相对原子质量,其数学表达式为__________________。
(4)若试管B的温度未冷却至室温,就读出量筒C中水的体积,这将会使所测定镁的相对原
子质量数据________(填“偏大”“偏小”或“无影响”)。
答案 (1)a h g b c f e d
(2)③②④① (3) (4)偏小
解析 (1)根据实验目的及各装置的特点分析可知:利用装置 A中的水压将E中稀盐酸压至
B 中,产生的气体通过将 D 中的水排入 C 中测量其体积,所以连接顺序为
a→h→g→b→c→f→e→d。
(3)由题意知:
Mg ~ H
2
M 22.4 L
M (V-V)×10-3 L
a b
所以M=。
(4)由于试管B未冷却至室温,会导致V变大,所以使Mg的相对原子质量偏小。
a
答题规范(2) 装置的气密性检查
装置的气密性检查必须在放入药品之前进行。
(1)气密性检查的基本思路
使装置内外压强不等,观察气泡或液面变化。
(2)气密性检查的答题规范简答题应注意答题规范,对装置的气密性检查可按如下文字进行答题:
①装置形成封闭体系→操作(微热、手捂、热毛巾捂、加水等)→描述现象→得出结论。
②微热法检查的关键词是封闭、微热、气泡、水柱。
③液差(封)法的关键词是封闭、液差。
④答题时易忽略的关键性的文字叙述:
a.将导管末端浸入水中;
b.关闭或者开启某些气体通道的活塞或弹簧夹;
c.加水至“将长颈漏斗下口浸没”。
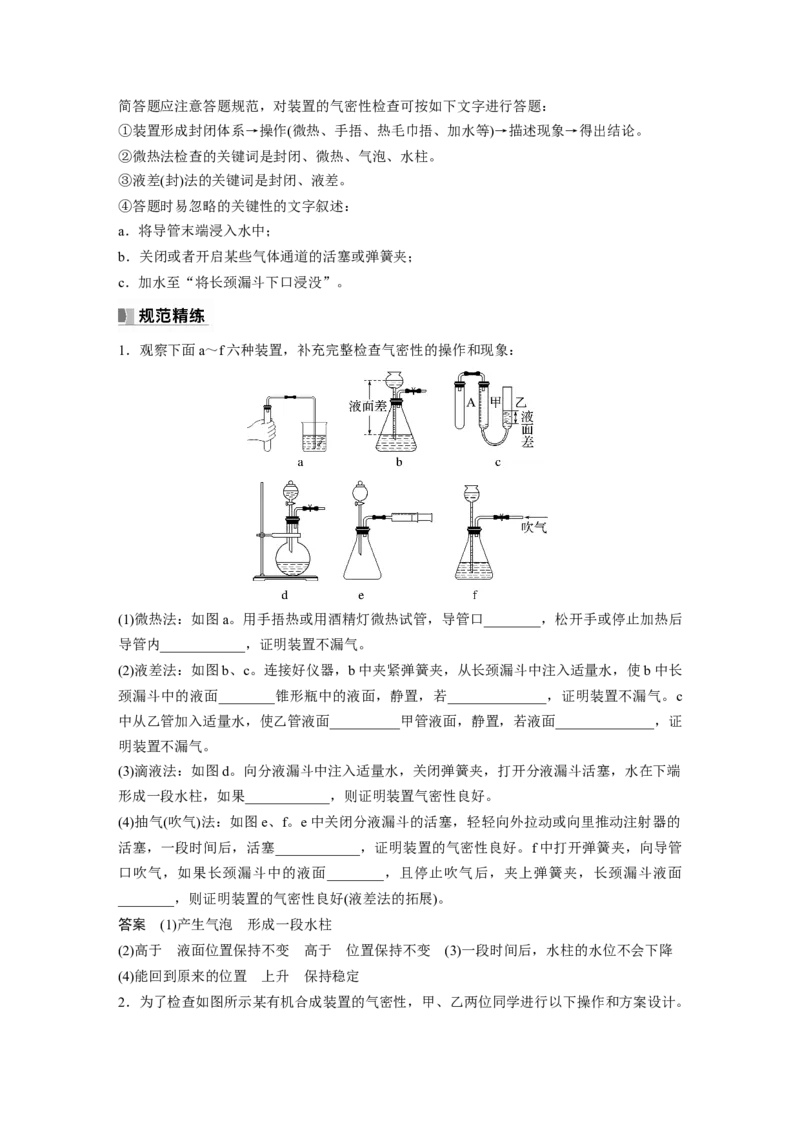
1.观察下面a~f六种装置,补充完整检查气密性的操作和现象:
(1)微热法:如图a。用手捂热或用酒精灯微热试管,导管口________,松开手或停止加热后
导管内____________,证明装置不漏气。
(2)液差法:如图b、c。连接好仪器,b中夹紧弹簧夹,从长颈漏斗中注入适量水,使b中长
颈漏斗中的液面________锥形瓶中的液面,静置,若______________,证明装置不漏气。c
中从乙管加入适量水,使乙管液面__________甲管液面,静置,若液面______________,证
明装置不漏气。
(3)滴液法:如图d。向分液漏斗中注入适量水,关闭弹簧夹,打开分液漏斗活塞,水在下端
形成一段水柱,如果____________,则证明装置气密性良好。
(4)抽气(吹气)法:如图e、f。e中关闭分液漏斗的活塞,轻轻向外拉动或向里推动注射器的
活塞,一段时间后,活塞____________,证明装置的气密性良好。f中打开弹簧夹,向导管
口吹气,如果长颈漏斗中的液面________,且停止吹气后,夹上弹簧夹,长颈漏斗液面
________,则证明装置的气密性良好(液差法的拓展)。
答案 (1)产生气泡 形成一段水柱
(2)高于 液面位置保持不变 高于 位置保持不变 (3)一段时间后,水柱的水位不会下降
(4)能回到原来的位置 上升 保持稳定
2.为了检查如图所示某有机合成装置的气密性,甲、乙两位同学进行以下操作和方案设计。(1)甲同学认为,用微热法便可检查装置气密性是否良好。经检验方案可行,则甲同学检查
装置气密性的操作方法、现象和结论是_______________________________________。
(2)乙同学认为只需关闭a处止水夹,打开b的玻璃活塞,观察液体能否顺利滴下便可检查其
气密性是否良好,该同学的方案可行吗?________(填“可行”或“不可行”),并解释原因:
________________________________________________________________________。
答案 (1)将e导管下端管口浸入盛水的烧杯中,关闭b的活塞,打开a处止水夹,微热d,
若e导管口有气泡冒出,冷却至室温后,又有一段水柱上升,证明气密性良好 (2)不可行
无论气密性是否良好,b中的液体均能顺利滴下
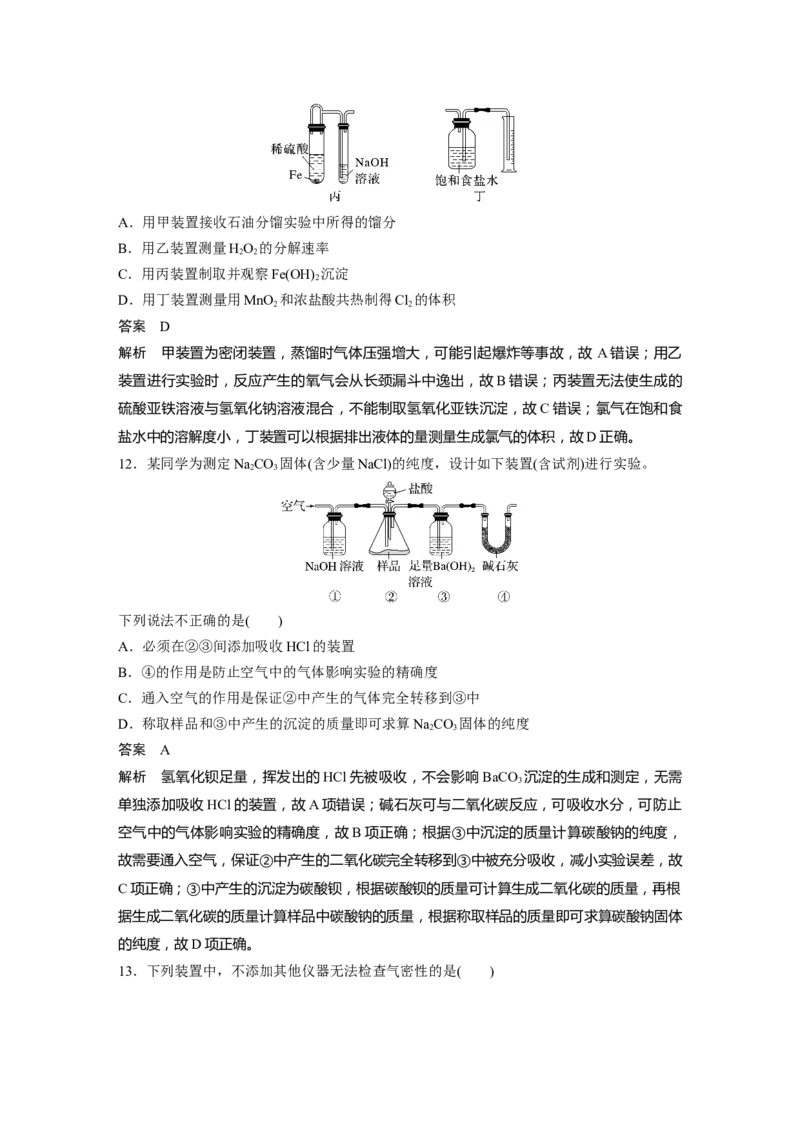
1.(2022·湖北,6)下列实验装置(部分夹持装置略)或现象错误的是( )
答案 C
解析 碳酸钠和碳酸氢钠都会因水解而使溶液显碱性,碳酸钠的碱性强于碳酸氢钠,滴入酚
酞溶液后,碳酸钠溶液呈红色,碳酸氢钠溶液呈浅红色,A正确;食盐水为中性,铁钉发生
吸氧腐蚀,试管中的气体减少,导管中形成一段水柱,B正确;钠燃烧温度在400 ℃以上,
玻璃表面皿不耐高温,故钠燃烧通常用坩埚或者燃烧匙,C错误。
2.(2020·江苏,5)实验室以CaCO 为原料,制备CO 并获得CaCl ·6H O晶体。下列图示装
3 2 2 2
置和原理不能达到实验目的的是( )答案 D
解析 A对,碳酸钙与稀盐酸反应可制备CO ,且为固液常温型反应,装置也正确;B对,
2
CO 密度比空气大,可以用向上排空气法收集;C对,分离固体与液体,可采用过滤的方法;
2
D错,CaCl ·6H O晶体可以通过蒸发浓缩、冷却结晶、过滤的方法制得,采用蒸发结晶法
2 2
易导致CaCl ·6H O失去结晶水。
2 2
3.(2021·天津,15)某化学小组同学利用一定浓度的 HO 溶液制备 O ,再用 O 氧化
2 2 2 2
C HOH,并检验氧化产物。
2 5
Ⅰ.制备O
2
该小组同学设计了如下气体发生装置(夹持装置省略)
(1)甲装置中主要仪器的名称为____________________________。
(2)乙装置中,用粘合剂将MnO 制成团,放在多孔塑料片上,连接好装置,气密性良好后打
2
开活塞K ,经长颈漏斗向试管中缓慢加入3% H O 溶液至____________。欲使反应停止,
1 2 2
关闭活塞K 即可,此时装置中的现象是__________________________________。
1
(3)丙装置可用于制备较多O ,催化剂铂丝可上下移动。制备过程中如果体系内压强过大,
2
安全管中的现象是______________________,此时可以将铂丝抽离HO 溶液,还可以采取
2 2
的安全措施是______________________________。
(4)丙装置的特点是______________(填序号)。
a.可以控制制备反应的开始和结束
b.可通过调节催化剂与液体接触的面积来控制反应的速率
c.与乙装置相比,产物中的O 含量高、杂质种类少
2
Ⅱ.氧化C HOH
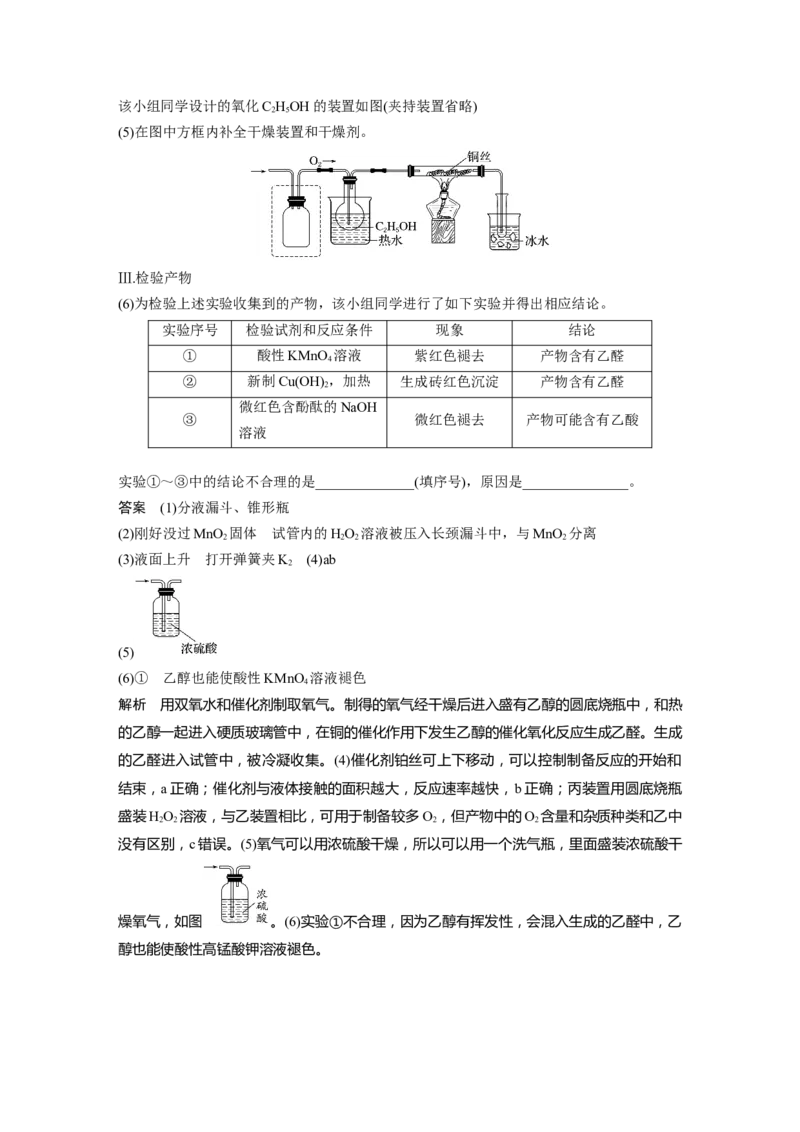
2 5该小组同学设计的氧化C HOH的装置如图(夹持装置省略)
2 5
(5)在图中方框内补全干燥装置和干燥剂。
Ⅲ.检验产物
(6)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验序号 检验试剂和反应条件 现象 结论
① 酸性KMnO 溶液 紫红色褪去 产物含有乙醛
4
② 新制Cu(OH) ,加热 生成砖红色沉淀 产物含有乙醛
2
微红色含酚酞的NaOH
③ 微红色褪去 产物可能含有乙酸
溶液
实验①~③中的结论不合理的是______________(填序号),原因是_______________。
答案 (1)分液漏斗、锥形瓶
(2)刚好没过MnO 固体 试管内的HO 溶液被压入长颈漏斗中,与MnO 分离
2 2 2 2
(3)液面上升 打开弹簧夹K (4)ab
2
(5)
(6)① 乙醇也能使酸性KMnO 溶液褪色
4
解析 用双氧水和催化剂制取氧气。制得的氧气经干燥后进入盛有乙醇的圆底烧瓶中,和热
的乙醇一起进入硬质玻璃管中,在铜的催化作用下发生乙醇的催化氧化反应生成乙醛。生成
的乙醛进入试管中,被冷凝收集。(4)催化剂铂丝可上下移动,可以控制制备反应的开始和
结束,a正确;催化剂与液体接触的面积越大,反应速率越快,b正确;丙装置用圆底烧瓶
盛装HO 溶液,与乙装置相比,可用于制备较多O,但产物中的O 含量和杂质种类和乙中
2 2 2 2
没有区别,c错误。(5)氧气可以用浓硫酸干燥,所以可以用一个洗气瓶,里面盛装浓硫酸干
燥氧气,如图 。(6)实验①不合理,因为乙醇有挥发性,会混入生成的乙醛中,乙
醇也能使酸性高锰酸钾溶液褪色。课时精练
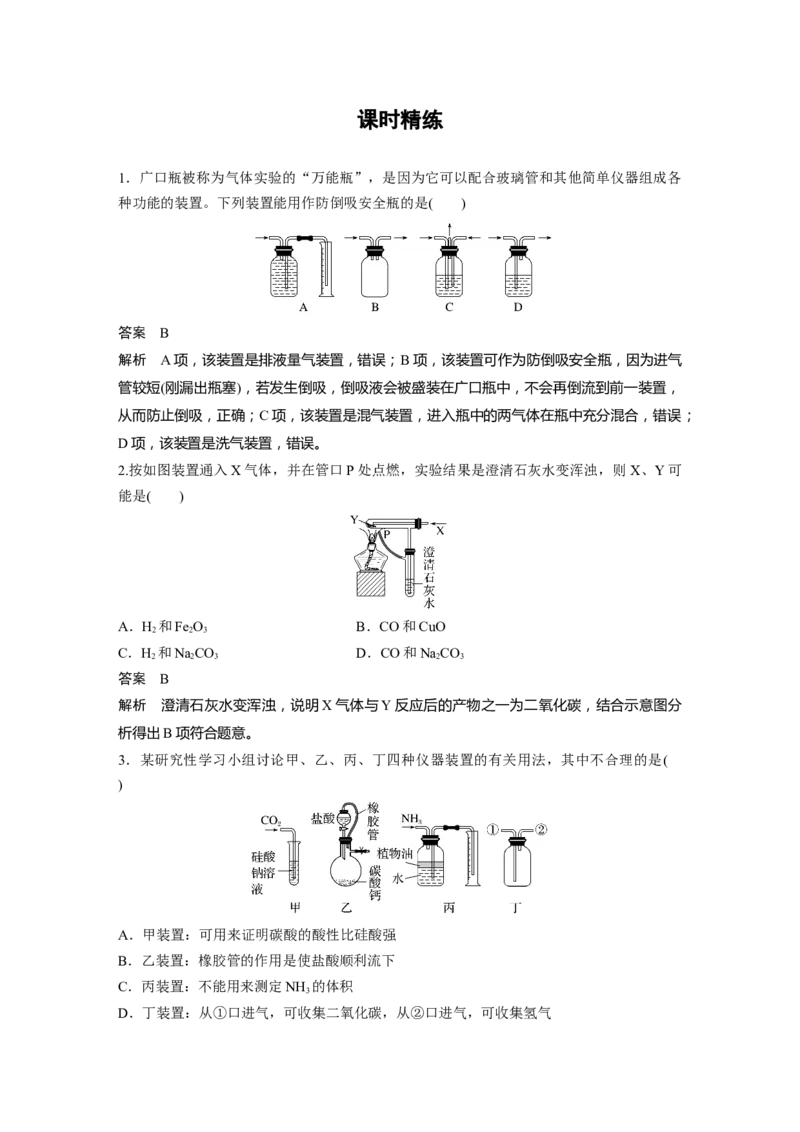
1.广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各
种功能的装置。下列装置能用作防倒吸安全瓶的是( )
答案 B
解析 A项,该装置是排液量气装置,错误;B项,该装置可作为防倒吸安全瓶,因为进气
管较短(刚漏出瓶塞),若发生倒吸,倒吸液会被盛装在广口瓶中,不会再倒流到前一装置,
从而防止倒吸,正确;C项,该装置是混气装置,进入瓶中的两气体在瓶中充分混合,错误;
D项,该装置是洗气装置,错误。
2.按如图装置通入X气体,并在管口P处点燃,实验结果是澄清石灰水变浑浊,则X、Y可
能是( )
A.H 和Fe O B.CO和CuO
2 2 3
C.H 和NaCO D.CO和NaCO
2 2 3 2 3
答案 B
解析 澄清石灰水变浑浊,说明X气体与Y反应后的产物之一为二氧化碳,结合示意图分
析得出B项符合题意。
3.某研究性学习小组讨论甲、乙、丙、丁四种仪器装置的有关用法,其中不合理的是(
)
A.甲装置:可用来证明碳酸的酸性比硅酸强
B.乙装置:橡胶管的作用是使盐酸顺利流下
C.丙装置:不能用来测定NH 的体积
3
D.丁装置:从①口进气,可收集二氧化碳,从②口进气,可收集氢气答案 C
解析 植物油能隔离氨气与水,可以将水排出,可以测定氨气的体积,C错误;导管长进短
出可收集密度比空气大的气体,导管短进长出可收集密度比空气小的气体,则从①口进气,
可收集二氧化碳,从②口进气,可收集氢气,D正确。
4.下述实验设计能够达到实验目的的是( )
答案 A
解析 该装置可用于吸收易溶于碱溶液的气体,并可防倒吸,A项正确;酸碱中和滴定需用
酸碱指示剂确定滴定终点,且NaOH溶液应用碱式滴定管盛放,B项错误;NO 易溶于水且
2
与水反应生成NO,不能用排水法收集NO ,C项错误;蒸干溶液不能使用坩埚,且FeCl 在
2 2
加热条件下水解生成 Fe(OH) ,且 Fe2+在空气中易被氧化成 Fe3+,蒸发灼烧最后得到
2
Fe O,不能得到无水FeCl ,D项错误。
2 3 2
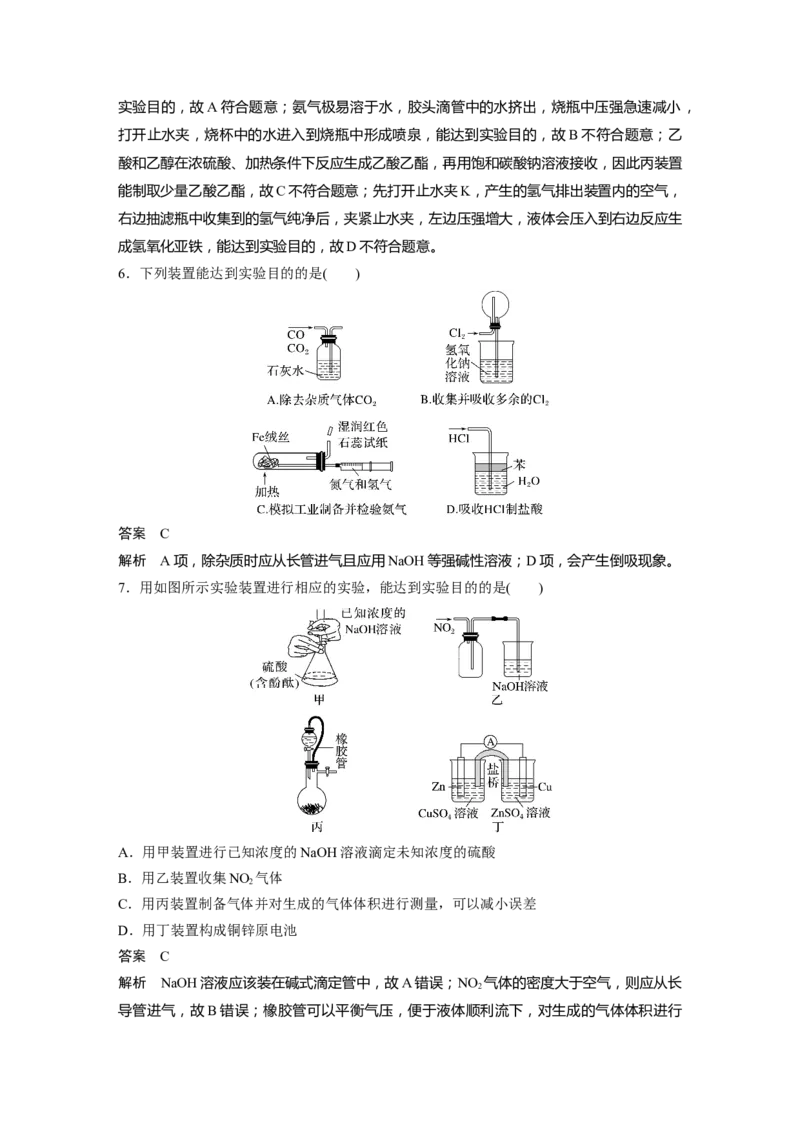
5.用下列装置进行实验(部分夹持仪器已省略),不能达到实验目的的是( )
A.用甲装置制备并收集NH
3
B.用乙装置进行NH 的喷泉实验
3
C.用丙装置制取少量乙酸乙酯
D.用丁装置制取氢氧化亚铁
答案 A
解析 氯化铵受热分解生成氨气和HCl,但在试管口两者会反应生成氯化铵,因此不能达到实验目的,故A符合题意;氨气极易溶于水,胶头滴管中的水挤出,烧瓶中压强急速减小,
打开止水夹,烧杯中的水进入到烧瓶中形成喷泉,能达到实验目的,故B不符合题意;乙
酸和乙醇在浓硫酸、加热条件下反应生成乙酸乙酯,再用饱和碳酸钠溶液接收,因此丙装置
能制取少量乙酸乙酯,故C不符合题意;先打开止水夹K,产生的氢气排出装置内的空气,
右边抽滤瓶中收集到的氢气纯净后,夹紧止水夹,左边压强增大,液体会压入到右边反应生
成氢氧化亚铁,能达到实验目的,故D不符合题意。
6.下列装置能达到实验目的的是( )
答案 C
解析 A项,除杂质时应从长管进气且应用NaOH等强碱性溶液;D项,会产生倒吸现象。
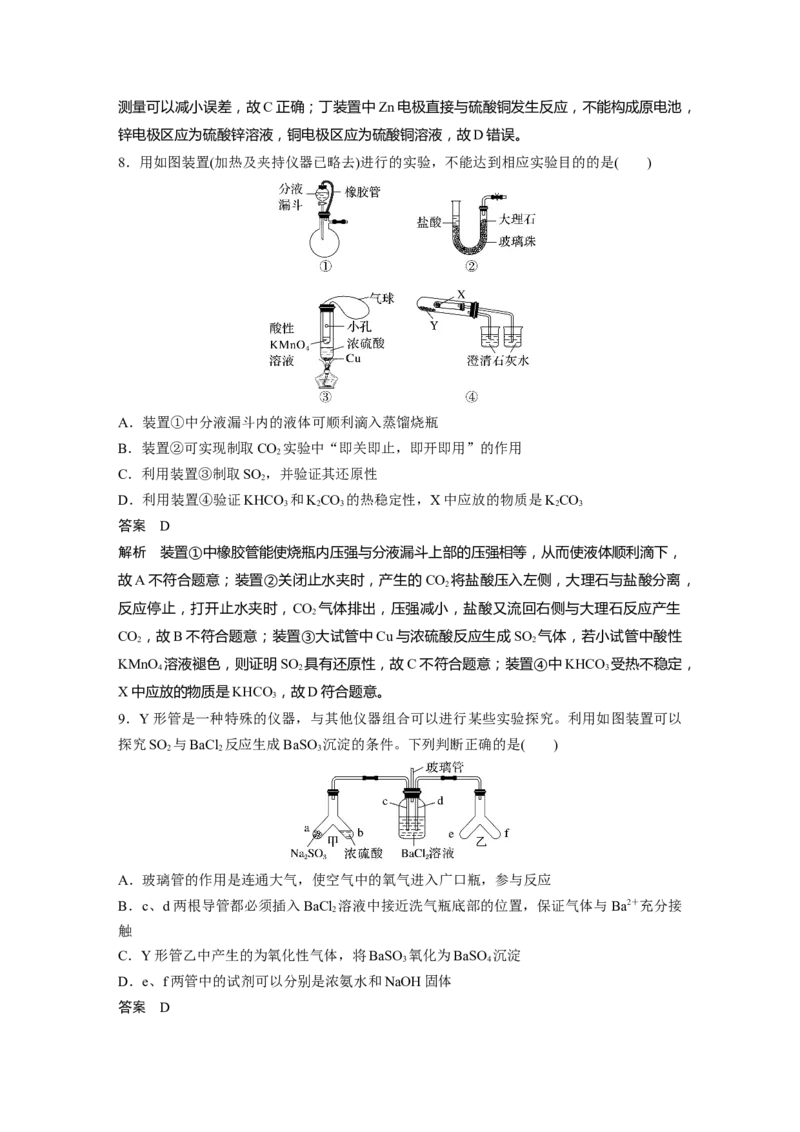
7.用如图所示实验装置进行相应的实验,能达到实验目的的是( )
A.用甲装置进行已知浓度的NaOH溶液滴定未知浓度的硫酸
B.用乙装置收集NO 气体
2
C.用丙装置制备气体并对生成的气体体积进行测量,可以减小误差
D.用丁装置构成铜锌原电池
答案 C
解析 NaOH溶液应该装在碱式滴定管中,故A错误;NO 气体的密度大于空气,则应从长
2
导管进气,故B错误;橡胶管可以平衡气压,便于液体顺利流下,对生成的气体体积进行测量可以减小误差,故C正确;丁装置中Zn电极直接与硫酸铜发生反应,不能构成原电池,
锌电极区应为硫酸锌溶液,铜电极区应为硫酸铜溶液,故D错误。
8.用如图装置(加热及夹持仪器已略去)进行的实验,不能达到相应实验目的的是( )
A.装置①中分液漏斗内的液体可顺利滴入蒸馏烧瓶
B.装置②可实现制取CO 实验中“即关即止,即开即用”的作用
2
C.利用装置③制取SO ,并验证其还原性
2
D.利用装置④验证KHCO 和KCO 的热稳定性,X中应放的物质是KCO
3 2 3 2 3
答案 D
解析 装置①中橡胶管能使烧瓶内压强与分液漏斗上部的压强相等,从而使液体顺利滴下,
故A不符合题意;装置②关闭止水夹时,产生的CO 将盐酸压入左侧,大理石与盐酸分离,
2
反应停止,打开止水夹时,CO 气体排出,压强减小,盐酸又流回右侧与大理石反应产生
2
CO ,故B不符合题意;装置③大试管中Cu与浓硫酸反应生成SO 气体,若小试管中酸性
2 2
KMnO 溶液褪色,则证明SO 具有还原性,故C不符合题意;装置④中KHCO 受热不稳定,
4 2 3
X中应放的物质是KHCO ,故D符合题意。
3
9.Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以
探究SO 与BaCl 反应生成BaSO 沉淀的条件。下列判断正确的是( )
2 2 3
A.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
B.c、d两根导管都必须插入BaCl 溶液中接近洗气瓶底部的位置,保证气体与Ba2+充分接
2
触
C.Y形管乙中产生的为氧化性气体,将BaSO 氧化为BaSO 沉淀
3 4
D.e、f两管中的试剂可以分别是浓氨水和NaOH固体
答案 D解析 该实验的目的是探究SO 与BaCl 溶液反应生成BaSO 沉淀的条件,根据“强酸制弱
2 2 3
酸”原理,若两种物质直接混合,不能得到BaSO 沉淀,若溶液显碱性,SO 转化为SO,
3 2
则可得到BaSO 沉淀。因为装置甲和乙都产生气体,会使试剂瓶内的压强增大,玻璃管的作
3
用是使试剂瓶内的压强保持和外界压强相等,A错误;若装置乙产生NH ,NH 极易溶于水,
3 3
直接插入溶液中易引起倒吸,B错误;若装置乙产生氧化性气体,可将SO氧化为SO,C错
误;装置乙中装入浓氨水和氢氧化钠固体可产生NH ,可使SO 与BaCl 反应生成BaSO ,
3 2 2 3
D正确。
10.关于下列各装置图的叙述不正确的是( )
A.装置①可验证HCl气体在水中的溶解性
B.装置②可用于收集H、NH 、Cl、HCl、NO 、NO等
2 3 2 2
C.装置③中X为四氯化碳,可用于吸收氨气或氯化氢
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
答案 B
解析 装置①中HCl易溶于水,滴入水后气球膨胀,A项正确;装置②中,左边长导管进气,
可收集密度比空气大的气体,如Cl、HCl、NO 等,右边短导管进气,可收集密度比空气小
2 2
的气体,如H 、NH 等,但NO不能用排空气法收集,B项不正确;四氯化碳的密度比水大,
2 3
四氯化碳在下层,氨气或氯化氢不溶于四氯化碳,可以防止倒吸,C项正确;氨气的密度比
空气小,可用向下排空气法收集,也可用碱石灰干燥,且多余的氨气可通过倒扣的漏斗用水
吸收,D项正确。
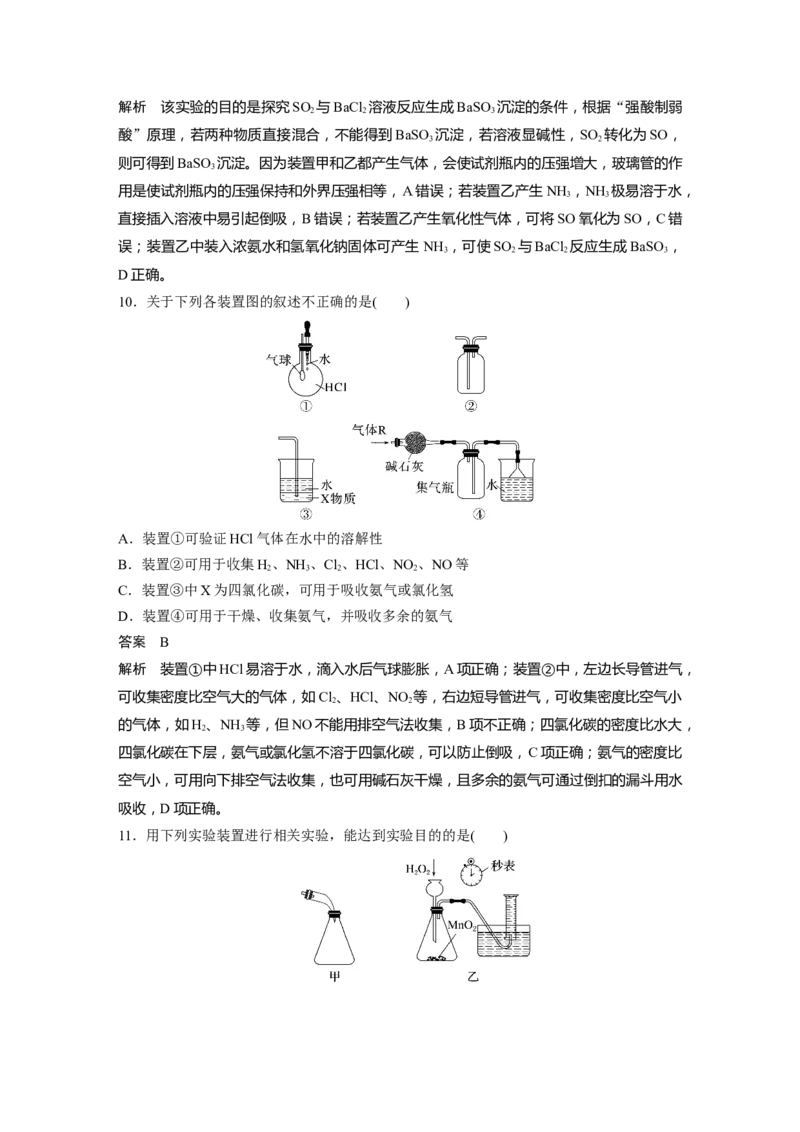
11.用下列实验装置进行相关实验,能达到实验目的的是( )A.用甲装置接收石油分馏实验中所得的馏分
B.用乙装置测量HO 的分解速率
2 2
C.用丙装置制取并观察Fe(OH) 沉淀
2
D.用丁装置测量用MnO 和浓盐酸共热制得Cl 的体积
2 2
答案 D
解析 甲装置为密闭装置,蒸馏时气体压强增大,可能引起爆炸等事故,故 A错误;用乙
装置进行实验时,反应产生的氧气会从长颈漏斗中逸出,故B错误;丙装置无法使生成的
硫酸亚铁溶液与氢氧化钠溶液混合,不能制取氢氧化亚铁沉淀,故C错误;氯气在饱和食
盐水中的溶解度小,丁装置可以根据排出液体的量测量生成氯气的体积,故D正确。
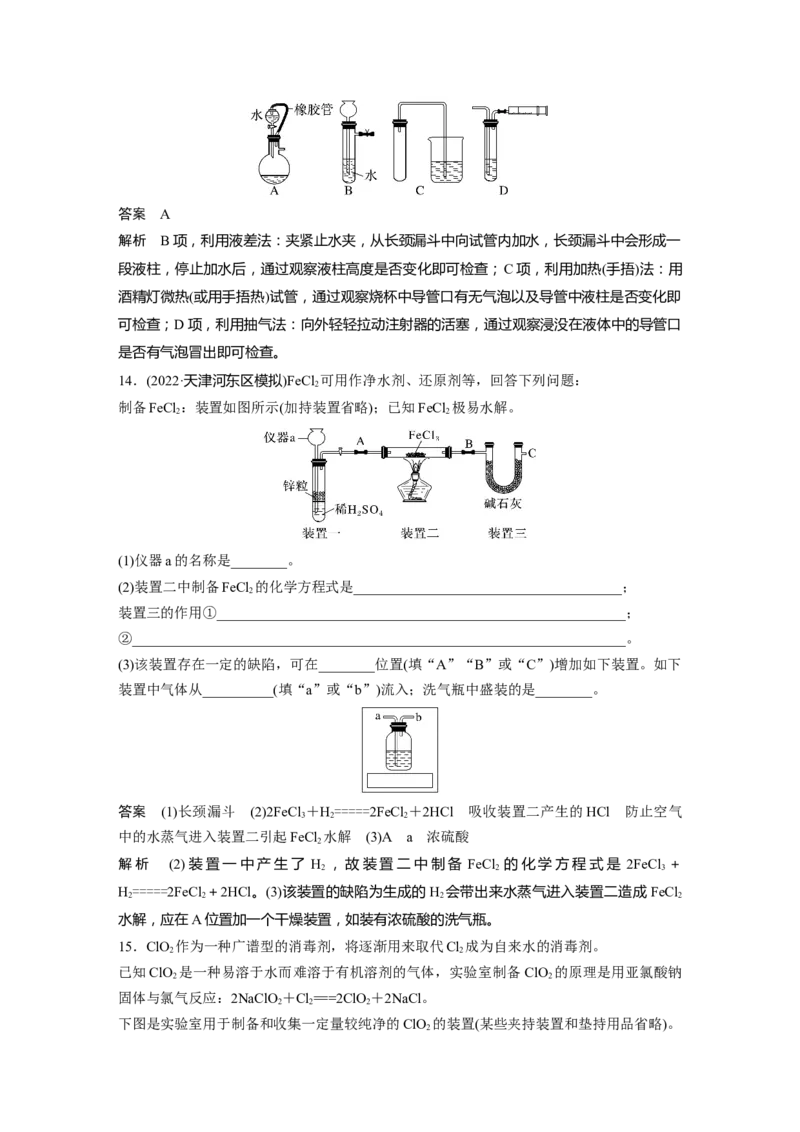
12.某同学为测定NaCO 固体(含少量NaCl)的纯度,设计如下装置(含试剂)进行实验。
2 3
下列说法不正确的是( )
A.必须在②③间添加吸收HCl的装置
B.④的作用是防止空气中的气体影响实验的精确度
C.通入空气的作用是保证②中产生的气体完全转移到③中
D.称取样品和③中产生的沉淀的质量即可求算NaCO 固体的纯度
2 3
答案 A
解析 氢氧化钡足量,挥发出的HCl先被吸收,不会影响BaCO 沉淀的生成和测定,无需
3
单独添加吸收HCl的装置,故A项错误;碱石灰可与二氧化碳反应,可吸收水分,可防止
空气中的气体影响实验的精确度,故B项正确;根据③中沉淀的质量计算碳酸钠的纯度,
故需要通入空气,保证②中产生的二氧化碳完全转移到③中被充分吸收,减小实验误差,故
C项正确;③中产生的沉淀为碳酸钡,根据碳酸钡的质量可计算生成二氧化碳的质量,再根
据生成二氧化碳的质量计算样品中碳酸钠的质量,根据称取样品的质量即可求算碳酸钠固体
的纯度,故D项正确。
13.下列装置中,不添加其他仪器无法检查气密性的是( )答案 A
解析 B项,利用液差法:夹紧止水夹,从长颈漏斗中向试管内加水,长颈漏斗中会形成一
段液柱,停止加水后,通过观察液柱高度是否变化即可检查;C项,利用加热(手捂)法:用
酒精灯微热(或用手捂热)试管,通过观察烧杯中导管口有无气泡以及导管中液柱是否变化即
可检查;D项,利用抽气法:向外轻轻拉动注射器的活塞,通过观察浸没在液体中的导管口
是否有气泡冒出即可检查。
14.(2022·天津河东区模拟)FeCl 可用作净水剂、还原剂等,回答下列问题:
2
制备FeCl :装置如图所示(加持装置省略);已知FeCl 极易水解。
2 2
(1)仪器a的名称是________。
(2)装置二中制备FeCl 的化学方程式是______________________________________;
2
装置三的作用①__________________________________________________________;
②______________________________________________________________________。
(3)该装置存在一定的缺陷,可在________位置(填“A”“B”或“C”)增加如下装置。如下
装置中气体从__________(填“a”或“b”)流入;洗气瓶中盛装的是________。
答案 (1)长颈漏斗 (2)2FeCl +H=====2FeCl +2HCl 吸收装置二产生的HCl 防止空气
3 2 2
中的水蒸气进入装置二引起FeCl 水解 (3)A a 浓硫酸
2
解析 (2)装置一中产生了 H ,故装置二中制备 FeCl 的化学方程式是 2FeCl +
2 2 3
H=====2FeCl +2HCl。(3)该装置的缺陷为生成的H 会带出来水蒸气进入装置二造成FeCl
2 2 2 2
水解,应在A位置加一个干燥装置,如装有浓硫酸的洗气瓶。
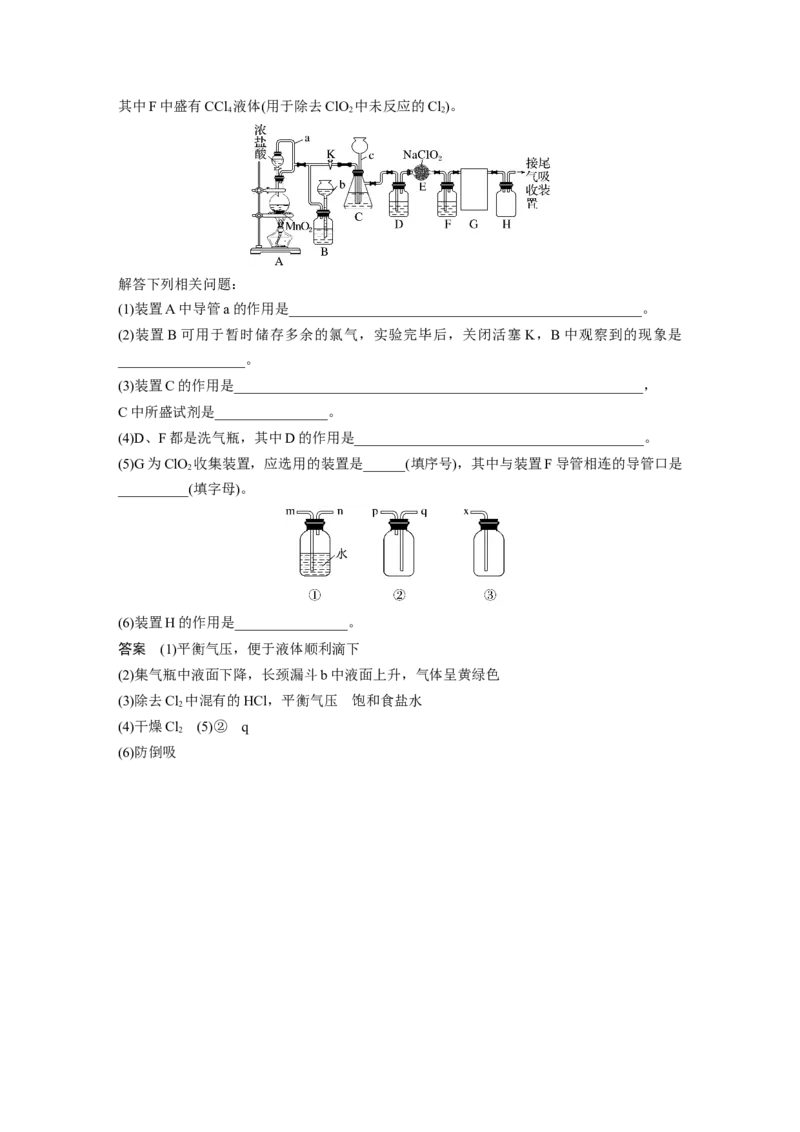
15.ClO 作为一种广谱型的消毒剂,将逐渐用来取代Cl 成为自来水的消毒剂。
2 2
已知ClO 是一种易溶于水而难溶于有机溶剂的气体,实验室制备 ClO 的原理是用亚氯酸钠
2 2
固体与氯气反应:2NaClO+Cl===2ClO +2NaCl。
2 2 2
下图是实验室用于制备和收集一定量较纯净的ClO 的装置(某些夹持装置和垫持用品省略)。
2其中F中盛有CCl 液体(用于除去ClO 中未反应的Cl)。
4 2 2
解答下列相关问题:
(1)装置A中导管a的作用是__________________________________________________。
(2)装置B可用于暂时储存多余的氯气,实验完毕后,关闭活塞K,B中观察到的现象是
__________________。
(3)装置C的作用是__________________________________________________________,
C中所盛试剂是________________。
(4)D、F都是洗气瓶,其中D的作用是_________________________________________。
(5)G为ClO 收集装置,应选用的装置是______(填序号),其中与装置F导管相连的导管口是
2
__________(填字母)。
(6)装置H的作用是________________。
答案 (1)平衡气压,便于液体顺利滴下
(2)集气瓶中液面下降,长颈漏斗b中液面上升,气体呈黄绿色
(3)除去Cl 中混有的HCl,平衡气压 饱和食盐水
2
(4)干燥Cl (5)② q
2
(6)防倒吸