文档内容
第 7 讲 物质的量浓度
[复习目标] 1.了解物质的量浓度的概念。2.掌握有关物质的量浓度的计算。3.掌握一定物质
的量浓度溶液配制的操作并能正确的进行误差分析。
考点一 物质的量浓度
1.物质的量浓度
(1)概念
物质的量浓度表示单位体积的溶液里所含溶质B的物质的量,也称为 B 的物质的量浓度 ,
符号为c 。
B
(2)表达式:c =,变形: n =c ·V;V=。
B B B
(3)常用单位: mol·L - 1 或mol/L。
(4)特点:对于某浓度的溶液,取出任意体积的溶液,其浓度、密度、质量分数均不变,但
所含溶质的质量、物质的量因体积不同而改变。
2.溶质的质量分数1.1 mol·L-1的NaCl溶液是指此溶液中含有1 mol Na+( )
2.从100 mL 5 mol·L-1 HSO 溶液中取出了10 mL,所得硫酸的物质的量浓度为0.5 mol·L-1
2 4
( )
3.将62 g Na O溶于水中,配成1 L溶液,所得溶质的物质的量浓度为1 mol·L-1( )
2
4.0.5 mol·L-1的稀硫酸中,c(H+)为1.0 mol·L-1( )
5.将25 g CuSO ·5H O晶体溶于75 g水中所得溶质的质量分数为25%( )
4 2
答案 1.× 2.× 3.× 4.√ 5.×
在进行有关物质的量浓度计算或判断时要注意:
(1)物质溶于水后溶质是否改变,如:
NaO、NaO――→NaOH,SO ――→HSO ,CuSO ·5H O――→CuSO 。
2 2 2 3 2 4 4 2 4
(2)是否是溶液的体积。
一、物质的量浓度与质量分数的计算
1.在标准状况下,将V L氨气溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此氨水的
物质的量浓度为______________ mol·L-1。
答案
解析 n(NH )= mol,
3
溶液体积为×10-3 L,
c= mol·L-1= mol·L-1。
2.将 25 g CuSO ·5H O 晶体溶于 75 g 水中,配成溶液,所得溶液的溶质质量分数为
4 2
________。
答案 16%
3.已知某饱和NaCl溶液的体积为V mL,密度为ρ g·cm-3,质量分数为w,物质的量浓度
为c mol·L-1,溶液中含NaCl的质量为m g。
(1)用m、V表示溶液的物质的量浓度:______________________________________。
(2)用w、ρ表示溶液的物质的量浓度:______________________________________。
(3)用c、ρ表示溶质的质量分数:___________________________________________。(4)用w表示该温度下NaCl的溶解度:______________________________________。
答案 (1) mol·L-1
(2) mol·L-1 (3)×100%
(4) g
解析 (1)c= mol·L-1= mol·L-1。
(2)c== mol·L-1。
(3)w=×100%=×100%。
(4)=,S= g。
二、溶液的稀释与混合
4.将 a mL 5 mol·L-1 NaCl 溶液稀释至 b mL,稀释后溶液中 Cl-的物质的量浓度为
________。
答案 mol·L-1
解析 将a mL 5 mol·L-1 NaCl溶液稀释至b mL,稀释后溶液中NaCl的物质的量不变,故
稀释后溶液中NaCl的物质的量浓度为= mol·L-1,则Cl-的物质的量浓度为 mol·L-1。
5.200 mL 0.3 mol·L-1 KSO 溶液和100 mL 0.2 mol·L-1 Fe (SO ) 溶液混合后不考虑混合后
2 4 2 4 3
溶液体积的变化,溶液中SO的物质的量浓度为________。
答案 0.4 mol·L-1
解析 200 mL 0.3 mol·L-1 KSO 溶液中SO的物质的量为0.2 L×0.3 mol·L-1=0.06 mol,100
2 4
mL 0.2 mol·L-1 Fe (SO ) 溶液中SO的物质的量为3×0.1 L×0.2 mol·L-1=0.06 mol,故混合
2 4 3
液中SO的物质的量为0.06 mol+0.06 mol=0.12 mol,由于混合后不考虑体积的变化,混合
后溶液的体积为0.3 L,混合液中SO的物质的量浓度为=0.4 mol·L-1。
6.下图是某学校实验室从市场买回的试剂标签上的部分内容。
硫酸 化学纯 CP 氨水 化学纯 CP
500 mL 500 mL
品名:硫酸 品名:氨水
化学式:HSO 化学式:NH
2 4 3
相对分子质量:98 相对分子质量:17
密度:1.84 g·cm-3 密度:0.88 g·cm-3
质量分数:98% 质量分数:25%
按要求回答下列问题:
(1)硫酸的物质的量浓度为________,氨水的物质的量浓度为________。
(2)各取5 mL与等质量的水混合后,c(H SO )______9.2 mol·L-1,c(NH )______6.45 mol·L-
2 4 3
1(填“>”“<”或“=”,下同)。
(3)各取5 mL与等体积的水混合后,w(H SO )______49%,w(NH )________12.5%。
2 4 3答案 (1)18.4 mol·L-1 12.9 mol·L-1
(2)< > (3)> <
解析 (1)利用c=计算,c(H SO )= mol·L-1=18.4 mol·L-1,c(NH )= mol·L-1≈12.9 mol·L
2 4 3
-1。
(2)硫酸的密度大于水,氨水的密度小于水,各取5 mL与等质量的水混合后,所得稀硫酸的
体积大于10 mL,稀氨水的体积小于10 mL,故有c(H SO )<9.2 mol·L-1,c(NH )>6.45 mol·L
2 4 3
-1。
(3)5 mL硫酸和5 mL氨水的质量分别为1.84 g·cm-3×5 mL=9.2 g、0.88 g·cm-3×5 mL=4.4
g,而5 mL水的质量约为5 g,故各取5 mL与等体积的水混合后,w(H SO )>49%,w(NH )
2 4 3
<12.5%。
(1)溶液体积和溶剂体积关系
①不能用水的体积代替溶液的体积,尤其是固体、气体溶于水,一般根据溶液的密度进行计
算:
V=。
②两溶液混合后的体积不是两种溶液的体积和。
(2)同溶质不同物质的量浓度溶液混合的计算
①混合后溶液体积保持不变时,cV+cV=c ·(V+V)。
1 1 2 2 混 1 2
②混合后溶液体积发生变化时,cV+cV=c V ,其中V =。
1 1 2 2 混 混 混
③两种稀溶液混合时,常近似看作密度都与水的密度相同。
考点二 一定物质的量浓度溶液的配制
1.容量瓶的构造及使用
(1)容量瓶上标有温度、规格和刻度线。常用规格有50 mL、100 mL、250 mL、500 mL、
1 000 mL等。
(2)容量瓶在使用前要检查是否漏水,其操作顺序为装水→盖塞→倒立→正立→玻璃塞旋转
180°→倒立。
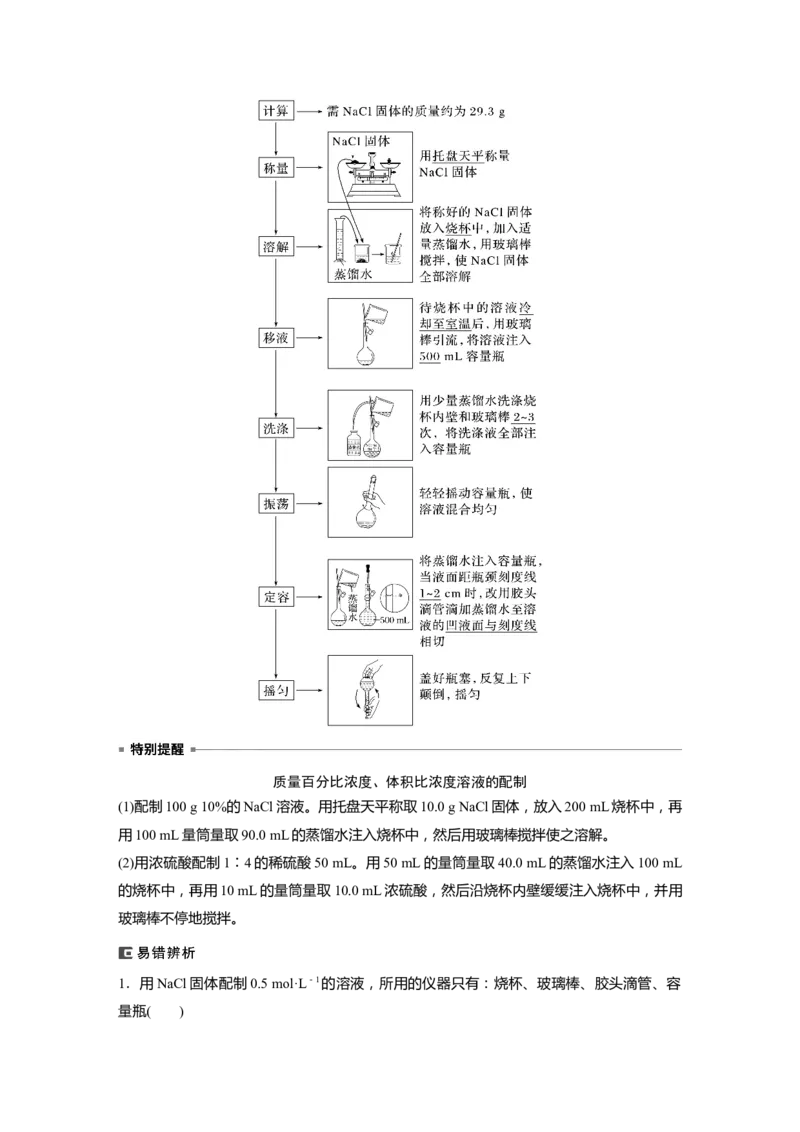
2.配制过程及操作
以配制500 mL 1.0 mol·L-1 NaCl溶液为例:质量百分比浓度、体积比浓度溶液的配制
(1)配制100 g 10%的NaCl溶液。用托盘天平称取10.0 g NaCl固体,放入200 mL烧杯中,再
用100 mL量筒量取90.0 mL的蒸馏水注入烧杯中,然后用玻璃棒搅拌使之溶解。
(2)用浓硫酸配制1∶4的稀硫酸50 mL。用50 mL的量筒量取40.0 mL的蒸馏水注入100 mL
的烧杯中,再用10 mL的量筒量取10.0 mL浓硫酸,然后沿烧杯内壁缓缓注入烧杯中,并用
玻璃棒不停地搅拌。
1.用NaCl固体配制0.5 mol·L-1的溶液,所用的仪器只有:烧杯、玻璃棒、胶头滴管、容
量瓶( )2.向容量瓶中转移液体时,引流用的玻璃棒可以接触容量瓶内壁( )
3.用量筒量取20 mL 0.500 0 mol·L-1 HSO 溶液于烧杯中,加水80 mL,配制成0.100 0 mol·L
2 4
-1 HSO 溶液( )
2 4
4.NaOH在烧杯里刚完全溶解时,立即将溶液转移到容量瓶( )
5.配制480 mL 1 mol·L-1的NaOH溶液,应用托盘天平称量 NaOH固体19.2 g,选用500
mL容量瓶( )
答案 1.× 2.√ 3.× 4.× 5.×
一、一定物质的量浓度溶液的配制
1.某同学在实验室配制500 mL 0.4 mol·L-1的NaCl溶液,他将配制过程按下列6步进行,
请你将他的配制过程补充完整。
(1)用托盘天平称取________g NaCl固体;
(2)将所称取的固体放入____________(填仪器名称)中,然后______________________;
(3)将上述溶液注入________(填仪器名称)中,用少量蒸馏水______________________;
(4)__________________,使溶液混合均匀;
(5)__________________,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切;
(6)盖好瓶塞,反复上下颠倒,摇匀。
答案 (1)11.7 (2)烧杯 加入适量蒸馏水,用玻璃棒搅拌,使NaCl固体全部溶解 (3)500
mL容量瓶 洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液注入容量瓶 (4)轻轻摇动容量瓶
(5)向容量瓶中注入蒸馏水至距刻度线1~2 cm处
2.某同学准备用98%的浓硫酸(ρ=1.84 g·cm-3)粗略配制1 mol·L-1的稀硫酸100 mL。实验
室提供下列备选仪器。
①玻璃棒 ②胶头滴管 ③100 mL容量瓶 ④托盘天平 ⑤50 mL烧杯 ⑥10 mL量筒
请你协助该同学,按配制溶液时仪器选用的先后顺序,将仪器进行排序。
答案 ⑥②⑤①③②
二、一定物质的量浓度溶液配制的误差分析
误差分析的思维流程
3.(1)从改变溶质的物质的量角度分析产生的误差(填“偏大”“偏小”或“无影响”)。
①配制450 mL 0.1 mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8 g:________。②配制500 mL 0.1 mol·L-1的硫酸铜溶液,用托盘天平称取胆矾8.0 g:________。
③配制NaOH溶液,用托盘天平称量NaOH时,托盘天平的两个托盘上放两张质量相等的
纸片,其他操作均正确:________。
④配制一定物质的量浓度的NaOH溶液,需称量溶质4.4 g,称量时物码放置颠倒:______。
⑤配制一定物质的量浓度的稀HSO 溶液时,用量筒量取浓硫酸时,仰视读数:________。
2 4
⑥定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线:________。
⑦配制一定物质的量浓度溶液时,烧杯及玻璃棒未洗涤:________。
答案 ①偏小 ②偏小 ③偏小 ④偏小 ⑤偏大 ⑥偏小 ⑦偏小
解析 ②所需胆矾的质量为0.5 L×0.1 mol·L-1×250 g·mol-1=12.5 g。③NaOH易吸水潮解。
④实际称量的NaOH固体质量为4 g-0.4 g=3.6 g。
(2)从改变溶液体积角度分析产生的误差(填“偏大”“偏小”或“无影响”)。
①配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容
量瓶中并定容:________。
②定容摇匀后,发现液面下降,继续加水至刻度线:________。
③定容时仰视刻度线:________。
④定容摇匀后少量溶液外流:________。
⑤容量瓶中原有少量蒸馏水:________。
答案 ①偏大 ②偏小 ③偏小 ④无影响 ⑤无影响
解析 ①NaOH溶于水放热,导致溶液的体积比室温时大,应恢复至室温后再移液、定容。
视线引起误差的分析方法
(1)仰视容量瓶刻度线[图(a)],导致溶液体积偏大,结果偏低。
(2)俯视容量瓶刻度线[图(b)],导致溶液体积偏小,结果偏高。
1.[2022·全国乙卷,27(1)]由 CuSO ·5H O 配制 CuSO 溶液,下列仪器中不需要的是
4 2 4
________________________________________(填仪器名称)。
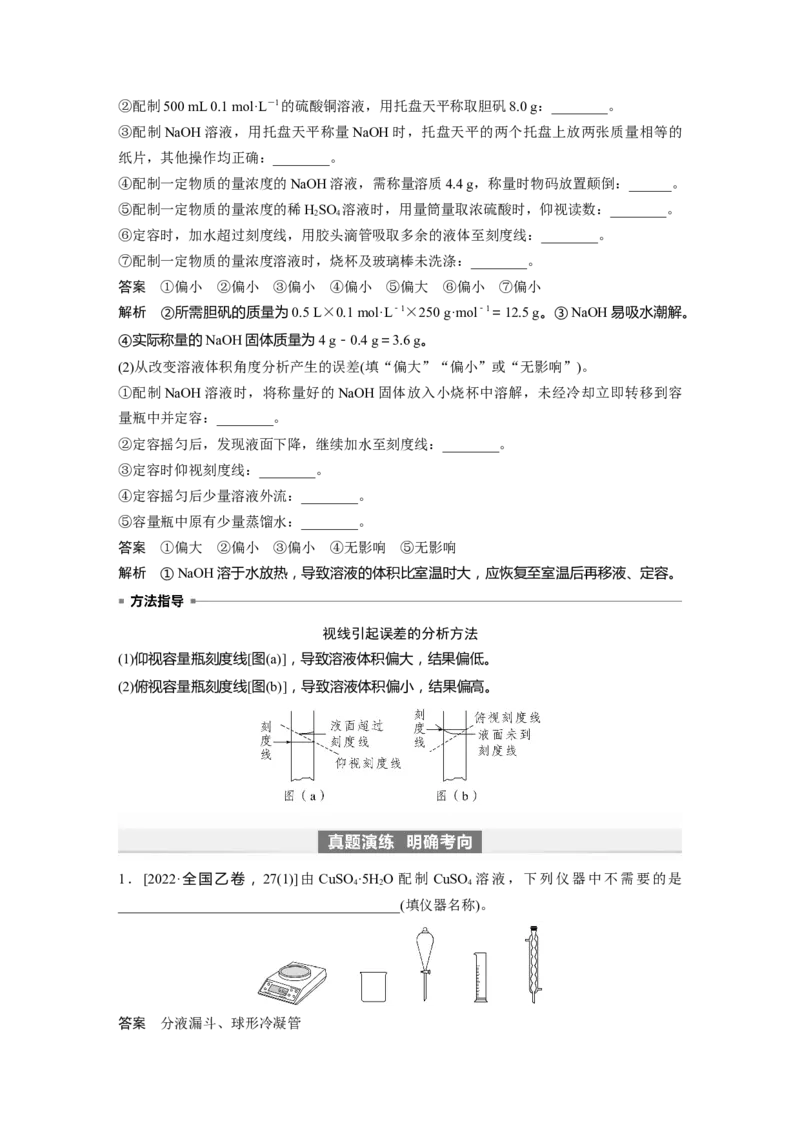
答案 分液漏斗、球形冷凝管2.[2020·全国卷Ⅰ,27(1)]由FeSO ·7H O固体配制0.10 mol·L-1 FeSO 溶液,需要的仪器有
4 2 4
药匙、玻璃棒、____________(从下列图中选择,写出名称)。
答案 烧杯、量筒、托盘天平
解析 根据用固体物质配制一定物质的量浓度溶液的方法可知,题图给出的仪器中还需要烧
杯、量筒和托盘天平。
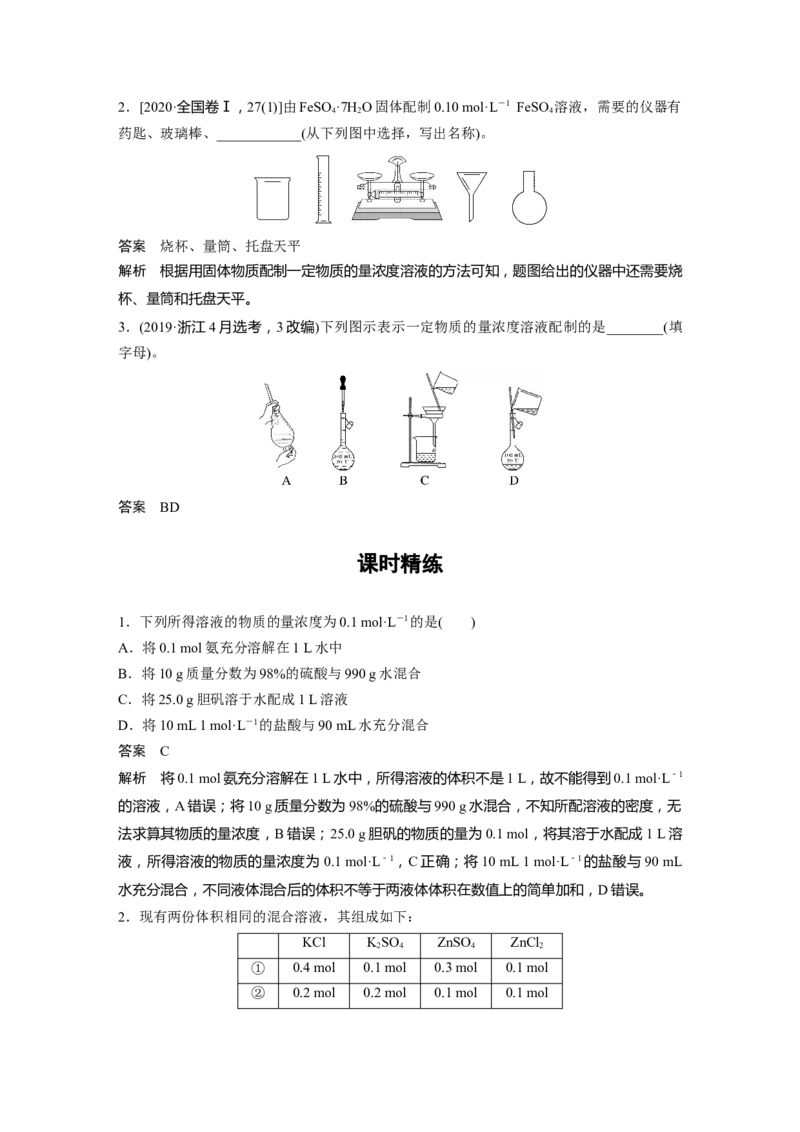
3.(2019·浙江4月选考,3改编)下列图示表示一定物质的量浓度溶液配制的是________(填
字母)。
答案 BD
课时精练
1.下列所得溶液的物质的量浓度为0.1 mol·L-1的是( )
A.将0.1 mol氨充分溶解在1 L水中
B.将10 g质量分数为98%的硫酸与990 g水混合
C.将25.0 g胆矾溶于水配成1 L溶液
D.将10 mL 1 mol·L-1的盐酸与90 mL水充分混合
答案 C
解析 将0.1 mol氨充分溶解在1 L水中,所得溶液的体积不是1 L,故不能得到0.1 mol·L-1
的溶液,A错误;将10 g质量分数为98%的硫酸与990 g水混合,不知所配溶液的密度,无
法求算其物质的量浓度,B错误;25.0 g胆矾的物质的量为0.1 mol,将其溶于水配成1 L溶
液,所得溶液的物质的量浓度为 0.1 mol·L-1,C正确;将10 mL 1 mol·L-1的盐酸与90 mL
水充分混合,不同液体混合后的体积不等于两液体体积在数值上的简单加和,D错误。
2.现有两份体积相同的混合溶液,其组成如下:
KCl KSO ZnSO ZnCl
2 4 4 2
① 0.4 mol 0.1 mol 0.3 mol 0.1 mol
② 0.2 mol 0.2 mol 0.1 mol 0.1 mol则两份溶液中各离子浓度( )
A.仅c(K+)相同 B.仅c(Cl-)相同
C.完全相同 D.完全不同
答案 A
解析 ①溶液中各离子的物质的量分别为K+:0.4 mol+2×0.1 mol=0.6 mol,Zn2+:0.3
mol+0.1 mol=0.4 mol,Cl-:0.4 mol+2×0.1 mol=0.6 mol,SO:0.1 mol+0.3 mol=0.4
mol;②溶液中各离子的物质的量分别为K+:0.2 mol+2×0.2 mol=0.6 mol,Zn2+:0.1 mol
+0.1 mol=0.2 mol,Cl-:0.2 mol+2×0.1 mol=0.4 mol,SO:0.2 mol+0.1 mol=0.3 mol,
所以只有c(K+)相同,A项正确。
3.在标准状况下,1体积水约溶解700体积氨气,所得溶液密度为0.9 g·cm-3,这种氨水的
物质的量浓度和溶质的质量分数分别为( )
A.18.4 mol·L-1 34.7%
B.20.4 mol·L-1 38.5%
C.18.4 mol·L-1 38.5%
D.20.4 mol·L-1 34.7%
答案 A
解析 设标准状况下,水是1 L,则溶质氨气是700 L,根据n=可知,溶质氨气的物质的量
n==31.25 mol,则根据m=nM可知,氨气的质量m=31.25 mol×17 g·mol-1=531.25 g,所
以溶质的质量分数w=×100%≈34.7%,又因为c=,所以溶液的物质的量浓度c= mol·L-
1≈18.4 mol·L-1。
4.取100 mL 0.3 mol·L-1和300 mL 0.25 mol·L-1的硫酸混合并稀释配成500 mL溶液,该混
合溶液中H+的物质的量浓度是( )
A.0.21 mol·L-1 B.0.42 mol·L-1
C.0.56 mol·L-1 D.0.26 mol·L-1
答案 B
解析 该混合溶液中H+的物质的量n(H+)=(0.1 L×0.3 mol·L-1+0.3 L×0.25 mol·L-1)×2=
0.21 mol,所以c(H+)==0.42 mol·L-1。
5.若20 g密度为d g·cm-3的硝酸钙溶液里含有1 g Ca2+,则NO的物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C.2.5d mol·L-1 D.1.25d mol·L-1
答案 C
解析 1 g钙离子的物质的量n==0.025 mol,该溶液中含有硝酸根离子的物质的量n=2n=
0.025 mol×2=0.05 mol,20 g该硝酸钙溶液的体积V=×10-3 L·mL-1= L,所以该溶液中
硝酸根离子的物质的量浓度c==2.5d mol·L-1,故选C。
6.(2022·天津滨海七校联考)将物质的量均为a mol的Na和Al一同投入m g足量水中,所得溶液的密度为ρ g·cm-3,则此溶液的物质的量浓度为( )
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
答案 A
解析 Na和Al一同投入m g足量水中时,发生反应的化学方程式为2Na+2HO===2NaOH
2
+H↑、2Al+2NaOH+2HO===2NaAlO +3H↑。由于Na、Al的物质的量均为a mol,结
2 2 2 2
合化学方程式可知共生成2a mol H ,所得溶液中只有NaAlO 一种溶质,其物质的量为a
2 2
mol。所得溶液的质量为m(Na)+m(Al)+m(H O)-m(H )=(46a+m) g,所得溶液的体积为
2 2
L,则该溶液的物质的量浓度为 mol·L-1。
7.下列说法正确的是( )
A.把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,硫酸的物质的量浓度为1.5 mol·L-1
2 4 2
B.把100 g 20%的NaCl溶液跟100 g HO混合后,NaCl溶液的溶质质量分数是10%
2
C.把200 mL 3 mol·L-1的BaCl 溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的c(Cl-)
2
仍然是3 mol·L-1
D.把100 mL 20%的NaOH溶液跟100 mL H O混合后,NaOH溶液的溶质质量分数是10%
2
答案 B
解析 把100 mL 3 mol·L-1的HSO 跟100 mL H O混合,溶液的总体积小于200 mL,硫酸
2 4 2
的物质的量浓度大于1.5 mol·L-1,A错误;与水混合前后,NaCl的质量不变,则把100 g
20%的NaCl溶液跟100 g H O混合后,NaCl溶液的溶质质量分数为×100%=10%,B正确;
2
3 mol·L-1的BaCl 溶液中氯离子浓度为6 mol·L-1,3 mol·L-1的KCl溶液中氯离子浓度为3
2
mol·L-1,混合后氯离子浓度在3~6 mol·L-1之间,C错误;氢氧化钠溶液的密度与水的密
度不相同,不知道氢氧化钠溶液的密度,无法计算混合后溶液的总质量,D错误。
8.若以w 和w 分别表示浓度为c mol·L-1和c mol·L-1的氨水的质量分数,且知2c =
1 2 1 2 1
c,则下列推断正确的是( )
2
A.2w=w B.2w=w
1 2 2 1
C.w>2w D.w<w<2w
2 1 1 2 1
答案 C
解析 根据c=得c =,c =,则===,=,根据氨水物质的量浓度越大,其密度越小,
1 2
由2c=c 得到ρ>ρ,则w>2w,故C正确。
1 2 1 2 2 1
9.配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒、②250 mL容量瓶、③
托盘天平和砝码、④500 mL容量瓶、⑤烧杯、⑥玻璃棒、⑦漏斗、⑧药匙、⑨胶头滴管
⑩250 mL烧瓶,需要用到的仪器按使用先后顺序排列正确的是( )
A.⑧③⑤⑥②⑨ B.②③⑦⑤⑥
C.②⑤⑦⑥① D.④③⑦⑤⑥
答案 A解析 一定规格的容量瓶只能配制相应体积的溶液,故应选择250 mL容量瓶;用药匙取用
固体药品,用托盘天平称量一定质量的药品(药品可放在烧杯中称量)后,在烧杯中溶解(可用
量筒量取水),并用玻璃棒搅拌,待溶液冷却至室温后转移到250 mL容量瓶中,转移过程中
需用玻璃棒引流,用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液转移到容量瓶中,
当加水至液面距离刻度线1~2 cm时,改用胶头滴管滴加至溶液凹液面恰好与刻度线相切,
盖好瓶塞,摇匀。所以需要用到的仪器及先后顺序为药匙、托盘天平和砝码、烧杯、量筒
(也可不用)、玻璃棒、250 mL容量瓶、胶头滴管,即⑧③⑤(①)⑥②⑨,A项符合。
10.实验室里需要配制480 mL 0.10 mol·L-1的硫酸铜溶液,下列实验用品及实验操作正确
的是( )
选项 容量瓶容积 溶质质量 实验操作
A 480 mL 硫酸铜:7.68 g 加入500 mL水
B 480 mL 胆矾:12.0 g 配成500 mL溶液
C 500 mL 硫酸铜:8.0 g 加入500 mL水
D 500 mL 胆矾:12.5 g 配成500 mL溶液
答案 D
解析 实验室里需要配制480 mL 0.10 mol·L-1 CuSO 溶液,由于没有480 mL规格的容量瓶,
4
根据“大而近”的原则需选择500 mL 容量瓶,溶质若为CuSO ,则需要8.0 g,若是胆矾则
4
需要12.5 g,应配成500 mL溶液而不是加入500 mL水。
11.室温时,甲、乙两同学配制氯化钠溶液。甲同学配制10%的NaCl溶液100 g,乙同学配
制1.0 mol·L-1的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36.0 g)。下列说法正确的是
( )
A.两同学所需溶质的质量相同
B.两同学所配溶液的质量相同
C.两同学所需实验仪器种类相同
D.甲同学所配的溶液浓度比乙同学的大
答案 D
解析 配制100 g 10%的NaCl溶液需要氯化钠的质量为 100 g×10%=10 g,配制100 mL 1.0
mol·L-1的NaCl溶液需要氯化钠的质量为0.1 L×1.0 mol·L-1×58.5 g·mol-1=5.85 g,二者需
要氯化钠的质量不相等,A错误;氯化钠溶液的密度大于1 g·mL-1,100 mL氯化钠溶液的
质量大于100 g,B错误;配制一定质量分数的氯化钠溶液,所需仪器有托盘天平、量筒、
烧杯、玻璃棒、药匙等;配制100 mL一定物质的量浓度的氯化钠溶液,需要的仪器有托盘
天平、烧杯、玻璃棒、药匙、100 mL容量瓶、胶头滴管等,需要的仪器不同,C错误;配
制10%的NaCl溶液100 g,其密度大于1 g·mL-1,所以100 g溶液的体积小于100 mL,10%
的NaCl溶液中氯化钠的物质的量为≈0.17 mol,其物质的量浓度大于1.7 mol·L-1,D正确。12.配制100 mL 1.00 mol·L-1 NaOH溶液的操作如下所示。下列说法不正确的是( )
A.操作1前称取NaOH的质量为4.0 g
B.操作2前NaOH溶液需恢复至室温
C.操作4若俯视刻度线定容,结果偏大
D.操作5后液面下降,需补充少量水至刻度线
答案 D
解析 操作1前称取NaOH的质量m(NaOH)=0.1 L×1.00 mol·L-1×40 g·mol-1=4.0 g,故A
正确;转移溶液之前应将溶液冷却至室温即操作2前NaOH溶液需恢复至室温,故B正确;
操作4若俯视刻度线定容,溶液体积偏小,物质的量浓度偏大,故 C正确;操作5后液面下
降,液体可能在容量瓶和瓶塞之间,不能补充水,故D错误。
13.现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液0.2 L,部分离子的浓度如下表所示:
离子种类 NH Mg2+ NO
物质的量浓度/(mol·L-1) 0.2 0.1 0.6
(1)混合液中,硝酸铵的物质的量为________,硝酸钾的质量为________________。
(2)该混合溶液中硝酸镁的物质的量浓度为__________________________________,
将该混合溶液加水稀释至体积为1 L,稀释后溶液中NO的物质的量浓度为_________。
(3)向该稀释后的溶液中通入标准状况下的NH ________L可使Mg2+沉淀完全,写出Mg2+沉
3
淀过程中的离子方程式:_______________________________________________。
答案 (1)0.04 mol 4.04 g
(2)0.1 mol·L-1 0.12 mol·L-1
(3)0.896 Mg2++2NH +2HO===Mg(OH) ↓+2NH
3 2 2
14.绿矾(FeSO ·7H O)在化学合成上用作还原剂及催化剂。工业上常用废铁屑溶于一定浓度
4 2
的硫酸溶液制备绿矾。
(1)98% 1.84 g·cm-3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4 g·cm-
3,50%的硫酸物质的量浓度为________(结果保留两位小数),50%的硫酸与30%的硫酸等体
积混合,混合酸的质量分数________(填“>”“<”或“=”)40%。
(2)将111.2 g绿矾(FeSO ·7H O,式量为278)在高温下加热,充分反应后生成Fe O 固体和
4 2 2 3
SO 、 SO 、 水 的 混 合 气 体 , 则 生 成 Fe O 的 质 量 为
2 3 2 3
____________________________________g;
SO 为________mol。
2
实验室可用以下方法制备莫尔盐晶体[(NH )SO ·FeSO ·6H O,式量为392]。
4 2 4 4 2(3)将4.88 g铁屑(含Fe O)与25 mL 3 mol·L-1 HSO 充分反应后,得到FeSO 和HSO 的混
2 3 2 4 4 2 4
合溶液,稀释溶液至100 mL,测得其pH=1。铁屑中Fe O 的质量分数是________(结果保
2 3
留两位小数)。
(4)向上述100 mL溶液中加入与该溶液中FeSO 等物质的量的(NH )SO 晶体,待晶体完全溶
4 4 2 4
解后蒸发掉部分水,冷却至t ℃,析出莫尔盐晶体12.360 g,剩余溶液的质量为82.560 g。t
℃时,计算(NH )SO ·FeSO ·6H O的溶解度为________(结果保留两位小数)。
4 2 4 4 2
答案 (1)7.14 mol·L-1 > (2)32 0.2 (3)65.57% (4)22.35 g
解析 (1)密度为1.4 g·cm-3、质量分数为50%的硫酸物质的量浓度c== mol·L-1≈7.14
mol·L-1;假如50%的硫酸与30%的硫酸密度相同,则混合后硫酸的质量分数为40%,由于
50%的硫酸的密度大于30%的硫酸的密度,所以等体积混合后溶液中硫酸的质量偏大,硫酸
的质量分数大于40%。(2)n(FeSO ·7H O)==0.4 mol,由2FeSO ·7H O=====Fe O +SO ↑+
4 2 4 2 2 3 2
SO ↑+14HO↑可知,生成Fe O 的质量为0.4 mol××160 g·mol-1=32 g,SO 的物质的量
3 2 2 3 2
为0.4 mol×=0.2 mol。(3)根据题意知,溶液中剩余酸的物质的量 n(H SO )=0.1 mol·L-
2 4
1××0.1 L=0.005 mol,则参加反应的n(H SO )=0.025 L×
2 4
3 mol·L-1-0.005 mol=0.07 mol;设铁的物质的量是m mol,氧化铁的物质的量是n mol,
发生反应的化学方程式为 Fe+Fe O +3HSO ===3FeSO +3HO、Fe+HSO ===FeSO +
2 3 2 4 4 2 2 4 4
H↑,则根据固体的质量和硫酸的物质的量可知,56m+160n=4.88,m-n+3n=0.07,解
2
得n=0.02,m=0.03,所以铁屑中Fe O 的质量分数是×100%≈65.57%。(4)根据以上分析
2 3
结合原子守恒知,n(FeSO )=n(Fe)+2n(Fe O)=(0.03+0.04) mol=0.07 mol,根据莫尔盐的
4 2 3
化学式知,n[(NH )SO ·FeSO ·6H O]=n(FeSO )=0.07 mol,溶液中莫尔盐的质量为 0.07
4 2 4 4 2 4
mol×392 g·mol-1-12.360 g=15.08 g,设莫尔盐的溶解度为x,则=,解得x≈22.35 g。
15.人体血液里Ca2+的浓度一般采用m g·cm-3来表示。抽取一定体积的血样,加适量的草
酸铵[(NH )C O]溶液,可析出草酸钙(CaC O)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得
4 2 2 4 2 4
草酸(H C O),再用酸性KMnO 溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习
2 2 4 4
小组设计如下实验步骤测定血液样品中Ca2+的浓度。
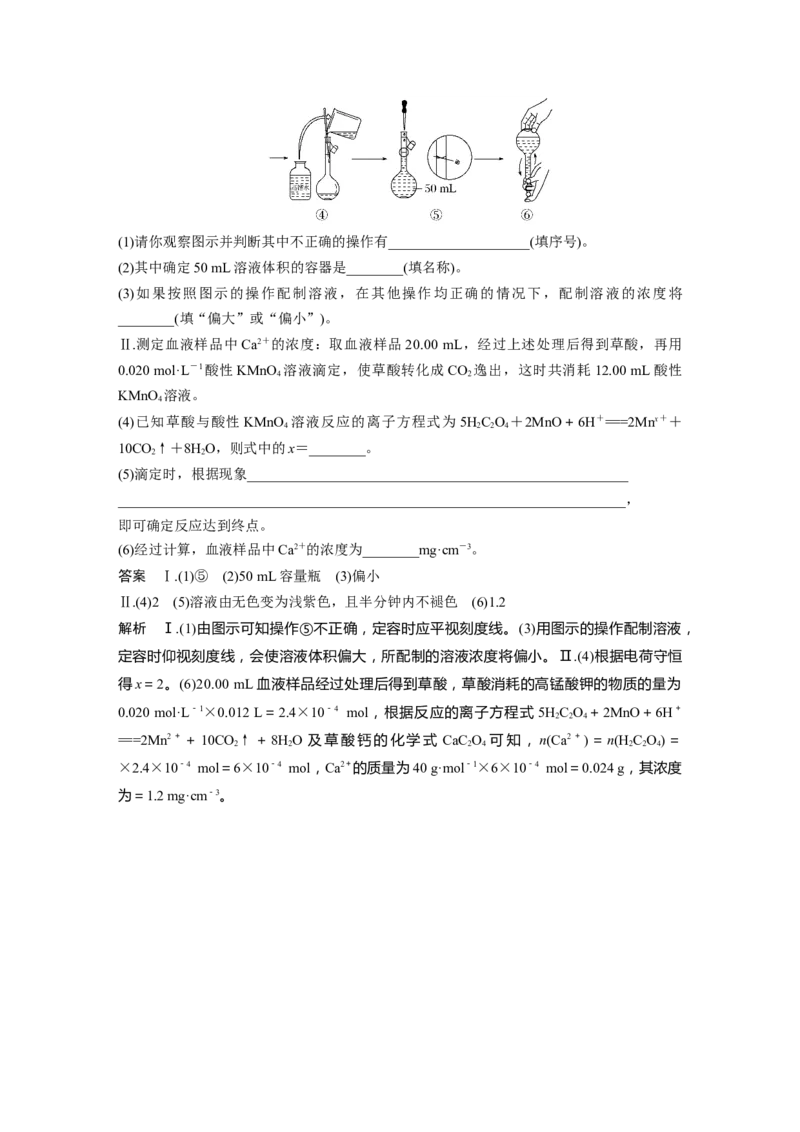
Ⅰ.配制酸性KMnO 标准溶液:如图是配制50 mL酸性KMnO 标准溶液的过程示意图。
4 4(1)请你观察图示并判断其中不正确的操作有____________________(填序号)。
(2)其中确定50 mL溶液体积的容器是________(填名称)。
(3)如果按照图示的操作配制溶液,在其他操作均正确的情况下,配制溶液的浓度将
________(填“偏大”或“偏小”)。
Ⅱ.测定血液样品中Ca2+的浓度:取血液样品20.00 mL,经过上述处理后得到草酸,再用
0.020 mol·L-1酸性KMnO 溶液滴定,使草酸转化成CO 逸出,这时共消耗12.00 mL酸性
4 2
KMnO 溶液。
4
(4)已知草酸与酸性KMnO 溶液反应的离子方程式为5HC O +2MnO+6H+===2Mnx++
4 2 2 4
10CO↑+8HO,则式中的x=________。
2 2
(5)滴定时,根据现象______________________________________________________
________________________________________________________________________,
即可确定反应达到终点。
(6)经过计算,血液样品中Ca2+的浓度为________mg·cm-3。
答案 Ⅰ.(1)⑤ (2)50 mL容量瓶 (3)偏小
Ⅱ.(4)2 (5)溶液由无色变为浅紫色,且半分钟内不褪色 (6)1.2
解析 Ⅰ.(1)由图示可知操作⑤不正确,定容时应平视刻度线。(3)用图示的操作配制溶液,
定容时仰视刻度线,会使溶液体积偏大,所配制的溶液浓度将偏小。Ⅱ.(4)根据电荷守恒
得x=2。(6)20.00 mL血液样品经过处理后得到草酸,草酸消耗的高锰酸钾的物质的量为
0.020 mol·L-1×0.012 L=2.4×10-4 mol,根据反应的离子方程式 5HC O +2MnO+6H+
2 2 4
===2Mn2++10CO↑+8HO 及草酸钙的化学式 CaC O 可知,n(Ca2+)=n(H C O)=
2 2 2 4 2 2 4
×2.4×10-4 mol=6×10-4 mol,Ca2+的质量为40 g·mol-1×6×10-4 mol=0.024 g,其浓度
为=1.2 mg·cm-3。