文档内容
第 52 讲 水的电离和溶液的 pH
[复习目标] 1.了解水的电离、离子积常数(K )。2.了解溶液pH的含义及其测定方法,能进
w
行pH的简单计算。
考点一 水的电离与水的离子积常数
1.水的电离和水的离子积常数
2.填写外界条件对水的电离平衡的具体影响
改变条件 平衡移动方向 K 水的电离程度 c(OH-) c(H+)
w
HCl 逆 不变 减小 减小 增大
NaOH 逆 不变 减小 增大 减小
NaCO 正 不变 增大 增大 减小
2 3
NaHSO 逆 不变 减小 减小 增大
4
加热 正 增大 增大 增大 增大
3.计算 (H+)或 (OH-)
(1)室温下,0.01 mol·L-1的盐酸中, (H+)=______________________________。
(2)室温下,pH=4的亚硫酸溶液中, (H+)=_____________________________。
(3)室温下,pH=10的KOH溶液中, (OH-)=___________________________。
(4)室温下,pH=4的NH Cl溶液中, (H+)=_____________________________。
4
(5)室温下,pH=10的CHCOONa溶液中, (OH-)=____________。
3
答案 (1)1×10-12 mol·L-1(2)1×10-10 mol·L-1
(3)1×10-10 mol·L-1 (4)1×10-4 mol·L-1
(5)1×10-4 mol·L-1
溶液中 (H+)或 (OH-)的计算及应用(以室温为例)
(1)酸、碱抑制水的电离,酸溶液中求c(OH-),即 (H+)= (OH-)=c(OH-),碱溶液
中求c(H+),即 (OH-)= (H+)=c(H+)。
(2)水解的盐促进水的电离,故 (H+)等于显性离子的浓度。
(3)酸式盐溶液
酸式酸根以电离为主: (H+)= (OH-)=c(OH-)。
酸式酸根以水解为主: (H+)= (OH-)=c(OH-)。
1.任何水溶液中均存在H+和OH-,且水电离出的c(H+)和c(OH-)相等( )
2. 将水加热,K 和c(H+) 均增大( )
w
3.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同( )
3 4
4.温度一定时,在纯水中通入少量SO ,水的电离平衡不移动,K 不变( )
2 w
答案 1.√ 2.√ 3.× 4.×
1.某温度下,向c(H+)=1.0×10-6 mol·L-1的蒸馏水中加入NaHSO 晶体,保持温度不变,
4
测得溶液的c(H+)=1.0×10-2 mol·L-1。下列对该溶液的叙述不正确的是( )
A.该温度高于25 ℃
B.由水电离出来的H+的浓度为1.0×10-10 mol·L-1
C.加入NaHSO 晶体抑制水的电离
4
D.取该溶液加水稀释100倍,溶液中的c(OH-)减小
答案 D
解析 该温度下蒸馏水中的c(H+)大于25 ℃时纯水中的c(H+),水的电离为吸热过程,A项
正确;此温度下K =1.0×10-12,故该NaHSO 溶液中c(OH-)= mol·L-1=1.0× 10-10
w 4
mol·L-1,由水电离出的c(H+)与溶液中的c(OH-)相等,B项正确;NaHSO 电离出的H+抑制
4
了水的电离,C项正确;加水稀释时,溶液中c(H+)减小,而K 不变,故c(OH-)增大,D项
w
错误。
2.常温时,纯水中由水电离出的c(H+)=a mol·L-1,pH=1的盐酸中由水电离出的c(H+)=b mol·L-1,0.1 mol·L-1的盐酸与0.1 mol·L-1的氨水等体积混合后,由水电离出的c(H+)=
c mol·L-1,则a、b、c的关系正确的是( )
A.a>b=c B.c>a>b
C.c>b>a D.b>c>a
答案 B
解析 盐酸抑制水的电离,所以ba,故B正确。
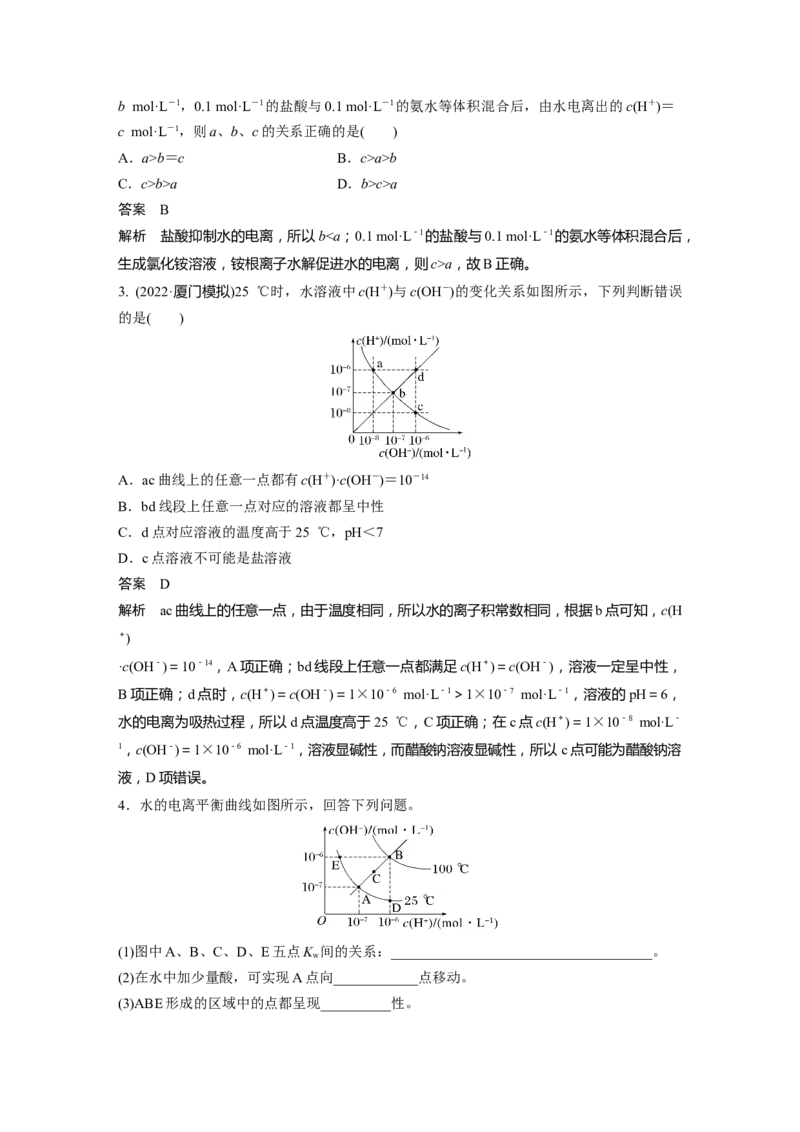
3. (2022·厦门模拟)25 ℃时,水溶液中c(H+)与c(OH-)的变化关系如图所示,下列判断错误
的是( )
A.ac曲线上的任意一点都有c(H+)·c(OH-)=10-14
B.bd线段上任意一点对应的溶液都呈中性
C.d点对应溶液的温度高于25 ℃,pH<7
D.c点溶液不可能是盐溶液
答案 D
解析 ac曲线上的任意一点,由于温度相同,所以水的离子积常数相同,根据b点可知,c(H
+)
·c(OH-)=10-14,A项正确;bd线段上任意一点都满足c(H+)=c(OH-),溶液一定呈中性,
B项正确;d点时,c(H+)=c(OH-)=1×10-6 mol·L-1>1×10-7 mol·L-1,溶液的pH=6,
水的电离为吸热过程,所以d点温度高于25 ℃,C项正确;在c点c(H+)=1×10-8 mol·L-
1,c(OH-)=1×10-6 mol·L-1,溶液显碱性,而醋酸钠溶液显碱性,所以c点可能为醋酸钠溶
液,D项错误。
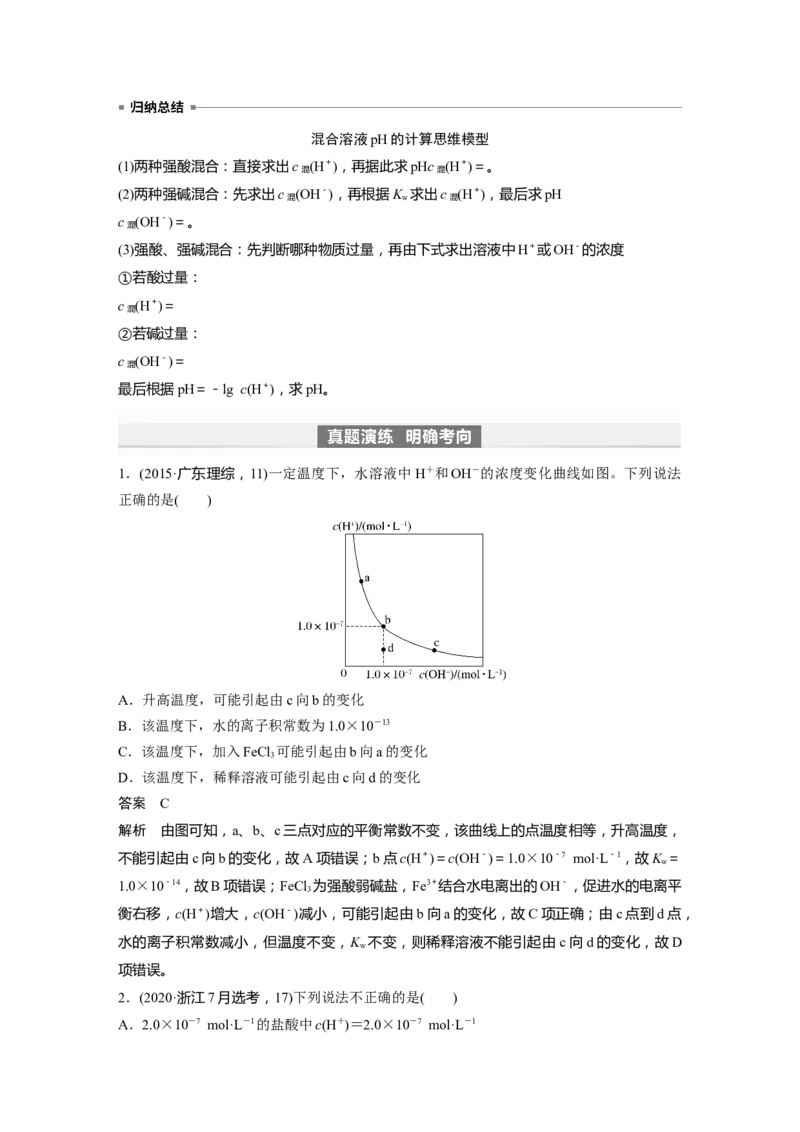
4.水的电离平衡曲线如图所示,回答下列问题。
(1)图中A、B、C、D、E五点K 间的关系:_____________________________________。
w
(2)在水中加少量酸,可实现A点向____________点移动。
(3)ABE形成的区域中的点都呈现__________性。(4)若在B点温度下,pH=2的硫酸溶液中, (H+)=________ mol·L-1。
答案 (1)B>C>A=D=E (2)D (3)碱
(4)1×10-10
正确理解水的电离平衡曲线
(1)曲线上的任意点的K 都相同,即c(H+)·c(OH-)相同,温度相同。
w
(2)曲线外的任意点与曲线上任意点的K 不同,温度不同。
w
(3)实现曲线上点之间的转化需保持温度相同,改变酸碱性;实现曲线上点与曲线外点之间
的转化一定改变温度。
考点二 溶液的酸碱性与 pH
1.溶液的酸碱性
溶液呈酸碱性的本质:溶液的酸碱性取决于c(H+)和c(OH-)的相对大小
溶液的酸碱性 c(H+)与c(OH-)比较 常温下溶液pH
酸性溶液 c(H+)>c(OH-) <7
中性溶液 c(H+)=c(OH-) =7
碱性溶液 c(H+)<c(OH-) >7
2.溶液的pH及测定方法
(1)关系:pH= - lg c (H + )。
(2)范围:0~14。
(3)测定方法:用镊子夹取一小块试纸放在洁净的玻璃片或表面皿上,用玻璃棒蘸取待测液
点在试纸的中央,变色后与标准比色卡对照。
(4)溶液酸碱性的另外一种表示——pOH
①pOH= - lg c (OH - );
②常温下:pH+pOH=14。
1.任何温度下,利用H+和OH-浓度的相对大小均可判断溶液的酸碱性( )
2.pH<7的溶液一定显酸性( )
3.c(H+)=的溶液一定显中性( )
4.常温下能使甲基橙显黄色的溶液一定显碱性( )5.用pH试纸测得某氯水的pH为5( )
6.用湿润的pH试纸测定盐酸和醋酸溶液的pH,醋酸溶液的误差更大( )
答案 1.√ 2.× 3.√ 4.× 5.× 6.×
一、酸碱溶液混合后酸碱性的判断
1.常温下,两种溶液混合后酸碱性的判断(在括号中填“酸性”“碱性”或“中性”)。
(1)相同浓度的HCl和NaOH溶液等体积混合( )
(2)相同浓度的CHCOOH和NaOH溶液等体积混合( )
3
(3)相同浓度的NH ·H O和HCl溶液等体积混合( )
3 2
(4)pH=2的HSO 和pH=12的NaOH溶液等体积混合( )
2 4
(5)pH=3的HCl和pH=10的NaOH溶液等体积混合( )
(6)pH=3的HCl和pH=12的NaOH溶液等体积混合( )
(7)pH=2的CHCOOH和pH=12的NaOH溶液等体积混合( )
3
(8)pH=2的HSO 和pH=12的NH ·H O等体积混合( )
2 4 3 2
答案 (1)中性 (2)碱性 (3)酸性 (4)中性 (5)酸性 (6)碱性 (7)酸性 (8)碱性
酸碱溶液混合后酸碱性的判断规律
(1)等浓度等体积的一元酸与一元碱混合的溶液——“谁强显谁性,同强显中性”。
(2)室温下c (H+)=c (OH-),即pH之和等于14时,一强一弱等体积混合——“谁弱谁过
酸 碱
量,谁弱显谁性”。
(3)已知强酸和强碱的pH,等体积混合(25 ℃时):
①pH之和等于14,呈中性;
②pH之和小于14,呈酸性;
③pH之和大于14,呈碱性。
二、溶液pH的计算
2.常温下,下列关于溶液稀释的说法正确的是( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.pH=4的HSO 溶液加水稀释100倍,溶液中由水电离产生的c(H+)=1×10-6 mol·L-1
2 4
C.将1 L 0.1 mol·L-1的Ba(OH) 溶液稀释为2 L,pH=13
2
D.pH=8的NaOH溶液稀释100倍,其pH=6
答案 C
解析 A 项,pH=3 的醋酸溶液在稀释过程中电离平衡正向移动,稀释 100 倍时,
3c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
答案 C
解析 根据HNO 和CHCOOH的电离常数,可知酸性:HNO>CH COOH,相同pH的两种
2 3 2 3
酸溶液,稀释相同倍数时,弱酸的pH变化较小,故曲线Ⅰ代表CHCOOH溶液,A项错误;
3
两种酸溶液中水的电离受到抑制,b点溶液pH小于c点溶液pH,则b点对应酸电离出的c(H
+)大,对水的电离抑制程度大,故水的电离程度:b点c(HNO),故
a 3 2
n(CHCOOH)>n(HNO),因此与NaOH恰好中和后,溶液中n(Na+)不同,D项错误。
3 2
课时精练
1.(2022·陕西咸阳模拟)水是生命之源,也是生活中最常见的溶剂。下列有关水的说法正确
的是( )
A.水是弱电解质,其电离方程式为2HO===HO++OH-
2 3
B.水分子之间存在氢键,因此水比HS更稳定
2C.常温下,由水电离出c(H+)=1×10-12 mol·L-1的溶液可能呈碱性
D.水和金属单质或非金属单质反应时一定是水中的氢元素被还原生成氢气
答案 C
解析 水是弱电解质,不完全电离,电离方程式为2HOHO++OH-,A错误;水比HS
2 3 2
稳定是因为O—H的键能大,与氢键无关,氢键影响的是物理性质,B错误;水与氯气反应
时,水既不被还原也不被氧化,D错误。
2.(2022·山西省应县一中模拟)25 ℃时,有关水的电离,下列叙述正确的是( )
A.向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
w
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.将水加热,K 增大,c(H+)不变
w
答案 B
解析 向水中加入稀氨水,由于氨水的电离,增大了水中的 c(OH-),使水的电离平衡逆向
移动,c(OH-)增大,A错误;向水中加入少量固体硫酸氢钠,c(H+)增大,但由于溶液的温
度不变,所以K 不变,B正确;向水中加入少量固体CHCOONa,由于CHCOO-与水电离
w 3 3
出的H+结合,导致水的电离平衡正向移动,c(H+)降低,C错误;将水加热,K 增大,c(H
w
+)增大,D错误。
3.25 ℃时,在等体积的①pH=0的HSO 溶液、②0.05 mol·L-1的Ba(OH) 溶液、③pH=
2 4 2
10的NaS溶液、④pH=5的NH NO 溶液中,发生电离的水的物质的量之比是( )
2 4 3
A.1∶10∶1010∶109
B.1∶5∶(5×109)∶(5×108)
C.1∶20∶1010∶109
D.1∶10∶104∶109
答案 A
解析 HSO 与Ba(OH) 抑制水的电离,NaS与NH NO 促进水的电离。25 ℃时,pH=0的
2 4 2 2 4 3
HSO 溶液中:c (H O)=c(OH-)= mol·L-1=10-14 mol·L-1;同理可计算其余溶液中水电
2 4 电离 2
离的浓度依次为②为10-13 mol·L-1,③为10-4 mol·L-1,④为10-5 mol·L-1,同温同体积
时,物质的量之比等于浓度之比,则物质的量之比为 10-14∶10-13∶10-4∶10-5=
1∶10∶1010∶109,故A正确。
4.常温下,下列叙述不正确的是( )
A.c(H+)>c(OH-)的溶液一定显酸性
B.pH=3的弱酸溶液与pH=11的强碱溶液等体积混合后溶液呈酸性
C.pH=5的硫酸溶液稀释到原来的500倍,稀释后c(SO)与c(H+)之比约为1∶10
D.中和10 mL 0.1 mol·L-1醋酸溶液与100 mL 0.01 mol·L-1醋酸溶液所需NaOH的物质的量
不同答案 D
解析 pH=3的弱酸溶液与pH=11的强碱溶液等体积混合,弱酸浓度大,有剩余,反应后
溶液呈酸性,B正确;pH=5的硫酸溶液稀释到原来的500倍,则溶液接近于中性,c(H+)
约为10-7 mol·L-1,c(SO)==10-8 mol·L-1,则c(SO)∶c(H+)=1∶10,C正确;两份醋酸
的物质的量相同,则所需NaOH的物质的量相同,D错误。
5.已知液氨的性质与水相似。T ℃时,NH +NH NH+NH,NH的平衡浓度为1×
3 3
10-15 mol·L-1,则下列说法正确的是( )
A.在此温度下液氨的离子积为1×10-17
B.在液氨中放入金属钠,可生成NaNH
2
C.恒温下,在液氨中加入NH Cl,可使液氨的离子积减小
4
D.降温,可使液氨电离平衡逆向移动,且c(NH)<c(NH)
答案 B
解析 由电离方程式知,NH与NH的离子平衡浓度相等,都为1×10-15 mol·L-1,根据水
的离子积得液氨的离子积K=c(NH)·c(NH)=1×10-30,A项错误;离子积只与温度有关,与
离子浓度无关,C项错误;因为电离吸热,所以降温平衡逆向移动,c(NH)、c(NH)都减小但
相等,D项错误。
6.下列事实中,能说明MOH是弱碱的是( )
A.0.1 mol·L-1 MOH溶液可以使酚酞溶液变红
B.常温下,0.1 mol·L-1 MOH溶液中c(OH-)<0.1 mol·L-1
C.MOH溶液的导电能力比NaOH溶液弱
D.等体积的0.1 mol·L-1 MOH溶液与0.1 mol·L-1盐酸恰好完全反应
答案 B
解析 0.1 mol·L-1 MOH溶液可以使酚酞溶液变红,说明MOH能电离出氢氧根离子,但不
能说明MOH是弱电解质,A错误;常温下,0.1 mol·L-1 MOH溶液中,c(OH-)<0.1 mol·L-
1,说明MOH没有完全电离,则MOH为弱碱,B正确;等体积的0.1 mol·L-1 MOH溶液与
0.1 mol·L-1盐酸混合,无论MOH是强碱还是弱碱,都恰好完全反应,D错误。
7.下列叙述正确的是( )
A.95 ℃纯水的pH<7,说明加热可导致水呈酸性
B.室温下,pH=3的醋酸溶液,稀释10倍后pH=4
C.室温下,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
D.0.2 mol·L-1的盐酸与等体积水混合后pH=1
答案 D
解析 A项错误,水的电离吸热,加热促进电离,c(H+)>10-7 mol·L-1,但仍呈中性;B项
错误,稀释促进醋酸的电离,pH=3的醋酸溶液,稀释10倍后3<pH<4;C项错误,pH=
3的醋酸溶液中醋酸的浓度远大于10-3 mol·L-1,而pH=11的氢氧化钠溶液中氢氧化钠的浓度为10-3 mol·L-1,所以二者等体积混合后醋酸过量,溶液显酸性;D项正确,溶液体积
扩大一倍,溶液中氢离子浓度变为0.1 mol·L-1。
8.已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA与b
w
mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
答案 C
解析 判断溶液呈中性的依据是c(H+)=c(OH-)。A项中,a=b,酸碱恰好完全反应生成正
盐和水,由于酸碱强弱未知,不能确定溶液的酸碱性;B项中未说明温度为25 ℃,故混合
溶液的pH=7时不一定呈中性;C项混合溶液中,c(H+)·c(OH-)=K ,因为c(H+)= mol·
w
L-1,则c(OH-)= mol·L-1,c(H+)=c(OH-),故溶液呈中性;D项中c(H+)+c(B+)=c(OH
-)+c(A-),只能说明溶液中电荷守恒,无法判断溶液的酸碱性。
9.25 ℃时,体积为V、pH=a的某一元强酸溶液与体积为V、pH=b的某一元强碱溶液均
a b
匀混合后,溶液的pH=7,已知b=6a,V<V,下列有关a的说法正确的是( )
a b
A.a可能等于1 B.a一定大于2
C.a一定小于2 D.a一定等于2
答案 C
解析 由b=6a>7得a>,由混合溶液的pH=7得n(H+)=n(OH-),即V×10-a=V×
a b
10b-14,得=10a+b-14;由于V<V ,即10a+b-14<1,得a+b-14<0,结合b=6a得a<2,
a b
综合知,<a<2,故选C项。
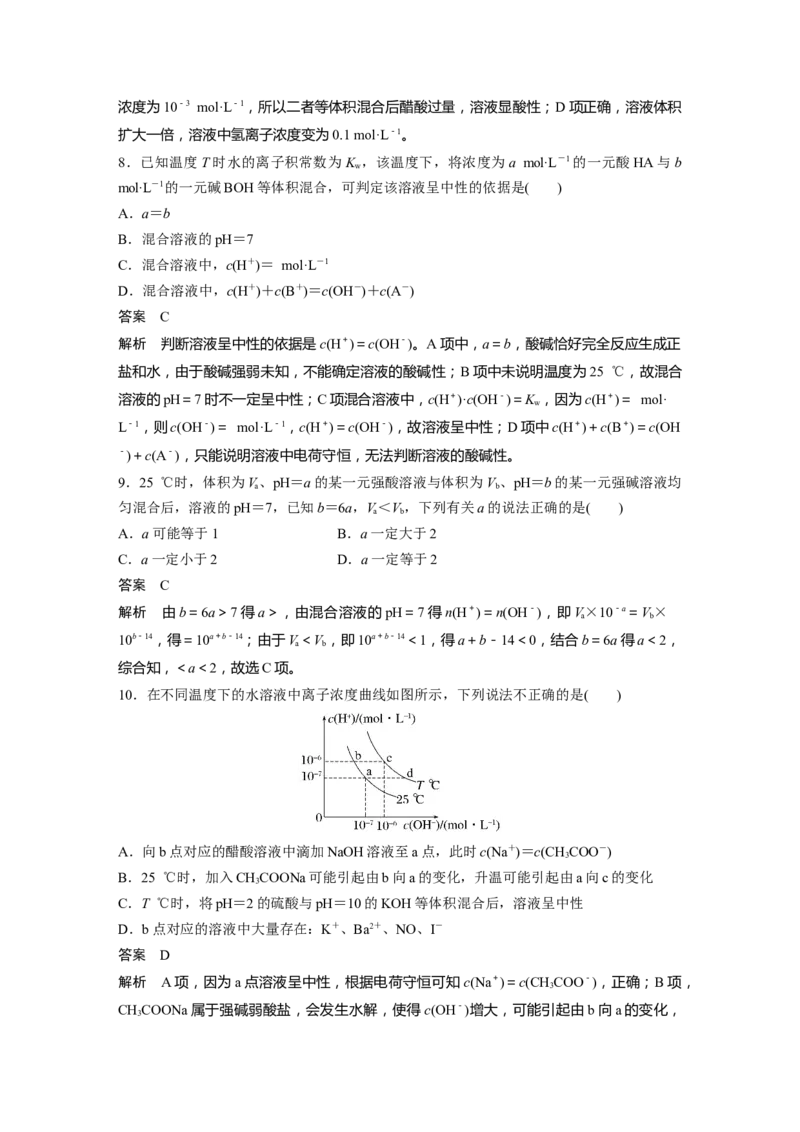
10.在不同温度下的水溶液中离子浓度曲线如图所示,下列说法不正确的是( )
A.向b点对应的醋酸溶液中滴加NaOH溶液至a点,此时c(Na+)=c(CHCOO-)
3
B.25 ℃时,加入CHCOONa可能引起由b向a的变化,升温可能引起由a向c的变化
3
C.T ℃时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液呈中性
D.b点对应的溶液中大量存在:K+、Ba2+、NO、I-
答案 D
解析 A项,因为a点溶液呈中性,根据电荷守恒可知 c(Na+)=c(CHCOO-),正确;B项,
3
CHCOONa属于强碱弱酸盐,会发生水解,使得 c(OH-)增大,可能引起由b向a的变化,
3升温溶液中的c(OH-)和c(H+)同时同等程度地增大,所以可能引起由a向c的变化,正确;
C项,由图像知T ℃时K =10-12,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液
w
呈中性,正确;D项,由图像知b点对应的溶液呈酸性,溶液中NO、I-在酸性条件下发生
氧化还原反应,不能大量存在,错误。
11.如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是( )
A.两条曲线间任意点均有c(H+)·c(OH-)=K
w
B.M区域内(边界除外)任意点均有c(H+)<c(OH-)
C.温度:T<T
1 2
D.XZ线段上任意点均有pH=7
答案 D
解析 温度越高,水的电离程度越大,电离出的c(H+)与c(OH-)越大,所以T >T ,C项正
2 1
确;XZ线段上任意点都有c(H+)=c(OH-),只有当c(H+)=10-7 mol·L-1时,才有pH=7,
D项错误。
12. 已知常温时HClO的K=3.0×10-8,HF的K=3.5×10-4,现将pH和体积都相同的次
a a
氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示,下列叙述正确的是(
)
A.曲线Ⅱ为氢氟酸稀释时pH变化曲线
B.取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗氢氟酸的体积较小
C.b点溶液中水的电离程度比c点溶液中水的电离程度小
D.从b点到d点,溶液中保持不变(HR代表HClO或HF)
答案 D
解析 A项,酸性越强,加水稀释时溶液pH变化越大,HF酸性强于HClO,加水稀释时
HF的pH变化大,所以曲线Ⅰ代表HF稀释时pH变化曲线,错误;B项,pH相同的两种酸,
越弱的酸其浓度越大,HClO酸性弱于HF,所以中和相同体积、相同浓度的 NaOH溶液,
消耗HClO的体积较小,错误;D项,溶液中==,平衡常数只随温度的改变而改变,所以从b点到d点,溶液中保持不变,正确。
13.常温下,浓度均为c 、体积均为V 的MOH和ROH两种碱液分别加水稀释至体积为
0 0
V,溶液pH随lg 的变化如图甲所示;当pH=b时,两曲线出现交叉点x,如图乙所示。下
列叙述正确的是( )
A.c、V 均不能确定其数值大小
0 0
B.电离常数K (MOH)≈1.1×10-4
b
C.x点处两种溶液中水的电离程度相等
D.lg 相同时,将两种溶液同时升高相同的温度,则增大
答案 C
解析 根据图知,ROH加水稀释10倍,溶液的pH减小1,说明ROH完全电离,为强电解
质,则MOH为弱电解质。常温下浓度为c 的ROH溶液的pH=13,且ROH为强电解质,
0
则c =0.1 mol·L-1,所以能确定初始浓度,A错误;lg =0时,MOH溶液的pH=12,c =
0 0
0.1 mol·L-1,电离常数K (MOH)==≈1.1×10-3,B错误;x点两种溶液的pH相等,所以
b
二者抑制水的电离程度相等,C正确;升高温度促进MOH的电离,所以lg 相同时,升高温
度c(R+)不变,c(M+)增大,则减小,D错误。
14.已知水在25 ℃和100 ℃时,其电离平衡曲线如图所示:
(1)25 ℃时,将pH=9的NaOH溶液与pH=4的硫酸溶液混合,所得混合溶液的pH=7,则
NaOH溶液与硫酸溶液的体积比为__________。
(2)100 ℃时,若100体积pH=a的某强酸溶液与1体积pH=b的某强碱溶液混合后溶液呈
中性,则a与b之间应满足的关系是__________。
(3)曲线A所对应的温度下,pH=2的HCl溶液和pH=11的某BOH溶液中,若水的电离程
度分别用α、α 表示,则α__________α(填“大于”“小于”“等于”或“无法确定”)。
1 2 1 2
(4)曲线B对应的温度下,将0.02 mol·L-1 Ba(OH) 溶液与等物质的量浓度的NaHSO 溶液等
2 4
体积混合后,混合溶液的pH=________。答案 (1)10∶1 (2)a+b=14 (3)小于 (4)10
解析 (1)25 ℃时,pH=9的NaOH溶液,c(OH-)=10-5 mol·L-1;pH=4的HSO 溶液,
2 4
c(H+)=10-4 mol·L-1;若所得混合溶液的pH=7,则c(OH-)·V(NaOH)=c(H+)·V(H SO )。
2 4
故NaOH溶液与HSO 溶液的体积比为V(NaOH)∶V(H SO )=c(H+)∶c(OH-)=10∶1。
2 4 2 4
(2)100 ℃时,水的离子积常数 K =1×10-12。100体积pH=a的某强酸溶液中 n(H+)=
w
100× 10-a mol=102-a mol,1体积pH=b的某强碱溶液中n(OH-)= mol=10b-12 mol。混
合后溶液呈中性,102-a mol=10b-12 mol,2-a=b-12,所以a+b=14。
(3)曲线A所对应的温度是25 ℃,pH=2的HCl溶液,c (H+)=10-12 mol·L-1;pH=11的
水
某BOH溶液中,c (H+)=10-11 mol·L-1;水电离产生的H+的浓度越大,水的电离程度就
水
越大,则α<α。
1 2
(4)混合溶液中c(OH-)==0.01 mol·L-1。由于该温度下水的离子积常数K =10-12,所以c(H
w
+)=10-10 mol·L-1,所得混合液的pH=10。