文档内容
第 51 讲 弱电解质的电离平衡
[复习目标] 1.理解弱电解质在水溶液中的电离平衡。2.理解电离常数的含义,掌握电离常
数的应用并能进行相关计算。
考点一 弱电解质的电离平衡及影响因素
1.电离平衡的建立
在一定条件下(如温度、压强等),当弱电解质电离产生离子的速率和离子结合成分子的速率
相等时,电离过程达到了平衡。
平衡建立过程如图所示:
2.电离平衡的特征
3.外因对电离平衡的影响
(1)以0.1 mol·L-1 CHCOOH溶液为例,填写外界条件对CHCOOH(aq)CHCOO-(aq)+H
3 3 3
+
(aq) ΔH>0的影响。改变条件 平衡移动方向 n(H+) c(H+) 导电能力
加水稀释 向右 增大 减小 减弱
加入少量冰醋酸 向右 增大 增大 增强
通入HCl(g) 向左 增大 增大 增强
加NaOH(s) 向右 减小 减小 增强
加CHCOONa(s) 向左 减小 减小 增强
3
升高温度 向右 增大 增大 增强
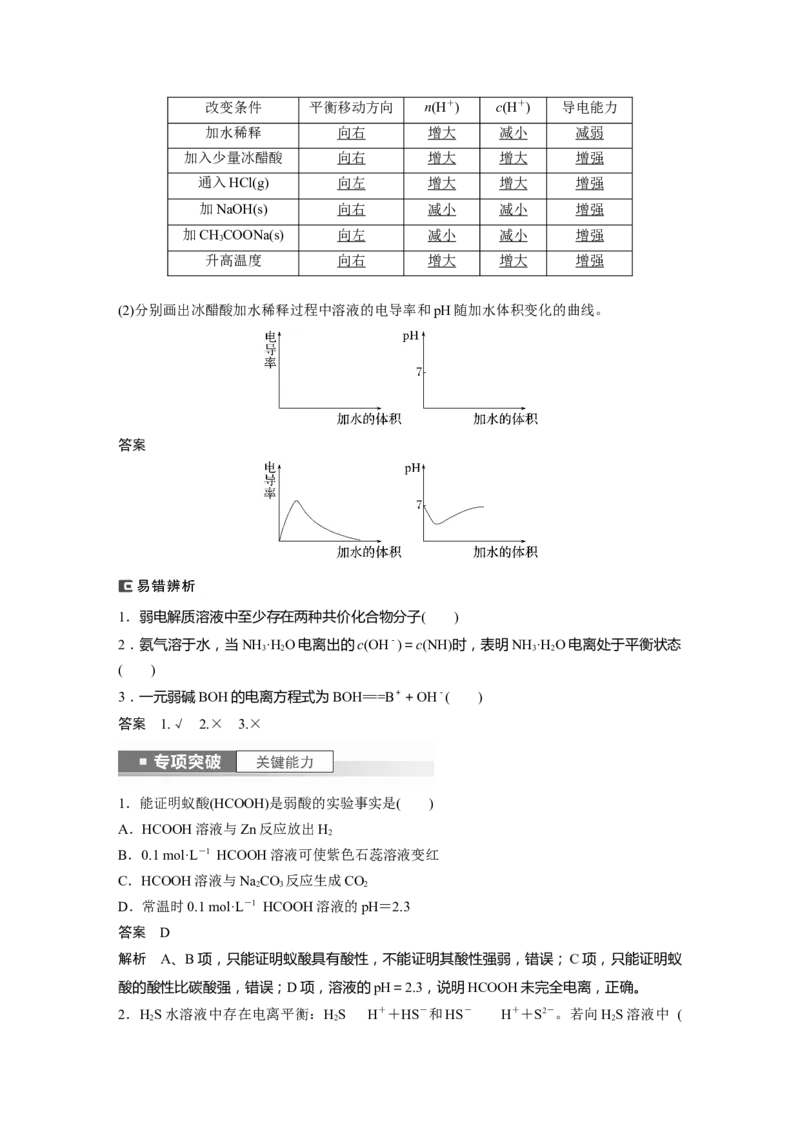
(2)分别画出冰醋酸加水稀释过程中溶液的电导率和pH随加水体积变化的曲线。
答案
1.弱电解质溶液中至少存在两种共价化合物分子( )
2.氨气溶于水,当NH ·H O电离出的c(OH-)=c(NH)时,表明NH ·H O电离处于平衡状态
3 2 3 2
( )
3.一元弱碱BOH的电离方程式为BOH===B++OH-( )
答案 1.√ 2.× 3.×
1.能证明蚁酸(HCOOH)是弱酸的实验事实是( )
A.HCOOH溶液与Zn反应放出H
2
B.0.1 mol·L-1 HCOOH溶液可使紫色石蕊溶液变红
C.HCOOH溶液与NaCO 反应生成CO
2 3 2
D.常温时0.1 mol·L-1 HCOOH溶液的pH=2.3
答案 D
解析 A、B项,只能证明蚁酸具有酸性,不能证明其酸性强弱,错误;C项,只能证明蚁
酸的酸性比碳酸强,错误;D项,溶液的pH=2.3,说明HCOOH未完全电离,正确。
2.HS水溶液中存在电离平衡:HSH++HS-和HS-H++S2-。若向HS溶液中 (
2 2 2)
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO 气体,平衡向左移动,溶液pH增大
2
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
答案 C
解析 加水促进电离,但氢离子浓度减小,A项错误;通入过量SO 气体发生反应:2HS+
2 2
SO ===3S↓+2HO,当SO 过量时溶液显酸性,而且酸性比HS强,pH减小,B项错误;
2 2 2 2
滴加新制氯水,发生反应:Cl +HS===2HCl+S↓,平衡向左移动,溶液pH减小,C项正
2 2
确;加入少量硫酸铜固体,发生反应:HS+Cu2+===CuS↓+2H+,H+浓度增大,D项错误。
2
3.常温下,①100 mL 0.01 mol·L-1的CHCOOH溶液,②10 mL 0.1 mol·L-1的CHCOOH
3 3
溶液。用“>”“=”或“<”填写下列问题。
(1)c(CHCOO-):①________②。
3
(2)电离程度:①________②。
(3)在上述两种溶液中加入足量锌片。开始时的反应速率:①________②,反应结束生成相
同状况下H 的体积:①________②。
2
(4)与同浓度的NaOH溶液完全反应消耗NaOH溶液的体积:①________②。
答案 (1)< (2)> (3)< = (4)=
考点二 电离平衡常数及应用
1.概念
在一定条件下,弱电解质达到电离平衡时,溶液中电离所生成的各种离子浓度(幂次方)的乘
积与溶液中未电离的分子浓度的比值是一个常数,这个常数叫做电离平衡常数,简称电离常
数,用K(弱酸用K,弱碱用K )表示。
a b
2.表达式
一元弱酸HA 一元弱碱BOH
电离方程式 HAH++A- BOHB++OH-
电离常数表达式 K= K =
a b
3.特点
(1)电离平衡常数与温度有关,与浓度无关,升高温度,K增大。
(2)电离平衡常数反映弱电解质的相对强弱,K越大,表示弱电解质越易电离,酸性或碱性
越强。(3)多元弱酸的各步电离常数的大小关系是K >K >K ……,当K ≫K 时,计算多元弱酸中
a1 a2 a3 a1 a2
的c(H+)或比较多元弱酸酸性的相对强弱时,通常只考虑第一步电离。
4.电离度
(1)概念
在一定条件下的弱电解质达到电离平衡时,已经电离的电解质分子数占原电解质分子总数的
百分比。
(2)表示方法
α=×100%,也可表示为α=×100%。
(3)影响因素
①相同温度下,同一弱电解质,浓度越大,其电离度(α)越小。
②相同浓度下,同一弱电解质,温度越高,其电离度(α)越大。
1.同一弱电解质,浓度不同其电离常数一定不同( )
2.弱电解质的电离平衡右移,电离常数一定增大( )
3.某一弱电解质,电离度越大,电离常数就越大( )
4.常温下,依据K (H CO)>K (H PO ),可知碳酸的酸性比磷酸强( )
a1 2 3 a2 3 3
答案 1.× 2.× 3.× 4.×
一、利用电离常数判断弱电解质(酸碱性)的相对强弱
1.部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HS HCO HClO
2 2 3
电离平衡 K =1.1×10-7 K =4.5×10-7
a1 a1
K=1.77×10-4 K=4.0×10-8
a a
常数(25℃) K =1.3×10-13 K =4.7×10-11
a2 a2
按要求回答下列问题:
(1)HCOOH、HS、HCO、HClO的酸性由强到弱的顺序为________________________。
2 2 3
(2)相同浓度的HCOO-、HS-、S2-、HCO、CO、ClO-结合H+的能力由强到弱的顺序为
________________________________________________________________________
________________________________________________________________________。
(3)运用上述电离常数及物质的特性判断下列化学方程式不正确的是________(填序号)。
①次氯酸与NaHCO 溶液的反应:HClO+HCO===ClO-+HO+CO↑
3 2 2
②少量CO 通入NaClO溶液中:CO+HO+2ClO-===CO+2HClO
2 2 2
③少量CO 通入NaClO溶液中:CO+HO+ClO-===HCO+HClO
2 2 2
④硫化氢通入NaClO溶液中:HS+ClO-===HS-+HClO
2
⑤碳酸钠滴入足量甲酸溶液中:2HCOOH+CO===2HCOO-+CO↑+HO
2 2答案 (1)HCOOH>HCO>HS>HClO
2 3 2
(2)S2->CO>ClO->HS->HCO>HCOO-
(3)①②④
二、判断微粒浓度比值的大小
2.常温下,将0.1 mol·L-1的CHCOOH溶液加水稀释,请填写下列表达式中的数据变化情
3
况(填“变大”“变小”或“不变”)。
(1)________;
(2)________;
(3)________;
(4)________;
(5)________。
答案 (1)变小 (2)变大 (3)变小 (4)不变
(5)不变
解析 (1)将该式变为=或稀释时醋酸的电离平衡正向移动,n(CHCOOH)减小,n(H+)增大
3
因而其比值变小。
(2)将该式变为=或稀释时醋酸的电离平衡正向移动,n(CHCOOH)减小,n(CHCOO-)增大
3 3
因而其比值变大。
(5)将该式变为=,故比值不变。
判断溶液中微粒浓度比值的三种方法
(1)将浓度之比转化为物质的量之比进行比较,这样分析起来可以忽略溶液体积的变化,只
需分析微粒数目的变化即可。
(2)“假设法”,如上述问题(3),假设无限稀释,c(CHCOO-)趋近于0,c(H+)趋于10-7mol·L
3
-1,故比值变小。
(3)“凑常数”,解题时将某些粒子的浓度比值乘以或除以某种粒子的浓度,转化为一个常
数与某种粒子浓度的乘积或相除的关系。
1.(2020·北京,11)室温下,对于1 L 0.1 mol·L-1醋酸溶液。下列判断正确的是( )
A.该溶液中CHCOO-的粒子数为6.02×1022
3
B.加入少量CHCOONa固体后,溶液的pH降低
3
C.滴加NaOH溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1 mol
3 3
D.与NaCO 溶液反应的离子方程式为CO+2H+===HO+CO↑
2 3 2 2
答案 C
解析 醋酸属于弱电解质,则0.1 mol醋酸中CHCOO-的粒子数小于6.02×1022,A错误;
3加入少量CHCOONa固体,抑制醋酸的电离,溶液的pH升高,故B错误;根据元素质量
3
守恒,n(CHCOO-)+n(CHCOOH)=0.1 mol,故C正确;醋酸的酸性强于碳酸,则根据强
3 3
酸制取弱酸,醋酸与NaCO 溶液反应生成醋酸钠、二氧化碳和水,醋酸是弱电解质,离子
2 3
反应中不能拆写,故D错误。
2.(2022·全国乙卷,13)常温下,一元酸HA的K(HA)=1.0×10-3。在某体系中,H+与A-
a
不能穿过隔膜,未电离的HA可自由穿过该膜(如图所示)。
设溶液中c (HA)=c(HA)+c(A-),当达到平衡时,下列叙述正确的是( )
总
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
B.溶液Ⅱ中的HA的电离度[]为
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c (HA)之比为10-4
总
答案 B
解析 常温下,溶液Ⅰ的pH=7.0,则溶液Ⅰ中c(H+)=c(OH-)=1×10-7 mol·L-1,c(H+)
<c(OH-)+c(A-),A错误;常温下,溶液Ⅱ的pH=1.0,溶液中c(H+)=0.1 mol·L-1,
K(HA)==1.0×10-3,c (HA)=c(HA)+c(A-),则=1.0×10-3,解得=,B正确;根据题
a 总
意,未电离的HA可自由穿过隔膜,故溶液Ⅰ和Ⅱ中的c(HA)相等,C错误;常温下,溶液
Ⅰ的pH=7.0,溶液Ⅰ中c(H+)=1×10-7 mol·L-1,K(HA)==1.0×10-3,c (HA)=c(HA)
a 总
+c(A-),=1.0×10-3,溶液Ⅰ中c (HA)=(104+1)c(HA);溶液Ⅱ中,由B项解析可知c
总 总
(HA)=1.01 c(HA),未电离的HA可自由穿过隔膜,故溶液Ⅰ和Ⅱ中的c(HA)相等,溶液Ⅰ
和Ⅱ中c (HA)之比为[(104+1)c(HA)]∶[1.01c(HA)]=(104+1)∶1.01≈104,D错误。
总
3.[2020·天津,16(5)节选]已知 25 ℃碳酸电离常数为 K 、K ,当溶液 pH=12 时,
a1 a2
c(H CO)∶c(HCO)∶c(CO)=1∶____________∶______________。
2 3
答案 1012·K 1024·K ·K
a1 a1 a2
解析 HCO 是二元弱酸,分步发生电离:HCOHCO+H+、HCOCO+H+,则有
2 3 2 3
K =、K =,从而可得K ·K =。当溶液pH=12时,c(H+)=10-12 mol·L-1,代入K 、
a1 a2 a1 a2 a1
K ·K 可得c(H CO)∶c(HCO)=1∶(1012·K ),c(H CO)∶c(CO)=1∶(1024·K ·K ),综合可
a1 a2 2 3 a1 2 3 a1 a2
得c(H CO)∶c(HCO)∶c(CO)=1∶(1012·K )∶(1024·K ·K )。
2 3 a1 a1 a2
课时精练
1.下列说法正确的有( )①不溶于水的盐都是弱电解质 ②可溶于水的盐都是强电解质 ③0.5 mol·L-1一元酸溶液
中H+浓度一定为0.5 mol·L-1 ④强酸溶液中的c(H+)不一定大于弱酸溶液中的c(H+) ⑤
电解质溶液导电的原因是溶液中有自由移动的阴、阳离子 ⑥熔融的电解质都能导电
A.1个 B.2个 C.3个 D.4个
答案 B
解析 ①溶解性与电解质强弱无关,错误;②醋酸铅是弱电解质,可溶于水,可溶于水的盐
不一定都是强电解质,错误;③0.5 mol·L-1一元弱酸溶液中H+浓度小于0.5 mol·L-1,错误;
⑥HCl是电解质,熔融HCl不导电,熔融的电解质不一定能导电,错误。
2.室温下,下列事实不能说明NH ·H O为弱电解质的是( )
3 2
A.0.1 mol·L-1的氨水中c(OH-)<0.1 mol·L-1
B.0.1 mol·L-1的氨水中c(NH)<0.1 mol·L-1
C.相同条件下,浓度均为0.1 mol·L-1的NaOH溶液和氨水,氨水的导电能力弱
D.0.1 mol·L-1的氨水能使无色酚酞溶液变红
答案 D
解析 NH ·H O为弱电解质,氨水中存在电离平衡NH ·H ONH+OH-,故0.1 mol·L-1
3 2 3 2
的氨水中c(OH-)、c(NH)均小于0.1 mol·L-1,A、B两项能说明NH ·H O为弱电解质;相同
3 2
条件下,浓度均为0.1 mol·L-1的NaOH溶液和氨水,氨水的导电能力弱,说明氨水中离子
浓度小于同浓度的NaOH溶液,C项能说明氨水中存在NH ·H O的电离平衡,NH ·H O为
3 2 3 2
弱电解质;氨水能使无色酚酞溶液变红,只能说明 NH ·H O电离出OH-,但不能说明
3 2
NH ·H O是部分电离,D项不能说明NH ·H O为弱电解质。
3 2 3 2
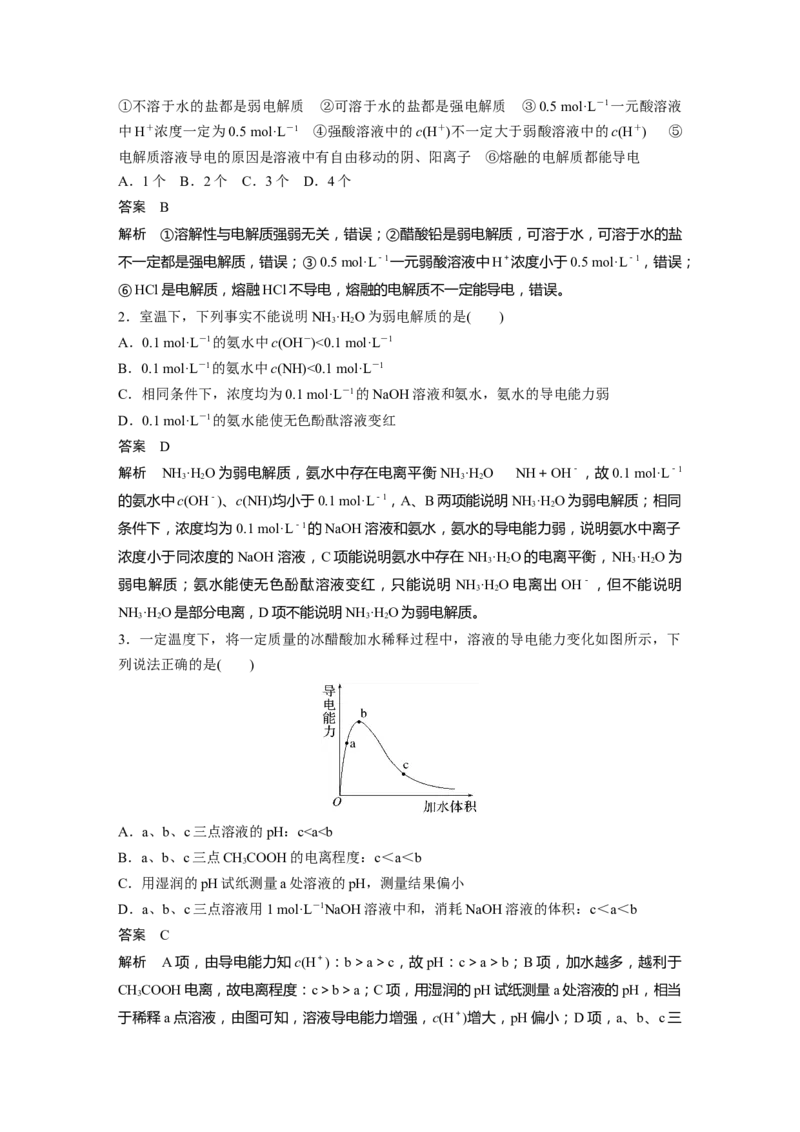
3.一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下
列说法正确的是( )
A.a、b、c三点溶液的pH:c7
答案 A
解析 因醋酸是弱酸,在稀释过程中c(H+)减小,c(OH-)增大,减小,A项正确;加水稀释
溶液,促进电离,则溶液中导电粒子的数目增多,B项错误;加水稀释时,溶液的体积增大
的倍数大于n(H+)增加的倍数,则c(H+)减小,C项错误;加入氢氧化钠溶液的量未知,不能判定混合溶液的pH,D项错误。
7.(2022·深圳模拟)硼酸(H BO)的电离方程式为HBO +HOB(OH)+H+。已知常温下,
3 3 3 3 2
K(H BO)=5.4×10-10、K(CHCOOH)=1.75×10-5。下列说法错误的是( )
a 3 3 a 3
A.HBO 为一元酸
3 3
B.0.01 mol·L-1 HBO 溶液的pH≈6
3 3
C.常温下,等浓度溶液的pH:CHCOONa>NaB(OH)
3 4
D.NaOH溶液溅到皮肤时,可用大量水冲洗,再涂上硼酸溶液
答案 C
解析 根据题意可知HBO 只存在一步电离,所以为一元酸,A正确;设0.01 mol·L-1
3 3
HBO 溶液中c(H+)=x,则c[B(OH)]也可近似认为等于x,则有K(H BO)==5.4×10-10,
3 3 a 3 3
解得x≈2.3×10-6 mol·L-1,所以pH≈6,B正确;K(H BO)Z2-,A不正确;根据已知电离常数判断,HX是弱酸,故X-发生水解被消
耗,c(Na+)>c(X-),B不正确;从表格中电离平衡常数的大小判断酸性:HX>HY-,故根据
相对强的酸制相对弱的酸,C正确;根据电离平衡常数判断酸性:HYHZ,D不正确。
2 2
11.25 ℃时,用0.1 mol·L-1的CHCOOH溶液滴定20 mL 0.1 mol·L-1的NaOH溶液,当滴
3
加V mL CH COOH溶液时,混合溶液的pH=7。已知CHCOOH的电离常数为K,忽略混
3 3 a
合时引起的溶液体积的变化,下列关系式正确的是( )
A.K= B.V=
a
C.K= D.K=
a a
答案 A
解析 混合溶液的pH=7,说明醋酸过量,混合溶液中c(CHCOOH)≈ mol·L-1,根据电荷
3
守恒:c(Na+)+c(H+)=c(CHCOO-)+c(OH-)及c(H+)=c(OH-)可得,c(Na+)=c(CHCOO-)
3 3
= mol·L-1,则K==,A项正确。
a
12.HC O 是一种二元弱酸,HC O 溶液中各粒子浓度在其总浓度中所占比值叫其分布系
2 2 4 2 2 4
数,常温下某浓度的HC O 溶液中各粒子分布系数随pH的变化如图所示,据此分析,下列
2 2 4
说法不正确的是( )A.曲线a代表HC O,曲线b代表C O
2 2 4 2
B.常温下0.1 mol·L-1的NaHC O 溶液显酸性
2 4
C.常温下,HC O 的电离平衡常数K =10-4.30
2 2 4 a2
D.pH从1.30~4.30时,先增大后减小
答案 D
解析 随着pH的增大,草酸分子的浓度逐渐减小,草酸氢根离子的浓度逐渐增大,pH继
续升高,草酸氢根离子的浓度又逐渐减小,而草酸根离子的浓度开始逐渐增大,因此曲线 a
代表HC O,曲线b代表C O,A正确;根据图像可知当草酸氢根离子和草酸根离子浓度相
2 2 4 2
等时,pH=4.30,所以草酸的第二步电离平衡常数K ==10-4.30,C正确;根据图像可知
a2
pH从1.30~4.30时,逐渐减小,D项错误。
13.食醋(主要成分CHCOOH)、纯碱(Na CO)和小苏打(NaHCO )均为家庭厨房中常用的物
3 2 3 3
质。已知:
弱酸 CHCOOH HCO HNO HCN
3 2 3 2
电离 K =4.3×10-7
a1
K=1.8×10-5 K=5.0×10-4 K=6.2×10-10
a a a
常数 K =5.6×10-11
a2
请回答下列问题:
(1)CH COO-、HCO、CO、NO、CN-结合质子(H+)的能力由小到大的顺序为
3
________________________。
(2)CO 通入 NaNO 溶液中能否生成 HNO ?________(填“能”或“否”),理由是
2 2 2
________________________________________________________________________。
(3) 少 量 CO 通 入 足 量 NaCN 溶 液 中 , 反 应 的 离 子 方 程 式 为
2
________________________________________________________________________。
(4)常温下,将20 mL 0.10 mol·L-1 CHCOOH溶液和20 mL 0.10 mol·L-1 HNO 溶液分别与
3 2
20 mL 0.10 mol·L-1 NaHCO 溶液混合(混合后溶液体积变化忽略不计)。
3
①反应开始时,v(CHCOOH)______v(HNO)(填“>”“<”或“=”,下同)。
3 2
②充分反应后,两溶液中c(CHCOO-)______c(NO)。
3
(5)25 ℃时,向CHCOOH溶液中加入一定量的NaHCO ,所得溶液的pH=6,则混合液中
3 3
=__________。
(6)常温下,下列方法可以使0.1 mol·L-1CHCOOH的电离程度增大的是____________(填字
3
母)。a.加入少量的稀盐酸 b.加热溶液
c.加水稀释 d.加入少量冰醋酸
答案 (1)NO<CHCOO-<HCO<CN-<CO
3
(2)否 HCO 的K 小于HNO 的K,HCO 比HNO 的酸性弱
2 3 a1 2 a 2 3 2
(3)CO +HO+CN-===HCN+HCO
2 2
(4)①< ②< (5)18 (6)bc