文档内容
原电池作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-8,25 题为三星,9—18,26-28 为四星,19-24 为五星。
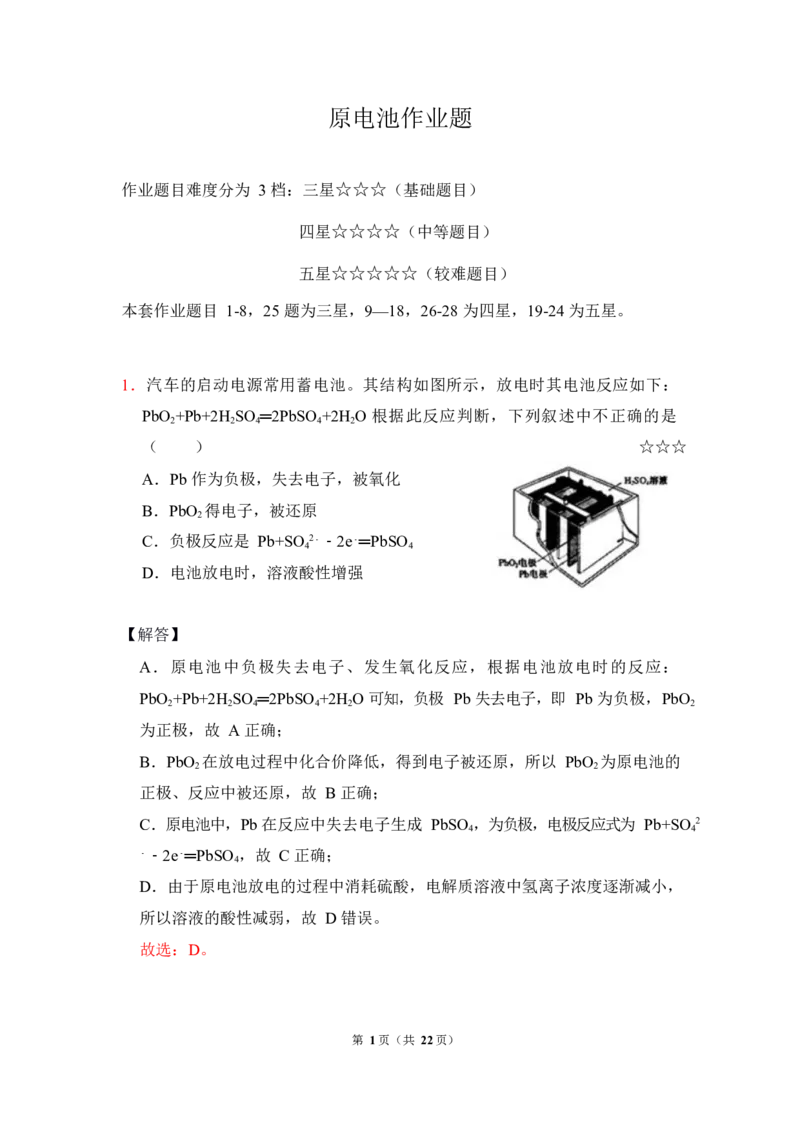
1.汽车的启动电源常用蓄电池。其结构如图所示,放电时其电池反应如下:
PbO +Pb+2H SO ═2PbSO +2H O 根据此反应判断,下列叙述中不正确的是
2 2 4 4 2
( ) ☆☆☆
A.Pb 作为负极,失去电子,被氧化
B.PbO 得电子,被还原
2
C.负极反应是 Pb+SO 2﹣﹣2e﹣═PbSO
4 4
D.电池放电时,溶液酸性增强
【解答】
A.原电池中负极失去电子、发生氧化反应,根据电池放电时的反应:
PbO +Pb+2H SO ═2PbSO +2H O 可知,负极 Pb 失去电子,即 Pb 为负极,PbO
2 2 4 4 2 2
为正极,故 A 正确;
B.PbO 在放电过程中化合价降低,得到电子被还原,所以 PbO 为原电池的
2 2
正极、反应中被还原,故 B 正确;
C.原电池中,Pb 在反应中失去电子生成 PbSO ,为负极,电极反应式为 Pb+SO 2
4 4
﹣﹣2e﹣═PbSO ,故 C 正确;
4
D.由于原电池放电的过程中消耗硫酸,电解质溶液中氢离子浓度逐渐减小,
所以溶液的酸性减弱,故 D 错误。
故选:D。
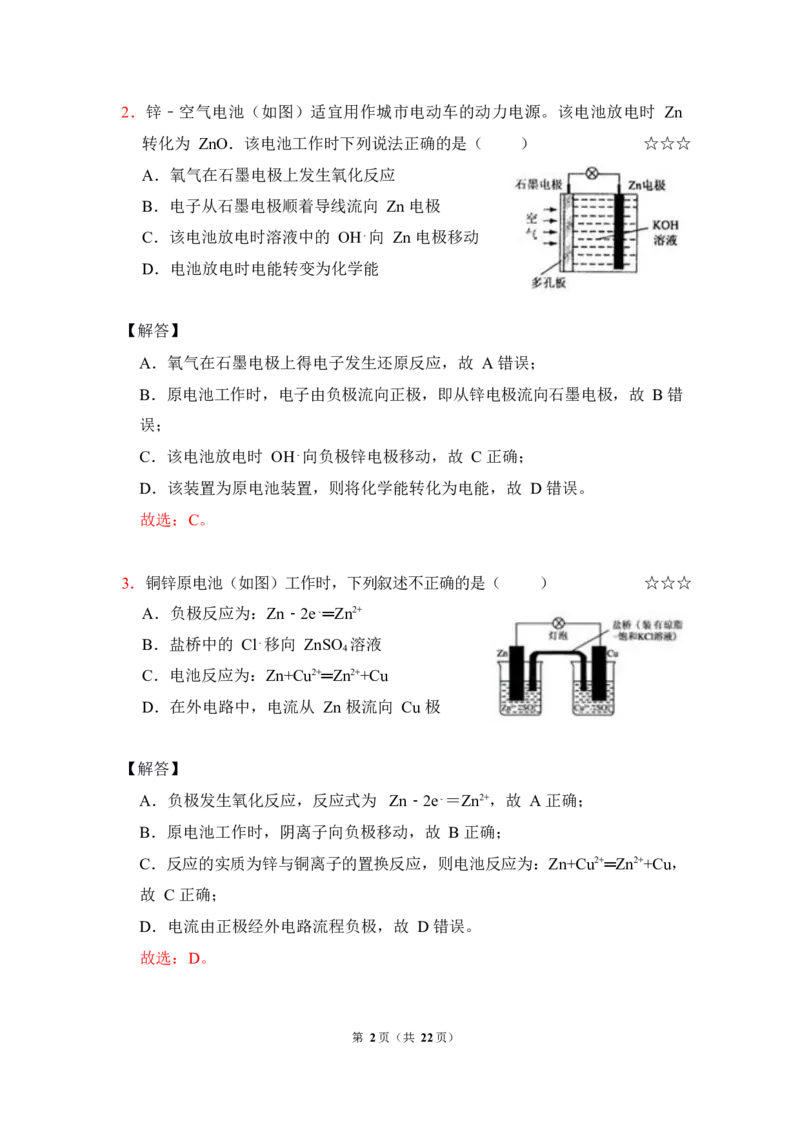
第 1页(共 22页)2.锌﹣空气电池(如图)适宜用作城市电动车的动力电源。该电池放电时 Zn
转化为 ZnO.该电池工作时下列说法正确的是( ) ☆☆☆
A.氧气在石墨电极上发生氧化反应
B.电子从石墨电极顺着导线流向 Zn 电极
C.该电池放电时溶液中的 OH﹣向 Zn 电极移动
D.电池放电时电能转变为化学能
【解答】
A.氧气在石墨电极上得电子发生还原反应,故 A 错误;
B.原电池工作时,电子由负极流向正极,即从锌电极流向石墨电极,故 B 错
误;
C.该电池放电时 OH﹣向负极锌电极移动,故 C 正确;
D.该装置为原电池装置,则将化学能转化为电能,故 D 错误。
故选:C。
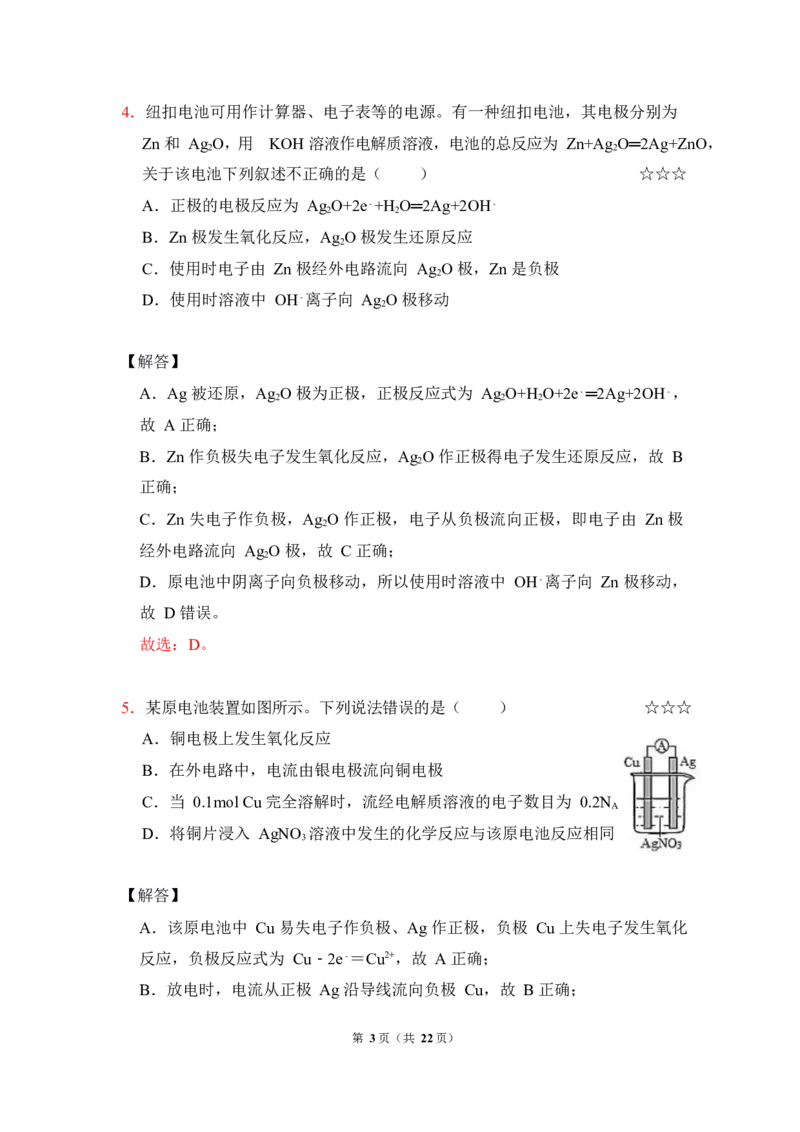
3.铜锌原电池(如图)工作时,下列叙述不正确的是( ) ☆☆☆
A.负极反应为:Zn﹣2e﹣═Zn2+
B.盐桥中的 Cl﹣移向 ZnSO 溶液
4
C.电池反应为:Zn+Cu2+═Zn2++Cu
D.在外电路中,电流从 Zn 极流向 Cu 极
【解答】
A.负极发生氧化反应,反应式为 Zn﹣2e﹣=Zn2+,故 A 正确;
B.原电池工作时,阴离子向负极移动,故 B 正确;
C.反应的实质为锌与铜离子的置换反应,则电池反应为:Zn+Cu2+═Zn2++Cu,
故 C 正确;
D.电流由正极经外电路流程负极,故 D 错误。
故选:D。
第 2页(共 22页)4.纽扣电池可用作计算器、电子表等的电源。有一种纽扣电池,其电极分别为
Zn 和 Ag O,用 KOH 溶液作电解质溶液,电池的总反应为 Zn+Ag O═2Ag+ZnO,
2 2
关于该电池下列叙述不正确的是( ) ☆☆☆
A.正极的电极反应为 Ag O+2e﹣+H O═2Ag+2OH﹣
2 2
B.Zn 极发生氧化反应,Ag O 极发生还原反应
2
C.使用时电子由 Zn 极经外电路流向 Ag O 极,Zn 是负极
2
D.使用时溶液中 OH﹣离子向 Ag O 极移动
2
【解答】
A.Ag 被还原,Ag O 极为正极,正极反应式为 Ag O+H O+2e﹣═2Ag+2OH﹣,
2 2 2
故 A 正确;
B.Zn 作负极失电子发生氧化反应,Ag O 作正极得电子发生还原反应,故 B
2
正确;
C.Zn 失电子作负极,Ag O 作正极,电子从负极流向正极,即电子由 Zn 极
2
经外电路流向 Ag O 极,故 C 正确;
2
D.原电池中阴离子向负极移动,所以使用时溶液中 OH﹣离子向 Zn 极移动,
故 D 错误。
故选:D。
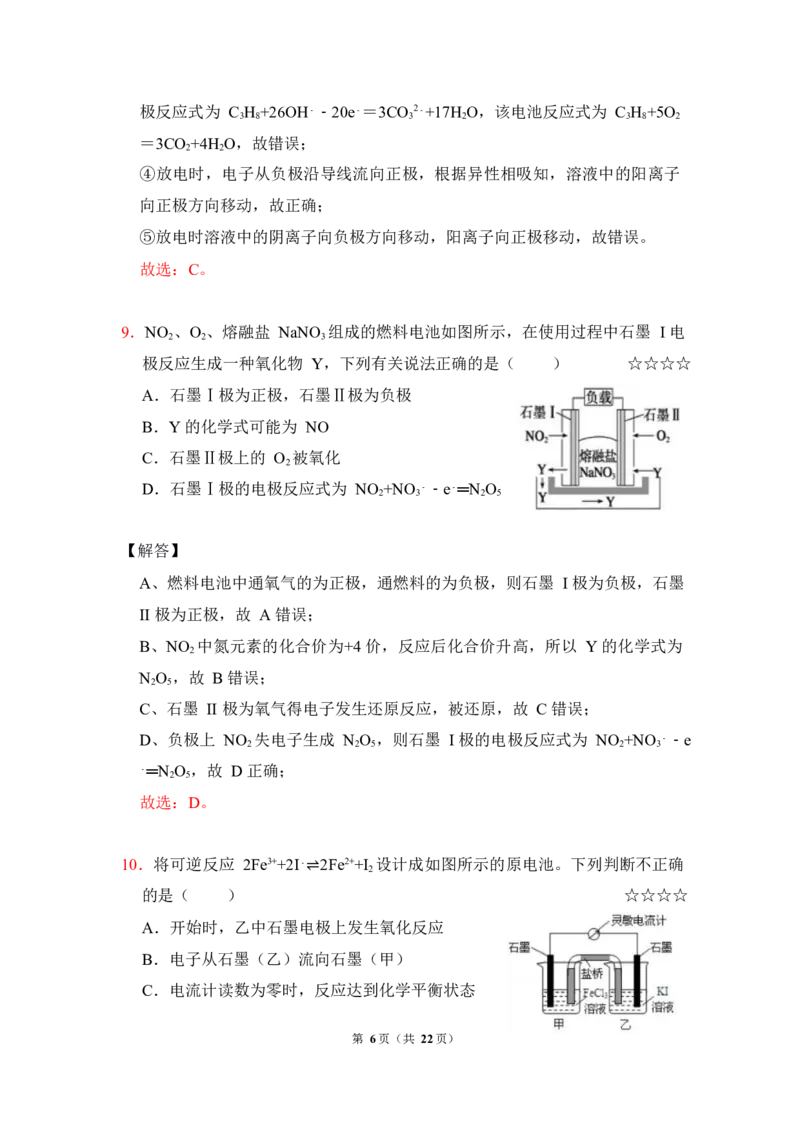
5.某原电池装置如图所示。下列说法错误的是( ) ☆☆☆
A.铜电极上发生氧化反应
B.在外电路中,电流由银电极流向铜电极
C.当 0.1mol Cu 完全溶解时,流经电解质溶液的电子数目为 0.2N
A
D.将铜片浸入 AgNO 溶液中发生的化学反应与该原电池反应相同
3
【解答】
A.该原电池中 Cu 易失电子作负极、Ag 作正极,负极 Cu 上失电子发生氧化
反应,负极反应式为 Cu﹣2e﹣=Cu2+,故 A 正确;
B.放电时,电流从正极 Ag 沿导线流向负极 Cu,故 B 正确;
第 3页(共 22页)C.电子不进入电解质溶液,电解质溶液中阴阳离子定向移动形成电流,故 C
错误;
D.该原电池的电极反应式为:负极:Cu﹣2e﹣=Cu2+正极:Ag
+
+e﹣=Ag,故
总反应为 Cu+2Ag =Cu2++2Ag.铜片与硝酸银反应的离子方程式为 Cu+2Ag
+ +
=Cu2++2Ag,所以将铜片浸入 AgNO 溶液中发生的化学反应与该原电池反应
3
相同,故 D 正确。
故选:C。
6.碱性电池具有容量大、放电电流大的特点,而被广泛应用。锌锰碱性电池以
KOH 溶液为电解液,反应式为 Zn(s)+2MnO( s)+H O(l)═Zn(OH) +Mn O
2 2 2 2 3
(s)。说法错误的是( ) ☆☆☆
A.电池工作时,锌失去电子
B.电池工作时,电子经过电解质溶液从负极到正极
C.电池正极的电极反应式为 2MnO (s)+H O(l)+2e﹣═Mn O (s)+2OH
2 2 2 3
﹣(aq)
D.外电路中每通过 0.2mol 电子,锌的质量理论上减小 6.5g
【解答】
A.根据电池反应式知,锌失电子发生氧化反应,则锌作负极,故 A 正确;
B.电子不经过溶液,由负极经外电路流向正极,故 B 错误;
C.正极材料为 MnO ,发生还原反应,电极反应式为 2MnO (s)+H O(l)
2 2 2
+2e﹣=Mn O (s)+2OH﹣,故 C 正确;
2 3
D.外电路中每通过 0.2mol 电子,则消耗 0.1mol 电子,则锌的质量理论上减
小 6.5g,故 D 正确。
故选:B。
7.如图是一种应用广泛的锂电池,LiPF 是电解质,SO(CH ) 作溶剂,反应
6 3 2
原理是 4Li+FeS =Fe+2Li S。下列说法错误的是( ) ☆☆☆
2 2
A.外电路中电流的方向是由 b 极到 a 极
第 4页(共 22页)B.b 极反应式是 FeS
2
+4Li
+
+4e﹣=Fe+2Li
2
S
C.可以用水代替 SO(CH ) 作溶剂
3 2
D.金属锂密度小,单位质量放电量较大
【解答】
A、原电池中电子从负极沿外电路流向正极,原电池中 a 为负极,所以电子是
由 a 极流向 b 极,则电流的方向是由 b 极到 a 极,故 A 正确;
B、正极反应式为 FeS
2
+4Li
+
+4e﹣═Fe+2Li
2
S,故 B 正确;
C、负极材料锂与水反应,所以不可以用水代替 SO(CH ) 作溶剂,故 C 错
3 2
误;
D、金属锂密度小,单位质量其物质的量较大,转移电子数较多,放电量大,
故 D 正确。
故选:C。
8.将两个铂电极放置在 KOH 溶液中,然后向两极分别通入 C H 与 O ,即可产
3 8 2
生电流。下列叙述正确的是( ) ☆☆☆
①通入 C H 的电极为正极
3 8
②正极的电极反应式为 O +2H O+4e﹣═4OH
2 2
﹣
③通入 C H 的电极反应式为 C H +5O +20e﹣═3CO +4H O
3 8 3 8 2 2 2
④放电时溶液中的阳离子向正极方向移动
⑤放电时溶液中的阴离子向正极方向移动
A.①② B.②③ C.②④ D.①⑤
【解答】
①通入 C H 的电极上失电子发生氧化反应,则为负极,通入氧气的电极为正
3 8
极,故错误;
②正极上氧气得电子和水反应生成氢氧根离子,电极反应式为 O +2H O+4e
2 2
﹣
═4OH﹣,故正确;
③通入 C H 的电极上丙烷失电子和氢氧根离子反应生成碳酸根离子和水,电
3 8第 5页(共 22页)极反应式为 C H +26OH﹣﹣20e﹣=3CO 2﹣+17H O,该电池反应式为 C H +5O
3 8 3 2 3 8 2
=3CO +4H O,故错误;
2 2
④放电时,电子从负极沿导线流向正极,根据异性相吸知,溶液中的阳离子
向正极方向移动,故正确;
⑤放电时溶液中的阴离子向负极方向移动,阳离子向正极移动,故错误。
故选:C。
9.NO 、O 、熔融盐 NaNO 组成的燃料电池如图所示,在使用过程中石墨 I 电
2 2 3
极反应生成一种氧化物 Y,下列有关说法正确的是( ) ☆☆☆☆
A.石墨Ⅰ极为正极,石墨Ⅱ极为负极
B.Y 的化学式可能为 NO
C.石墨Ⅱ极上的 O 被氧化
2
D.石墨Ⅰ极的电极反应式为 NO +NO ﹣﹣e﹣═N O
2 3 2 5
【解答】
A、燃料电池中通氧气的为正极,通燃料的为负极,则石墨 I 极为负极,石墨
II 极为正极,故 A 错误;
B、NO 中氮元素的化合价为+4 价,反应后化合价升高,所以 Y 的化学式为
2
N O ,故 B 错误;
2 5
C、石墨 II 极为氧气得电子发生还原反应,被还原,故 C 错误;
D、负极上 NO 失电子生成 N O ,则石墨 I 极的电极反应式为 NO +NO ﹣﹣e
2 2 5 2 3
﹣═N O ,故 D 正确;
2 5
故选:D。
10.将可逆反应 2Fe3++2I﹣ 2Fe2++I 设计成如图所示的原电池。下列判断不正确
2
的是( ) ☆☆☆☆
⇌
A.开始时,乙中石墨电极上发生氧化反应
B.电子从石墨(乙)流向石墨(甲)
C.电流计读数为零时,反应达到化学平衡状态
第 6页(共 22页)D.电流计读数为零后,在甲中溶入 FeCl 固体,乙中石墨电极为负极
2
【解答】
A.因乙中 I﹣失去电子放电,元素的化合价升高,则发生氧化反应,故 A 正
确;
B.电子从原电池的负极沿导线流向正极,所以电子从石墨(乙)流向石墨(甲),
故 B 正确;
C.当电流计为零时,说明没有电子发生转移,则反应达到平衡,故 C 正确;
D.当加入 Fe2+,导致平衡逆向移动,则 Fe2+失去电子生成 Fe3+,作为负极,
而乙中石墨成为正极,故 D 错误。
故选:D。
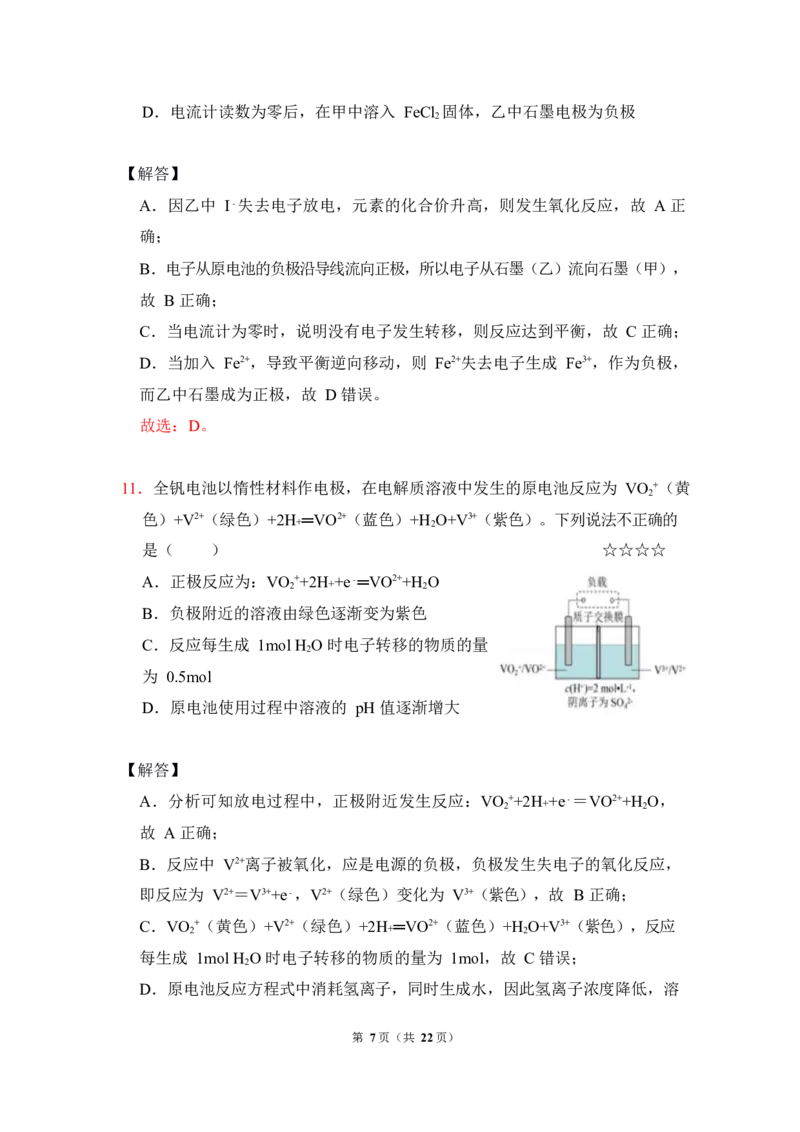
11.全钒电池以惰性材料作电极,在电解质溶液中发生的原电池反应为 VO +(黄
2
色)+V2+(绿色)+2H ═VO2+(蓝色)+H O+V3+(紫色)。下列说法不正确的
+ 2
是( ) ☆☆☆☆
A.正极反应为:VO
2
++2H
+
+e﹣═VO2++H
2
O
B.负极附近的溶液由绿色逐渐变为紫色
C.反应每生成 1mol H O 时电子转移的物质的量
2
为 0.5mol
D.原电池使用过程中溶液的 pH 值逐渐增大
【解答】
A.分析可知放电过程中,正极附近发生反应:VO
2
++2H
+
+e﹣=VO2++H
2
O,
故 A 正确;
B.反应中 V2+离子被氧化,应是电源的负极,负极发生失电子的氧化反应,
即反应为 V2+=V3++e﹣,V2+(绿色)变化为 V3+(紫色),故 B 正确;
C.VO +(黄色)+V2+(绿色)+2H ═VO2+(蓝色)+H O+V3+(紫色),反应
2 + 2
每生成 1mol H O 时电子转移的物质的量为 1mol,故 C 错误;
2
D.原电池反应方程式中消耗氢离子,同时生成水,因此氢离子浓度降低,溶
第 7页(共 22页)液 pH 增大,故 D 正确。
故选:C。
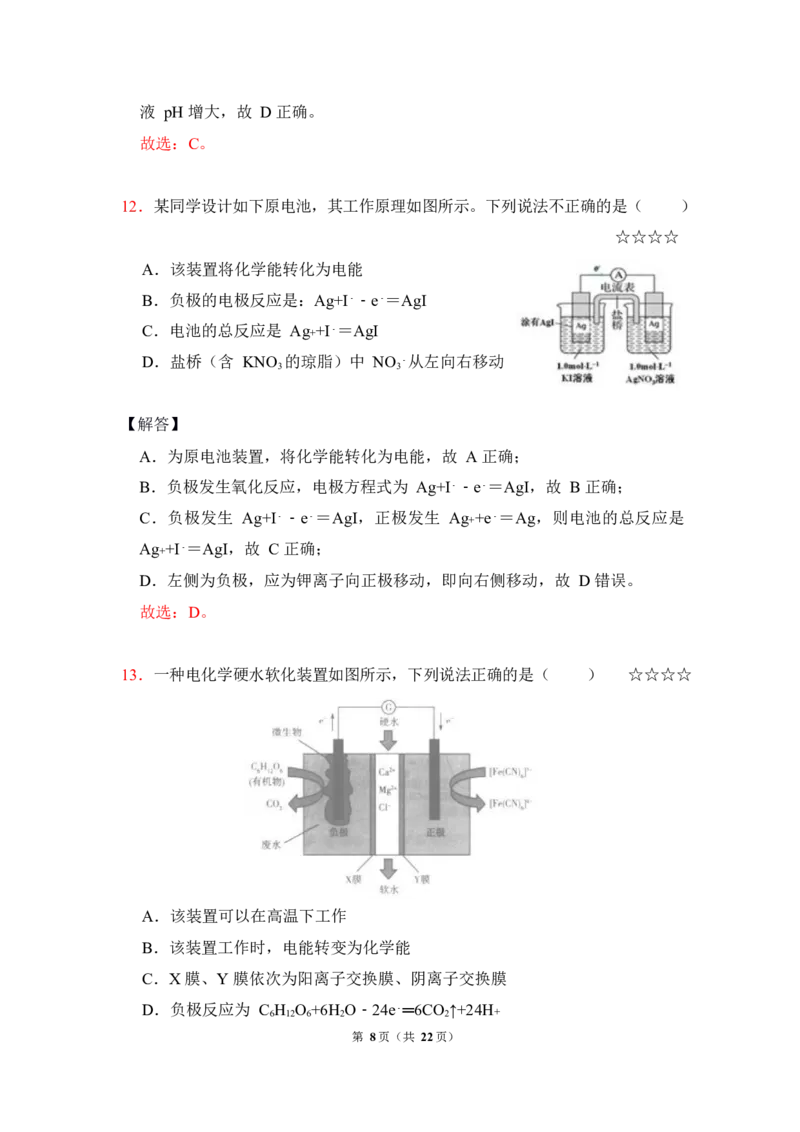
12.某同学设计如下原电池,其工作原理如图所示。下列说法不正确的是( )
☆☆☆☆
A.该装置将化学能转化为电能
B.负极的电极反应是:Ag+I﹣﹣e﹣=AgI
C.电池的总反应是 Ag
+
+I﹣=AgI
D.盐桥(含 KNO 的琼脂)中 NO ﹣从左向右移动
3 3
【解答】
A.为原电池装置,将化学能转化为电能,故 A 正确;
B.负极发生氧化反应,电极方程式为 Ag+I﹣﹣e﹣=AgI,故 B 正确;
C.负极发生 Ag+I﹣﹣e﹣=AgI,正极发生 Ag
+
+e﹣=Ag,则电池的总反应是
Ag
+
+I﹣=AgI,故 C 正确;
D.左侧为负极,应为钾离子向正极移动,即向右侧移动,故 D 错误。
故选:D。
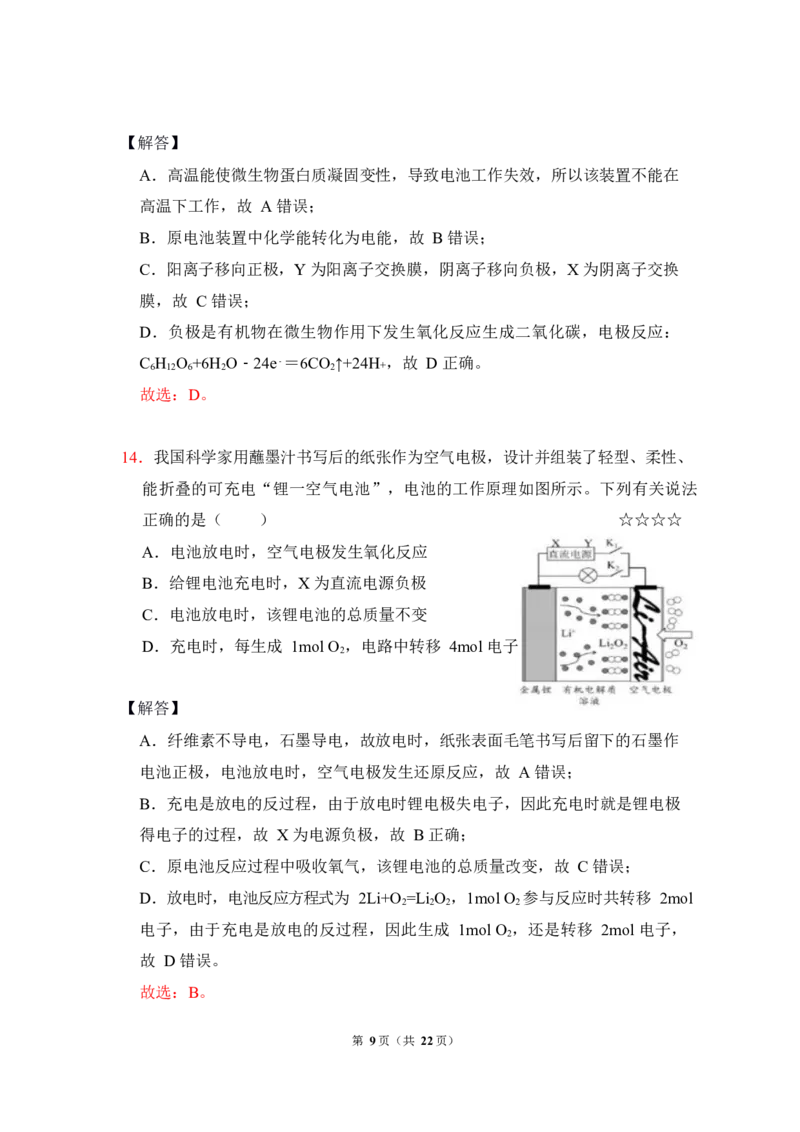
13.一种电化学硬水软化装置如图所示,下列说法正确的是( ) ☆☆☆☆
A.该装置可以在高温下工作
B.该装置工作时,电能转变为化学能
C.X 膜、Y 膜依次为阳离子交换膜、阴离子交换膜
D.负极反应为 C
6
H
12
O
6
+6H
2
O﹣24e﹣═6CO
2
↑+24H
+
第 8页(共 22页)【解答】
A.高温能使微生物蛋白质凝固变性,导致电池工作失效,所以该装置不能在
高温下工作,故 A 错误;
B.原电池装置中化学能转化为电能,故 B 错误;
C.阳离子移向正极,Y 为阳离子交换膜,阴离子移向负极,X 为阴离子交换
膜,故 C 错误;
D.负极是有机物在微生物作用下发生氧化反应生成二氧化碳,电极反应:
C
6
H
12
O
6
+6H
2
O﹣24e﹣=6CO
2
↑+24H
+
,故 D 正确。
故选:D。
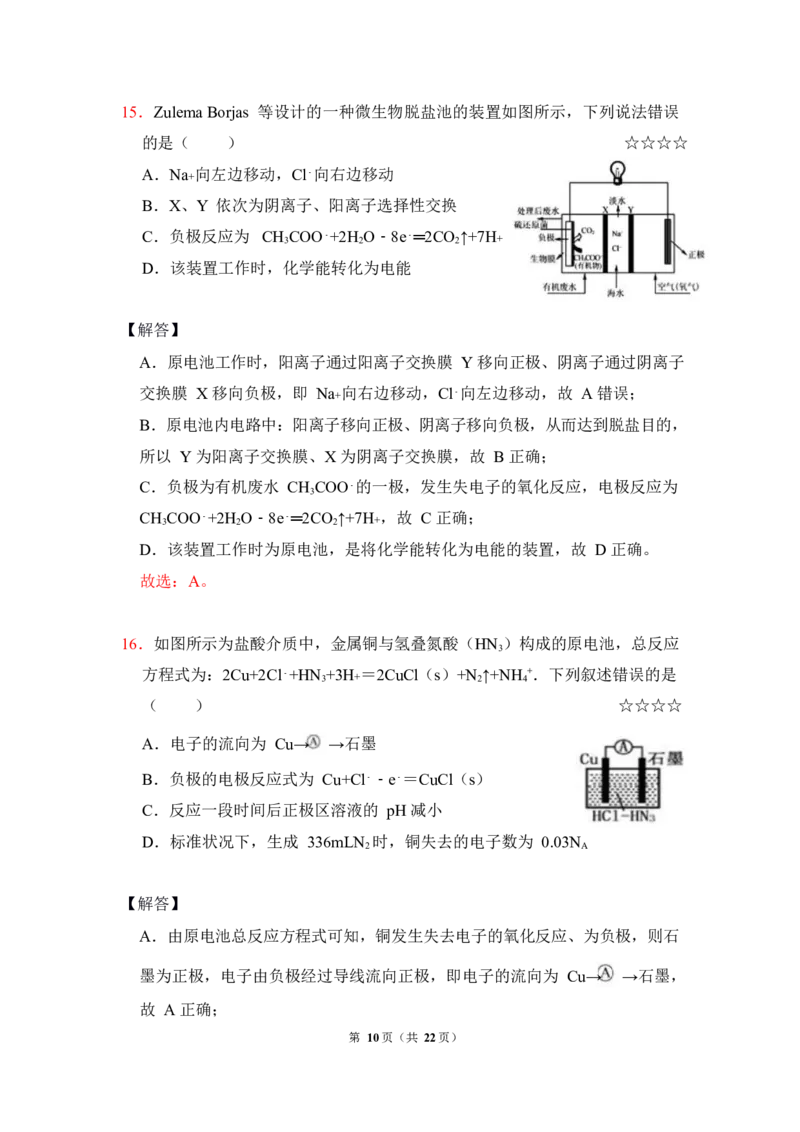
14.我国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、
能折叠的可充电“锂一空气电池”,电池的工作原理如图所示。下列有关说法
正确的是( ) ☆☆☆☆
A.电池放电时,空气电极发生氧化反应
B.给锂电池充电时,X 为直流电源负极
C.电池放电时,该锂电池的总质量不变
D.充电时,每生成 1mol O ,电路中转移 4mol 电子
2
【解答】
A.纤维素不导电,石墨导电,故放电时,纸张表面毛笔书写后留下的石墨作
电池正极,电池放电时,空气电极发生还原反应,故 A 错误;
B.充电是放电的反过程,由于放电时锂电极失电子,因此充电时就是锂电极
得电子的过程,故 X 为电源负极,故 B 正确;
C.原电池反应过程中吸收氧气,该锂电池的总质量改变,故 C 错误;
D.放电时,电池反应方程式为 2Li+O =Li O ,1mol O 参与反应时共转移 2mol
2 2 2 2
电子,由于充电是放电的反过程,因此生成 1mol O ,还是转移 2mol 电子,
2
故 D 错误。
故选:B。
第 9页(共 22页)15.Zulema Borjas 等设计的一种微生物脱盐池的装置如图所示,下列说法错误
的是( ) ☆☆☆☆
A.Na
+
向左边移动,Cl﹣向右边移动
B.X、Y 依次为阴离子、阳离子选择性交换
C.负极反应为 CH
3
COO﹣+2H
2
O﹣8e﹣═2CO
2
↑+7H
+
D.该装置工作时,化学能转化为电能
【解答】
A.原电池工作时,阳离子通过阳离子交换膜 Y 移向正极、阴离子通过阴离子
交换膜 X 移向负极,即 Na
+
向右边移动,Cl﹣向左边移动,故 A 错误;
B.原电池内电路中:阳离子移向正极、阴离子移向负极,从而达到脱盐目的,
所以 Y 为阳离子交换膜、X 为阴离子交换膜,故 B 正确;
C.负极为有机废水 CH COO﹣的一极,发生失电子的氧化反应,电极反应为
3
CH
3
COO﹣+2H
2
O﹣8e﹣═2CO
2
↑+7H
+
,故 C 正确;
D.该装置工作时为原电池,是将化学能转化为电能的装置,故 D 正确。
故选:A。
16.如图所示为盐酸介质中,金属铜与氢叠氮酸(HN )构成的原电池,总反应
3
方程式为:2Cu+2Cl﹣+HN
3
+3H
+
=2CuCl(s)+N
2
↑+NH
4
+.下列叙述错误的是
( ) ☆☆☆☆
A.电子的流向为 Cu→ →石墨
B.负极的电极反应式为 Cu+Cl﹣﹣e﹣=CuCl(s)
C.反应一段时间后正极区溶液的 pH 减小
D.标准状况下,生成 336mLN 时,铜失去的电子数为 0.03N
2 A
【解答】
A.由原电池总反应方程式可知,铜发生失去电子的氧化反应、为负极,则石
墨为正极,电子由负极经过导线流向正极,即电子的流向为 Cu→ →石墨,
故 A 正确;
第 10页(共 22页)B.负极为铜电极,结合电池反应得到负极的电极反应式为 Cu+Cl﹣﹣e﹣=CuCl
(s),故 B 正确;
C.原电池正极电极反应:HN
3
+3H
+
+2e﹣=N
2
+NH
4
+,由于消耗了氢离子,所
以正极区溶液 pH 增大,故 C 错误;
D.负极的电极反应式为 Cu+Cl﹣﹣e﹣=CuCl(s),正极电极反应:HN
3
+3H
+
+2e
ꢁꢁꢁꢁꢁꢁꢁꢁꢁꢁꢁꢁꢁꢁ鑀୯୯ʞ끄
﹣=N+NH+,标准状况下,n(N)ꢀ ꢀꢀ0.015mol,则电子转移 0.03mol,
2 4 2 ꢀꢀ鑀Ǥ끄
Ͷꢀܮꢀ
即铜转移的电子数为 0.03N ,故 D 正确。
A
故选:C。
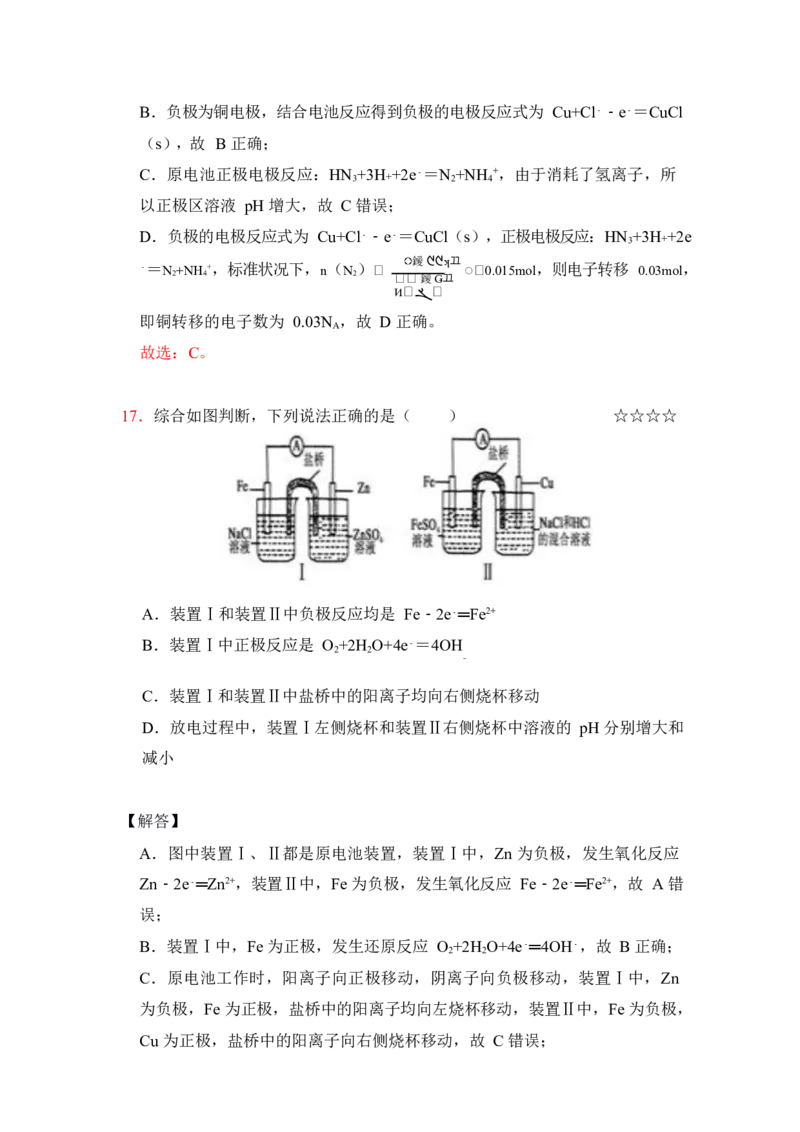
17.综合如图判断,下列说法正确的是( ) ☆☆☆☆
A.装置Ⅰ和装置Ⅱ中负极反应均是 Fe﹣2e﹣═Fe2+
B.装置Ⅰ中正极反应是 O +2H O+4e﹣=4OH
2 2
﹣
C.装置Ⅰ和装置Ⅱ中盐桥中的阳离子均向右侧烧杯移动
D.放电过程中,装置Ⅰ左侧烧杯和装置Ⅱ右侧烧杯中溶液的 pH 分别增大和
减小
【解答】
A.图中装置Ⅰ、Ⅱ都是原电池装置,装置Ⅰ中,Zn 为负极,发生氧化反应
Zn﹣2e﹣═Zn2+,装置Ⅱ中,Fe 为负极,发生氧化反应 Fe﹣2e﹣═Fe2+,故 A 错
误;
B.装置Ⅰ中,Fe 为正极,发生还原反应 O +2H O+4e﹣═4OH﹣,故 B 正确;
2 2
C.原电池工作时,阳离子向正极移动,阴离子向负极移动,装置Ⅰ中,Zn
为负极,Fe 为正极,盐桥中的阳离子均向左烧杯移动,装置Ⅱ中,Fe 为负极,
Cu 为正极,盐桥中的阳离子向右侧烧杯移动,故 C 错误;第 11页(共 22页)D.放电过程中,装置Ⅰ左侧烧杯,发生还原反应 O +2H O+4e﹣═4OH﹣,生
2 2
成碱,装置 II 右侧烧杯中,发生还原反应 2H
+
+2e﹣═H
2
↑,消耗盐酸,故溶液
的 pH 均增大,故 D 错误。
故选:B。
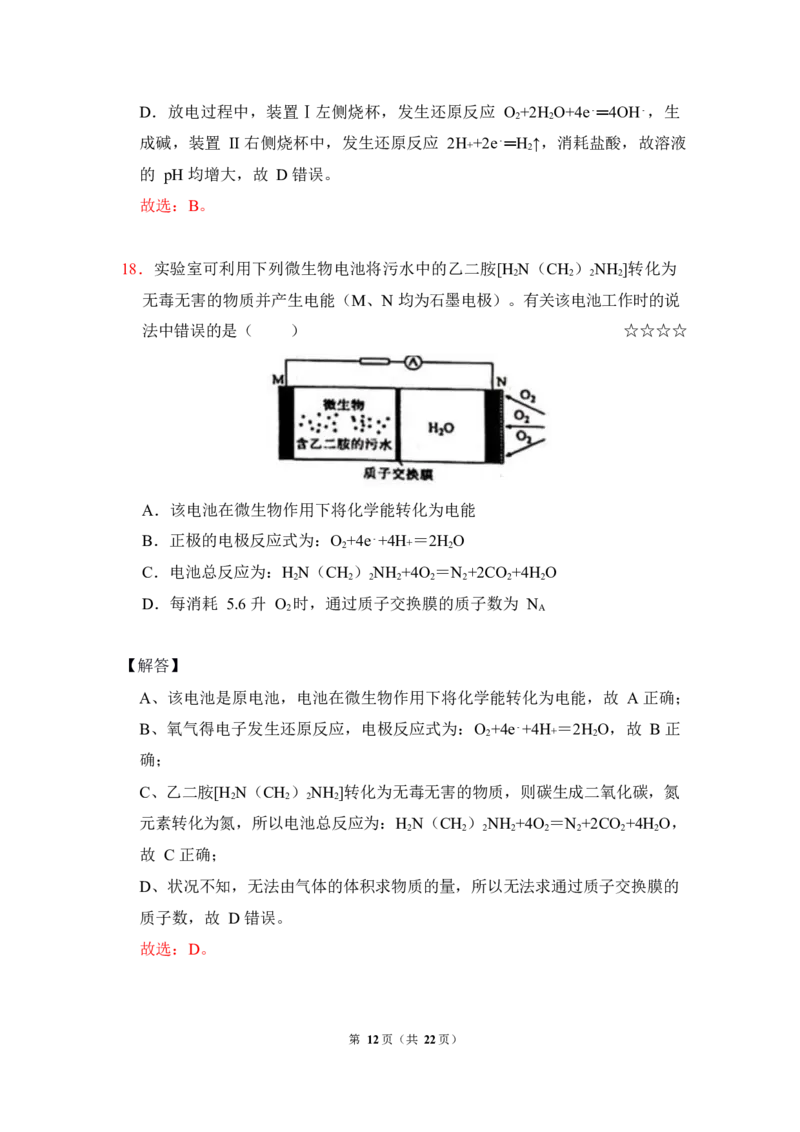
18.实验室可利用下列微生物电池将污水中的乙二胺[H N(CH ) NH ]转化为
2 2 2 2
无毒无害的物质并产生电能(M、N 均为石墨电极)。有关该电池工作时的说
法中错误的是( ) ☆☆☆☆
A.该电池在微生物作用下将化学能转化为电能
B.正极的电极反应式为:O
2
+4e﹣+4H
+
=2H
2
O
C.电池总反应为:H N(CH ) NH +4O =N +2CO +4H O
2 2 2 2 2 2 2 2
D.每消耗 5.6 升 O 时,通过质子交换膜的质子数为 N
2 A
【解答】
A、该电池是原电池,电池在微生物作用下将化学能转化为电能,故 A 正确;
B、氧气得电子发生还原反应,电极反应式为:O
2
+4e﹣+4H
+
=2H
2
O,故 B 正
确;
C、乙二胺[H N(CH ) NH ]转化为无毒无害的物质,则碳生成二氧化碳,氮
2 2 2 2
元素转化为氮,所以电池总反应为:H N(CH ) NH +4O =N +2CO +4H O,
2 2 2 2 2 2 2 2
故 C 正确;
D、状况不知,无法由气体的体积求物质的量,所以无法求通过质子交换膜的
质子数,故 D 错误。
故选:D。
第 12页(共 22页)19.银质器皿日久表面会逐渐变黑,这是生成了 Ag S 的缘故。根据电化学原理
2
可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器浸入该溶液
中,一段时间后发现黑色会褪去。下列说法正确的是( ) ☆☆☆☆☆
A.银器为正极,Ag S 生成 Ag 单质与硫单质
2
B.该过程中总反应为 2Al+3Ag S=6Ag+Al S
2 2 3
C.黑色褪去的原因是黑色 Ag S 转化为白色 AgCl
2
D.处理过程中银器质量首先不断减轻,最后不再改变
【解答】
A.银作正极,正极上 Ag S 得电子作氧化剂,在反应中被还原生成单质银,
2
同时生成硫离子,故 A 错误;
B.Al S 在溶液中不能存在,会发生双水解反应生成 H S 和 Al(OH) ,故 B
2 3 2 3
错误;
C.黑色褪去是 Ag S 转化为 Ag 而不是 AgCl,故 C 错误;
2
D.银表面的 Ag S 得电子,析出单质银,电极反应式为 Ag S+2e﹣+2H O=
2 2 2
2Ag+2OH﹣+H S↑,所以银器质量减小,完全反应后质量不再改变,故 D 正确。
2
故选:D。
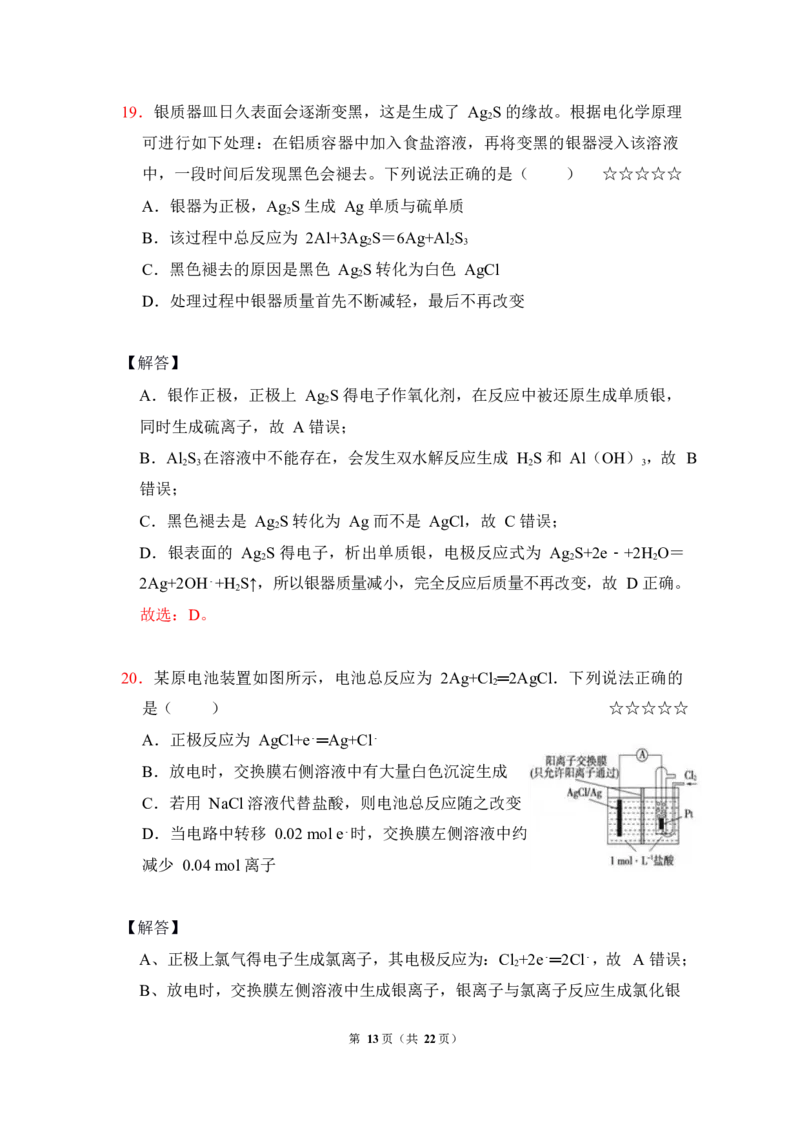
20.某原电池装置如图所示,电池总反应为 2Ag+Cl ═2AgCl.下列说法正确的
2
是( ) ☆☆☆☆☆
A.正极反应为 AgCl+e﹣═Ag+Cl﹣
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用 NaCl 溶液代替盐酸,则电池总反应随之改变
D.当电路中转移 0.02 mol e﹣时,交换膜左侧溶液中约
减少 0.04 mol 离子
【解答】
A、正极上氯气得电子生成氯离子,其电极反应为:Cl +2e﹣═2Cl﹣,故 A 错误;
2
B、放电时,交换膜左侧溶液中生成银离子,银离子与氯离子反应生成氯化银
第 13页(共 22页)沉淀,所以交换膜左侧溶液中有大量白色沉淀生成,故 B 错误;
C、电池总反应为 2Ag+Cl ═2AgCl 可知,用 NaCl 溶液代替盐酸,电池的总反
2
应不变,故 C 错误;
D、放电时,当电路中转移 0.02mol e﹣时,交换膜左则会有 0.02mol 氢离子通
过阳离子交换膜向正极移动,同时会有 0.02molAg 失去 0.02mol 电子生成银离
子,银离子会与氯离子反应生成氯化银沉淀,所以氯离子会减少 0.02mol,则
交换膜左侧溶液中共约减少 0.04mol 离子,故 D 正确。
故选:D。
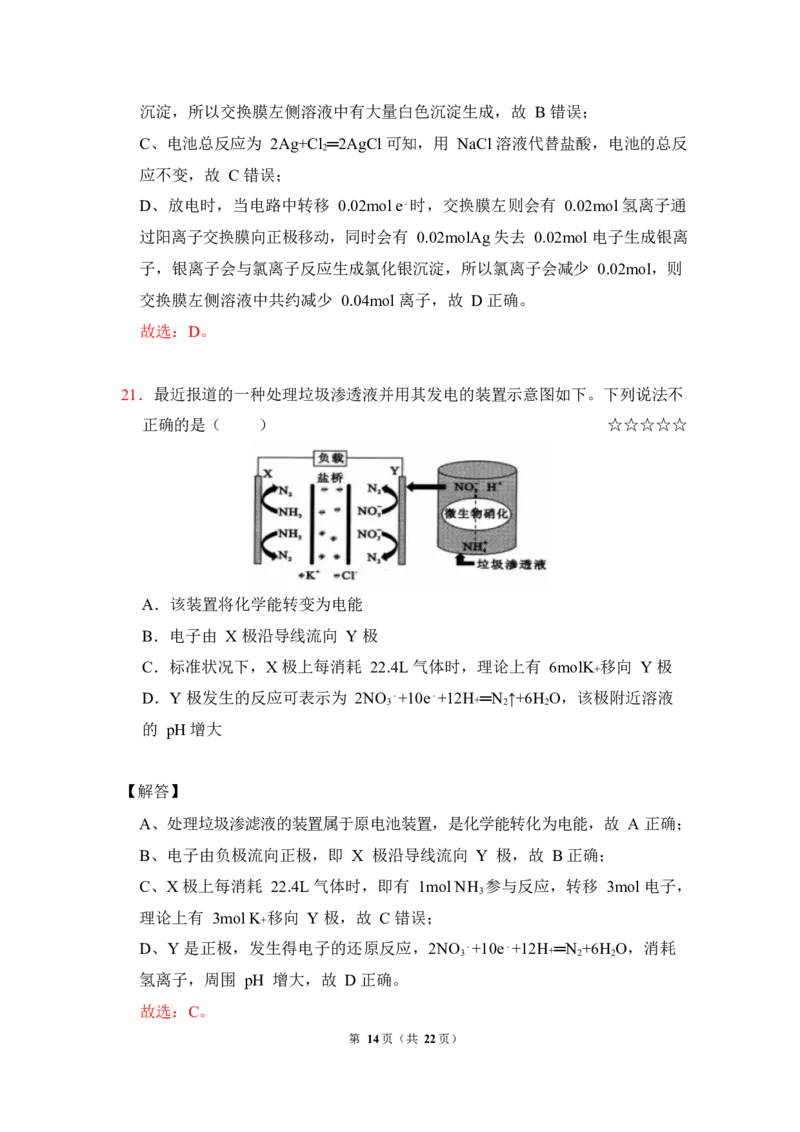
21.最近报道的一种处理垃圾渗透液并用其发电的装置示意图如下。下列说法不
正确的是( ) ☆☆☆☆☆
A.该装置将化学能转变为电能
B.电子由 X 极沿导线流向 Y 极
C.标准状况下,X 极上每消耗 22.4L 气体时,理论上有 6molK 移向 Y 极
+
D.Y 极发生的反应可表示为 2NO
3
﹣+10e﹣+12H
+
═N
2
↑+6H
2
O,该极附近溶液
的 pH 增大
【解答】
A、处理垃圾渗滤液的装置属于原电池装置,是化学能转化为电能,故 A 正确;
B、电子由负极流向正极,即 X 极沿导线流向 Y 极,故 B 正确;
C、X 极上每消耗 22.4L 气体时,即有 1mol NH 参与反应,转移 3mol 电子,
3
理论上有 3mol K 移向 Y 极,故 C 错误;
+
D、Y 是正极,发生得电子的还原反应,2NO
3
﹣+10e﹣+12H
+
═N
2
+6H
2
O,消耗
氢离子,周围 pH 增大,故 D 正确。
故选:C。
第 14页(共 22页)22.磷酸亚佚锂( LiFePO )电池(如图所示)是新能源汽车的动力电池之一。
4
M 电极是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传
导 Li 的高分子材料,隔膜只允许 Li 通过,电池的总反应为
+ +
放电
Li C +Li FePO ꢀ LiFePO +6C。下列说法正确的是( ) ☆☆☆☆☆
X 6 1﹣x 4 4
充电
A.放电时,Li 向 M 电极移动
+
B.充电时电路中每通过 0.5mol 电子,就有 36g 碳和金属锂复合在一起
C.放电时,M 电极的电极反应为 C x﹣﹣xe﹣=6C
6
D.充电时,N 电极的电极反应为 LiFePO
4
﹣xe﹣=xLi
+
+Li
1﹣x
FePO
4
【解答】
A、放电时阳离子移向正极 N,所以 Li 从 M 边移向 N 边,故 A 错误;
+
B、充电时,M 极连接电源的负极,反应式为 6C+xLi
+
+xe﹣=Li
x
C
6
,所以电路
୯ʞ
中通过 0.5mol 电子,消耗 gC,故 B 错误;
ꢀꢀ
C、放电时,M 是负极,发生失电子的氧化反应,电极反应式为:Li C ﹣xe
x 6
﹣
=6C+xLi ,故 C 错误;
+
D、充电时,N 极连接电源的正极,电极反应式与正极相反,则反应式为:
LiFePO
4
﹣xe﹣═Li
1﹣x
FeO
4
+xLi
+
,故 D 正确。
故选:D。
23.利用生物燃料电池原理研究室温下氨的合成,电池工作时 MV2+/MV 在电极
+
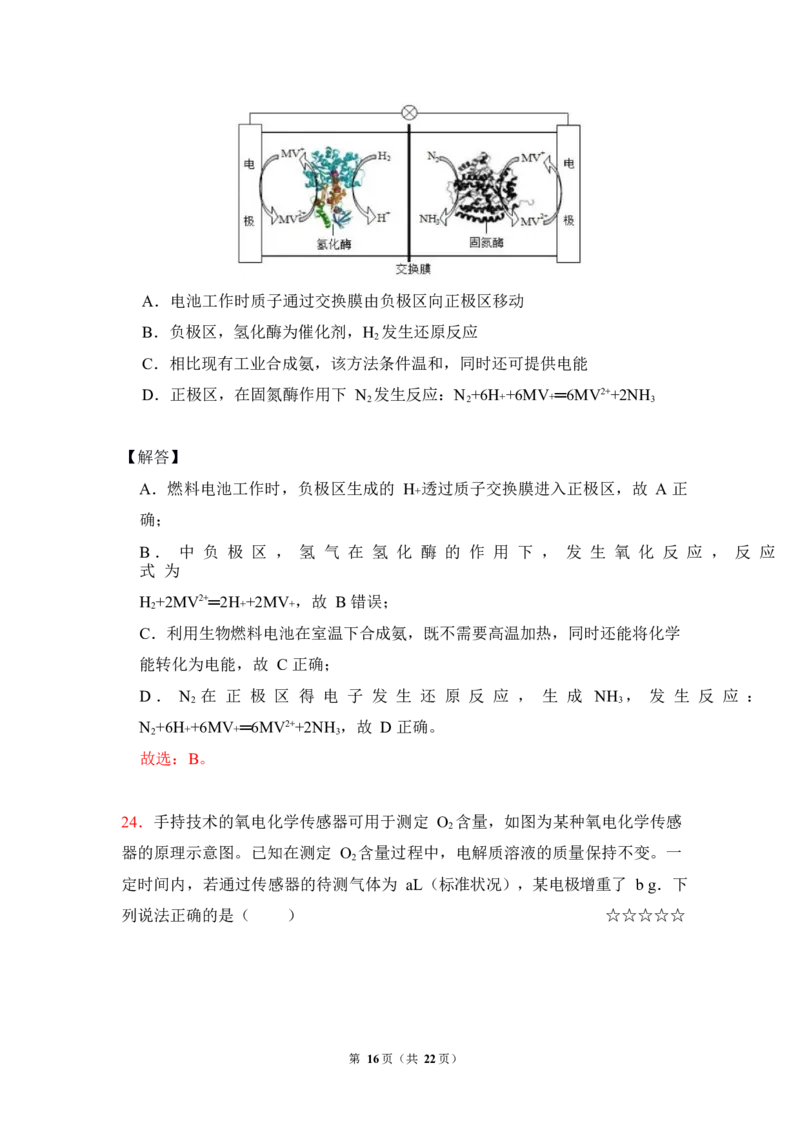
与酶之间传递电子,示意图如图所示。下列说法错误的是( ) ☆☆☆☆☆第 15页(共 22页)A.电池工作时质子通过交换膜由负极区向正极区移动
B.负极区,氢化酶为催化剂,H 发生还原反应
2
C.相比现有工业合成氨,该方法条件温和,同时还可提供电能
D.正极区,在固氮酶作用下 N 发生反应:N +6H +6MV ═6MV2++2NH
2 2 + + 3
【解答】
A.燃料电池工作时,负极区生成的 H 透过质子交换膜进入正极区,故 A 正
+
确;
B . 中 负 极 区 , 氢 气 在 氢 化 酶 的 作 用 下 , 发 生 氧 化 反 应 , 反 应
式 为
H +2MV2+═2H +2MV ,故 B 错误;
2 + +
C.利用生物燃料电池在室温下合成氨,既不需要高温加热,同时还能将化学
能转化为电能,故 C 正确;
D . N 在 正 极 区 得 电 子 发 生 还 原 反 应 , 生 成 NH , 发 生 反 应 :
2 3
N +6H +6MV ═6MV2++2NH ,故 D 正确。
2 + + 3
故选:B。
24.手持技术的氧电化学传感器可用于测定 O 含量,如图为某种氧电化学传感
2
器的原理示意图。已知在测定 O 含量过程中,电解质溶液的质量保持不变。一
2
定时间内,若通过传感器的待测气体为 aL(标准状况),某电极增重了 b g.下
列说法正确的是( ) ☆☆☆☆☆
第 16页(共 22页)A.氧电化学传感器工作时,电流由 Pb 电极通过外电路流向 Pt 电极
B.Pb 上发生的电极反应式为 Pb﹣2e﹣+2OH﹣═Pb(OH) ↓
2
ꢀꢀ
C.反应过程中转移电子的物质的量为 b
Ǥ
ꢀꢀꢀ
D.待测气体中氧气的物质的量的分数为
ꢀꢀꢀݑ
【解答】
A.得电子发生还原反应的电极是正极、失电子发生氧化反应的电极是负极,
电子由 Pb 电极通过外电路流向 Pt 电极,故 A 错误;
B.在测定 O 含量过程中,电解质溶液的质量保持不变,说明 Pt 电极消耗的
2
氧气与 Pb 电极上得到的 O 原子质量相等,其电池反应式为 2Pb+O =2PbO,
2
所以 Pb 电极上 Pb 失电子和 OH﹣反应生成 PbO,电极反应式为 2Pb+4OH﹣﹣
4e﹣═2PbO+2H O,故 B 错误;
2
C.放电过程中,Pb 电极质量增加,增加的质量为氧元素质量,如果电极质
ꢀꢀ ꢀ
量增加 bg,则生成 n(PbO)=n(O)ꢀ ꢀ
ꢀꢀʞꢀͶꢀ mol,根据 2Pb+4OH﹣﹣
ܮꢀ ꢀꢀʞ
4e﹣═2PbO+2H O 得转移 n(e﹣)=2n(PbO)=0.125bmol,故 C 错误;
2
ꢀꢀ ꢀꢀ
D . 根 据 转 移 电 子 相 等 得 n ( bmol , 氧 气 体
ꢀ ୯
O 2 ) ꢀ n ( PbO ) ꢀ ꢀ 积
ꢀꢀ ꢀ ꢀꢀꢀ
ꢀ bmol×22.4L/mol=0.7bL,待测氧气体积分数ꢀ 鑀ꢁ ꢀ ,故 D 正确。
ꢁ
୯ꢀ 끄 ꢀꢀꢀݑ
ݑ끄
故选:D。
25.将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。若该电
池中两电极的总质量为 60g,工作一段时间后,取出锌片和银片洗净干燥后称量,总质量为 47g,则产生标况下的氢气 升,导线上转移的电子
第 17页(共 22页)N 。 ☆☆☆
A
【解答】
银片和锌片分别作原电池的正负极,当发生反应时,负极材料失电子变成离
子进入溶液,质量减少;正极材料不参加反应,所以本题质量减少的量是锌
的质量。锌减少的质量为 60g﹣47g=13g,设生成氢气的体积是 V,转移电子
是 x。
Zn+H SO =ZnSO +H ↑ 2e
2 4 4 2
﹣
65g 22.4L 2
13g V x
ꢀꢀꢀ鑀Ǥꢀꢀ୯ ꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁꢀꢁ୯
ʞꢀ ʞꢀ
即产生氢气的体积为 mol=0.4mol,数目是 0.4N 。
A
L=4.48L,xꢀ
故答案为:4.48;0.4。
26.原电池可将化学能转化为电能。若 Fe、Cu 和浓硝酸构成原电池,负极是
(填“Cu”或“Fe”); 若 Zn、Ag 和稀盐酸构成原电池,正极发生 反应(填
“氧化“或还原”)。质量相同的铜棒和锌棒用导线连接后插入 CuSO 溶液中,
4
一段时间后,取出洗净、干燥、称量,二者质量差为 12.9g。则导线中通过的
电子的物质的量是 mol。 ☆☆☆☆
【解答】
该原电池中,Fe 和浓硝酸发生钝化现象,Cu 易和浓硝酸发生氧化反应而作负
极,Fe 作正极;Zn、Ag 和稀盐酸构成的原电池中,Zn 易失电子作负极、Ag
作正极,正极上得电子被还原,发生还原反应;质量相同的铜棒和锌棒用导
线连接后插入 CuSO 溶液中,负极上 Zn 失电子生成锌离子进入溶液,正极上
4
铜离子得电子生成 Cu,一段时间后,二者质量差为 12.9g,二者质量差为溶解
的 Zn 和析出的 Cu 质量之和,设转移电子物质的量为 n,则二者质量差=
ꢀ ꢀ
(65ꢀ ꢀ64ꢀ
ꢀꢀ ꢀꢀ
)g=12.9g,n=0.2mol,
故答案为:Cu;还原;0.2。第 18页(共 22页)27.通常氢氧燃料电池有酸式和碱式两种,试回答下列问题: ☆☆☆☆
(1)在酸式介质中,负极反应的物质为 ,正极反应的物质为 ,
酸式电池的电极反应:负极: ,正极: ,电解质溶液 pH 的变
化 (填“变大”,“变小”,“不变”)
(2)在碱式介质中,碱式电池的电极反应:负极: ,正极: ,
电解质溶液 pH 的变化 (填“变大”,“变小”,“不变”)
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不
正确的是 。
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀 HSO、KOH 为介质的氢氧燃料电池的负极电极反应式相同
2 4
D.以稀 HSO、KOH 为介质的氢氧燃料电池的总反应式相同
2 4
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:
放电
3Zn+2KFeO+8HO 3Zn(OH)+2Fe(OH)+4KOH。
2 4 2 2 3
充电
⇌
①该电池放电时负极反应式为 。
②放电时每转移 3mol 电子,正极有 mol KFeO 被还原。
2 4
(5)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。电
放电
池反应式为:Li MnO+Li LiMnO,下列有关说法不正确的是 。
1﹣x 4 x 4
充电
⇌
A.放电时电池的正极反应式为:Li
1﹣x
MnO
4
+xLi
+
+xe﹣═LiMnO
4
B.放电过程中,石墨没有得失电子
C.该电池也能在 KOH 溶液的环境中正常工作
D.充电时电池上标有“﹣”的电极应与外接电源的负极相连。
【解答】
(1)在酸性氢氧燃料电池中,石墨作电极,在负极由氢气失电子生成氢离子,
电极反应为 2H
2
﹣4e﹣=4H
+
;在正极由氧气得电子生成氢氧根离子,生成的氢
氧根离子结合氢离子生成水,电极反应为 O
2
+4e﹣+4H
+
=2H
2
O,总电极反应式为
第 19页(共 22页)2H+O2HO,水的总量增加,故 pH 变大
2 2 2
故答案为:H;O;2H
2 2
2
﹣4e﹣=4H
+
;O
2
+4e﹣+4H
+
=2H
2
O;变大;
(2)在碱式介质中,氢气在负极失去电子生成氢离子,氢离子结合氢氧根离
子生成水,电极反应式为 2H
﹣4e﹣+4OH﹣=2HO;氧气在正极得电子生成氢氧
2 2
根离子,电极反应式为 O+4e﹣+2HO=4OH﹣,总电极反应式为 2H+O=2HO,水
2 2 2 2 2
的总量增加,故 pH 变小
故答案为:2H
﹣4e﹣+4OH﹣=2HO;O+4e﹣+2HO=4OH﹣;变小;
2 2 2 2
(3)A、电解获得 H 消耗较多的能量,而在催化剂作用下利用太阳能来分解
2
HO 获得 H 更为科学,故 A 正确;
2 2
B、氢氧燃料电池产物 HO 无污染,能有效保护环境,故 B 正确;
2
C、以稀 HSO、KOH 为介质的氢氧燃料电池的负极电极反应式分别为:H﹣2e
2 4 2
﹣═4H
+
,H
2
﹣2e﹣+2OH﹣=2H
2
O,不相同,故 C 错误;
D、以稀 HSO、KOH 为介质的氢氧燃料电池的总反应式均为 2H+O=2HO,故 D
2 4 2 2 2
正确。
故答案为:C;
(4)①放电时,负极上锌失电子发生氧化反应,电极反应式为:
Zn﹣2e﹣+2OH﹣═Zn(OH),
2
故答案为:Zn﹣2e﹣+2OH﹣═Zn(OH);
2
②放电时,正极上 1mol KFeO 得 3mol 电子发生还原反应生成
2 4
1mol Fe(OH),所以每转移 3mol 电子,正极有 1mol KFeO 被还原
3 2 4
故答案为:1;
(5)A、根据总反应式可知 Li 失去电子,电池负极反应式为:xLi﹣xe﹣═xLi
+
,
由总反应式减去负极反应式可得放电时的正极反应式为:
Li +xLi
4
1﹣x
MnO
+
+xe﹣═LiMnO
4
,故 A 正确;
放电
B、放电过程中,根据总反应式 Li MnO+Li LiMnO,可判断石墨没有电子
1﹣x 4 x 4
充电
⇌
得失,故 B 正确;
C、Li 能与 KOH 溶液中的 HO 反应,导致电池无法正常工作,故 C 错误;
2
D、充电过程是放电的逆向过程,外界电源的负极提供的电子使原电池负极获第 20页(共 22页)得电子发生还原反应,所以标有“﹣”的电极应与外接电源的负极相连,故 D
正确。
故答案为:C。
28.化学电源在通讯、交通及日常生活中有着广泛的应用.请回答下列问题:
☆☆☆☆
(1)锌锰电池是最早使用的干电池,两极材料分别是锌和石墨棒,电池内部
填充的是糊状的 MnO 和 NHCl,该电池的负极材料是: ,由于使用寿
2 4
命短,易腐蚀用电器,电解质更换为 KOH,电极反应产物为 Zn(OH) 和 MnO
2
(OH),试写出碱性锌锰干电池的负极反应式:
(2)铅蓄电池是使用广泛的充电电池,其电极材料分别是 Pb 和 PbO,电解
2
液为稀硫酸.工作时该电池总反应式为 Pb+PbO+2HSO═2PbSO+2HO 根据上述
2 2 4 4 2
情况判断:
①正极材料是 ;负极的电极反应式: .
②工作时,电解质溶液的密度 (填“增大”“减小”或“不变”),电
解质溶液中的阴离子移向 极,电流由 极流向 极(填电
极材料的化学式).
③当铅蓄电池向外电路提供 1mol 电子时,理论上负极板的质量增加 g.
(3)锂离子电池是一种高能电池,可用于心脏起搏器.该电池的电极材料分
别为锂和碳,电解液是 LiAlCl-SOCl.电池的总反应可表示为 4Li+2SOCl═
4 2 2
4LiCl+S+SO↑.
2
请回答下列问题:
①电池的负极材料为 ,发生的电极反应为:
②组装该电池必须在无水、无氧的条件下进行,原因是: .
【解答】
(1)锌锰电池失电子的一极为负极,则 Zn 失电子为负极;碱性条件下,Zn
失电子生成 Zn(OH),负极的电极方程式为:Zn﹣2e﹣+2OH﹣═Zn(OH);
2 2
故答案为:Zn;Zn﹣2e﹣+2OH﹣═Zn(OH);
2
第 21页(共 22页)(2)①根据电池反应式知,Pb 元素化合价由 0 价、+4 价变为+2 价,得电子
化合价降低的反应物为正极,则 PbO 为正极;失电子化合价升高的金属为负
2
极,则 Pb 为负极,负极的电极方程式为 Pb﹣2e
﹣+SO 2﹣═PbSO,
4
4
故答案为:PbO;Pb﹣2e﹣+SO 2﹣═PbSO;
2 4
4
②放电时,正负极上都消耗硫酸,同时生成硫酸铅沉淀,溶液的密度减小,
电解质溶液中阳离子向正极移动、阴离子向负极移动,即阴离子向 Pb 极移动;
电流从正极流向负极,即从 PbO 极向 Pb 极移动;
2
故答案为:减小; Pb; PbO;Pb;
2
(3)①电池的负极材料为锂,其电极反应式为:Li﹣e﹣═Li
+
,
故答案为:锂;Li﹣e﹣═Li
+
;
②Li 是活泼金属,能与水氧气等发生反应,所以组装该电池必须在无水、无
氧的条件下进行,
故答案为:锂能与水、氧气发生化学反应.第 22页(共 22页)