文档内容
钠及其化合物作业题
作业题目难度分为 3 档:三星☆☆☆(基础题目)
四星☆☆☆☆(中等题目)
五星☆☆☆☆☆(较难题目)
本套作业题目 1-5,11-12,14-15 题为三星,6—10,13 为四星,16 为四星
1.下列有关钠的物理性质的叙述中正确的是( ) ☆☆☆
①银白色金属; ②质软,可以用小刀切割; ③熔点低于 100℃;
④密度比水小; ⑤热和电的良导体.
A.①②④ B.①②③④ C.①③④ D.①②③④⑤
【解答】
钠是第 IA 族元素,为银白色金属单质,有金属光泽;质地较软,可以用小刀切
割;将钠放入水中,钠会立即熔成小球,说明熔点较低;钠能浮在水面上,说明
钠的密度较小,钠是金属,含有自由移动的电子,所以是热和电的良导体;
故选 D.
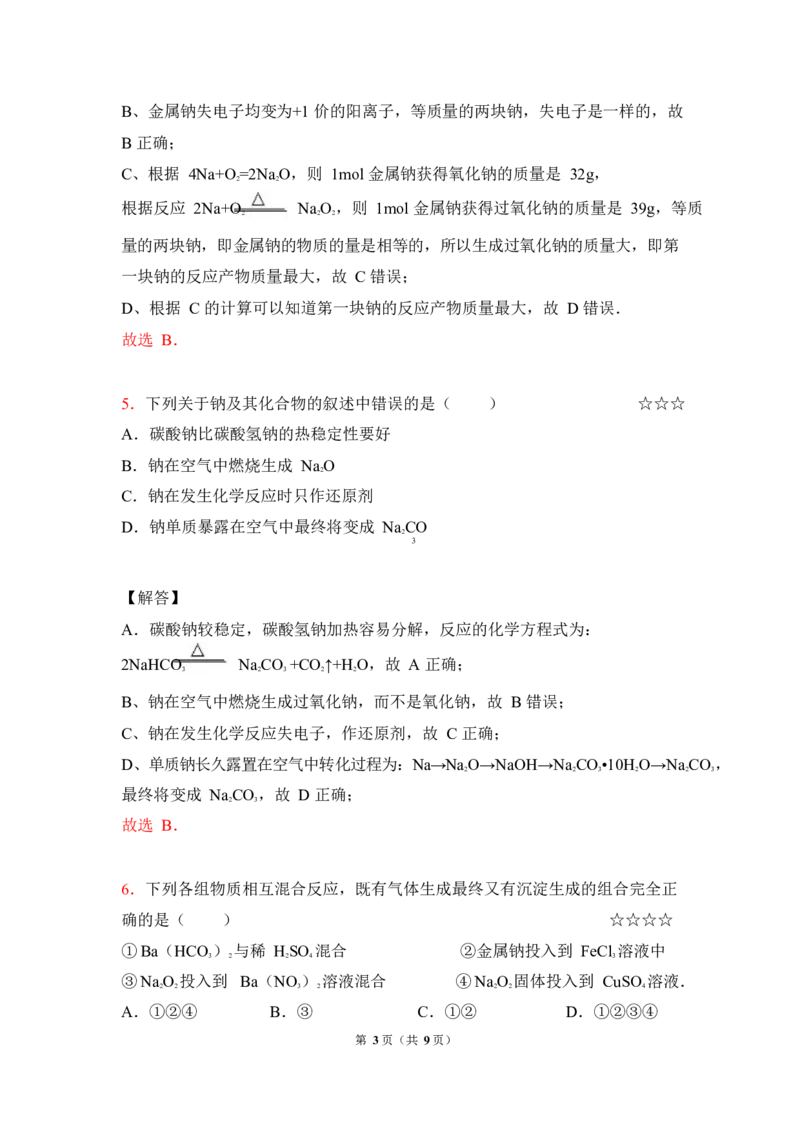
2.如图,烧杯中盛有等体积的水和煤油,现将一小块金属钠加入烧杯中,试推
断能观察到的实验现象应是( ) ☆☆☆
A.钠悬浮在煤油层中 B.钠静止在两液面之间
C.钠沉入水底下 D.钠在两液体界面附近上下跳动
【解答】
因钠的密度比水小,比煤油大,因此介于两者之间,在与水反应生成气体后被气
体带离水层,进入煤油层后停止反应又下沉,如此往复,直至钠反应完.故 D
正确;
故选 D.
第 1页(共 9页)3.关于 Na 的描述正确的是( ) ☆☆☆
①Na 在自然界中既以游离态又以化合态形式存在;
②金属 Na 着火可以用泡沫灭火器救火;
③实验室中少量的 Na 保存在煤油里;
④Na﹣K 合金做原子反应堆的导热剂;
⑤Na 比 Cu 活泼,因而 Na 可以从 CuCl 溶液中置换出 Cu;
2
⑥Na 在空气中燃烧,主要产物是 NaO.
2 2
A.①③④⑤⑥ B.③④⑥ C.③④ D.全部
【解答】
①因 Na 的性质很活泼,在自然界中只能以化合态形式存在,故①错误;
②因金属 Na 着火后生成了过氧化钠,过氧化钠可以与二氧化碳反应生成碳酸钠
和氧气,燃烧更剧烈,所以不能用泡沫灭火器救火,故②错误;
③因实验室中少量的 Na 保存在煤油里,故③正确;
④Na﹣K 合金做原子反应堆的导热剂,故④正确;
⑤因钠与盐溶液反应时,先与水反应,然后生成的碱再与盐反应,所以 Na 不能
从 CuCl 溶液中置换出 Cu,故⑤错误;
2
⑥Na 在空气中燃烧生成 NaO,故⑥正确;
2 2
故选:B.
4.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中
充分反应,则下列说法正确的是( ) ☆☆☆
A.第一块钠失去电子多 B.两块钠失去电子一样多
C.第二块钠的反应产物质量最大 D.两块钠的反应产物质量一样大
【解答】
A、金属钠失电子均变为+1 价的阳离子,等质量的两块钠,失电子是一样的,故
A 错误;
第 2页(共 9页)B、金属钠失电子均变为+1 价的阳离子,等质量的两块钠,失电子是一样的,故
B 正确;
C、根据 4Na+O=2NaO,则 1mol 金属钠获得氧化钠的质量是 32g,
2 2
根据反应 2Na+O NaO,则 1mol 金属钠获得过氧化钠的质量是 39g,等质
2 2 2
量的两块钠,即金属钠的物质的量是相等的,所以生成过氧化钠的质量大,即第
一块钠的反应产物质量最大,故 C 错误;
D、根据 C 的计算可以知道第一块钠的反应产物质量最大,故 D 错误.
故选 B.
5.下列关于钠及其化合物的叙述中错误的是( ) ☆☆☆
A.碳酸钠比碳酸氢钠的热稳定性要好
B.钠在空气中燃烧生成 NaO
2
C.钠在发生化学反应时只作还原剂
D.钠单质暴露在空气中最终将变成 NaCO
2
3
【解答】
A.碳酸钠较稳定,碳酸氢钠加热容易分解,反应的化学方程式为:
2NaHCO NaCO +CO↑+HO,故 A 正确;
3 2 3 2 2
B、钠在空气中燃烧生成过氧化钠,而不是氧化钠,故 B 错误;
C、钠在发生化学反应失电子,作还原剂,故 C 正确;
D、单质钠长久露置在空气中转化过程为:Na→NaO→NaOH→NaCO•10HO→NaCO,
2 2 3 2 2 3
最终将变成 NaCO,故 D 正确;
2 3
故选 B.
6.下列各组物质相互混合反应,既有气体生成最终又有沉淀生成的组合完全正
确的是( ) ☆☆☆☆
①Ba(HCO) 与稀 HSO 混合 ②金属钠投入到 FeCl 溶液中
3 2 2 4 3
③NaO 投入到 Ba(NO) 溶液混合 ④NaO 固体投入到 CuSO 溶液.
2 2 3 2 2 2 4
A.①②④ B.③ C.①② D.①②③④
第 3页(共 9页)【解答】
①碳酸氢钡和硫酸发生复分解反应,反应方程式为:
Ba(HCO)+HSO=BaSO↓+2HO+2CO↑,所以符合题意,故①正确;
3 2 2 4 4 2 2
②Na 先和水反应,然后 NaOH 再和氯化铁发生复分解反应,反应方程式为:
6Na+6HO+2FeCl=2Fe(OH)↓+6NaCl+3H↑,所以符合题意,故②正确;
2 3 3 2
③NaO 投入到 Ba(NO) 溶液混合,过氧化钠先和水反应生成氢氧化钠和氧气
2 2 3 2
2NaO+2HO=4NaOH+O↑,生成的氢氧化钠和硝酸钡溶液不反应无沉淀生成,故③
2 2 2 2
错误;
④过氧化钠先和水反应生成氢氧化钠,然后 NaOH 再和 CuSO 反应发生复分解反
4
应,反应方程式为:2NaO+2HO=4NaOH+O↑、2NaOH+CuSO=Cu(OH)↓+NaSO,
2 2 2 2 4 2 2 4
所以符合题意,故④正确;
故选 A.
7.将少量金属钠分别投入下列物质的水溶液中,有气体放出,且溶液质量减轻
(不考虑水的挥发)的是( ) ☆☆☆☆
A.HCl B.NaOH C.KSO D.CuSO
2 4
4
【解答】
A、钠和水的反应方程式为:2Na+2HO=2NaOH+H↑,生成的氢氧化钠和盐酸反应
2 2
生成盐和水,反应方程式为:NaOH+HCl=NaCl+HO,所以溶液质量增加,溶液增
2
加的质量=m(Na)﹣m(H),故 A 不符合.
2
B、钠和水的反应方程式为:2Na+2HO=2NaOH+H↑,所以溶液质量增加,溶液增
2 2
加的质量=m(Na)﹣m(H),故 B 不符合.
2
C、钠和水的反应方程式为:2Na+2HO=2NaOH+H↑,生成的氢氧化钠和硫酸钾不
2 2
反应,所以溶液增加的质量=m(Na)﹣m(H),故 C 不符合.
2
D、钠和水的反应方程式为:2Na+2HO=2NaOH+H↑,生成的氢氧化钠和硫酸铜反
2 2
应,反应方程式为:2NaOH+CuSO=NaSO+Cu(OH)↓,将两个方程式相加得
4 2 4 2
第 4页(共 9页)2Na+2HO+CuSO=H↑+NaSO+Cu(OH)↓,根据方程式知,溶液的离子减少,减
2 4 2 2 4 2
轻的质量=m(Cu(OH))﹣m(Na)+m(H),故 D 符合.
2 2
故选 D.
8.在一定温度下,向饱和 NaOH 溶液中投入一小块金属钠,充分反应后恢复到原
来的温度,下列叙述合理的是( ) ☆☆☆☆
A.NaOH 溶液浓度增大,并放出 H
2
B.溶液中 NaOH 的质量分数不变,有 H 放出
2
C.溶液的总质量增大,有 H 放出
2
D.溶液的总质量不变,有 H 放出
2
【解答】
A.温度不变,氢氧化钠的溶解度不变,溶剂减少,溶质析出,但溶液浓度不变,
故 A 错误;
B.温度不变,氢氧化钠的溶解度不变,所以其质量分数不变,钠和水反应放出
氢气,故 B 正确;
C.钠和水反应导致溶剂的量减少且有氢气生成,溶质析出,所以溶液质量减少,
故 C 错误;
D.钠和水反应导致溶剂的量减少且有氢气生成,溶质析出,所以溶液质量减少,
故 D 错误;
故选 B.
9.把 2.3g Na 放入水中,要使 100 个水分子中含有 1 个 Na ,所需水的质量是( )
+
☆☆☆☆
A.184g B.181.8g C.180g D.183.6g
【解答】
钠的物质的量= =0.1mol,钠和水的反应方程式为:2Na+2HO=2NaOH+H↑,
2 2
根据原子守恒得 n(Na)=n(Na )=0.1mol,根据方程式知,反应中参加反应的
+
第 5页(共 9页)水的物质的量 n(Na)=n(HO)=0.1mol,使 100 个水分子中含有 1 个 Na ,则溶
2 +
液中水的物质的量=100n(Na )=100n(Na)=10mol,
+
则需要水的质量=(0.1+10)mol×18g/mol=181.8g.
故选 B.
10.将 2.3g 金属钠放入 100g 水中,完全反应后溶液中溶质的质量分数为( )
☆☆☆☆
A. B.
C. D.
【解答】
设 2.3 克金属钠与水反应生成氢氧化钠的质量为 X,生成氢气质量为 Y,
2Na+2HO═2NaOH+H↑
2 2
46 80 2
2.3g X Y
根据:
解得 X=4g;Y=0.1g,
反应后所得溶液的质量分数: ×100%.
故选 D.
11.下列关于 NaCO 和 NaHCO 的说法中,不正确的是( ) ☆☆☆
2 3 3
A.均易溶于水 B.均为白色固体
C.受热均易分解 D.均能与盐酸反应
【解答】
A、NaCO 和 NaHCO 属于钠盐,都极易溶于水,故 A 正确;
2 3 3
B、NaCO 和 NaHCO 均为白色固体,故 B 正确;
2 3 3
C、NaCO 加热不分解,NaHCO 加热分解,故 C 错误;
2 3 3
第 6页(共 9页)D、NaCO 和 NaHCO 都能够和酸反应生成二氧化碳,故 D 正确;
2 3 3
故选:C.
12.化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )
☆☆☆
①钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等
②K、Na 合金可作原子反应堆的导热剂
③发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
④NaO 既可作呼吸面具中 O 的来源,又可漂白织物、麦杆、羽毛等
2 2 2
⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂
⑥明矾常作为消毒剂.
A.①②③④ B.①②③④⑤ C.①②③④⑥ D.①②③④⑤⑥
【解答】
①金属钠的化学性质强于金属钛,可以将金属钛、钽、铌、锆等从其熔融态的盐
中置换出来,所以可以用来冶炼金属钛、钽、铌、锆等,故正确.
②K、Na 合金熔点低,可作原子反应堆的导热剂,故正确.
③碳酸氢钠和酸反应生成二氧化碳,所以发酵粉中主要含有碳酸氢钠,能使焙制
出的糕点疏松多孔,故正确.
④NaO 和二氧化碳反应生成氧气,且又有强氧化性,有漂白性,所以 NaO 既可
2 2 2 2
作呼吸面具中 O 的来源,又可漂白织物、麦杆、羽毛等,故正确.
2
⑤碳酸钠碱性较强,所以不能用来治疗胃酸过多,碳酸氢钠在医疗上是治疗胃酸
过多的一种药剂,故错误.
⑥明矾是强酸弱碱盐能水解生成氢氧化铝胶体,胶体具有吸附性,所以可作净水
剂,不能作消毒剂,故错误.
故选:A.
13.1mol 过氧化钠与 2mol 碳酸氢钠固体混合后,在密闭的容器中加热充分反应,
排出气体物质后冷却,残留的固体物质是( ) ☆☆☆☆
第 7页(共 9页)A.NaCO、NaO B.NaCO
2 3 2 2 2
3
C.NaOH、NaCO D.NaO、NaOH、NaCO
2 3 2 2 2
3
【解答】
碳酸氢钠不稳定受热分解,方程式:2NaHCO NaCO+CO↑+HO,2mol 碳酸
3 2 3 2 2
氢钠分解生成 1mo NaCO、1mol CO、1mol HO,
2 3 2 2
则:2NaHCO NaCO+CO↑+HO, 2NaO+2CO═2NaCO+O,
3 2 3 2 2 2 2 2 2 3 2
2mol 1mol 1mol 1mol 1mol 1mol 1mol
则过氧化钠恰好与碳酸氢钠分解生成的二氧化碳反应,排出气体物质后冷却,残
留的固体物质为 1mol NaCO,
2 3
故选:B.
14.下列六种物质:①NaO ②NaO ③NaCl ④NaCO 溶液⑤NaOH⑥NaHCO,其中
2 2 2 2 3 3
不能跟 CO 反应的是( ) ☆☆☆
2
A.③⑥ B.②③ C.①④ D.⑤⑥
【解答】
①NaO 能和二氧化碳反应:NaO+CO=NaCO,故错误;
2 2 2 2 3
②NaO 能和二氧化碳反应:2NaO+2CO=2NaCO+O,故错误;
2 2 2 2 2 2 3 2
③NaCl 溶液不能和二氧化碳反应,故正确;
④NaCO 溶液能和二氧化碳反应:NaCO+CO+HO=2NaHCO,故错误;
2 3 2 3 2 2 3
⑤NaOH 溶液能和二氧化碳反应:2NaOH+CO=NaCO+HO 或 NaOH+CO=NaHCO,故错
2 2 3 2 2 3
误;
⑥NaHCO 溶液不能和二氧化碳反应,故正确;
3
故选 A.
15.下列有关 NaCO 和 NaHCO 的说法中,正确的是( ) ☆☆☆
2 3 3
A.热稳定性:NaCO<NaHCO
2 3
3
B.相同温度下在水中的溶解度:NaCO<NaHCO
2 3
3
第 8页(共 9页)C.取 1 mol•L
﹣1 的两种溶液,分别滴加澄清石灰水,有沉淀生成的是 NaCO 溶液
2 3
D.取等质量的两种固体分别与等浓度等体积的盐酸反应,生成气泡较快的是
NaHCO 溶液
3
【解答】
A.因 2NaHCO NaCO+CO↑+HO,而碳酸钠加热不分解,故 A 错误;
3 2 3 2 2
B.在饱和 NaCO 溶液中通入过量二氧化碳可生成 NaHCO 沉淀,可说明水中的溶
2 3 3
解度:NaCO>NaHCO,故 B 错误;
2 3 3
C.加入澄清的石灰水,NaCO 溶液和 NaHCO 溶液都能生成 CaCO 沉淀,故 C 错误;
2 3 3 3
D.NaHCO
3
与盐酸反应只需一步即放出二氧化碳气体:HCO ﹣+H
+
=CO
2
↑+H
2
O,而 Na
2
CO
3 3
要和 HCl 反应放出二氧化碳气体需两步:CO 2﹣+H
+
=HCO ﹣,HCO ﹣+H
+
=CO
2
↑+H
2
O,故
3 3 3
NaHCO 与盐酸反应更剧烈,反应速率更快,故 D 正确.
3
故选 D.
16.把一定浓度的 NaOH 溶液分成两等份,一份密闭保存,另一份敞口放置,几
天后分别与相同浓度的盐酸反应,都恰好完全反应时,若第一份用去盐酸 VmL,
1
第二份用去盐酸 VmL,则两者的关系为( ) ☆☆☆☆☆
2
A.V=V B.V>V C.V<V D.不能确定
1 2 1 2 1 2
【解答】
氢氧化钠敞口放置,则 2NaOH+CO=NaCO+HO,NaCO+2HCl=2NaCl+HO+CO↑;氢
2 2 3 2 2 3 2 2
氧化钠和盐酸反应生成氯化钠和水 NaOH+HCl=NaCl+HO,根据钠元素守恒,氢氧
2
化钠中和碳酸钠中钠离子的物质的量是相等的,再和盐酸反应,都得到的是氯化
钠溶液,n(Na
+
)=n(Cl﹣),根据氯元素守恒,所以二者消耗的盐酸的物质的量
是相等的,即用相同浓度的盐酸的体积是一样多的.
故选 A.
第 9页(共 9页)