文档内容
选择题突破十一 B 组 能力提升练
1.(2024·山东临沂一模)实验室提供的玻璃仪器有圆底烧瓶、玻璃棒、烧杯、酒精灯、量筒、容量瓶、
漏斗(非玻璃仪器任选),选用上述仪器能完成的实验是 ( )
A.重结晶法提纯苯甲酸
B.配制0.1 mol·L-1硫酸溶液
C.乙醇的消去反应
D.四氯化碳萃取碘水中的碘
2.(2024·黑吉辽卷)下列实验方法或试剂使用合理的是( )
选项 实验目的 实验方法或试剂
A 检验NaBr溶液中是否含有Fe2+ K[Fe(CN) ]溶液
3 6
B 测定KHS溶液中c(S2-) 用AgNO 溶液滴定
3
C 除去乙醇中少量的水 加入金属Na,过滤
D 测定KClO溶液的pH 使用pH试纸
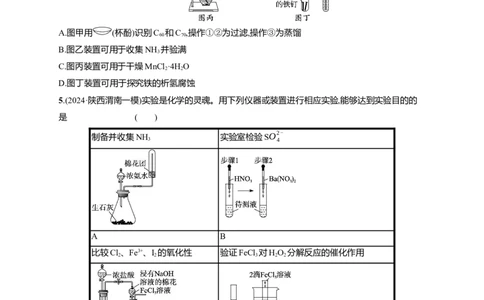
3.(2024·山东聊城一模)ClO 可用于自来水消毒,ClO 是一种黄绿色气体,易溶于水,与碱反应会生成Cl
2 2
O- 与ClO-
;下列有关实验室制备ClO 的实验原理和装置不能达到实验目的的是( )
2 3 2
A.用装置甲获取SO
2
B.用装置乙制备ClO
2
C.用装置丙吸收ClO
2
D.用装置丁处理尾气
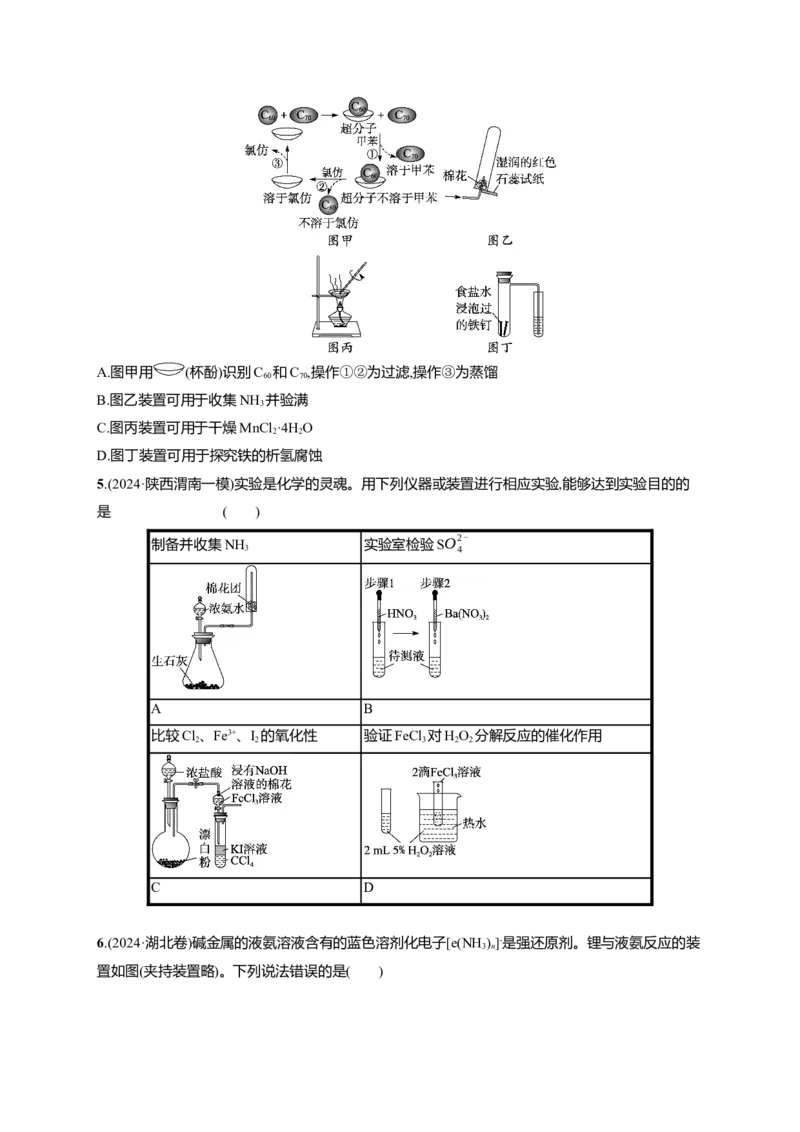
4.(2024·辽宁辽阳一模)下列说法正确的是( )A.图甲用 (杯酚)识别C 和C ,操作①②为过滤,操作③为蒸馏
60 70
B.图乙装置可用于收集NH 并验满
3
C.图丙装置可用于干燥MnCl ·4H O
2 2
D.图丁装置可用于探究铁的析氢腐蚀
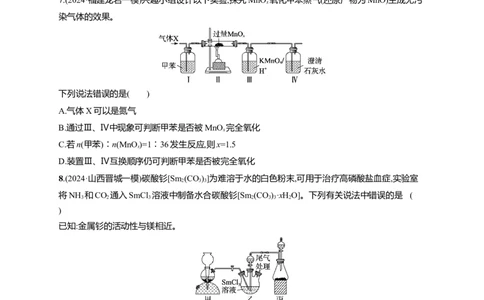
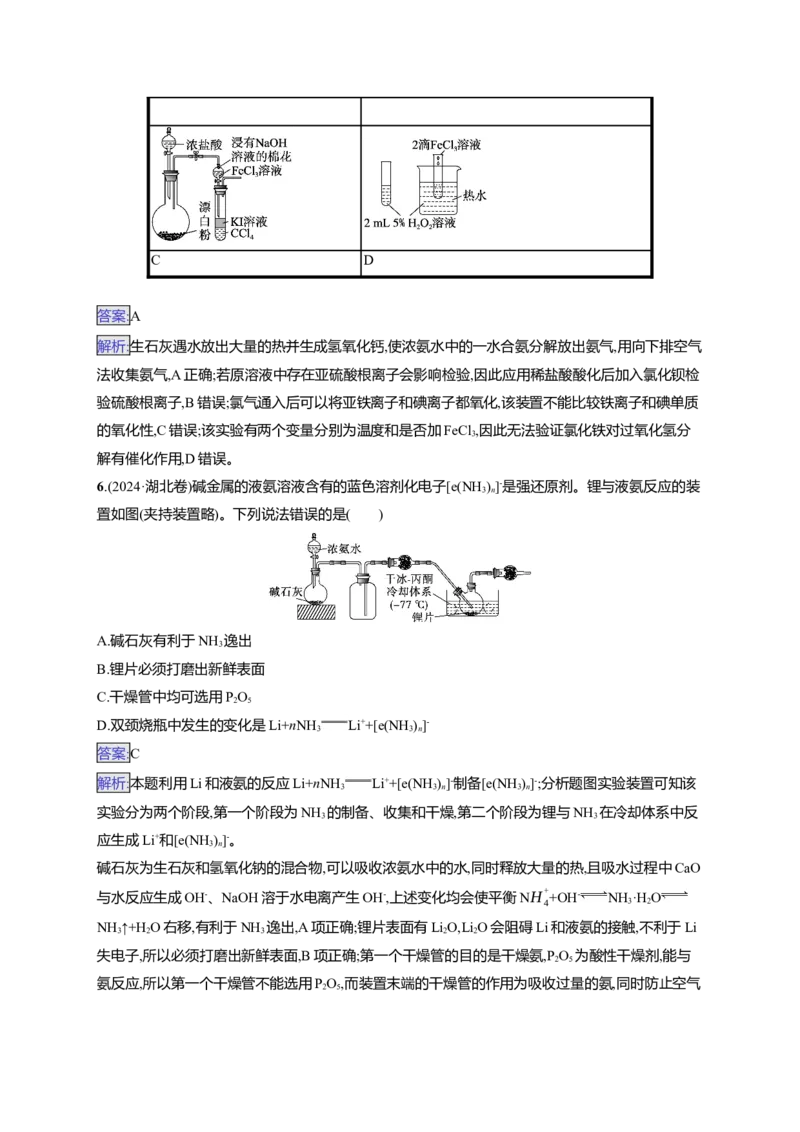
5.(2024·陕西渭南一模)实验是化学的灵魂。用下列仪器或装置进行相应实验,能够达到实验目的的
是 ( )
制备并收集NH
实验室检验SO2-
3 4
A B
比较Cl、Fe3+、I 的氧化性 验证FeCl 对HO 分解反应的催化作用
2 2 3 2 2
C D
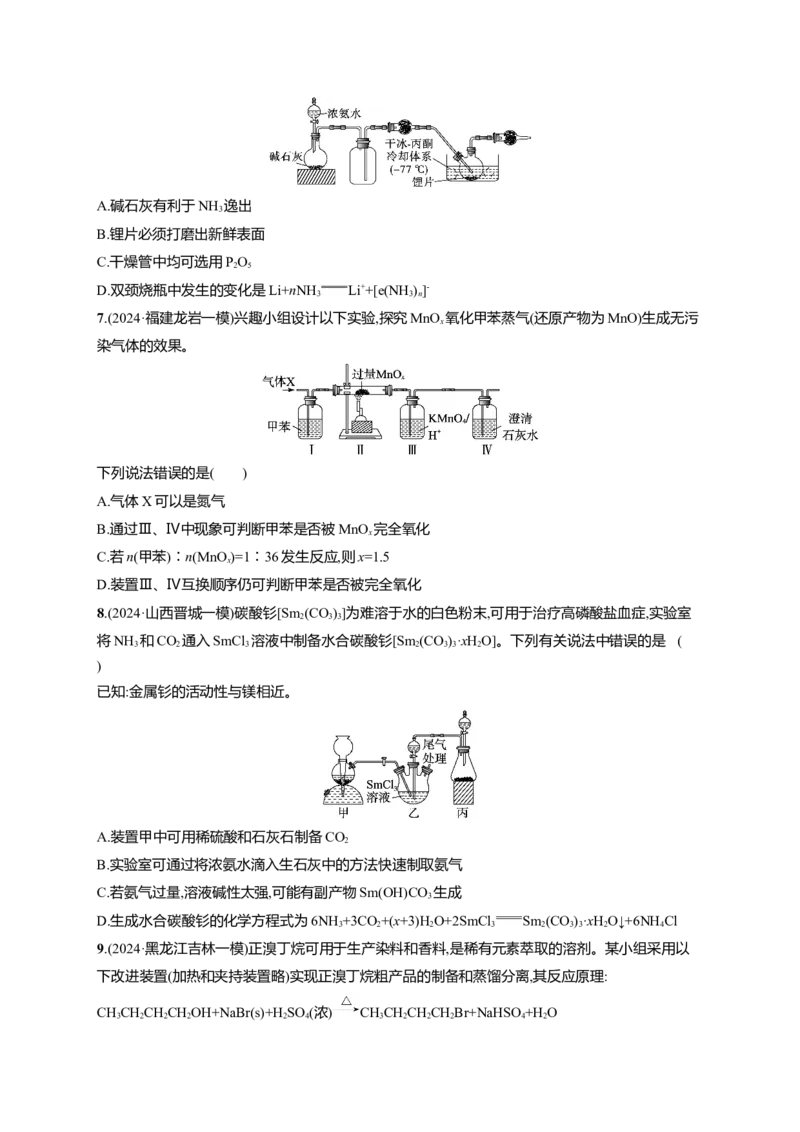
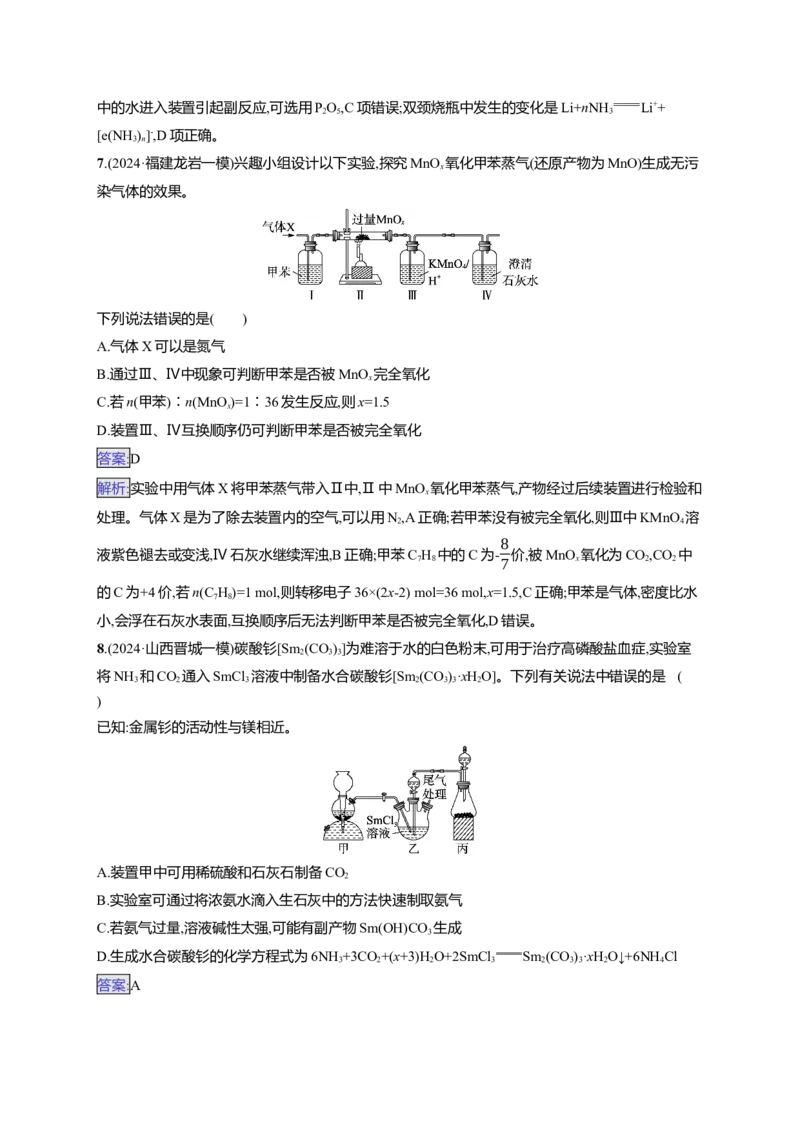
6.(2024·湖北卷)碱金属的液氨溶液含有的蓝色溶剂化电子[e(NH )]-是强还原剂。锂与液氨反应的装
3 n
置如图(夹持装置略)。下列说法错误的是( )A.碱石灰有利于NH 逸出
3
B.锂片必须打磨出新鲜表面
C.干燥管中均可选用PO
2 5
D.双颈烧瓶中发生的变化是Li+nNH Li++[e(NH)]-
3 3 n
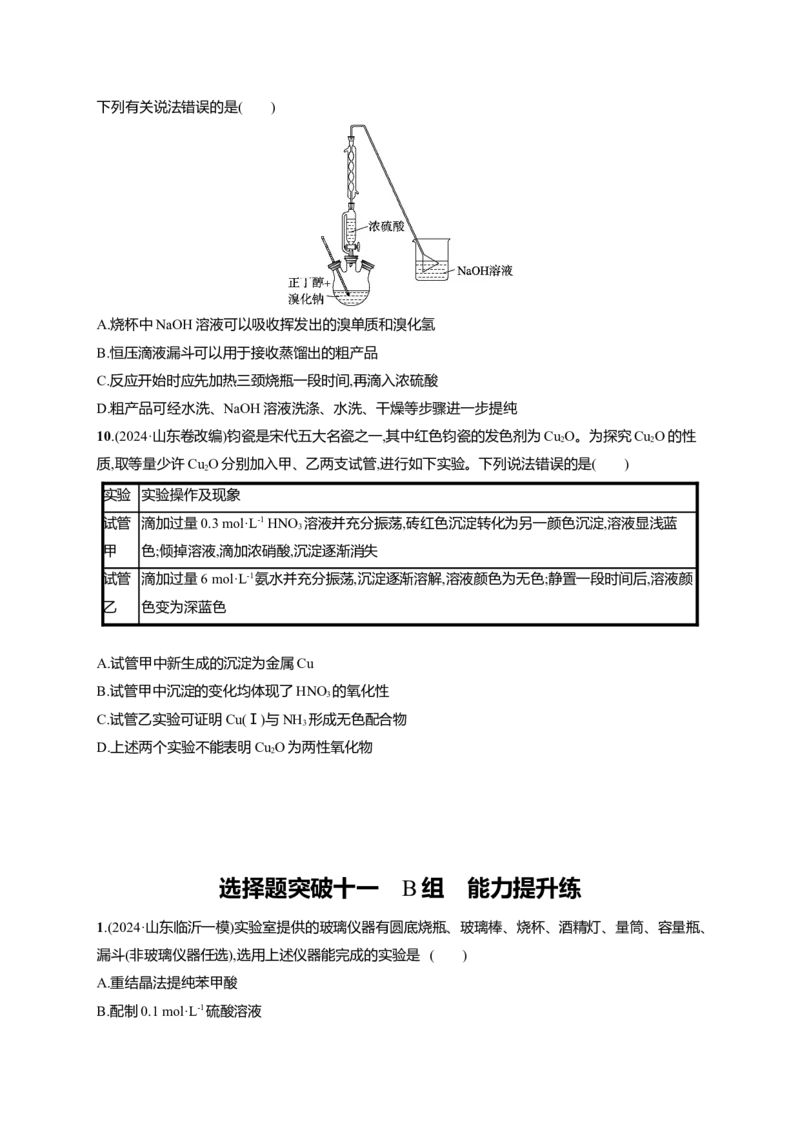
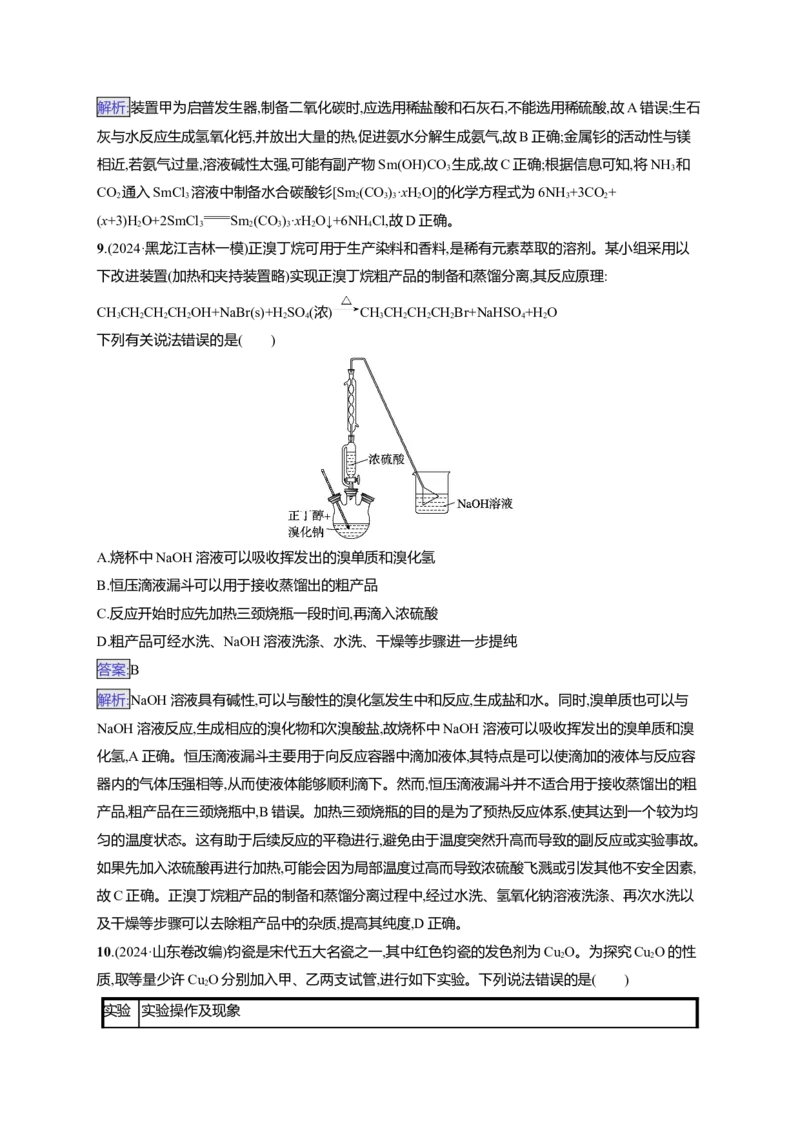
7.(2024·福建龙岩一模)兴趣小组设计以下实验,探究MnO 氧化甲苯蒸气(还原产物为MnO)生成无污
x
染气体的效果。
下列说法错误的是( )
A.气体X可以是氮气
B.通过Ⅲ、Ⅳ中现象可判断甲苯是否被MnO 完全氧化
x
C.若n(甲苯)∶n(MnO)=1∶36发生反应,则x=1.5
x
D.装置Ⅲ、Ⅳ互换顺序仍可判断甲苯是否被完全氧化
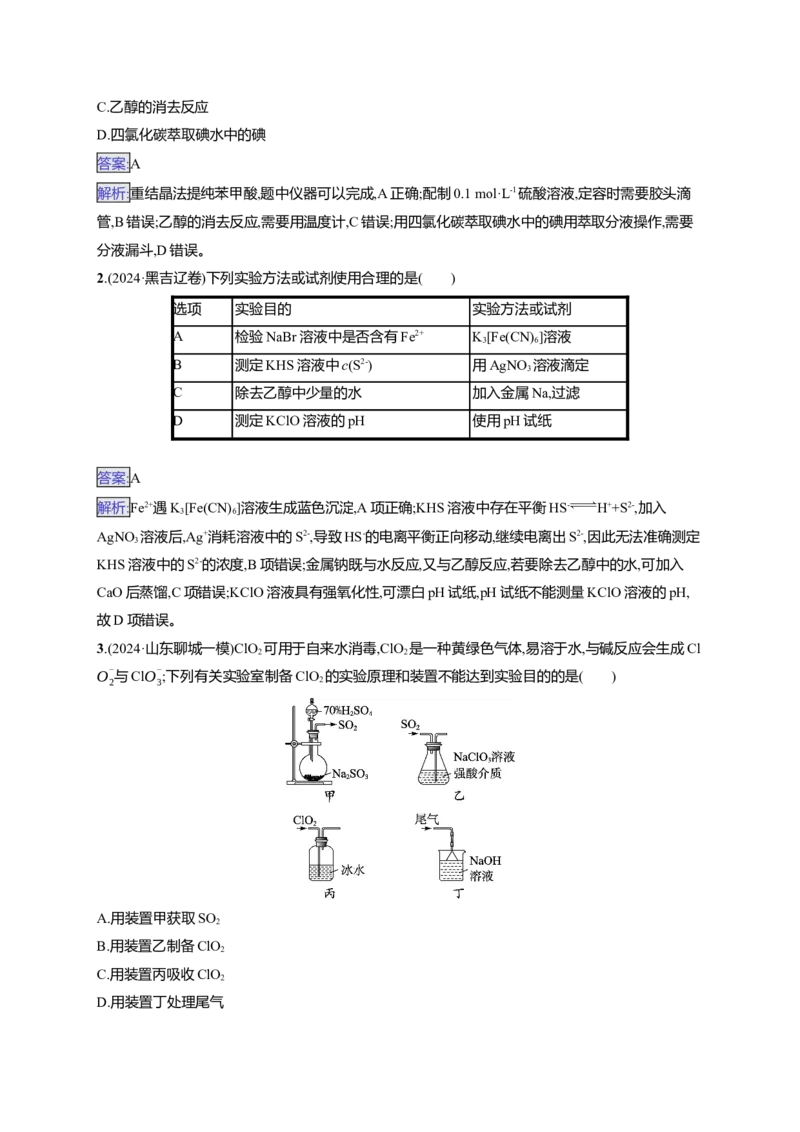
8.(2024·山西晋城一模)碳酸钐[Sm (CO)]为难溶于水的白色粉末,可用于治疗高磷酸盐血症,实验室
2 3 3
将NH 和CO 通入SmCl 溶液中制备水合碳酸钐[Sm (CO)·xHO]。下列有关说法中错误的是 (
3 2 3 2 3 3 2
)
已知:金属钐的活动性与镁相近。
A.装置甲中可用稀硫酸和石灰石制备CO
2
B.实验室可通过将浓氨水滴入生石灰中的方法快速制取氨气
C.若氨气过量,溶液碱性太强,可能有副产物Sm(OH)CO 生成
3
D.生成水合碳酸钐的化学方程式为6NH +3CO +(x+3)H O+2SmCl Sm (CO)·xHO↓+6NH Cl
3 2 2 3 2 3 3 2 4
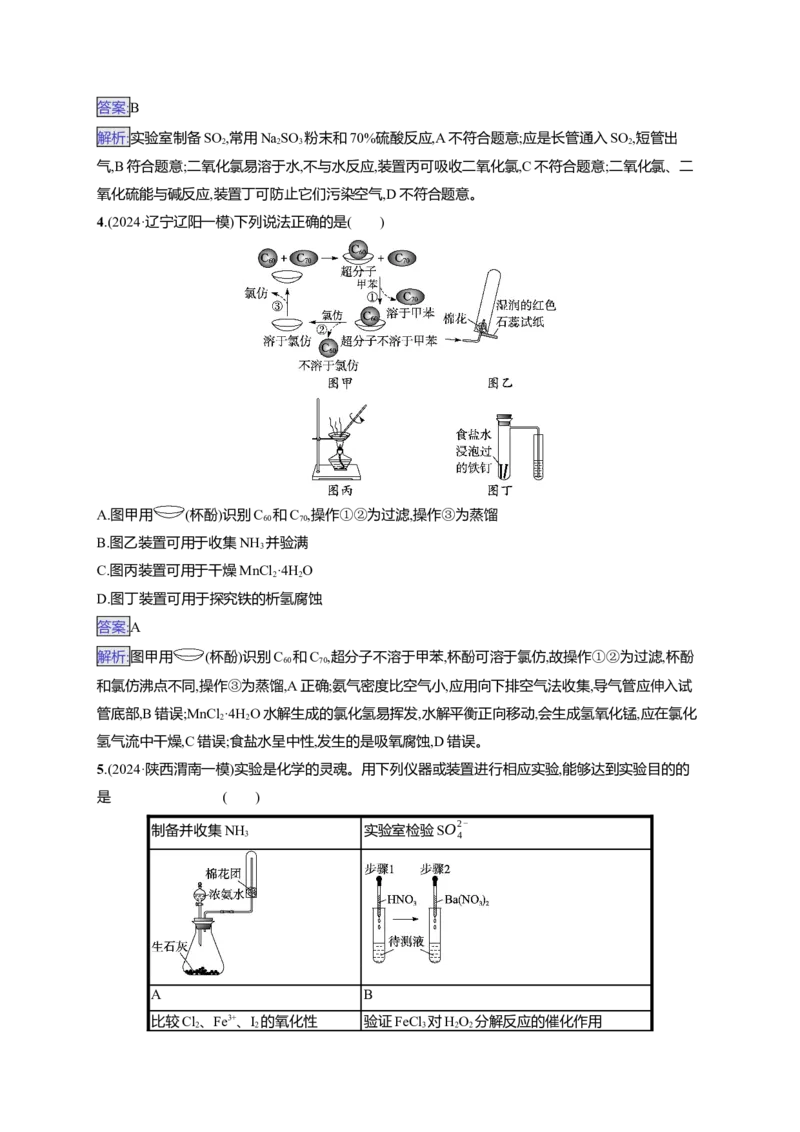
9.(2024·黑龙江吉林一模)正溴丁烷可用于生产染料和香料,是稀有元素萃取的溶剂。某小组采用以
下改进装置(加热和夹持装置略)实现正溴丁烷粗产品的制备和蒸馏分离,其反应原理:
CHCHCHCHOH+NaBr(s)+H SO (浓) CHCHCHCHBr+NaHSO +H O
3 2 2 2 2 4 3 2 2 2 4 2下列有关说法错误的是( )
A.烧杯中NaOH溶液可以吸收挥发出的溴单质和溴化氢
B.恒压滴液漏斗可以用于接收蒸馏出的粗产品
C.反应开始时应先加热三颈烧瓶一段时间,再滴入浓硫酸
D.粗产品可经水洗、NaOH溶液洗涤、水洗、干燥等步骤进一步提纯
10.(2024·山东卷改编)钧瓷是宋代五大名瓷之一,其中红色钧瓷的发色剂为Cu O。为探究Cu O的性
2 2
质,取等量少许Cu O分别加入甲、乙两支试管,进行如下实验。下列说法错误的是( )
2
实验 实验操作及现象
试管 滴加过量0.3 mol·L-1 HNO 溶液并充分振荡,砖红色沉淀转化为另一颜色沉淀,溶液显浅蓝
3
甲 色;倾掉溶液,滴加浓硝酸,沉淀逐渐消失
试管 滴加过量6 mol·L-1氨水并充分振荡,沉淀逐渐溶解,溶液颜色为无色;静置一段时间后,溶液颜
乙 色变为深蓝色
A.试管甲中新生成的沉淀为金属Cu
B.试管甲中沉淀的变化均体现了HNO 的氧化性
3
C.试管乙实验可证明Cu(Ⅰ)与NH 形成无色配合物
3
D.上述两个实验不能表明Cu O为两性氧化物
2
选择题突破十一 B 组 能力提升练
1.(2024·山东临沂一模)实验室提供的玻璃仪器有圆底烧瓶、玻璃棒、烧杯、酒精灯、量筒、容量瓶、
漏斗(非玻璃仪器任选),选用上述仪器能完成的实验是 ( )
A.重结晶法提纯苯甲酸
B.配制0.1 mol·L-1硫酸溶液C.乙醇的消去反应
D.四氯化碳萃取碘水中的碘
答案:A
解析:重结晶法提纯苯甲酸,题中仪器可以完成,A正确;配制0.1 mol·L-1硫酸溶液,定容时需要胶头滴
管,B错误;乙醇的消去反应,需要用温度计,C错误;用四氯化碳萃取碘水中的碘用萃取分液操作,需要
分液漏斗,D错误。
2.(2024·黑吉辽卷)下列实验方法或试剂使用合理的是( )
选项 实验目的 实验方法或试剂
A 检验NaBr溶液中是否含有Fe2+ K[Fe(CN) ]溶液
3 6
B 测定KHS溶液中c(S2-) 用AgNO 溶液滴定
3
C 除去乙醇中少量的水 加入金属Na,过滤
D 测定KClO溶液的pH 使用pH试纸
答案:A
解析:Fe2+遇K[Fe(CN) ]溶液生成蓝色沉淀,A项正确;KHS溶液中存在平衡HS- H++S2-,加入
3 6
AgNO 溶液后,Ag+消耗溶液中的S2-,导致HS-的电离平衡正向移动,继续电离出S2-,因此无法准确测定
3
KHS溶液中的S2-的浓度,B项错误;金属钠既与水反应,又与乙醇反应,若要除去乙醇中的水,可加入
CaO后蒸馏,C项错误;KClO溶液具有强氧化性,可漂白pH试纸,pH试纸不能测量KClO溶液的pH,
故D项错误。
3.(2024·山东聊城一模)ClO 可用于自来水消毒,ClO 是一种黄绿色气体,易溶于水,与碱反应会生成Cl
2 2
O- 与ClO-
;下列有关实验室制备ClO 的实验原理和装置不能达到实验目的的是( )
2 3 2
A.用装置甲获取SO
2
B.用装置乙制备ClO
2
C.用装置丙吸收ClO
2
D.用装置丁处理尾气答案:B
解析:实验室制备SO ,常用NaSO 粉末和70%硫酸反应,A不符合题意;应是长管通入SO ,短管出
2 2 3 2
气,B符合题意;二氧化氯易溶于水,不与水反应,装置丙可吸收二氧化氯,C不符合题意;二氧化氯、二
氧化硫能与碱反应,装置丁可防止它们污染空气,D不符合题意。
4.(2024·辽宁辽阳一模)下列说法正确的是( )
A.图甲用 (杯酚)识别C 和C ,操作①②为过滤,操作③为蒸馏
60 70
B.图乙装置可用于收集NH 并验满
3
C.图丙装置可用于干燥MnCl ·4H O
2 2
D.图丁装置可用于探究铁的析氢腐蚀
答案:A
解析:图甲用 (杯酚)识别C 和C ,超分子不溶于甲苯,杯酚可溶于氯仿,故操作①②为过滤,杯酚
60 70
和氯仿沸点不同,操作③为蒸馏,A正确;氨气密度比空气小,应用向下排空气法收集,导气管应伸入试
管底部,B错误;MnCl ·4H O水解生成的氯化氢易挥发,水解平衡正向移动,会生成氢氧化锰,应在氯化
2 2
氢气流中干燥,C错误;食盐水呈中性,发生的是吸氧腐蚀,D错误。
5.(2024·陕西渭南一模)实验是化学的灵魂。用下列仪器或装置进行相应实验,能够达到实验目的的
是 ( )
制备并收集NH
实验室检验SO2-
3 4
A B
比较Cl、Fe3+、I 的氧化性 验证FeCl 对HO 分解反应的催化作用
2 2 3 2 2C D
答案:A
解析:生石灰遇水放出大量的热并生成氢氧化钙,使浓氨水中的一水合氨分解放出氨气,用向下排空气
法收集氨气,A正确;若原溶液中存在亚硫酸根离子会影响检验,因此应用稀盐酸酸化后加入氯化钡检
验硫酸根离子,B错误;氯气通入后可以将亚铁离子和碘离子都氧化,该装置不能比较铁离子和碘单质
的氧化性,C错误;该实验有两个变量分别为温度和是否加FeCl ,因此无法验证氯化铁对过氧化氢分
3
解有催化作用,D错误。
6.(2024·湖北卷)碱金属的液氨溶液含有的蓝色溶剂化电子[e(NH )]-是强还原剂。锂与液氨反应的装
3 n
置如图(夹持装置略)。下列说法错误的是( )
A.碱石灰有利于NH 逸出
3
B.锂片必须打磨出新鲜表面
C.干燥管中均可选用PO
2 5
D.双颈烧瓶中发生的变化是Li+nNH Li++[e(NH)]-
3 3 n
答案:C
解析:本题利用Li和液氨的反应Li+nNH Li++[e(NH)]-制备[e(NH )]-;分析题图实验装置可知该
3 3 n 3 n
实验分为两个阶段,第一个阶段为NH 的制备、收集和干燥,第二个阶段为锂与NH 在冷却体系中反
3 3
应生成Li+和[e(NH )]-。
3 n
碱石灰为生石灰和氢氧化钠的混合物,可以吸收浓氨水中的水,同时释放大量的热,且吸水过程中CaO
与水反应生成OH-、NaOH溶于水电离产生OH-,上述变化均会使平衡NH+
+OH- NH ·H O
4 3 2
NH ↑+H O右移,有利于NH 逸出,A项正确;锂片表面有LiO,Li O会阻碍Li和液氨的接触,不利于Li
3 2 3 2 2
失电子,所以必须打磨出新鲜表面,B项正确;第一个干燥管的目的是干燥氨,P O 为酸性干燥剂,能与
2 5
氨反应,所以第一个干燥管不能选用PO,而装置末端的干燥管的作用为吸收过量的氨,同时防止空气
2 5中的水进入装置引起副反应,可选用PO,C项错误;双颈烧瓶中发生的变化是Li+nNH Li++
2 5 3
[e(NH )]-,D项正确。
3 n
7.(2024·福建龙岩一模)兴趣小组设计以下实验,探究MnO 氧化甲苯蒸气(还原产物为MnO)生成无污
x
染气体的效果。
下列说法错误的是( )
A.气体X可以是氮气
B.通过Ⅲ、Ⅳ中现象可判断甲苯是否被MnO 完全氧化
x
C.若n(甲苯)∶n(MnO)=1∶36发生反应,则x=1.5
x
D.装置Ⅲ、Ⅳ互换顺序仍可判断甲苯是否被完全氧化
答案:D
解析:实验中用气体X将甲苯蒸气带入Ⅱ中,Ⅱ中MnO 氧化甲苯蒸气,产物经过后续装置进行检验和
x
处理。气体X是为了除去装置内的空气,可以用N,A正确;若甲苯没有被完全氧化,则Ⅲ中KMnO 溶
2 4
8
液紫色褪去或变浅,Ⅳ石灰水继续浑浊,B正确;甲苯C H 中的C为- 价,被MnO 氧化为CO,CO 中
7 8 7 x 2 2
的C为+4价,若n(C H)=1 mol,则转移电子36×(2x-2) mol=36 mol,x=1.5,C正确;甲苯是气体,密度比水
7 8
小,会浮在石灰水表面,互换顺序后无法判断甲苯是否被完全氧化,D错误。
8.(2024·山西晋城一模)碳酸钐[Sm (CO)]为难溶于水的白色粉末,可用于治疗高磷酸盐血症,实验室
2 3 3
将NH 和CO 通入SmCl 溶液中制备水合碳酸钐[Sm (CO)·xHO]。下列有关说法中错误的是 (
3 2 3 2 3 3 2
)
已知:金属钐的活动性与镁相近。
A.装置甲中可用稀硫酸和石灰石制备CO
2
B.实验室可通过将浓氨水滴入生石灰中的方法快速制取氨气
C.若氨气过量,溶液碱性太强,可能有副产物Sm(OH)CO 生成
3
D.生成水合碳酸钐的化学方程式为6NH +3CO +(x+3)H O+2SmCl Sm (CO)·xHO↓+6NH Cl
3 2 2 3 2 3 3 2 4
答案:A解析:装置甲为启普发生器,制备二氧化碳时,应选用稀盐酸和石灰石,不能选用稀硫酸,故A错误;生石
灰与水反应生成氢氧化钙,并放出大量的热,促进氨水分解生成氨气,故B正确;金属钐的活动性与镁
相近,若氨气过量,溶液碱性太强,可能有副产物Sm(OH)CO 生成,故C正确;根据信息可知,将NH 和
3 3
CO 通入SmCl 溶液中制备水合碳酸钐[Sm (CO)·xHO]的化学方程式为6NH +3CO +
2 3 2 3 3 2 3 2
(x+3)H O+2SmCl Sm (CO)·xHO↓+6NH Cl,故D正确。
2 3 2 3 3 2 4
9.(2024·黑龙江吉林一模)正溴丁烷可用于生产染料和香料,是稀有元素萃取的溶剂。某小组采用以
下改进装置(加热和夹持装置略)实现正溴丁烷粗产品的制备和蒸馏分离,其反应原理:
CHCHCHCHOH+NaBr(s)+H SO (浓) CHCHCHCHBr+NaHSO +H O
3 2 2 2 2 4 3 2 2 2 4 2
下列有关说法错误的是( )
A.烧杯中NaOH溶液可以吸收挥发出的溴单质和溴化氢
B.恒压滴液漏斗可以用于接收蒸馏出的粗产品
C.反应开始时应先加热三颈烧瓶一段时间,再滴入浓硫酸
D.粗产品可经水洗、NaOH溶液洗涤、水洗、干燥等步骤进一步提纯
答案:B
解析:NaOH溶液具有碱性,可以与酸性的溴化氢发生中和反应,生成盐和水。同时,溴单质也可以与
NaOH溶液反应,生成相应的溴化物和次溴酸盐,故烧杯中NaOH溶液可以吸收挥发出的溴单质和溴
化氢,A正确。恒压滴液漏斗主要用于向反应容器中滴加液体,其特点是可以使滴加的液体与反应容
器内的气体压强相等,从而使液体能够顺利滴下。然而,恒压滴液漏斗并不适合用于接收蒸馏出的粗
产品,粗产品在三颈烧瓶中,B错误。加热三颈烧瓶的目的是为了预热反应体系,使其达到一个较为均
匀的温度状态。这有助于后续反应的平稳进行,避免由于温度突然升高而导致的副反应或实验事故。
如果先加入浓硫酸再进行加热,可能会因为局部温度过高而导致浓硫酸飞溅或引发其他不安全因素,
故C正确。正溴丁烷粗产品的制备和蒸馏分离过程中,经过水洗、氢氧化钠溶液洗涤、再次水洗以
及干燥等步骤可以去除粗产品中的杂质,提高其纯度,D正确。
10.(2024·山东卷改编)钧瓷是宋代五大名瓷之一,其中红色钧瓷的发色剂为Cu O。为探究Cu O的性
2 2
质,取等量少许Cu O分别加入甲、乙两支试管,进行如下实验。下列说法错误的是( )
2
实验 实验操作及现象试管 滴加过量0.3 mol·L-1 HNO 溶液并充分振荡,砖红色沉淀转化为另一颜色沉淀,溶液显浅蓝
3
甲 色;倾掉溶液,滴加浓硝酸,沉淀逐渐消失
试管 滴加过量6 mol·L-1氨水并充分振荡,沉淀逐渐溶解,溶液颜色为无色;静置一段时间后,溶液颜
乙 色变为深蓝色
A.试管甲中新生成的沉淀为金属Cu
B.试管甲中沉淀的变化均体现了HNO 的氧化性
3
C.试管乙实验可证明Cu(Ⅰ)与NH 形成无色配合物
3
D.上述两个实验不能表明Cu O为两性氧化物
2
答案:B
解析:试管甲中,Cu O与稀硝酸反应得到另一沉淀,溶液显浅蓝色,反应的离子方程式为Cu O+2H+
2 2
Cu+Cu2++H O,反应中硝酸体现酸性,滴加浓硝酸后,沉淀Cu溶解,硝酸表现氧化性和酸性,A正确,B错
2
误;试管乙中,沉淀溶解,先得到无色溶液,后得到深蓝色溶液,说明反应后期有[Cu(NH )]2+生成,类比可
3 4
知Cu(Ⅰ)能与NH 形成无色配合物,C正确;由反应Cu O+2H+ Cu+Cu2++H O可知,Cu O不是碱性
3 2 2 2
氧化物,也不是两性氧化物,D正确。