文档内容
押江苏卷第 4-5 题
物质结构与性质
核心考点 考情统计 考向预测 备考策略
2023·江苏卷,4 1.了解原子核外电子排布的构造
原子结构与性
原理,能结合能量最低原理、泡利
质 元素周期 2022·江苏卷,4
原理、洪特规则书写1~36号元素
律
2021·江苏卷,5 基态原子的核外电子排布式和轨道
表示式;
考查元素周期律,弱化元素推断的 2.认识元素的原子半径、第一电
考查;考查杂化类型、分子空间构 离能、电负性等元素性质的周期性
2023·江苏卷,5 型、键角比较等。 变化;
化学键 分子
2022·江苏卷,5 3.分析常见简单分子的空间结
结构与性质
构,能利用相关理论解释简单的共
2021·江苏卷,6
价分子的空间结构,能根据分子结
构特点和键的极性来判断分子的极
性。
1.(2023·江苏卷,4)元素C、Si、Ge位于周期表中ⅣA族。下列说法正确的是
A.原子半径: B.第一电离能:
C.碳单质、晶体硅、SiC均为共价晶体 D.可在周期表中元素Si附近寻找新半导体材料
【答案】D
【解析】同主族元素原子半径从上往下原子半径增大,故原子半径: ,A错误;同周
期主族元素,从上往下原子半径增大,更易失电子,第一电离能: ,B错误;晶体
硅、SiC均为共价晶体,碳单质中金刚石为共价晶体,而石墨为混合晶体,C 为分子晶体,C错误;周期
60表中元素Si附近存在许多准金属,可在其周围寻找半导体材料,D正确。
2.(2023·江苏卷,5)氢元素及其化合物在自然界广泛存在且具有重要应用。 、 、 是氢元素的3
种核素,基态H原子 的核外电子排布,使得H既可以形成 又可以形成 ,还能形成 、 、
、 、 等重要化合物。下列说法正确的是
A. 、 、 都属于氢元素
B. 和 的中心原子轨道杂化类型均为
C. 分子中的化学键均为极性共价键
D. 晶体中存在Ca与 之间的强烈相互作用
【答案】A
【解析】 、 、 都属于氢元素,三者互为同位素,统称为氢元素,A正确; 和 的中心原
子轨道杂化类型均为 ,B错误; 分子中的化学键既存在O-H极性共价键,也存在O-O非极性共价
键,C错误; 晶体中存在Ca2+与 之间的离子键,为强烈相互作用,D错误。
3.(2022·江苏卷,3)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
【答案】A
【解析】核外电子排布相同的微粒,核电荷数越大,半径越小,A正确;F元素的非金属性强于O,F的电
负性大,B错误;钠的金属性强,容易失去电子,电离能小,C错误;Na的金属性强于Al,则NaOH的碱
性强于Al(OH) ,D错误。
3
4.(2022·江苏卷,5)下列说法正确的是A.金刚石与石墨烯中的 夹角都为
B. 、 都是由极性键构成的非极性分子
C.锗原子( )基态核外电子排布式为
D.ⅣA族元素单质的晶体类型相同
【答案】B
【解析】金刚石中的碳原子为正四面体结构, 夹角为109°28′,A错误; 的化学键为Si-H,为
极性键,为正四面体,正负电荷中心重合,为非极性分子; 的化学键为Si-Cl,为极性键,为正四面
体,正负电荷中心重合,为非极性分子,B正确;锗原子( )基态核外电子排布式为[Ar] ,C错误;
ⅣA族元素中的碳元素形成的石墨为混合晶体,而硅形成的晶体硅为原子晶体,D错误。
5.(2021·江苏卷,5)前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元
素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列说
法正确的是
A.原子半径:r(X)
2 3 3
最高价氧化物对应水化物的 HPO Mg(OH) >Al(OH) LiOHB;Mg>Al;N>O;P>S。
(4)元素电负性的递变性
①规律
同周期元素从左到右,电负性逐渐增大;同主族元素从上到下,电负性逐渐减小。②应用
3.σ键、π键的判断方法
(1)由轨道重叠方式判断
“头碰头”重叠为σ键,“肩并肩”重叠为π键。
(2)由共用电子对数判断
单键为σ键;双键或三键,其中一个为σ键,其余为π键。
(3)由成键轨道类型判断
s轨道形成的共价键全部是σ键;杂化轨道形成的共价键全部为σ键。
4.杂化轨道和空间结构的判断方法
(1)明确杂化轨道类型与分子结构的关系
杂化轨道类型 杂化轨道数目 分子构型 实例
sp 2 直线形 CO、BeCl 、HgCl
2 2 2
sp2 3 平面三角形 BF、BCl 、CHO
3 3 2
等性杂化:正四面体 CH、CCl 、NH
4 4
sp3 4 不等性杂化:具体情 NH (三角锥形)、HS、
3 2
况不同 HO(V形)
2
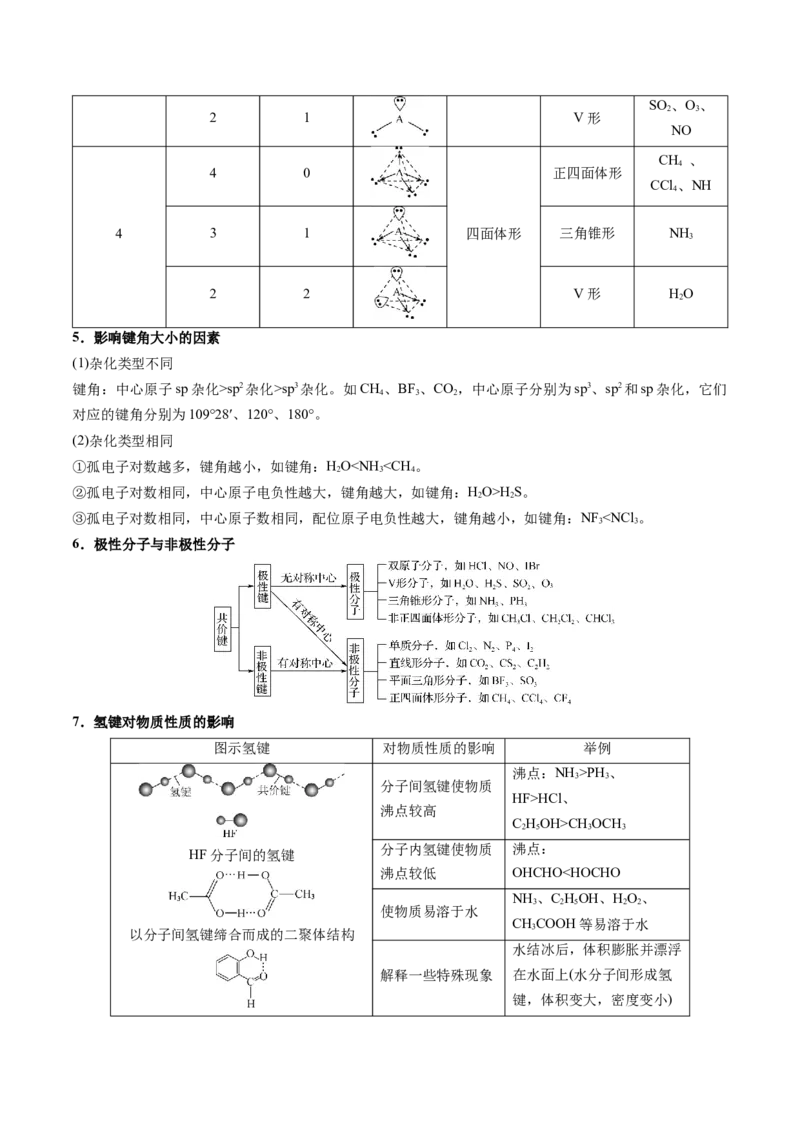
(2)价层电子对互斥模型和空间结构
分子或离子
价层电子 σ键电子 孤电子 电子对的 VSEPR 的
实例
对数 对数 对数 排列方式 模型名称 空间结构名
称
CO、CS、
2 2
2 2 0 直线形 直线形
BeCl
2
BF 、SO 、
3 3
3 3 0 平面三角形 平面三角形 NO、
COSO 、O、
2 3
2 1 V形
NO
CH 、
4
4 0 正四面体形
CCl 、NH
4
4 3 1 四面体形 三角锥形 NH
3
2 2 V形 HO
2
5.影响键角大小的因素
(1)杂化类型不同
键角:中心原子sp杂化>sp2杂化>sp3杂化。如CH 、BF 、CO ,中心原子分别为sp3、sp2和sp杂化,它们
4 3 2
对应的键角分别为109°28′、120°、180°。
(2)杂化类型相同
①孤电子对数越多,键角越小,如键角:HOHS。
2 2
③孤电子对数相同,中心原子数相同,配位原子电负性越大,键角越小,如键角:NF PH、
3 3
分子间氢键使物质
HF>HCl、
沸点较高
C HOH>CH OCH
2 5 3 3
分子内氢键使物质 沸点:
HF分子间的氢键
沸点较低 OHCHOχ(O) B. 原子半径:r(Al)>r(N)
C. 第一电离能:I(S)>I(O) D. 热稳定性:HS(g)>HO(g)
1 1 2 2
【答案】B
【解析】同周期从左到右,电负性增强,A项错误;Al核外三个电子层,N核外两个电子层,则Al的原子
半径大于N,B项正确;O的非金属性强于S,则O的第一电离能大于S,C项错误;非金属性越强,对应
气态氢化物越稳定,则稳定性:HO>HS,D项错误。
2 2
2.(2024·江苏连云港高三11月期中)元素Be、Mg、Ca位于周期表中ⅡA族。下列说法正确的是
A.电负性:
B.第一电离能:
C. 、 、 形成的晶体均为离子晶体
D.最高价氧化物的水化物的碱性:
【答案】B
【解析】同一主族元素,从上到下,电负性逐渐减小, ,A项错误;同一主族元
素,从上到下,第一电离能逐渐减小, ,B项正确; 与 相似,
形成的是共价键, 形成的晶体为分子晶体,C项错误;同一主族元素,从上到下,最高价氧化物的
水化物的碱性增强, ,D项错误。3.(2024·江苏常州教育学会高三11月期中学业水平监测)铁系超导材料Fe-Sm-As-F-O中基态Sm原子的
价电子排布为 。下列说法正确的是
A.Sm位于元素周期表中的f区 B.Fe成为阳离子时先失去3d轨道电子
C.氢化物的稳定性: D.第一电离能:
【答案】A
【解析】基态Sm原子的价电子排布为4f26s2,4f轨道未充满,则Sm位于元素周期表中的f区,A项正确;
Fe的价电子排布式为3d64s2,Fe生成阳离子时首先失去4s轨道上2个电子,再失去3d轨道上的电子,B
错误;非金属性:O>P>As,非金属性越强,简单氢化物越稳定,则氢化物的稳定性:AsH < H O,C项错误;
3 2
F、O位于第二周期,第二周期从左向右第一电离能呈增大趋势,且F、O属于VIIA、VIA族,则第一电离
能: I (F)> I (O),D项错误。
1 1
4.(2024·江苏泰州中学、宿迁中学、宜兴中学高三12月调研测试) 催化剂能催化
脱除烟气中的 ,反应为 。下列说法正确的是
A. 的电子式:
B. 的 模型名称:直线型
C. 的价电子排布图为:
D. 是极性键构成的非极性分子
【答案】C
【解析】 的电子式: ,A错误; 的价层电子对数是4, 模型名称:四面体形,,B
错误; 的价电子排布图为: ,C正确; 是极性键构成的极性分子,
极性向量和不为零,D错误。5.(2024·江苏南京盐城高三一模)十二烷基磺酸钠 常用作轻纺工业的乳化剂。下列说法项
正确的是
A. 为离子化合物 B.离子半径:
C.电离能: D.热稳定性:
【答案】A
【解析】 为钠离子和十二磺酸根离子构成的,为离子化合物,A项正确;电子层越多,半径
越大,电子层数一样,核电荷数越大,半径越小。钠离子和氧离子的电子层数一样多,钠离子的核电荷数
大,半径小,B项错误;同一周期随着原子序数变大,第一电离能变大,N的2p轨道为半充满稳定状态,
第一电离能大于同周期相邻元素, ,C项错误;非金属性越强,其元素形成的简单氢化
物越稳定,所以非金属性:O>N,热稳定性, ,D项错误。
6.(2024·江苏徐州第一中学、淮阴中学、姜堰中学高三联考)CrSi、Ge-GaAs、ZnGeAs 和SiC都是重要
2
的半导体化合物,下列说法错误的是
A.原子半径:r(Ga)>r(Ge)>r(As)
B.碳单质、晶体硅、SiC均为共价晶体
C.可在周期表中元素Si附近寻找新半导体材料
D.第一电离能:I(C)>I (Si)>I (Ge)
1 1 1
【答案】B
【解析】同周期从左到右,原子半径逐渐减小,原子半径:r(Ga)>r(Ge)>r(As),A正确;碳单质中金刚石、
晶体硅、SiC均为共价晶体,碳单质中C 则为分子晶体,B错误;可在周期表中元素Si附近寻找新半导体
60
材料,如Ga等,C正确;周期表中同主族从上到下,第一电离能变小,第一电离能:I(C)>I (Si)>I
1 1 1
(Ge),D正确。
7.(2024·江苏宿迁3月学情调研)Ga、 As、Se位于元素周期表第四周期。下列说法正确的是( )
A. 原子半径: r(Ga)r(As)>r(Se),A项错误;As为ⅤA元素,4p轨道为
半充满,第一电离能比同周期相邻元素都要大,B项正确;非金属性越强,电负性越大,χ(Ga) <χ(As)
<χ(Se),C项错误;Se为非金属元素,优良催化剂材料在过渡金属区域寻找,D项错误。
8.(2024·江苏苏州市名校高三大联考)利用 制取金属钾,下列说法正确的是
A.原子半径:
B.第一电离能:
C.金属性:
D.电解饱和食盐水可以制得金属
【答案】A
【解析】核外电子层数多的一定半径大,核外电子层数一样的,原子序数小半径大,所以原子半径:
,A正确;随着核电荷数的递增,元素的第一电离能呈现周期性变化。同一主族元素
从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,第一电离能由大变
小,同周期元素第一电离能从左到右有增大的趋势,所以第一电离能: ,B错误;
同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,第一
电离能由大变小,元素的金属性逐渐增强,金属性: ,C错误;电解NaCl水溶液所得产物为
NaOH、H、Cl,因为Na的还原性极强,极易把水还原生成氢气,不能与水共存,只有电解熔融NaCl才
2 2
能制得金属钠,D错误。
9.(2024·江苏泰州姜堰中学高三期中,)W、X、Y、Z是原子序数依次增大的四种短周期主族元素,W基
态原子只有一种自旋取向的电子,X最高正化合价与最低负化合价代数和为零,Y的单质在空气中含量最
高,Z位于第三周期,其基态原子s能级上的电子总数与p能级上的电子总数相等。下列说法正确的是
A.第一电离能 :Z>X>Y
B.简单气态氢化物的热稳定性:X>Y
C.X、Y均能与W形成含有非极性键的化合物
D.工业上制备Z单质是通过电解其氯化物的水溶液而获得【答案】C
【解析】W基态原子只有一种自旋取向的电子,则W为H,X最高正化合价与最低负化合价代数和为零,
则X为C,Y的单质在空气中含量最高,则Y为N,Z位于第三周期,其基态原子s能级上的电子总数与p
能级上的电子总数相等,则Z为Mg。第一电离能 :N>C>Mg,A项错误;简单气态氢化物的热稳定性:
NH >CH ,B项错误;C、N均能与H形成C H、NH 等含有非极性键的化合物,C项正确;工业上制备
3 4 2 4 2 4
Mg单质是通过电解其熔融氯化物而获得,D项错误。
10.(2024·江苏苏州高三期末)太阳能电池可由Si、GaP、GaAs等半导体材料构成。有关元素在元素周
期表中的位置如图所示,下列说法正确的是( )
A. 原子半径:r(Ga)PH
3 3
D. Ga的周期序数与族序数相等
【答案】B
【解析】同周期,原子序数的递增,原子半径减小,所以r(Ga)> r(As),A项错误;P最外层电子为半充满
状态,第一电离能大于相邻元素Si,B项正确;As为第四周期元素,P为第三周期元素,P的非金属性比
As强,热稳定性AsH NH >PH,B项错误;
3 3 2 3 3
N为ⅤA的元素,第一电离能比同周期相邻元素大,Mn为金属元素,在三者中第一电离能最小,故第一
电离能:N>O>Mn,C项正确;Z的最高价氧化物对应的水化物为HPO ,X最高价氧化物对应的水化物
3 4
为HNO,前者为中强酸而后者为强酸,D项错误。
3
13.(2024·江苏海安高级中学高三开学考试)A、B、C、D四种短周期元素,A元素原子的外围电子排布式为 ,B元素与A元素位于同一周期,其原子的核外有三个未成对电子,C元素位于第2周期,电
负性仅小于氟,D元素在短周期元素中第一电离能最小。下列说法正确的是
A.第一电离能: B.原子半径:
C.C、D两种元素组成的化合物一定不含共价键 D.简单气态氢化物的热稳定
性:
【答案】B
【解析】A、B、C、D四种短周期元素,A元素原子的外围电子排布式为 ,则A为C元素;C元素
位于第2周期,电负性仅次于氟,则C为O,B元素与A元素位于同一周期,其原子的原子核外有三个未
成对电子,则B为N元素;D元素在短周期元素中第一电离能最小,则D为Na元素。A为C,B为N,C
为O,同周期第一电离能越向右电离能越大,但是第ⅢA族和第ⅥA族反常,故第一电离能顺序为:
,A项错误;A为C,B为N,D为Na,电子层越多,半径越大,同周期,越靠右半径越小,故
原子半径 ,B项正确;C为O,D为Na,可以形成过氧化钠,其中含有共价键,C项错误;非金
属性越强,简单气态氢化物越稳定,由分析可知B为N,C为O,氧的非金属性较强,则简单气态氢化物
的热稳定性: ,D项错误。
考点二 化学键 分子结构与性质
14.(2024·江苏南京盐城高三一模)下列说法项正确的是
A.金刚石、石墨、 三者互为同位素 B. 分子中存在两个 键
C. 晶体中存在离子键与非极性共价键D.基态 原子的核外电子有6种空间运动状态
【答案】B
【解析】金刚石、石墨、 均是由碳元素形成的不同单质,三者互为同素异形体,A项错误; 分子
中含有碳碳三键,存在两个 键,B项正确; 晶体中存在离子键与极性共价键,没有非极性键,C
项错误;基态 原子的核外电子排布式为1s22s22p2,占有4个轨道,有4种空间运动状态,D项错误。
15.(2024·江苏苏州高三期末)含锂物质在能源方面有重要应用。锂在氧气中燃烧与 Mg相似,其燃烧热
为299 kJ·mol-1。锂与氮气反应得到的LiN可用作储氢材料。锂—空气电池是一种二次电池,放电时主要
3
产物为LiO,充电时阴极产物易形成固态枝晶,导致电池短路。目前应用广泛的是锂离子电池,例如,磷
2 2酸铁锂电池充电时锂离子由 LiFePO 电极迁移至石墨电极形成 LiC ,LiFePO 的前体 FePO 可由
4 x 4 4
NH HPO 、FeSO 、HO 在pH=2的条件下反应制得。
4 2 4 4 2 2
下列说法正确的是( )
A. Li O 中存在Li与O 的强烈相互作用
2 2 2
B. 锂—空气电池充电时形成枝晶的物质属于离子晶体
C. Fe2+的基态核外电子排布式为[Ar]3d54s1
D. PO中P原子轨道的杂化类型为sp3
【答案】D
【解析】LiO 中存在Li+与O的强烈相互作用,A项错误;锂-空气电池充电时形成枝晶是树状的金属Li,
2 2
属于金属晶体,B项错误;Fe2+的基态核外电子排布式为[Ar]3d6,C项错误;PO中P原子价电子对数为
5+3+0×4
=4,原子轨道杂化类型为sp3,D项正确。
2
16.(2024·江苏徐州第一中学、淮阴中学、姜堰中学高三联考)下列说法正确的是
A.S、S、S、S 互为同位素
2 4 6 8
B.SO 中S原子杂化轨道类型为sp2
2
C. Se核外电子排布式为 2 4
34
D.HS和HO的空间构型相同,且均为非极性分子
2 2
【答案】B
【解析】S、S、S、S 为硫元素形成的不同单质,应互为同素异形体,A错误;SO 中S的价层电子对数
2 4 6 8 2
为 ,故原子杂化轨道类型为sp2,B正确; Se位于第四周期第ⅥA族,核外电子排布式
34
为 ,C错误;HS和HO的中心原子均为sp3杂化,空间构型均为“V”型,故均为极性分子,
2 2
D错误。
17.(2024·江苏南通高三第二次调研测试)第四周期过渡元素形成的化合物具有重要作用。黄铜矿
(CuFeS)用Fe (SO ) 溶液浸泡后生成单质硫,所得CuSO 溶液可用于制取纳米Cu O,Cu O能与酸发生反
2 2 4 3 4 2 2
应。CuOTiO 可用于低温下催化氧化HCHO:HCHO(g)+O(g)=====CO(g)+HO(l)。CoCl 具有强氧化性,
x 2 2 2 2 3
可与盐酸反应生成氯气。由NaNO 、Co(NO ) 、HO 和CHCOOH反应生成的配合物Na[Co(NO )]可应用
2 3 2 2 2 3 3 2 6
于K+的鉴定。
下列说法正确的是( )A. Co位于元素周期表的ds区 B. NO和NO中N原子均采取sp2杂化
C. 1 mol[Co(NO )]3-中含有12 molσ键 D. 灼烧时火焰呈现紫色的物质一定是钾盐
2 6
【答案】B
【解析】Co价电子排布为3d74s2,属于Ⅷ族,位于周期表的d区,A项错误;NO中氮原子价电子数为
1/2(5+0×2+1)=3,NO中氮原子价电子数为1/2(5+0×3+1)=3,均为sp2杂化,B项正确;NO中存在两个
N-O键,属于σ键,Co2+与每个NO之间存在配位键,所以1 mol[Co(NO )]3-中含有18 molσ键,C项错
2 6
误;火焰呈紫色说明含有钾元素,也可能是KOH等,D项错误。
18.(2024·江苏苏州市名校高三大联考)卤族元素包括 等,位于周期表VIIA族。卤族元素
形成物质种类众多,磷可形成多种卤化物,其中固态 和 的结构分别是 和
。溴化碘 的化学性质与卤素相似。一种立方钙钛矿结构的金属卤化物晶胞如图所示。下列
说法正确的是
A.相同条件下, 的沸点依次递增
B. 中 与 间的相互作用是极性键
C. 和 中磷原子的杂化方式相同
D.图中所示金属卤化物中 周围最近的 数为12
【答案】C
【解析】含有氢键的氢化物熔沸点较高,HF分子间能形成氢键,所以熔沸点HF最高,HCl、HBr都是分
子晶体,相对分子质量越大,范德华力越大,熔沸点越高,因此沸点应为HF>HBr>HCl,A错误;HClO
的结构式为 ,H和Cl间没有形成化学键,B错误;PCl 分子的中心原子(P)的价层电子对数
3
,中心原子(P)采取sp3杂化, 的中心原子(P)的价层电子对数 ,中心原子(P)采取sp3杂化,二者磷原子的杂化方式相同,C正确;如图所示晶胞中,I-位于面心, 位
于顶角,I-周围最近的 数为4,D错误。
19.(2024·江苏扬州中学高三1月月考)周期表中ⅥA族元素及其化合物应用广泛。O 具有杀菌、消毒、
3
漂白等作用;HS是一种易燃的有毒气体(燃烧热为562.2 kJ/mol),常用于沉淀重金属离子;氯化亚砜
2
(SOCl )是重要的有机试剂;硒( Se)和碲( Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展
2 34 52
前景,Se是人体不可或缺的微量元素,工业上通过电解强碱性NaTeO 溶液制备Te。下列说法不正确的是
2 3
A.16O、17O、18O互为同位素 B.HO+和SOCl 的的中心原子杂化轨道类型均为sp3
3 2
C.HO 为极性分子 D.CaO 中阴阳离子数目比为2:1
2 2 2
【答案】D
【解析】16O、17O、18O是同种元素的不同种原子,互称同位素,A正确;HO+中O原子的价层电子对为3+
3
=4,故O采用sp3杂化,SOCl 中心原子S的价层电子对为3+ =4,故S采用sp3杂化,
2
B正确;HO 分子不是直线形的,两个氢原子在犹如半展开的书的两页上,氧原子则在书的夹缝上,如
2 2
,分子结构不对称,正负电荷重心不重合,为极性分子,C正确;过氧化钙中阴离子为过
氧根离子,1个过氧化钙含有1个钙离子和1个过氧根离子,阴阳离子数目之比为1:1,D错误。
20.(2024·江苏南通海安高三开学考试) B、Al、Ga位于元素周期表中ⅢA族。 为无色气体,主要用作
有机合成中的催化剂,极易水解生成 ( 在水中完全电离为 和 )和硼酸( )。硼酸是一
元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯 ,硼酸甲酯主要用作
热稳定剂、木材防腐剂等。下列说法正确的是
A.GaN晶体中存在配位键 B. 易溶于水C.Ga原子位于周期表中d区 D. 中B原子轨道杂化类型为
【答案】A
【解析】GaN的结构与晶体硅类似,Ga最外层有3个电子,而GaN中Ga与周围四个氮原子相连,因此
GaN晶体中存在配位键,A正确;挥发性的硼酸甲酯 ,酯是难溶于水,因此 难溶于
水,B错误;Ga原子价电子排布式为4s24p1,位于周期表中p区,C错误; 中B原子价层电子对数为
,其B原子轨道杂化类型为 ,D错误。
21.(2024·江苏泰州姜堰中学高三期中) “肼合成酶”以其中的 配合物为催化中心,可将 与
转化为肼 ,其反应历程如下所示。
下列说法正确的是
A. 、 和 均为非极性分子
B.催化中心的 提供孤电子对,N提供空轨道
C.反应过程中Fe元素的化合价发生了变化
D.将 替换为 ,反应可得
【答案】C
【解析】NH OH、NH 和HO分子中正负电荷中心不重合,均为极性分子,A项错误;催化中心的Fe2+提
2 3 2
供空轨道,N提供孤电子对形成配位键,B项错误;反应过程中Fe元素先失去电子,变为Fe3+,后又得到
电子,变为Fe2+,故反应过程中Fe元素的化合价发生了变化,C项正确;ND OD与NH 反应生成ND -
2 3 2
NH 和HDO,D项错误。
222.(2024·江苏扬州高邮高三开学考试)NCl 可发生水解反应 ,下列说法正
3
确的是
A. 中N原子杂化类型为 杂化 B. 为非极性分子
C. 分子空间构型为平面三角形 D. 的电子式为
【答案】D
【解析】NCl 分子中,N原子价电子数为1/2(5+1×3)=4,杂化方式为sp3杂化,A项错误;HO是V性结构,
3 2
为极性分子,B项错误;NH 为sp3杂化,空间构型为三角锥形,C项错误;HClO的电子式为 ,D
3
项正确。
23.(2024·江苏南京师范大学附属中学9月考试)下列说法正确的是
A. 是由极性键构成的极性分子
B. 与 互为同素异形体
C. 和 的中心原子杂化轨道类型均为
D.CaO晶体中 与 的相互作用具有饱和性和方向性
【答案】A
【解析】 是V形结构,由极性键构成的极性分子,A正确;同种元素形成的不同种单质,互称同素异形
体, 与 是化合物,B错误; 形成2个σ键,中心S原子孤电子对数为1, 形成
2个σ键,中心C原子孤电子对数为0,所以 和 的中心原子杂化轨道类型分别为 、 ,C错误;
CaO晶体中 与 的相互作用为离子键,离子键没有饱和性,D错误。
24.(2024·江苏南京六校联合体10月调研)下列说法正确的是
A.HO 是非极性分子 B.SO 中的∠O-S-O与SO 中的相等
2 2 3C.基态Se原子核外价电子排布式为4s24p4 D.VIA族元素氢化物的沸点从上到下依次增大
【答案】C
【解析】HO 是由极性共价键和非极性共价键构成,氧原子为sp3杂化,分子结构不对称,正负电荷中心
2 2
不重合,属于极性分子,A错误;SO 中心原子孤电子对数= 、价层电子对数=3+0=3,故S为
3
sp2杂化、空间构型为平面正三角形, SO 中中心原子孤电子对数= 、价层电子对数
=3+1=4,故S为sp3杂化、空间构型为三角锥形,则SO 中的∠O-S-O与SO 中的不相等,B错误;硒
3
是第四周期ⅥA族元素,故基态Se原子核外价电子排布式为4s24p4,C正确;VIA族元素氢化物中,HO
2
分子间能形成氢键,水的熔沸点最高,D错误。
25.(江苏省淮安市5校2023-2024学年高三上学期10月份联考,5)下列有关NH
2
OH、NH3、 、
的说法正确的是
A.NH OH 难溶于水
2
B. 的空间构型为直线形
C.NH 的键角比 中的大
3
D.1mol [Cu(NH )]2⁺中含有 4mol σ键
3 4
【答案】C
【解析】NH OH能和水形成分子间氢键,所以易溶于水,A错误; 的价层电子数为2+ =3,
2
含有1对孤电子对,VSEPR模型为平面三角形,其空间构型为V形,B错误; 中N原子价层电子对
个数=2+ =4且含有2个孤电子对,NH 中N原子价层电子对个数=3+ =4且含有1个孤电
3
子对,孤电子对之间的排斥力大于孤电子对和成键电子对之间的排斥力,所以NH 的键角比 中的大,
3
C正确;1mol [Cu(NH )]2⁺中含有4mol Cu-Nσ键和12molN-Hσ键,即共16molσ键,D错误。
3 4