文档内容
热点强化练 6 含硫化合物的制备和性质探究
1.(2020·湖南长郡中学高三月考)实验室利用SO 和Cl 在活性炭作用下制取
2 2
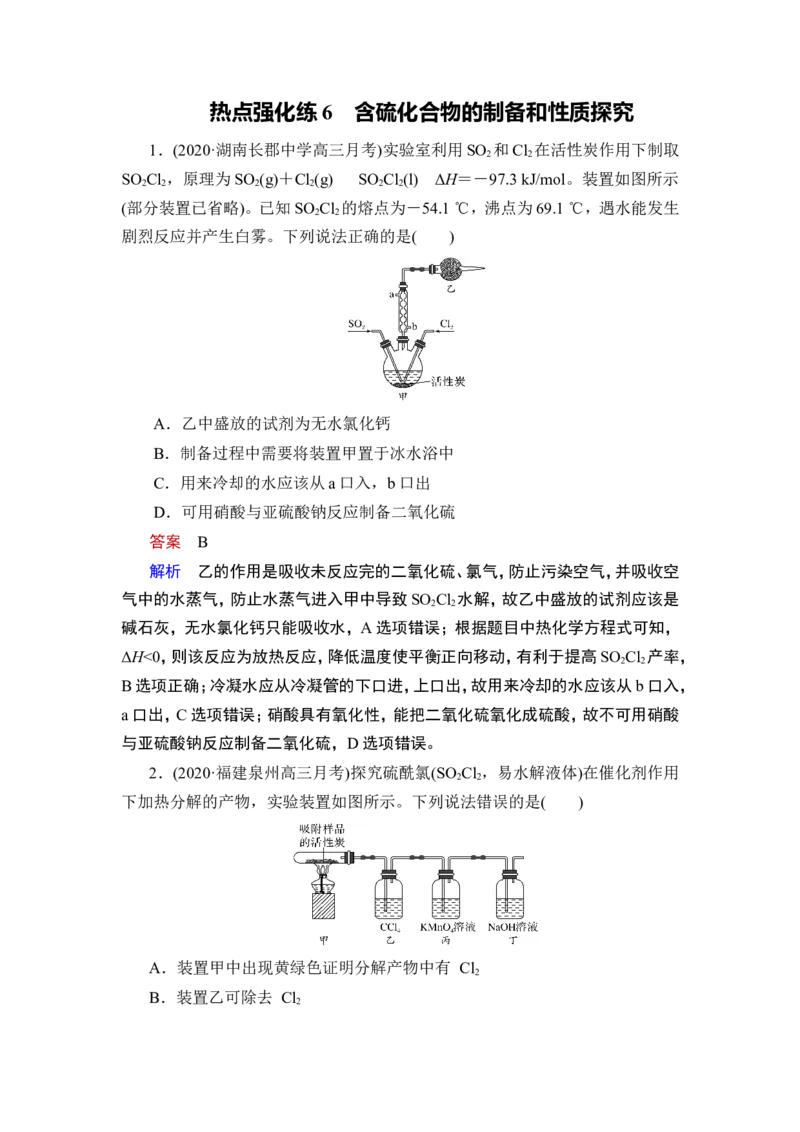
SO Cl ,原理为SO (g)+Cl (g)SO Cl (l) ΔH=-97.3 kJ/mol。装置如图所示
2 2 2 2 2 2
(部分装置已省略)。已知SO Cl 的熔点为-54.1 ℃,沸点为69.1 ℃,遇水能发生
2 2
剧烈反应并产生白雾。下列说法正确的是( )
A.乙中盛放的试剂为无水氯化钙
B.制备过程中需要将装置甲置于冰水浴中
C.用来冷却的水应该从a口入,b口出
D.可用硝酸与亚硫酸钠反应制备二氧化硫
答案 B
解析 乙的作用是吸收未反应完的二氧化硫、氯气,防止污染空气,并吸收空
气中的水蒸气,防止水蒸气进入甲中导致SO Cl 水解,故乙中盛放的试剂应该是
2 2
碱石灰,无水氯化钙只能吸收水,A选项错误;根据题目中热化学方程式可知,
ΔH<0,则该反应为放热反应,降低温度使平衡正向移动,有利于提高SO Cl 产率,
2 2
B选项正确;冷凝水应从冷凝管的下口进,上口出,故用来冷却的水应该从b口入,
a口出,C选项错误;硝酸具有氧化性,能把二氧化硫氧化成硫酸,故不可用硝酸
与亚硫酸钠反应制备二氧化硫,D选项错误。
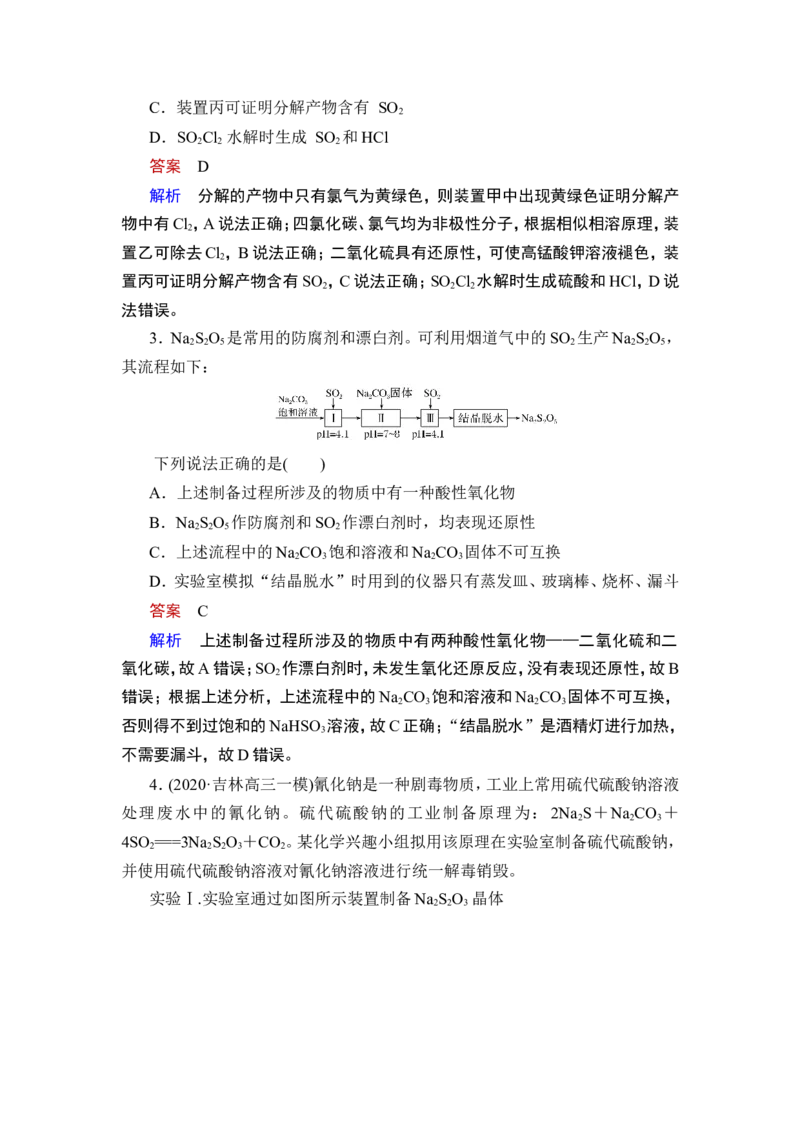
2.(2020·福建泉州高三月考)探究硫酰氯(SO Cl ,易水解液体)在催化剂作用
2 2
下加热分解的产物,实验装置如图所示。下列说法错误的是( )
A.装置甲中出现黄绿色证明分解产物中有 Cl
2
B.装置乙可除去 Cl
2C.装置丙可证明分解产物含有 SO
2
D.SO Cl 水解时生成 SO 和HCl
2 2 2
答案 D
解析 分解的产物中只有氯气为黄绿色,则装置甲中出现黄绿色证明分解产
物中有Cl ,A说法正确;四氯化碳、氯气均为非极性分子,根据相似相溶原理,装
2
置乙可除去Cl ,B说法正确;二氧化硫具有还原性,可使高锰酸钾溶液褪色,装
2
置丙可证明分解产物含有SO ,C说法正确;SO Cl 水解时生成硫酸和HCl,D说
2 2 2
法错误。
3.Na S O 是常用的防腐剂和漂白剂。可利用烟道气中的SO 生产Na S O ,
2 2 5 2 2 2 5
其流程如下:
下列说法正确的是( )
A.上述制备过程所涉及的物质中有一种酸性氧化物
B.Na S O 作防腐剂和SO 作漂白剂时,均表现还原性
2 2 5 2
C.上述流程中的Na CO 饱和溶液和Na CO 固体不可互换
2 3 2 3
D.实验室模拟“结晶脱水”时用到的仪器只有蒸发皿、玻璃棒、烧杯、漏斗
答案 C
解析 上述制备过程所涉及的物质中有两种酸性氧化物——二氧化硫和二
氧化碳,故A错误;SO 作漂白剂时,未发生氧化还原反应,没有表现还原性,故B
2
错误;根据上述分析,上述流程中的Na CO 饱和溶液和Na CO 固体不可互换,
2 3 2 3
否则得不到过饱和的NaHSO 溶液,故C正确;“结晶脱水”是酒精灯进行加热,
3
不需要漏斗,故D错误。
4.(2020·吉林高三一模)氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液
处理废水中的氰化钠。硫代硫酸钠的工业制备原理为:2Na S+Na CO +
2 2 3
4SO ===3Na S O +CO 。某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,
2 2 2 3 2
并使用硫代硫酸钠溶液对氰化钠溶液进行统一解毒销毁。
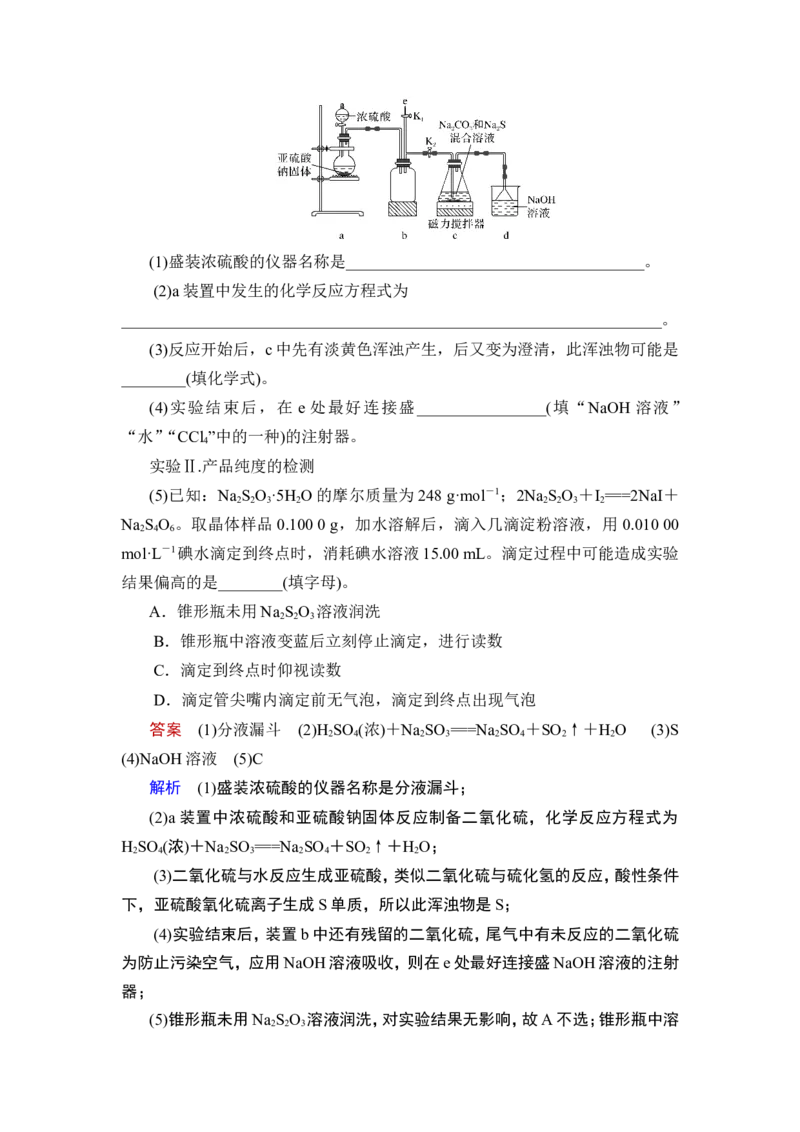
实验Ⅰ.实验室通过如图所示装置制备Na S O 晶体
2 2 3(1)盛装浓硫酸的仪器名称是_____________________________________。
(2)a装置中发生的化学反应方程式为
___________________________________________________________________。
(3)反应开始后,c中先有淡黄色浑浊产生,后又变为澄清,此浑浊物可能是
________(填化学式)。
(4)实验结束后,在 e 处最好连接盛________________(填“NaOH 溶液”
“水”“CCl ”中的一种)的注射器。
4
实验Ⅱ.产品纯度的检测
(5)已知:Na S O ·5H O的摩尔质量为248 g·mol-1;2Na S O +I ===2NaI+
2 2 3 2 2 2 3 2
Na S O 。取晶体样品0.100 0 g,加水溶解后,滴入几滴淀粉溶液,用 0.010 00
2 4 6
mol·L-1碘水滴定到终点时,消耗碘水溶液15.00 mL。滴定过程中可能造成实验
结果偏高的是________(填字母)。
A.锥形瓶未用Na S O 溶液润洗
2 2 3
B.锥形瓶中溶液变蓝后立刻停止滴定,进行读数
C.滴定到终点时仰视读数
D.滴定管尖嘴内滴定前无气泡,滴定到终点出现气泡
答案 (1)分液漏斗 (2)H SO (浓)+Na SO ===Na SO +SO ↑+H O (3)S
2 4 2 3 2 4 2 2
(4)NaOH溶液 (5)C
解析 (1)盛装浓硫酸的仪器名称是分液漏斗;
(2)a装置中浓硫酸和亚硫酸钠固体反应制备二氧化硫,化学反应方程式为
H SO (浓)+Na SO ===Na SO +SO ↑+H O;
2 4 2 3 2 4 2 2
(3)二氧化硫与水反应生成亚硫酸,类似二氧化硫与硫化氢的反应,酸性条件
下,亚硫酸氧化硫离子生成S单质,所以此浑浊物是S;
(4)实验结束后,装置b中还有残留的二氧化硫,尾气中有未反应的二氧化硫
为防止污染空气,应用NaOH溶液吸收,则在e处最好连接盛NaOH溶液的注射
器;
(5)锥形瓶未用Na S O 溶液润洗,对实验结果无影响,故A不选;锥形瓶中溶
2 2 3液变蓝后立刻停止滴定,进行读数,消耗碘水的体积偏小,造成实验结果偏低,故
B不选;滴定到终点时仰视读数,读取的碘水体积偏大,造成实验结果偏高,故C
选;滴定管尖嘴内滴定前无气泡,滴定到终点出现气泡,碘水体积偏小,造成实验
结果偏低,故D不选;答案选C。
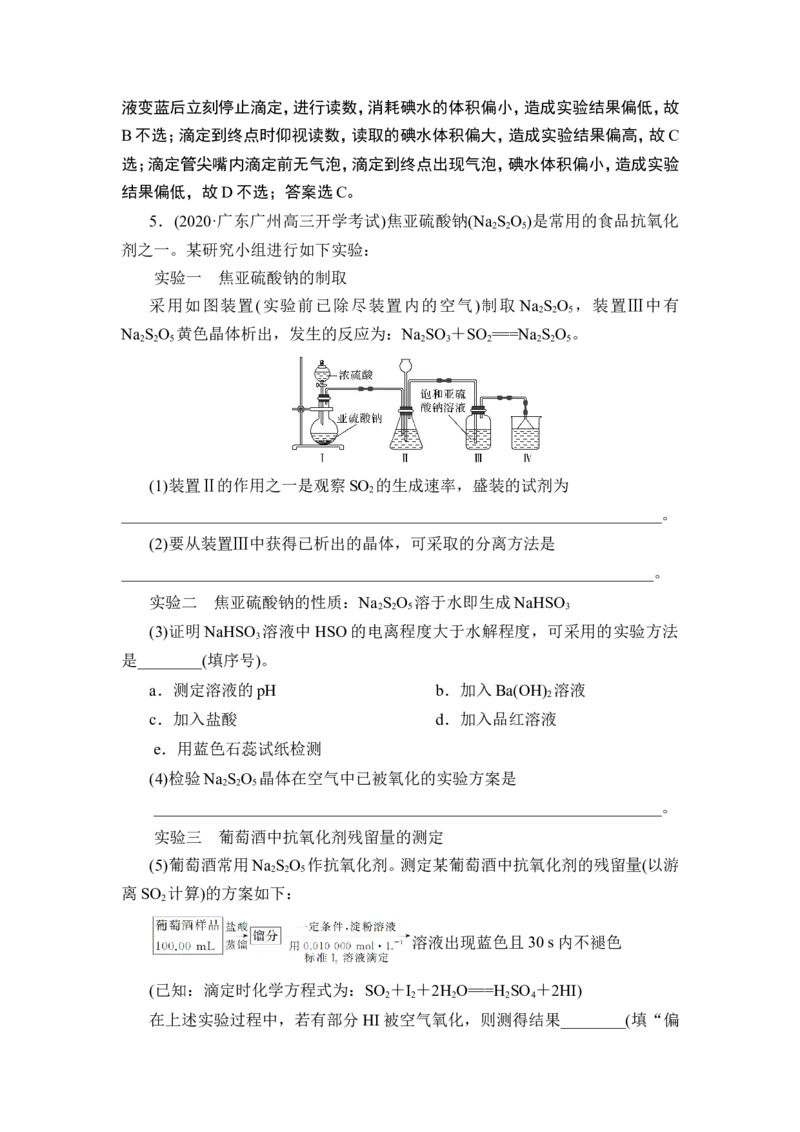
5.(2020·广东广州高三开学考试)焦亚硫酸钠(Na S O )是常用的食品抗氧化
2 2 5
剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
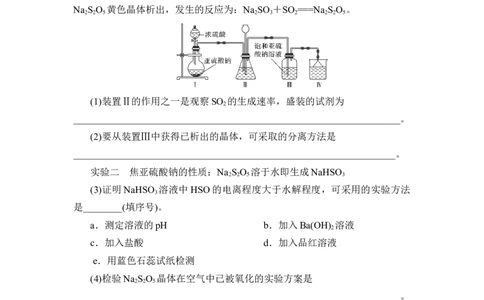
采用如图装置(实验前已除尽装置内的空气)制取 Na S O ,装置Ⅲ中有
2 2 5
Na S O 黄色晶体析出,发生的反应为:Na SO +SO ===Na S O 。
2 2 5 2 3 2 2 2 5
(1)装置Ⅱ的作用之一是观察SO 的生成速率,盛装的试剂为
2
___________________________________________________________________。
(2)要从装置Ⅲ中获得已析出的晶体,可采取的分离方法是
__________________________________________________________________。
实验二 焦亚硫酸钠的性质:Na S O 溶于水即生成NaHSO
2 2 5 3
(3)证明NaHSO 溶液中HSO的电离程度大于水解程度,可采用的实验方法
3
是________(填序号)。
a.测定溶液的pH b.加入Ba(OH) 溶液
2
c.加入盐酸 d.加入品红溶液
e.用蓝色石蕊试纸检测
(4)检验Na S O 晶体在空气中已被氧化的实验方案是
2 2 5
_______________________________________________________________。
实验三 葡萄酒中抗氧化剂残留量的测定
(5)葡萄酒常用Na S O 作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游
2 2 5
离SO 计算)的方案如下:
2
溶液出现蓝色且30 s内不褪色
(已知:滴定时化学方程式为:SO +I +2H O===H SO +2HI)
2 2 2 2 4
在上述实验过程中,若有部分HI被空气氧化,则测得结果________(填“偏高”“偏低”或“不变”)。
答案 (1)饱和NaHSO 溶液 (2)过滤 (3)ae (4)取少量Na S O 晶体于试
3 2 2 5
管中,加适量水溶解,滴加足量盐酸,振荡,再滴入氯化钡溶液,有白色沉淀生成
(5)偏低
解析 (1)二氧化硫易溶于水,不溶于饱和亚硫酸氢钠溶液,为防止二氧化硫
溶于水,同时能观察SO 的生成速率,装置Ⅱ中应盛有饱和亚硫酸氢钠溶液;
2
(2)装置Ⅲ中析出的固体为Na S O 黄色晶体,固液分离应采用过滤的方法;
2 2 5
(3)NaHSO 溶液中HSO的电离程度大于水解程度,溶液呈酸性,测定溶液的
3
pH,可以确定溶液酸碱性;酸性溶液可以使湿润蓝色石蕊试纸变红,而加入
Ba(OH) 溶液、HCl溶液、品红溶液都不能说明溶液呈酸性;
2
(4)Na S O 中S元素的化合价为+4价,可能会被空气中氧气氧化为+6价的
2 2 5
硫酸根离子,检验Na S O 晶体在空气中已被氧化实际上就是用盐酸、氯化钡溶
2 2 5
液检验样品中是否含有硫酸根离子,检验的步骤为取少量Na S O 晶体于试管中
2 2 5
加入适量水溶解,滴加足量盐酸,振荡,再滴加氯化钡溶液,有白色沉淀生成;
(5)若有部分HI被空气氧化又生成I ,导致消耗标准I 溶液的体积偏小,则测
2 2
得结果偏低。
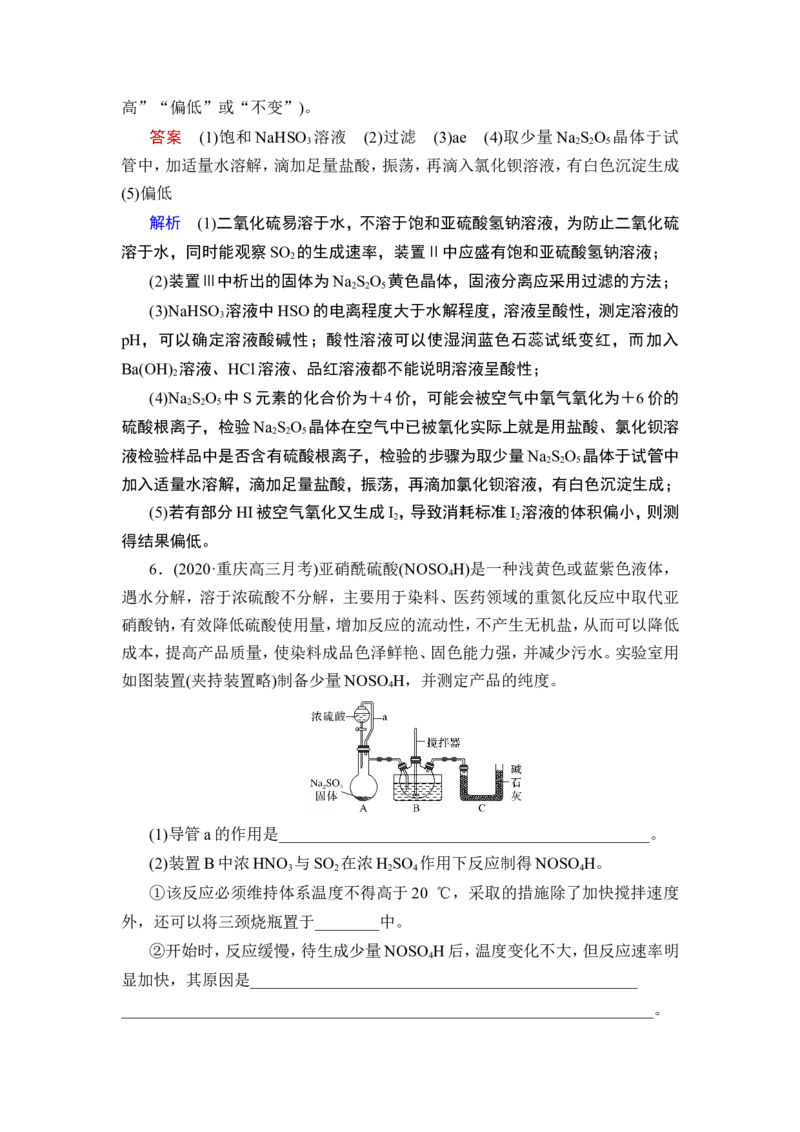
6.(2020·重庆高三月考)亚硝酰硫酸(NOSO H)是一种浅黄色或蓝紫色液体,
4
遇水分解,溶于浓硫酸不分解,主要用于染料、医药领域的重氮化反应中取代亚
硝酸钠,有效降低硫酸使用量,增加反应的流动性,不产生无机盐,从而可以降低
成本,提高产品质量,使染料成品色泽鲜艳、固色能力强,并减少污水。实验室用
如图装置(夹持装置略)制备少量NOSO H,并测定产品的纯度。
4
(1)导管a的作用是______________________________________________。
(2)装置B中浓HNO 与SO 在浓H SO 作用下反应制得NOSO H。
3 2 2 4 4
①该反应必须维持体系温度不得高于20 ℃,采取的措施除了加快搅拌速度
外,还可以将三颈烧瓶置于________中。
②开始时,反应缓慢,待生成少量NOSO H后,温度变化不大,但反应速率明
4
显加快,其原因是________________________________________________
__________________________________________________________________。③该实验装置存在可能导致NOSO H产量降低的缺陷是
4
______________________________________________________________。
④装置C的作用是______________________________________________。
⑤已知亚硝酸不稳定,易分解,发生反应2HNO ===NO ↑+NO↑+H O。请
2 2 2
写出NOSO H遇水分解时发生反应的化学方程式
4
___________________________________________________________________。
(3)已知:2KMnO +5NOSO H+2H O===K SO +2MnSO +5HNO +
4 4 2 2 4 4 3
2H SO 。在上述反应中NOSO H体现了________(填“氧化”或“还原”)性。
2 4 4
答案 (1)平衡分液漏斗与烧瓶内的压强,使浓硫酸顺利流下 (2)①冷水浴
②生成的 NOSO H 作该反应的催化剂 ③装置 A 中的水蒸气会进入 B 中使
4
NOSO H 水解 ④防止空气中的水蒸气进入 B 中使 NOSO H 水解;吸收尾气
4 4
SO ,防止污染环境 ⑤2NOSO H+H O===2H SO (浓)+NO↑+NO ↑ (3)还
2 4 2 2 4 2
原
解析 装置A是利用亚硫酸钠和浓硫酸反应:Na SO +H SO ===Na SO +
2 3 2 4 2 4
SO ↑+H O制取SO ,制取的SO 通入B装置中,HNO 与SO 在浓H SO 作用
2 2 2 2 3 2 2 4
下在冷水浴中反应制得NOSO H,由于亚硝酰硫酸(NOSO H)遇水分解,且装置A
4 4
中制得的SO 属于大气污染物,不能直接排放到大气中,则装置C中的碱石灰的
2
作用是吸收SO ,防止空气中的水蒸气进入装置B中。
2
(1)根据分析,导管a的作用是平衡分液漏斗与烧瓶内的压强,使浓硫酸顺利
流下;
(2)①该反应必须维持体系温度不得高于20 ℃,采取的措施除了加快搅拌速
度外,还可以将三颈烧瓶置于冷水浴中;
②开始反应缓慢,待生成少量NOSO H后,温度变化不大,但反应速度明显
4
加快,其原因是:生成的NOSO H作为反应的催化剂;
4
③由于亚硝酰硫酸(NOSO H)遇水分解,该实验装置存在可能导致NOSO H
4 4
产量降低的缺陷是装置A中的水蒸气会进入B中使NOSO H水解;
4
④根据分析,装置C的作用是防止空气中的水蒸气进入B中使NOSO H水解
4
吸收尾气SO ,防止污染环境;
2
⑤已知亚硝酸不稳定,易分解,发生反应2HNO ===NO ↑+NO↑+H O。
2 2 2
NOSO H遇水分解时发生反应的化学方程式 2NOSO H+H O===2H SO +NO↑
4 4 2 2 4
+NO ↑;
2
(3)在上述反应中NOSO H转化为硫酸盐和硝酸,硫元素的化合价没有发生
4变化,N元素的化合价由+3价升高到+5价,失电子发生氧化反应,体现了还原
性。