文档内容
第 03 讲 氧化还原反应
1.成语是中华民族灿烂文化中的瑰宝,许多成语中蕴含着丰富的化学原理,下列成语中涉及氧化还
原反应的是
A.铁杵成针 B.闭门造车 C.抱薪救火 D.刻舟求剑
2.氧化还原反应在许多领域里都有涉及,对人类的生产和生活意义重大。下列生产生活过程中,不
涉及氧化还原反应的是
A.在高温条件下冶炼黑色金属锰、铬等B.施入土壤的肥料由铵态氮转化为硝态氮
C.用蓄电池为电动汽车供电 D.用氯化铵溶液去除铁锈
3.下列物质的应用中,与氧化还原反应无关的是
A.用含Fe O 的铁矿石冶炼Fe B.用NaO 作潜水艇的供氧剂
2 3 2 2
C.用NaOH作沉淀剂去除粗盐水中的Mg2+ D.以NH 为原料制备HNO
3 3
4.反应 中,还原剂是
A. B.HCl C. D.
5.下列物质之间的转化,需要加入氧化剂才能实现的是
A. B.
C. D.
6.在45~ 50°C时,臭氧(O )可以将碘氧化为碘酸碘[I(IO )]。反应的化学方程式如下:
3 3 3
9O+2I =I(IO)+ 9O 。下列说法正确的是
3 2 3 3 2
A.O 既不是氧化剂也不是还原剂
3
B.I(IO ) 中碘元素的化合价均为+5
3 3
C.氧化性:I(IO )>I
3 3 2
D.氧化性:I> I(IO )
2 3 3
7.三氟化氯(ClF )可应用于航天工业,是一种很强的氧化剂和氟化剂,它能与大多数有机和无机材料
3
甚至塑料反应,可以使许多材料不接触火源就燃烧。下列分析错误的是A.可以代替HO 充当火箭推进剂中的氧化剂
2 2
B.能与一些金属反应生成氯化物和氟化物
C.三氟化氯可用于清洁化学气相沉积的反应舱附着的半导体物质
D.ClF 与水按照1:2反应生成两种强酸
3
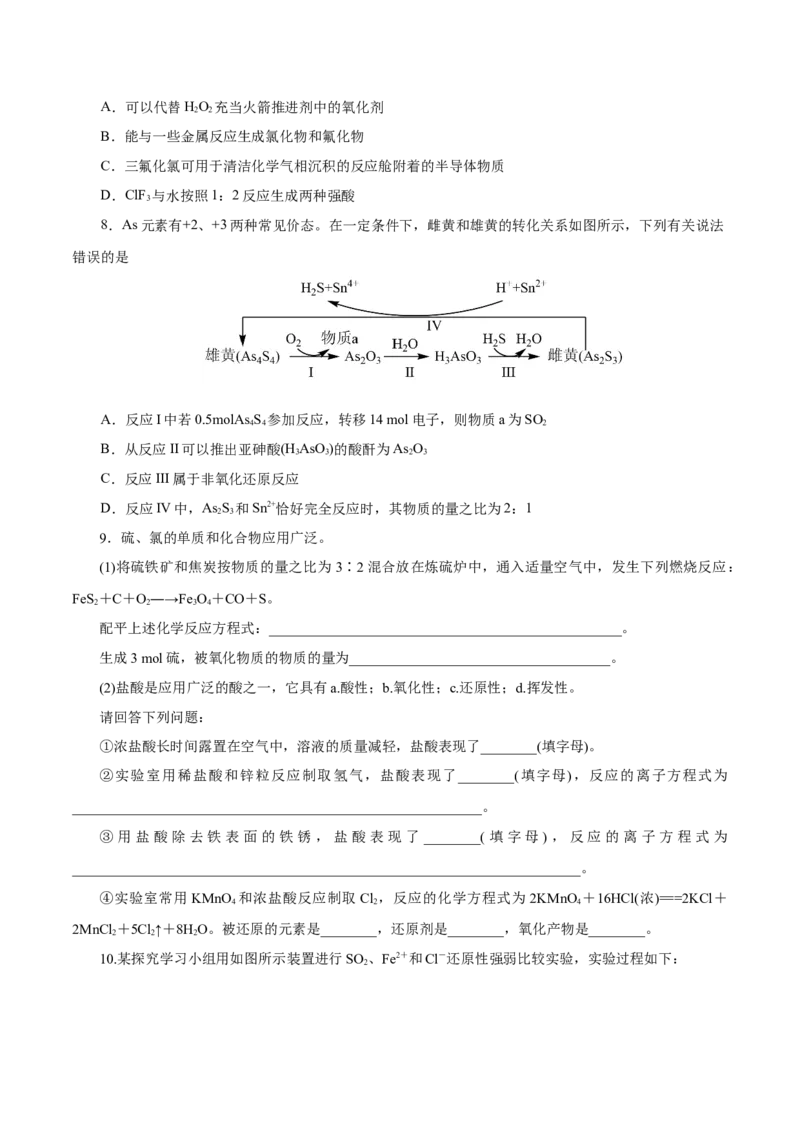
8.As元素有+2、+3两种常见价态。在一定条件下,雌黄和雄黄的转化关系如图所示,下列有关说法
错误的是
A.反应I中若0.5molAs S 参加反应,转移14 mol电子,则物质a为SO
4 4 2
B.从反应II可以推出亚砷酸(H AsO )的酸酐为As O
3 3 2 3
C.反应III属于非氧化还原反应
D.反应IV中,As S 和Sn2+恰好完全反应时,其物质的量之比为2:1
2 3
9.硫、氯的单质和化合物应用广泛。
(1)将硫铁矿和焦炭按物质的量之比为 3∶2混合放在炼硫炉中,通入适量空气中,发生下列燃烧反应:
FeS+C+O―→Fe O+CO+S。
2 2 3 4
配平上述化学反应方程式:__________________________________________________。
生成3 mol硫,被氧化物质的物质的量为_____________________________________。
(2)盐酸是应用广泛的酸之一,它具有a.酸性;b.氧化性;c.还原性;d.挥发性。
请回答下列问题:
①浓盐酸长时间露置在空气中,溶液的质量减轻,盐酸表现了________(填字母)。
②实验室用稀盐酸和锌粒反应制取氢气,盐酸表现了________(填字母),反应的离子方程式为
__________________________________________________________。
③用盐酸除去铁表面的铁锈,盐酸表现了 ________(填字母),反应的离子方程式为
________________________________________________________________________。
④实验室常用KMnO 和浓盐酸反应制取Cl ,反应的化学方程式为 2KMnO +16HCl(浓)===2KCl+
4 2 4
2MnCl +5Cl↑+8HO。被还原的元素是________,还原剂是________,氧化产物是________。
2 2 2
10.某探究学习小组用如图所示装置进行SO 、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
2Ⅰ.先向B中的FeCl 溶液(约10 mL)中通入Cl,当B中溶液变黄时,停止通气。
2 2
Ⅱ.打开活塞b,使约2 mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO 气体。
2
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为__________,目的是_________________________________。
(2)实验室制备氯气的化学方程式为__________________________________________。
(3)过程Ⅲ中一定发生反应的离子方程式为____________________________________;过程Ⅳ中检验取
出溶液中是否含有硫酸根离子的操作是________________________________________________。
(4)该小组对SO 、Fe2+和Cl-还原性强弱比较期望达到的结论是_________________。
2
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明
SO 、Fe2+和Cl-还原性强弱关系的是__________________。
2
过程Ⅱ中检出离子 过程Ⅳ中检出离子
甲 有Fe3+无Fe2+ 有SO
乙 既有Fe3+又有Fe2+ 有SO
丙 有Fe3+无Fe2+ 有Fe2+
11.关于反应4CO+SiH =======4CO+2HO+SiO,下列说法正确的是
2 4 2 2
A.CO是氧化产物 B.SiH 发生还原反应
4
C.氧化剂与还原剂的物质的量之比为1∶4 D.生成1molSiO 时,转移8mol电子
2
12.溴化钾(KBr)可作为分析试剂、感光剂、神经镇静剂等,工业上制取溴化钾的方法之一为:先将尿
素(H NCONH)加到KCO 溶液中,然后在不断搅拌下缓慢注入液溴,随即发生反应:
2 2 2 3
3KCO+H NCONH+3Br =6KBr+4CO ↑+N ↑+2H O。下列有关此反应的说法正确的是
2 3 2 2 2 2 2 2
A.尿素作还原剂,CO、N 是氧化产物
2 2
B.若制取1mol KBr,转移电子数目为2N
A
C.此方法成本低,且制得的KBr纯净
D.实验室中KBr密封保存在无色广口瓶中13.实验室中为研究不同物质之间的反应进行如下实验。下列说法正确的是
A.丙为还原产物,丁为氧化产物
B.上述有4个氧化还原反应
C.每生成标准状况下 气体丙,消耗
D.若 完全反应,转移 个电子( 为阿伏加德罗常数的值)
14.汽车尾气常用三效催化剂处理,其表面物质转化关系如图所示。下列说法正确的是
A.该过程的催化剂是Ba(NO )
3 2
B.转化过程中,氮元素均被还原
C.还原过程中生成0.1molN,转移电子数为2mol
2
D.三效催化剂使汽车尾气中污染物转化为无毒物质
15.次磷酸钠(NaH PO )可用作药物和镀镍时的还原剂,反应原理为CuSO +2NaHPO +2NaOH=
2 2 4 2 2
Cu+2NaH PO +Na SO +H ↑。下列说法错误的是
2 3 2 4 2
A.参加反应的NaH PO 有 被CuSO 氧化
2 2 4
B.若1 mol H PO 最多消耗2 mol NaOH,则NaH PO 是酸式盐
3 3 2 3
C.反应中每转移6.02 ×1023个e- ,则生成标准状况下5.6 L H
2
D.NaH PO 和H 均是还原产物
2 3 2
16.高铜酸钾是一种难溶于水的黑色粉末状固体,与高铁酸钾性质相似。可以由四羟基合铜酸钾和次
溴酸在冰水浴中合成:① (未配平)。高铜酸钾在酸性条件下不稳定:② (未配平)。下列说法不正确的是
A.①中氧化剂和还原剂的物质的量之比为1:2
B.②若有标况下5.6L 生成,转移电子
C.②中 既表现氧化性,又表现还原性
D.由①②可知氧化性强弱顺序为:
17.以FeSO 为原料制备锂离子电池的电极材料磷酸亚铁锂(LiFePO )的流程如下:
4 4
下列说法错误的是
A.“沉铁”步骤反应的离子方程式为:2Fe2++H O+2H PO =2FePO↓+2H O+4H+
2 2 3 4 4 2
B.“沉铁”步骤中的氧化剂HO 可以用O 来代替
2 2 3
C.“煅烧”步骤中氧化剂与还原剂的物质的量之比为2:1
D.“煅烧”步骤中每消耗1mol Li CO 时,生成3mol氧化产物
2 3
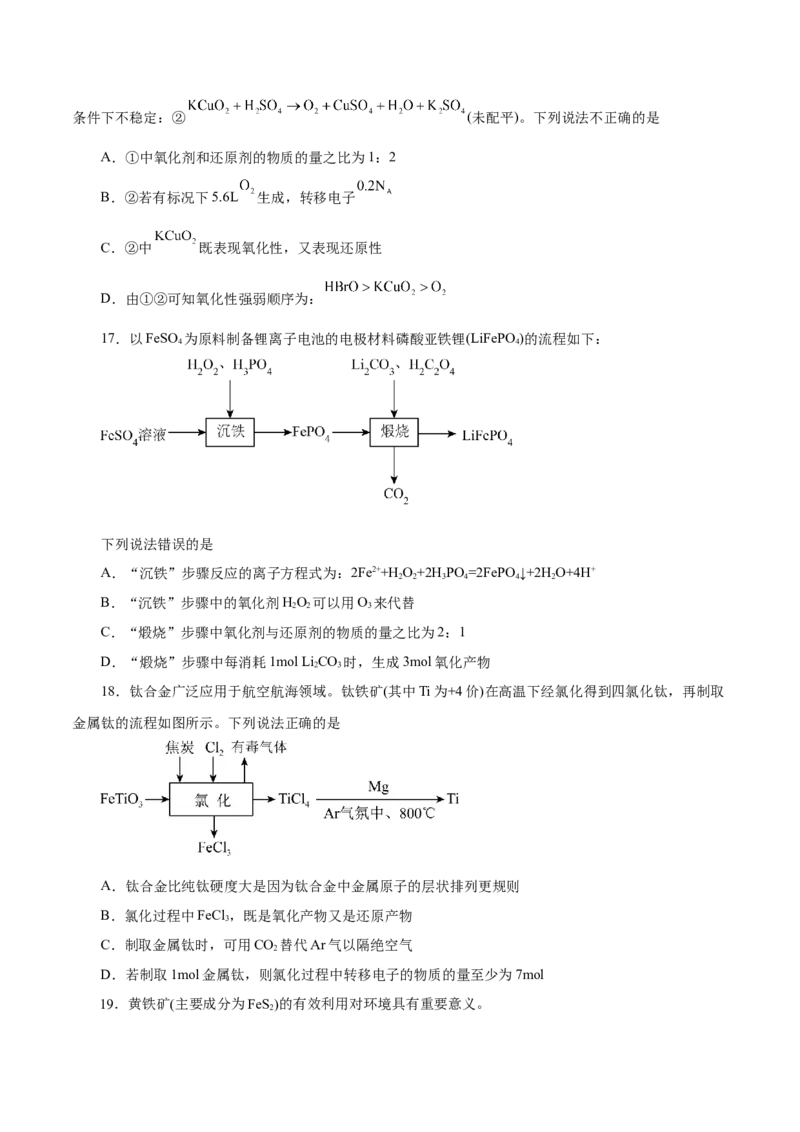
18.钛合金广泛应用于航空航海领域。钛铁矿(其中Ti为+4价)在高温下经氯化得到四氯化钛,再制取
金属钛的流程如图所示。下列说法正确的是
A.钛合金比纯钛硬度大是因为钛合金中金属原子的层状排列更规则
B.氯化过程中FeCl ,既是氧化产物又是还原产物
3
C.制取金属钛时,可用CO 替代Ar气以隔绝空气
2
D.若制取1mol金属钛,则氯化过程中转移电子的物质的量至少为7mol
19.黄铁矿(主要成分为FeS)的有效利用对环境具有重要意义。
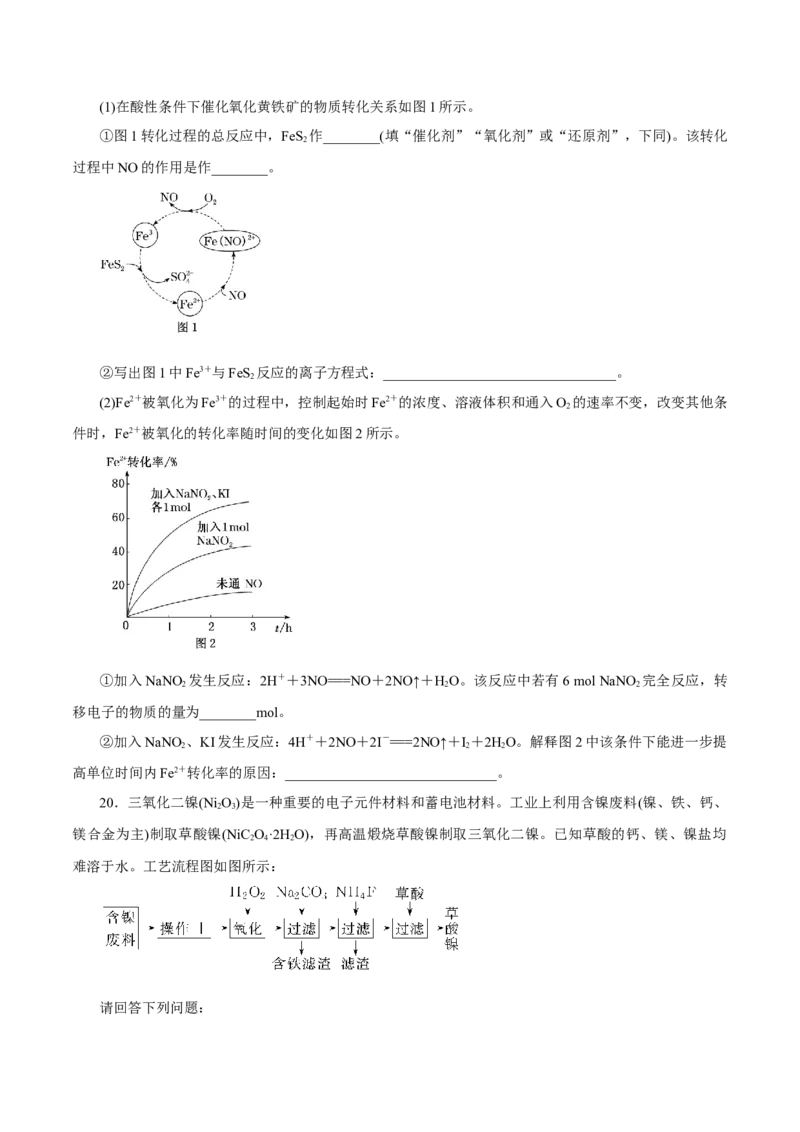
2(1)在酸性条件下催化氧化黄铁矿的物质转化关系如图1所示。
①图1转化过程的总反应中,FeS 作________(填“催化剂”“氧化剂”或“还原剂”,下同)。该转化
2
过程中NO的作用是作________。
②写出图1中Fe3+与FeS 反应的离子方程式:_________________________________。
2
(2)Fe2+被氧化为Fe3+的过程中,控制起始时Fe2+的浓度、溶液体积和通入O 的速率不变,改变其他条
2
件时,Fe2+被氧化的转化率随时间的变化如图2所示。
①加入NaNO 发生反应:2H++3NO===NO+2NO↑+HO。该反应中若有6 mol NaNO 完全反应,转
2 2 2
移电子的物质的量为________mol。
②加入NaNO 、KI发生反应:4H++2NO+2I-===2NO↑+I +2HO。解释图2中该条件下能进一步提
2 2 2
高单位时间内Fe2+转化率的原因:______________________________。
20.三氧化二镍(NiO)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、
2 3
镁合金为主)制取草酸镍(NiC O·2H O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均
2 4 2
难溶于水。工艺流程图如图所示:
请回答下列问题:(1)加入HO 发生的主要反应的离子方程式为_________________________________。
2 2
(2)草酸镍(NiC O·2H O)在热空气中干燥脱水后在高温下煅烧,可制得Ni O ,同时获得混合气体,该
2 4 2 2 3
混合气体的主要成分为(水除外)______________________________________________。
(3)工业上还可用电解法制取Ni O ,用NaOH溶液调NiCl 溶液的pH至7.5,加入适量NaSO 后利用
2 3 2 2 4
惰性电极电解。电解过程中产生的Cl 有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。ClO-
2
氧化Ni(OH) 生成Ni O 的离子方程式为___________________________。
2 2 3
1.(2020·浙江卷)反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化产物与还原产物的物质的
2 2 2 2
量之比是( )
A. 1:2 B. 1:1 C. 2:1 D. 4:1
2.(2020·北京卷)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl
2
C.NO D.NaO
2 2
3.(2019·浙江选考)反应8NH +3Cl N+6NH Cl,被氧化的NH 与被还原的Cl 的物质的量之比
3 2 2 4 3 2
为( )
A.2∶3 B.8∶3 C.6∶3 D.3∶2
4. (2018·北京卷)下列实验中的颜色变化,与氧化还原反应无关的是( )
选项 A B C D
NaOH溶液滴 石蕊溶液滴入 NaS溶液滴入 热铜丝插入稀
实验 2
入FeSO 溶液中 氯水中 AgCl浊液中 硝酸中
4
产生白色沉淀,随 溶液变红,随 沉淀由白色逐 产生无色气体,随
现象
后变为红褐色 后迅速褪色 渐变为黑色 后变为红棕色