文档内容
第九章 化学实验基础及综合实验
能力提升检测卷
时间:90分钟 分值:100分
可能用到的相对原子质量:H 1 C 12 N14 O16 V 51 Fe 56
一、选择题(每小题有一至二个正确选项,共16*3分)
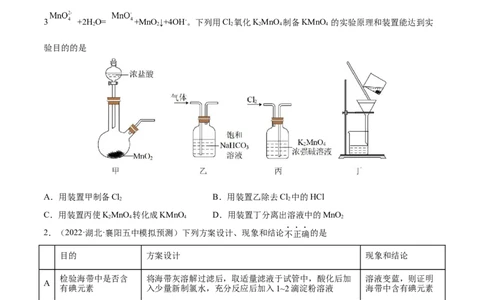
1.(2022·山东临沂·三模)已知锰酸钾(K MnO )在浓的强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3 +2H O= +MnO↓+4OH-。下列用Cl 氧化KMnO 制备KMnO 的实验原理和装置能达到实
2 2 2 2 4 4
验目的的是
A.用装置甲制备Cl B.用装置乙除去Cl 中的HCl
2 2
C.用装置丙使KMnO 转化成KMnO D.用装置丁分离出溶液中的MnO
2 4 4 2
2.(2022·湖北·襄阳五中模拟预测)下列方案设计、现象和结论不正确的是
目的 方案设计 现象和结论
检验海带中是否含 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加 溶液变蓝,则证明
A
有碘元素 入少量新制氯水,充分反应后加入1~2滴淀粉溶液 海带中含有碘元素
取少量淀粉于锥形瓶中,以固液比1∶10加入稀硫酸,
鉴定淀粉是否完全 溶液未变蓝,则证
B 牛皮纸封口,在120℃下水解30min,取适量水解液于试
水解 明淀粉已完全水解
管中,加入少量碘-碘化钾溶液
检验CO还原 溶液变血红色,则
将适量反应后的固体溶于稀盐酸中,取少量溶解液于试
C 的生成物中是否含 证明还原产物中含
管中,滴加硫氰化钾溶液
有
有
在一支洁净的试管中滴加几滴氨水,将湿润的红色石蕊 若试纸由红色变为
D 氨水中NH 检验
3 试纸粘在玻璃棒上靠近试管口,观察试纸颜色变化。 蓝色,则有NH
33.(2022·海南海口·二模)用如图所示装置进行下列实验,装置正确并能达到实验目的的是
选项 ①中试剂 2中溶液 实验目的
酸性高锰酸钾溶
A 浓硫酸、无水乙醇(沸石) 检验有乙烯气体生成
液
B Cu、浓硫酸 溴水 验证 的还原性
C 乙醇、乙酸、浓硫酸 饱和碳酸钠溶液 制取乙酸乙酯
D 澄清石灰水
验证 的热稳定性
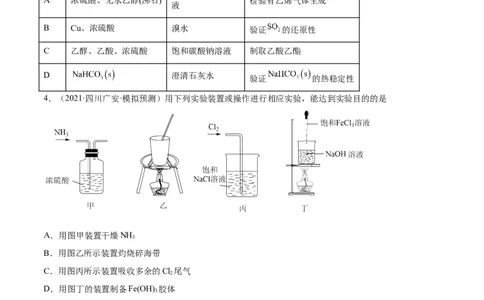
4.(2021·四川广安·模拟预测)用下列实验装置或操作进行相应实验,能达到实验目的的是
A.用图甲装置干燥NH
3
B.用图乙所示装置灼烧碎海带
C.用图丙所示装置吸收多余的Cl 尾气
2
D.用图丁的装置制备Fe(OH) 胶体
3
5.(2022·内蒙古包头·一模)根据下列实验操作及现象,所得结论正确的是
选项 实验操作 现象 结论
相同温度下,分别向NaA和NaB稀溶液中
A NaB溶液红色更深 酸的强弱:HA > HB
滴加酚酞试液
向纯碱固体中滴加足量稀硫酸,将产生的气
B 水玻璃变浑浊 非金属性:S>C>Si
体通入水玻璃中
C 将酸性KMnO 溶液滴入烯丙醇(CH=CH- 溶液的紫红色褪去 烯丙醇中含有碳碳双键
4 2CHOH)中
2
产生有刺激性气味的气 原溶液中定含有 或
D 向某待测溶液中滴加稀硫酸
体
6.(2022·广东惠州·二模)“汲水而上,于釜中煎炼,顷刻结盐,色成至白”(《天工开物》生产井盐)。
上述古代研究成果中涉及的物质分离操作是
A.蒸馏 B.萃取分液 C.蒸发结晶 D.趁热过滤
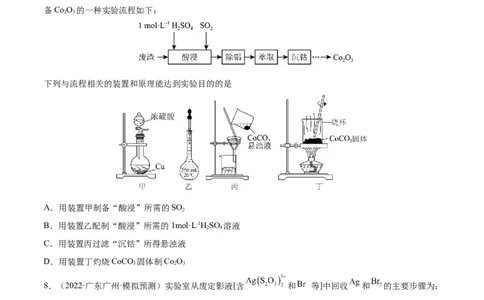
7.(2022·山东青岛·模拟预测)以含钴废渣(主要成分CoO、Co O,还含有Al O、ZnO等杂质)为原料制
2 3 2 3
备Co O 的一种实验流程如下:
2 3
下列与流程相关的装置和原理能达到实验目的的是
A.用装置甲制备“酸浸”所需的SO
2
B.用装置乙配制“酸浸”所需的1mol·L-1HSO 溶液
2 4
C.用装置丙过滤“沉钴”所得悬浊液
D.用装置丁灼烧CoCO 固体制Co O
3 2 3
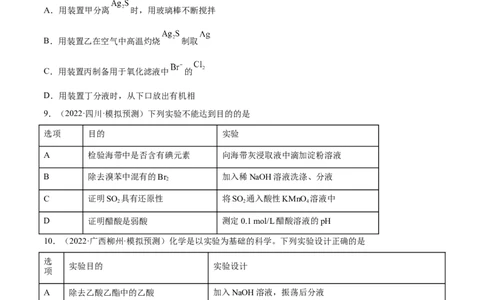
8.(2022·广东广州·模拟预测)实验室从废定影液[含 和 等]中回收 和 的主要步骤为:
向废定影液中加入 溶液沉银,过滤、洗涤及干燥,灼烧 制 ,制取 并通入滤液氧化 ,
用苯萃取分液。其中部分操作的装置如图,下列叙述正确的是A.用装置甲分离 时,用玻璃棒不断搅拌
B.用装置乙在空气中高温灼烧 制取
C.用装置丙制备用于氧化滤液中 的
D.用装置丁分液时,从下口放出有机相
9.(2022·四川·模拟预测)下列实验不能达到目的的是
选项 目的 实验
A 检验海带中是否含有碘元素 向海带灰浸取液中滴加淀粉溶液
B 除去溴苯中混有的Br 加入稀NaOH溶液洗涤、分液
2
C 证明SO 具有还原性 将SO 通入酸性KMnO 溶液中
2 2 4
D 证明醋酸是弱酸 测定0.1 mol/L醋酸溶液的pH
10.(2022·广西柳州·模拟预测)化学是以实验为基础的科学。下列实验设计正确的是
选
实验目的 实验设计
项
A 除去乙酸乙酯中的乙酸 加入NaOH溶液,振荡后分液
B 验证非金属性:O>S 向 溶液中通入 ,观察溶液变浑浊
C 由 溶液制备无水 将 溶液加热蒸干
配制100mL一定物质的量浓度的 准确称取NaOH固体,放入100mL的容量瓶中,加水溶解,
D
NaOH溶液 振荡摇匀,定容
11.(2022·河北·模拟预测)下列说法不正确的是
A.钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火B.油脂、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应
C.除去干燥 中混有的少量 ,可将混合气体依次通过盛有酸性 溶液、浓硫酸的洗气瓶
D.“中和滴定”实验中,锥形瓶用蒸馏水洗涤后即可使用,滴定管用蒸馏水洗涤后,需经润洗方可使用
12.(2022·四川雅安·三模)下列操作与现象、结论均正确的是
选
操作与现象 结论
项
A 向FeSO 溶液中加入少量的NaO 粉末,产生红褐色沉淀 硫酸亚铁已变质
4 2 2
钠的密度大于乙醇的密度,且生成的气
B 在乙醇中加入一小块钠,钠沉入底部并观察到气泡产生
体为氢气
用CaCl 溶液可鉴别KHCO 溶液和
C 向NaHCO 溶液中加入CaCl 溶液,产生白色沉淀 2 3
3 2 (NH )CO 溶液
4 2 3
向Cu(NO ) 溶液中加入含淀粉的KI溶液,溶液变蓝色,
D 3 2 白色沉淀是CuI
并生成白色沉淀 2
13.(2022·山西晋中·二模)下列实验中,现象及结论都正确,且二者之间有因果关系的是
选项 实验操作 现象 结论
A 向FeI 溶液中通入少量Cl 溶液变黄 Cl 的氧化性强于Fe3+
2 2 2
向NaCl、NaBr的混合稀溶液中滴入少量稀AgNO 有浅黄色
B 3 K (AgCl) > K (AgBr)
溶液 沉淀生成 sp sp
C 常温下,向NaHS溶液中滴加石蕊试液 溶液变蓝 K >K (H S)·K (H S)
w a1 2 a2 2
向盛有2 mL一定浓度的Na [Ag(S O)]
3 2 3 2 产生黄色沉
D [Ag(S O)]3- 能够完全电离
淀 2 3 2
溶液的试管中,滴入5滴2 mol· L-1KI溶液
14.(2022·山东潍坊·二模)下列由实验现象所得结论正确的是
A.取补铁口服液的上层清液,滴加酸性KMnO 溶液,溶液紫色褪去,证明口服液中含有Fe2+
4
B.向盛有0.01mol/L的CHCOONa溶液的小试管中滴加酚酞溶液,溶液变红,再加入少量CHCOONa固
3 3
体,溶液红色加深,证明CHCOONa水解程度增大
3
C.向盛有稀硝酸的试管中加入铜片,加热,试管口出现红棕色气体,证明铜与稀硝酸反应生成NO
2
D.将溴乙烷与氢氧化钠的醇溶液共热,产物通入到溴水中,溴水褪色,证明溴乙烷发生消去反应
15.(2022·湖南·模拟预测)下列实验操作不当的是
A.用稀硫酸和锌粒制取 时,为了加快反应速率,取用的锌粒纯度越高越好B.用标准HCl溶液滴定 溶液来测定其浓度,选择甲基橙为指示剂
C.用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有 而不含
D.常压蒸馏时,加入液体的体积不超过圆底烧瓶容积的三分之二
16.(2022·湖南·株洲市九方中学二模)氧化铍(BeO)在航天航空等领域有着广泛的应用。一种以预处理后
的硅铍矿(主要含BeO、Fe O、SiO 和FeO等)为原料提取BeO的流程如下图所示:
2 3 2
已知:Be(OH) 具有两性,在强碱性溶液中可转化为BeO 。下列说法错误的是
2
A.“酸浸”步骤所得“滤渣①”的主要成分为Si
B.“滤液②”经处理后可获得副产品NaSO ·10H O
2 4 2
C.“碱溶”时,主要反应为Be(OH) +2OH-=BeO +2HO
2 2
D.“水解”时,适当增大溶液pH有利于提高BeO的提取率
二、主观题(共5小题,共52分)
17.(2022·湖南·模拟预测)(11分)硝基苯可用于生产染料、香料、炸药等。实验室可用浓硫酸、浓硝
酸、苯为原料制备一定量的硝基苯(硝基苯的密度为1.2g·cm-3,沸点210℃;苯的密度为0.88g·cm-3,沸点
为80.1℃)。
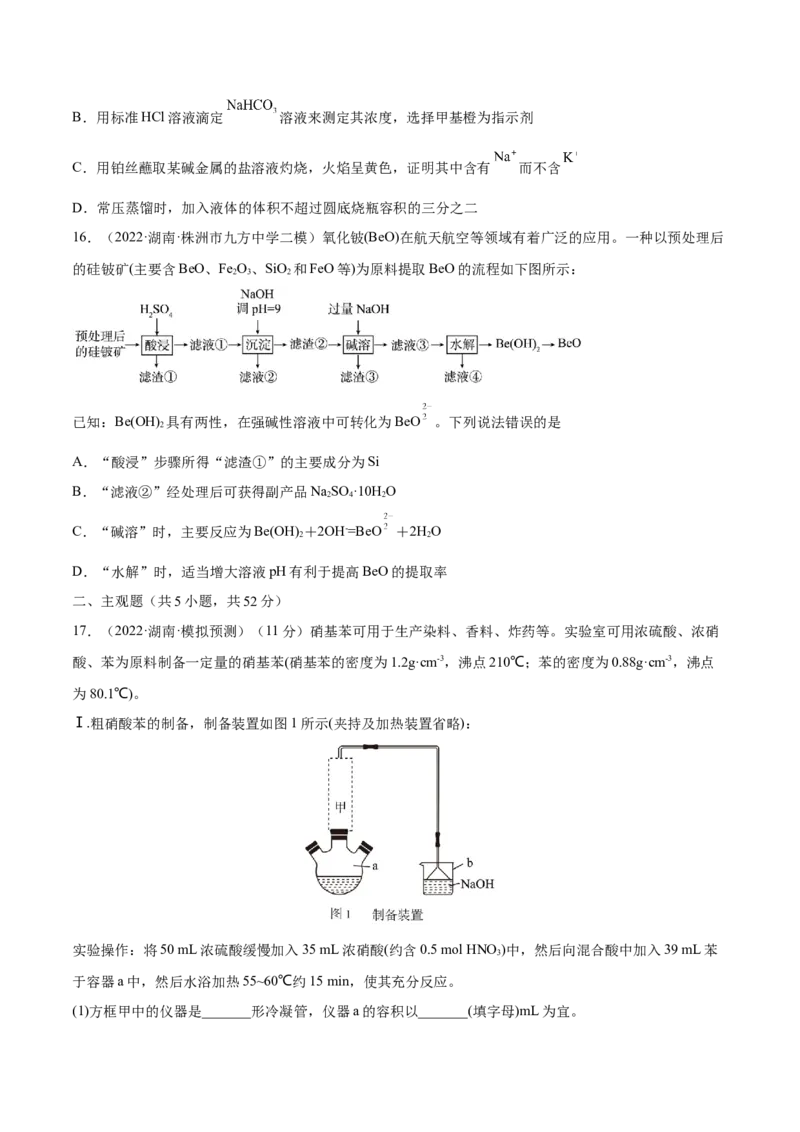
Ⅰ.粗硝酸苯的制备,制备装置如图1所示(夹持及加热装置省略):
实验操作:将50 mL浓硫酸缓慢加入35 mL浓硝酸(约含0.5 mol HNO )中,然后向混合酸中加入39 mL苯
3
于容器a中,然后水浴加热55~60℃约15 min,使其充分反应。
(1)方框甲中的仪器是_______形冷凝管,仪器a的容积以_______(填字母)mL为宜。A.150 B.200 C.500 D.1000
(2)若将硝酸加入硫酸中,除易导致液体溅出,还易产生的不良后果是_______ , 水浴加热时,除需要水
浴锅、热源外,还必须使用的一种玻璃仪器是_______。
Ⅱ.硝基苯精制
实验操作:将a中混合液与适量稀NaOH溶液混合,然后进行操作X,接着依次进行水洗→Y→蒸馏(蒸馏
装置如图2所示)。
(3)操作X的主要内容是_______,水洗的目的是_______,操作Y所用试剂应具有的一种性质是_______。
(4)蒸馏过程中仪器c至少需要使用_______个(次);向乙中通冷却水与加热烧瓶的顺序是_______,若最终
得到36mL精制产品,则硝基苯的产率是_______(保留三位有效数字)。
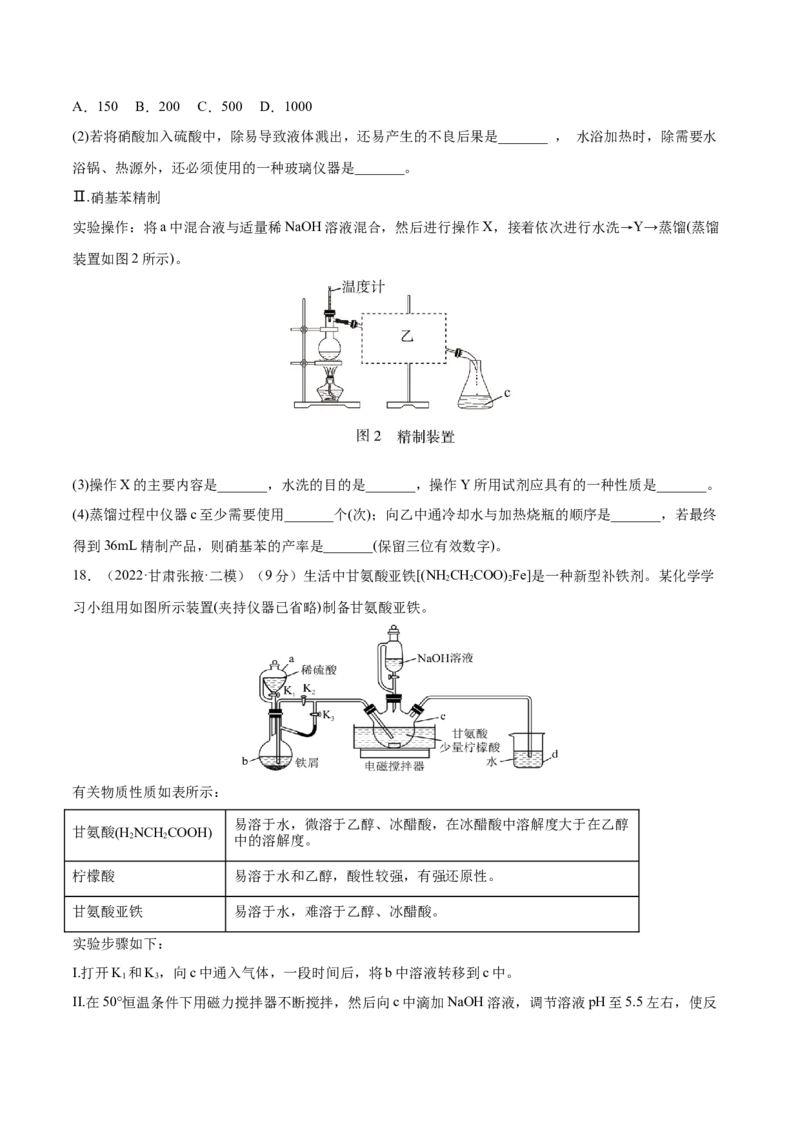
18.(2022·甘肃张掖·二模)(9分)生活中甘氨酸亚铁[(NH CHCOO) Fe]是一种新型补铁剂。某化学学
2 2 2
习小组用如图所示装置(夹持仪器已省略)制备甘氨酸亚铁。
有关物质性质如表所示:
易溶于水,微溶于乙醇、冰醋酸,在冰醋酸中溶解度大于在乙醇
甘氨酸(H NCH COOH)
2 2 中的溶解度。
柠檬酸 易溶于水和乙醇,酸性较强,有强还原性。
甘氨酸亚铁 易溶于水,难溶于乙醇、冰醋酸。
实验步骤如下:
I.打开K 和K,向c中通入气体,一段时间后,将b中溶液转移到c中。
1 3
II.在50°恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加NaOH溶液,调节溶液pH至5.5左右,使反应物充分反应。
III.反应完成后,向c中反应混合物中加入无水乙醇,生成白色沉淀,将沉淀过滤、洗涤得到粗产品,将粗
产品纯化后得精品。
回答下列问题:
(1)仪器a的名称为____;实验开始首先打开K 和K,向c中通入气体一段时间的目的是___;装置d的作
1 3
用是____。
(2)步骤I中将b中溶液转移到c中的操作是____。
(3)反应混合液中柠檬酸的作用除了调节溶液的pH外还有一个作用是____。
(4)在50℃恒温条件下用磁力搅拌器不断搅拌,然后向c中滴加NaOH溶液,调节溶液pH至5.5左右,pH
过低甘氨酸亚铁产率将下降,其原因为____。
(5)产品中Fe2+含量的检测:称取mg样品溶解于适量蒸馏水中,配制成250.0mL溶液。用移液管取出
25.00mL溶液于锥形瓶中,向其中加入一定量混酸进行酸化,用cmol·L-1的KMnO 标准溶液滴定至终点,
4
消耗KMnO 溶液的体积为VmL。滴定终点的现象为____;产品中Fe2+的质量分数为____。
4
19.(2022·江西景德镇·二模)(9分)长期以来,人们认为氮分子不能作配体形成配合物,直到1965年,
化学家Allen偶然制备出了第一个分子氮配合物,震惊了化学界。从此以后,人们对分子氮配合物进行了
大量的研究。利用下图装置以X: FeHCIL (L为一种有机分子)和Z:Na[B(C H)]为原料,在常温下直接
2 6 5 4
与氮气反应可以制备分子氮配合物Y: [FeH(N )L ][B(C H)|。
2 2 6 5 4
相关物质的性质
物质 相对分子质量 性质
X:FeHCIL 504.5 白色固体,易氧化,易溶于有机溶剂
2
橙色晶体,溶液中易氧化,固体较稳定,可溶于丙酮,难溶
Y:[FeH(N )L ][B(C H)] 816
2 2 6 5 4 于于石油醚。
Z:Na[B(C H)] 342 白色固体,易水解,易溶于丙酮,难溶于石油醚
6 5 4(1)组装好仪器,检查装置气密性,通入氮气一段时间。其目的是_______。
(2)向A中加入含X1.5g的120mL的丙酮溶液,B中加入含Z1.5g的50mL的丙酮溶液。仪器A的容积应为
_______ mL(填 250或500)。仪器B的名称为_______。
(3)继续通入氮气,慢慢将B中液体滴入到A中,打开磁力搅拌器揽拌30分钟,停止通气,冰水浴冷却,
析出大量橙色晶体,快速过滤,洗涤,干燥得到粗产品。写出生成产品的化学方程式_______。
(4)将粗产品溶于丙酮,过滤;将滤液真空蒸发得橙色固体,用_______洗涤橙色固体,干燥、称量得到产
品1.5g。计算本实验的产率_______ (用百分数表示, 保留1位小数)。
(5)人们之所以对分子氮配合物感兴趣,是因为某些分子氮配合物可以在常温常压下被还原为NH 。简述该
3
过程的意义_______。
20.(2022·河南河南·二模)(12分)硫酸氧钒( VOSO )是全钒液流储能系统中不可或缺的电解质,实验
4
室围绕VOSO 的相关实验如下:
4
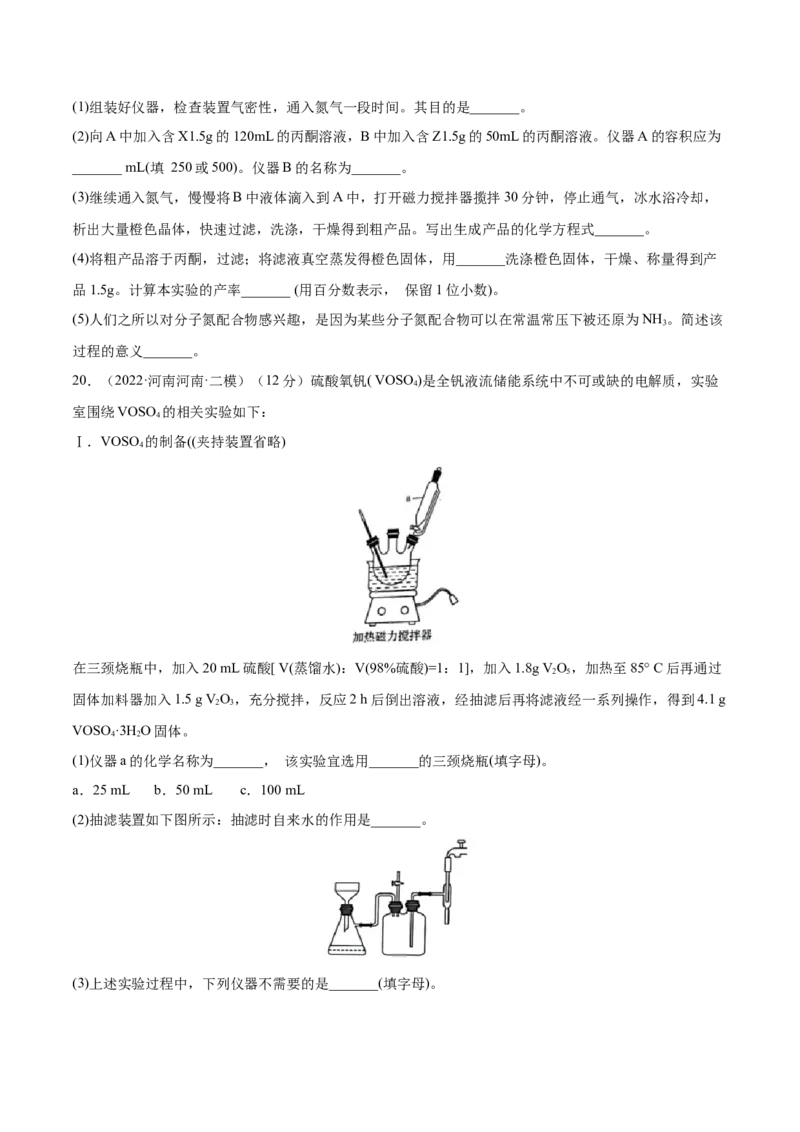
Ⅰ.VOSO 的制备((夹持装置省略)
4
在三颈烧瓶中,加入20 mL硫酸[ V(蒸馏水):V(98%硫酸)=1:1],加入1.8g VO,加热至85° C后再通过
2 5
固体加料器加入1.5 g V O,充分搅拌,反应2 h后倒出溶液,经抽滤后再将滤液经一系列操作,得到4.1 g
2 3
VOSO·3H O固体。
4 2
(1)仪器a的化学名称为_______, 该实验宜选用_______的三颈烧瓶(填字母)。
a.25 mL b.50 mL c.100 mL
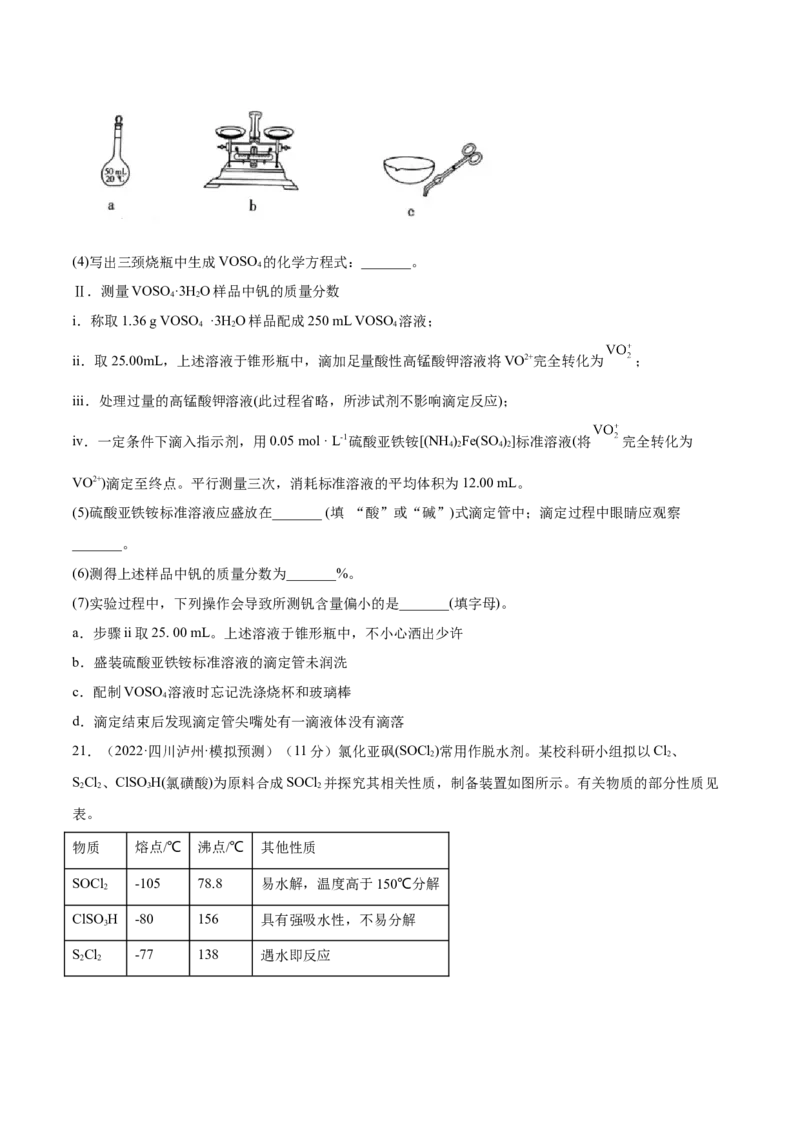
(2)抽滤装置如下图所示:抽滤时自来水的作用是_______。
(3)上述实验过程中,下列仪器不需要的是_______(填字母)。(4)写出三颈烧瓶中生成VOSO 的化学方程式:_______。
4
Ⅱ.测量VOSO·3H O样品中钒的质量分数
4 2
i.称取1.36 g VOSO ·3H O样品配成250 mL VOSO 溶液;
4 2 4
ii.取25.00mL,上述溶液于锥形瓶中,滴加足量酸性高锰酸钾溶液将VO2+完全转化为 ;
iii.处理过量的高锰酸钾溶液(此过程省略,所涉试剂不影响滴定反应);
iv.一定条件下滴入指示剂,用0.05 mol · L-1硫酸亚铁铵[(NH )Fe(SO )]标准溶液(将 完全转化为
4 2 4 2
VO2+)滴定至终点。平行测量三次,消耗标准溶液的平均体积为12.00 mL。
(5)硫酸亚铁铵标准溶液应盛放在_______ (填 “酸”或“碱”)式滴定管中;滴定过程中眼睛应观察
_______。
(6)测得上述样品中钒的质量分数为_______%。
(7)实验过程中,下列操作会导致所测钒含量偏小的是_______(填字母)。
a.步骤ii取25. 00 mL。上述溶液于锥形瓶中,不小心洒出少许
b.盛装硫酸亚铁铵标准溶液的滴定管未润洗
c.配制VOSO 溶液时忘记洗涤烧杯和玻璃棒
4
d.滴定结束后发现滴定管尖嘴处有一滴液体没有滴落
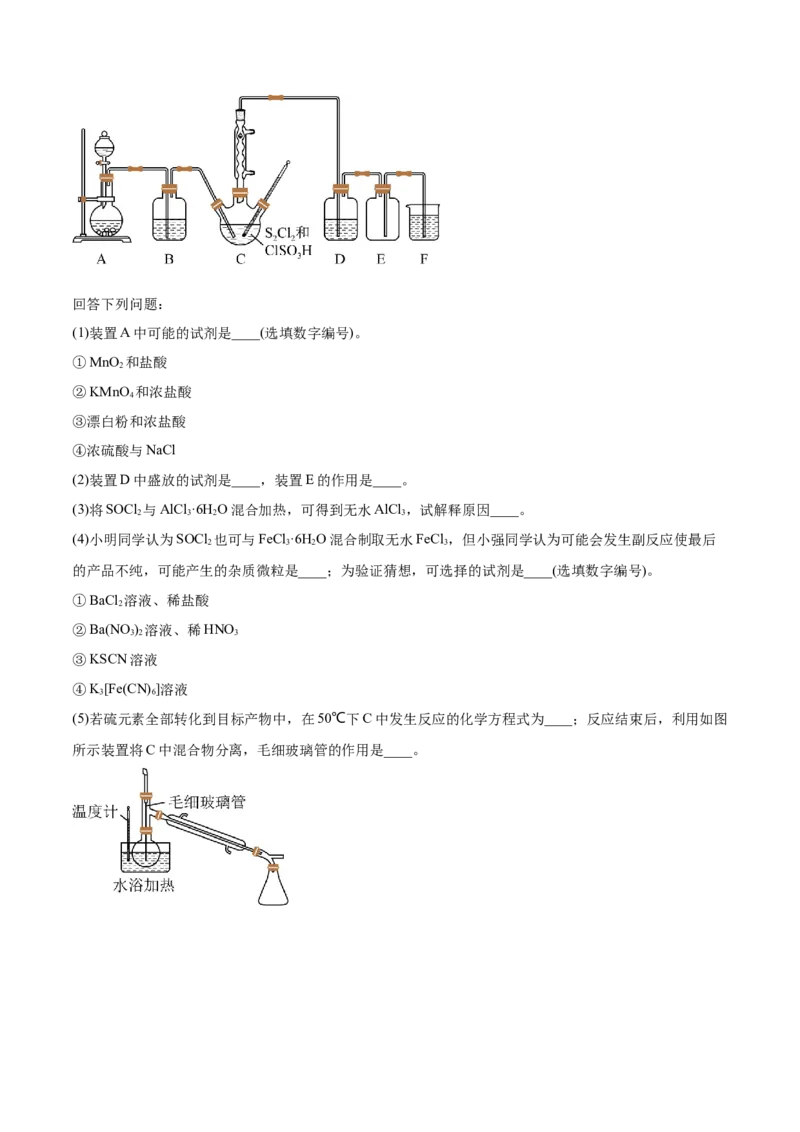
21.(2022·四川泸州·模拟预测)(11分)氯化亚砜(SOCl )常用作脱水剂。某校科研小组拟以Cl、
2 2
SCl、ClSOH(氯磺酸)为原料合成SOCl 并探究其相关性质,制备装置如图所示。有关物质的部分性质见
2 2 3 2
表。
物质 熔点/℃ 沸点/℃ 其他性质
SOCl -105 78.8 易水解,温度高于150℃分解
2
ClSOH -80 156 具有强吸水性,不易分解
3
SCl -77 138 遇水即反应
2 2回答下列问题:
(1)装置A中可能的试剂是____(选填数字编号)。
①MnO 和盐酸
2
②KMnO 和浓盐酸
4
③漂白粉和浓盐酸
④浓硫酸与NaCl
(2)装置D中盛放的试剂是____,装置E的作用是____。
(3)将SOCl 与AlCl ·6H O混合加热,可得到无水AlCl ,试解释原因____。
2 3 2 3
(4)小明同学认为SOCl 也可与FeCl ·6H O混合制取无水FeCl ,但小强同学认为可能会发生副反应使最后
2 3 2 3
的产品不纯,可能产生的杂质微粒是____;为验证猜想,可选择的试剂是____(选填数字编号)。
①BaCl 溶液、稀盐酸
2
②Ba(NO ) 溶液、稀HNO
3 2 3
③KSCN溶液
④K[Fe(CN) ]溶液
3 6
(5)若硫元素全部转化到目标产物中,在50℃下C中发生反应的化学方程式为____;反应结束后,利用如图
所示装置将C中混合物分离,毛细玻璃管的作用是____。