文档内容
考点 07 物质的量浓度
目录
.............................................................................................................................................1
1.高考真题考点分布...................................................................................................................................1
2.命题规律及备考策略...............................................................................................................................1
.............................................................................................................................................2
考法01 物质的量浓度及其计算...............................................................................................................2
考法02 配制一定物质的量浓度溶液.......................................................................................................5
.............................................................................................................................................9
1.高考真题考点分布
考点内容 考点分布
2024·甘肃卷,3分;2024·北京卷,3分;2024·江苏卷,3分;2023·重庆
一定物质的量浓度溶
卷,3分;2023·浙江卷,2分;2023·全国甲卷9题,6分;2022山东卷6
液的配制及误差分析
题,2分;2022·全国乙卷,2分;2022·广东卷;2021广东卷
物质的量浓度的计算 2022·海南卷7题,2分
2.命题规律及备考策略
【命题规律】
高频考点从近几年全国高考试题来看,有关物质的量浓度的考查主要体现在化学计算、一定物质的量浓度
溶液的配制、基本操作、误差分析等。
【备考策略】溶液稀释、同种溶质的溶液混合的计算
溶质的质量在稀释前后保持不变,即mw =mw
1 1 2 2
溶液
溶质的物质的量在稀释前后保持不变,即cV=cV
1 1 2 2
稀释
溶液质量守恒,m =m +m (体积一般不守恒,V ≠V +V )
稀 浓 水 稀 浓 水
混合前后溶质的物质的量保持不变,即cV+cV=c V (稀溶液混合时,常认为V
1 1 2 2 混 混 混
溶液 =V+V,进行粗略计算)
1 2
混合 溶液质量守恒,即ρV+ρV=ρ V
1 1 2 2 混 混
电荷守恒,如不同浓度的NaSO 溶液混合后仍存在c(Na+)=2c(SO)
2 4
【命题预测】
预计2025年高考会以新的情境载体考查物质的量浓度的计算、一定物质的量浓度的溶液的配制及误差分
析,题目难度一般适中,关注滴定实验中有关物质的量浓度的计算。考法01 物质的量浓度及其计算
1.物质的量浓度(c )
B
(1)概念:表示 的物质的量。
(2)表达式:c =,变形:n =c ·V,V=。
B B B
(3)常用单位:mol/L或 。
(4)特点:对于某浓度的溶液,取出任意体积的溶液,其浓度、密度、溶质质量分数均不变,但所含溶质的
、 因体积不同而改变。
2.溶质的质量分数
(1)概念:以溶液里溶质 与溶液 的比值表示溶液组成的物理量,一般用百分数表示,
也可用小数表示。
(2)表达式:w(B)=×100%。
【方法技巧】物质的量浓度与溶质质量分数之间的换算
c====,w= 。(ρ:g·cm-3)
3.物质的量浓度和溶质质量分数的比较
物质的量浓度c 溶质质量分数w
以单位体积溶液中所含溶质的物质的量来 以溶质质量与溶液质量的比值来表示溶
概念
表示溶液组成的物理量 液组成的物理量
溶质的单位
溶液的单位
表达式
两者关系 w=(M:摩尔质量,单位:g·mol-1;ρ:密度,单位:g·cm-3)
4.物质的量浓度计算的三种类型
(1)标准状况下气体溶质形成的溶液物质的量浓度的计算
c=
【易错提醒】溶液体积的单位是 L,根据密度计算溶液体积的单位一般是mL,要注意单位换算。
(2)溶液中溶质的质量分数与物质的量浓度的换算
计算公式:c=(c为溶质的物质的量浓度,单位 mol·L-1,ρ为溶液密度,单位 g·cm-3,w为溶质的质量分
数,M为溶质的摩尔质量,单位g·mol-1)。
(3)溶液稀释、同种溶质的溶液混合的计算
①溶液稀释
a.溶质的质量在稀释前后保持不变,即 。
b.溶质的物质的量在稀释前后保持不变,即 。
c.溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。②同种溶质的溶液混合:混合前后溶质的物质的量保持不变,即: 。
【易错提醒】
同一溶质的两种质量分数分别为a%、b%的溶液:
(1)等质量混合
1
两溶液混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),混合后溶液中溶质的质量分数w= (a%+
2
b%)。
(2)等体积混合
1
①当溶液密度大于1 g·cm-3时,等体积混合后,混合溶液的质量分数w> (a%+b%);
2
1
②当溶液密度小于1 g·cm-3时,等体积混合后,混合溶液的质量分数w< (a%+b%)。
2
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)1 mol·L-1 NaCl溶液是指此溶液中含有1 mol NaCl。( )
(2)1 L 水中溶解5.85 g NaCl所形成的溶液的物质的量浓度为0.1 mol·L-1。( )
(3)31 g Na O溶于水,配成1 L 溶液,c(Na O)=0.5 mol·L-1。( )
2 2
(4)将40 g SO 溶于60 g水中所得溶质的质量分数为40%。( )
3
(5)将25 g CuSO ·5HO晶体溶于75 g水中所得溶质的质量分数为16%。( )
4 2
(6)1 L 0.5 mol·L-1CaCl 溶液中,Ca2+与Cl-的物质的量浓度都是0.5 mol·L-1。( )
2
考向01 物质的量浓度
【例1】(2024·河北衡水·质检)下列关于物质的量浓度说法正确的是
A.0.3 mol·L-1的NaSO 溶液中含有Na+和 的总物质的量为0.9 mol
2 4
B.将NaO和NaO 各1 mol溶于水配成1 L溶液,所得溶液物质的量浓度不同
2 2 2
C.标况下22.4 L NH 溶于水配成1 L溶液,所得溶液浓度为1 mol·L-1
3
D.要配制100 mL 1 mol·L-1的硫酸铜溶液,需要胆矾1.6 g
【思维建模】 相同溶质、不同质量分数两溶液混合的规律
同一溶质、质量分数分别为a%、b%的两溶液混合。
(1)等体积混合
①当溶液密度大于1 g·cm-3时,必然是溶液浓度越大,密度越大,(如HSO、HNO、HCl、NaOH等多数溶
2 4 3
液)等体积混合后质量分数w>(a%+b%)。
②当溶液密度小于1 g·cm-3时,必然是溶液浓度越大,密度越小,(如酒精、氨水)等体积混合后,质量分
数w<(a%+b%)。
(2)等质量混合
两溶液等质量混合时(无论ρ>1 g·cm-3还是ρ<1 g·cm-3),则混合后溶液中溶质的质量分数w=(a%+
b%)。
以上规律可概括为“计算推理有技巧,有大必有小,均值均在中间找,谁多向谁靠”。考向02 有关气体溶于水的浓度计算
【例2】(2024·辽宁沈阳·二模)在标准状况下,将V L A气体(摩尔质量是M g/mol)溶于0.1L水中,所得
溶液的密度为d g/cm3,则此A的物质的量浓度为
A. B.
C. D.
【思维建模】气体溶质溶于水中制得溶液,其物质的量浓度和质量分数的计算
在标准状况下,1 L水中溶解某气体V L,所得溶液密度为ρ,则:c===
(ρ:g·cm-3),w=×100%==×100%。
考向03 溶液物质的量浓度综合计算
【例3】(2024·江苏徐州·二模)将m g铜粉和锌粉的混合物分成两等份,将其中一份加入200 mL的稀硝
酸中并加热,固体和硝酸恰好完全反应,并产生标准状况下的NO气体2.24 L;将另一份在空气中充分加
热,得到n g固体,将所得固体溶于上述稀硝酸,消耗硝酸的体积为V mL。下列说法不正确的是( )
A.V=150
B.硝酸的浓度为2 mol·L-1
C.m g铜粉和锌粉混合物的物质的量之和为0.15 mol
D.n=0.5m+2.4
【思维建模】
1.溶液稀释
(1)溶质的质量在稀释前后保持不变,即mw =mw 。
1 1 2 2
(2)溶质的物质的量在稀释前后保持不变,即cV=c V。
1 1 2 2
(3)溶液质量守恒,m(稀)=m(浓)+m(水)(体积一般不守恒)。
2.溶液混合,混合前后:cV+c V=c V ,其中V =m /ρ ,据此可进行相关计算。
1 1 2 2 混 混 混 混 混
【对点1】(2024·安徽亳州·模拟)血液中葡萄糖(简称血糖,分子式为C H O 的含量,常以“
6 12 6
”和“ ”为参考指标(1L=10dL),以“ ”表示时,人的血糖正常值在4.9~6.1 之
间。下列说法正确的是
A.葡萄糖的摩尔质量为180
B.无偿献血后,体内血糖浓度会变小
C.某病人lmL血液中含葡萄糖0.60mg,相当于
D.若病人的血糖检测结果为 血糖值在正常范围内
【对点2】(2024·辽宁葫芦岛·模拟)在t℃时,将agNH 完全溶于水,得到VmL溶液,设该溶液的密度为
3
ρg•cm-3,质量分数为ω,其中含N的物质的量为bmol(溶质按NH 计算)。下列叙述中不正确的是
3
A.溶质的质量分数ω= ×100%B.溶质的物质的量浓度c= mol•L-1
C.上述溶液中再加入VmL水后,所得溶液中物质的量浓度为原来的
D.上述溶液中再加入VmL水后,所得溶液中溶质的质量分数小于0.5ω
【对点3】(2024·黑龙江齐齐哈尔·模拟)在t℃时,将agNH 完全溶于水,得到VmL溶液,假设该溶液的
3
密度为ρg/mL,溶质质量分数为w,其中含有NH 的物质的量是bmol,下列叙述正确的是
A.溶质的质量分数w= ×100%
B.溶质的物质的量浓度c= mol/L
C.溶液中c(OH-)= mol/L+c(H+)
D.向上述溶液中加入VmL水,所得溶液的溶质质量分数大于0.5w
考法02 配制一定物质的量浓度溶液
1.主要仪器
托盘天平、药匙、量筒、玻璃棒、 、 、 。
2.容量瓶的结构及使用
(1)结构及用途
(2)查漏操作
3.配制过程
Ⅰ.以配制100 mL 1.00 mol/L NaCl溶液为例。
(1)计算:需NaCl固体的质量为 g。
(2)称量:根据计算结果,用 称量NaCl固体 g。
(3)溶解:将称好的NaCl固体放入烧杯中,加适量蒸馏水溶解,并用玻璃棒搅拌。
(4)移液:待烧杯中的溶液 后,用玻璃棒引流将溶液注入 mL容量瓶。(5)洗涤:用适量蒸馏水洗涤烧杯内壁和玻璃棒 次,洗涤液 ,轻轻摇动容量瓶,使溶
液混合均匀。
(6)定容:将蒸馏水注入容量瓶,当液面距瓶颈刻度线 cm时,改用 滴加蒸馏水至
。
(7)摇匀:盖好瓶塞,反复上下颠倒,摇匀。
(8)装瓶、贴签。
Ⅱ.配制流程图(如下图所示):
【易错提醒】
(1)做需要补充仪器的实验题时,要学会“有序思考”——按照实验的先后顺序、步骤,思考每一步所
需仪器,然后与已知仪器对比,就一定不会漏写某种仪器。
(2)容量瓶的规格,常见的有100 mL、250 mL、500 mL、1 000 mL。
(3)所用定量仪器量筒、托盘天平的精确度。
4.误差分析方法:结合实验操作判断是“m”还是“V”引起的误差。以配制NaOH溶液为例,具体分析如下:
因变量
能引起误差的一些操作 c/(mol·L-1)
m V
砝码与物品颠倒(使用游码) 减小 —
用滤纸称NaOH 减小 —
向容量瓶注液时少量溅出 减小 —
未洗涤烧杯和玻璃棒 减小 —
定容时,水多,用滴管吸出 减小 —
定容摇匀后液面下降再加水 — 增大定容时仰视刻度线 — 增大
砝码沾有其他物质或已生锈(未脱落) 增大 —
未冷却至室温就注入容量瓶定容 — 减小
定容时俯视刻度线 — 减小
定容后经振荡、摇匀,静置液面下降 — —
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)用 配制100 mL 0.1000 mol·L-1的KCr O 溶液。
2 2 7
(2)用固体NaCl配制0.5 mol·L-1的溶液,所用的仪器只有:烧杯、玻璃棒、胶头滴管、容量瓶。
(3)NaOH在烧杯里刚完全溶解时,立即将溶液转移到容量瓶。
(4)配制480 mL 1 mol·L-1的NaOH溶液,应用托盘天平称量NaOH固体19.2 g,选用500 mL容量瓶。
考向01 仪器的使用及配制步骤
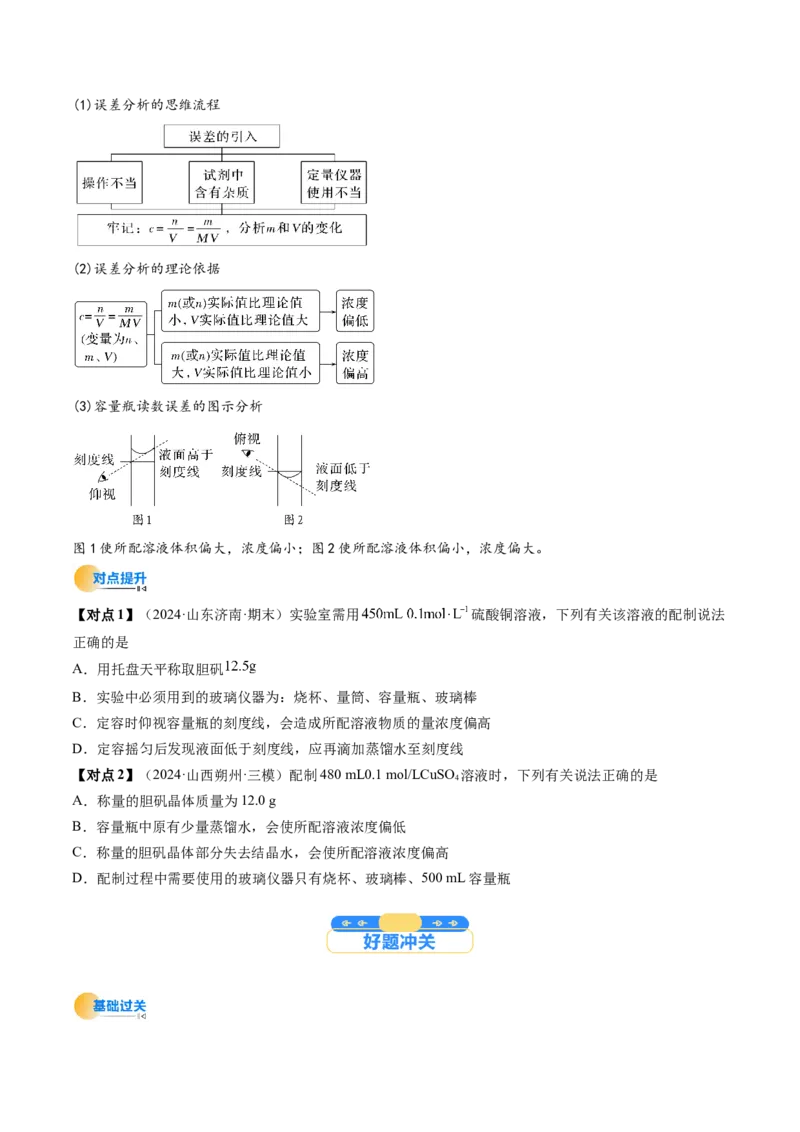
【例1】(2024·江西南昌·一模)实验室用18.4 mol⋅L-1的浓硫酸配制1.0 mol·L-1的稀硫酸100 mL,并用来
测定稀硫酸与Zn反应的速率,完成上述实验,下列部分仪器选用合理的是
A.①②③⑥ B.①④⑤⑥ C.②③⑥⑧ D.②③⑦⑧
【思维建模】
1.选用容量瓶的原则——“大而近”,如需90 mL溶液,则选用100 mL容量瓶。
2.选用容量瓶时,应指明其规格。
3.往容量瓶中转移液体时,用玻璃棒引流,玻璃棒末端应在容量瓶刻度线以下。
考向02 溶液配制的误差分析
【例2】(2024·百师联盟·联考)某化学小组的同学要配制500 mL 0.6 mol/L的NaOH溶液,具体操作如下:
①用托盘天平称取12.0 g NaOH固体时所用时间较长;②向小烧杯中加水使氢氧化钠溶解并冷却至室温;
③把溶液转移到洗净但未干燥的容量瓶中,洗涤烧杯和玻璃棒三次并将洗涤液也转移到容量瓶中,振荡摇
匀;④向容量瓶中加水定容,定容时俯视刻度线;⑤定容后塞上容量瓶塞子,上下颠倒摇匀,摇匀后发现
液面低于刻度线,用胶头滴管补加蒸馏水至刻度线。以上操作中会使所得溶液浓度偏低的有几项?( )
A.1 B.2 C.3 D.4
【思维建模】(1)误差分析的思维流程
(2)误差分析的理论依据
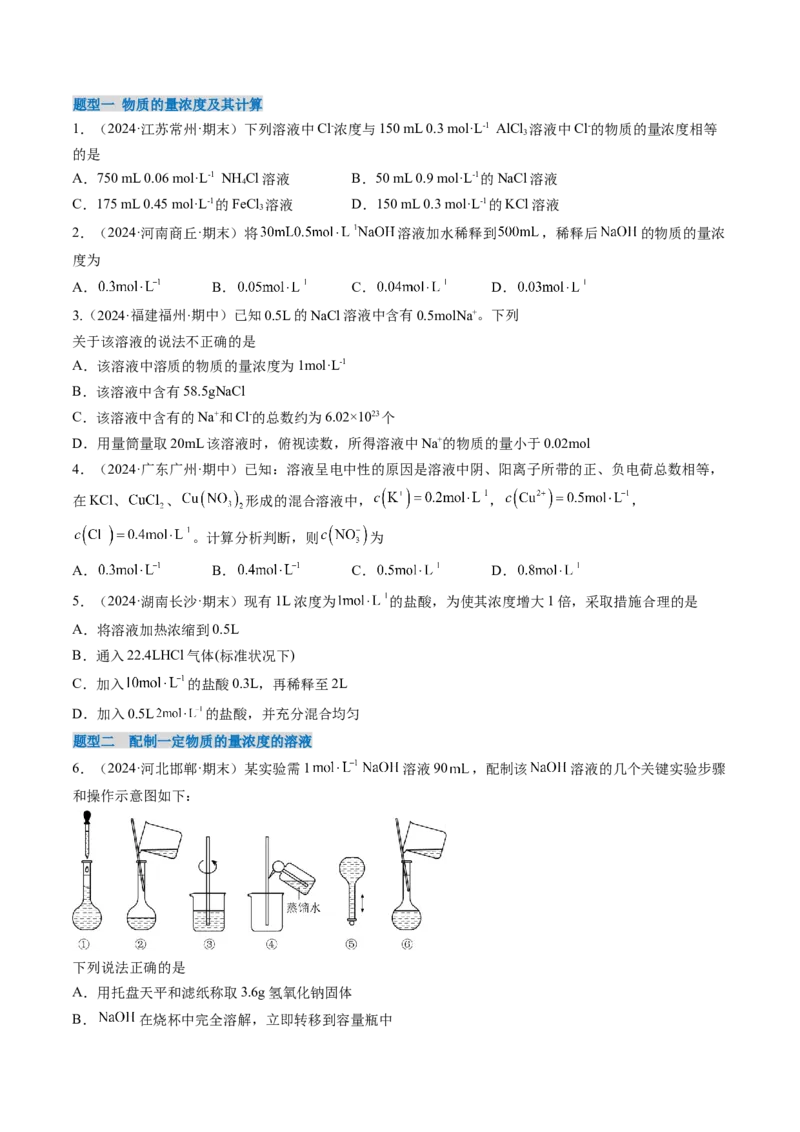
(3)容量瓶读数误差的图示分析
图1使所配溶液体积偏大,浓度偏小;图2使所配溶液体积偏小,浓度偏大。
【对点1】(2024·山东济南·期末)实验室需用 硫酸铜溶液,下列有关该溶液的配制说法
正确的是
A.用托盘天平称取胆矾
B.实验中必须用到的玻璃仪器为:烧杯、量筒、容量瓶、玻璃棒
C.定容时仰视容量瓶的刻度线,会造成所配溶液物质的量浓度偏高
D.定容摇匀后发现液面低于刻度线,应再滴加蒸馏水至刻度线
【对点2】(2024·山西朔州·三模)配制480 mL0.1 mol/LCuSO 溶液时,下列有关说法正确的是
4
A.称量的胆矾晶体质量为12.0 g
B.容量瓶中原有少量蒸馏水,会使所配溶液浓度偏低
C.称量的胆矾晶体部分失去结晶水,会使所配溶液浓度偏高
D.配制过程中需要使用的玻璃仪器只有烧杯、玻璃棒、500 mL容量瓶题型一 物质的量浓度及其计算
1.(2024·江苏常州·期末)下列溶液中Cl-浓度与150 mL 0.3 mol·L-1 AlCl 溶液中Cl-的物质的量浓度相等
3
的是
A.750 mL 0.06 mol·L-1 NH Cl溶液 B.50 mL 0.9 mol·L-1的NaCl溶液
4
C.175 mL 0.45 mol·L-1的FeCl 溶液 D.150 mL 0.3 mol·L-1的KCl溶液
3
2.(2024·河南商丘·期末)将 溶液加水稀释到 ,稀释后 的物质的量浓
度为
A. B. C. D.
3.(2024·福建福州·期中)已知0.5L的NaCl溶液中含有0.5molNa+。下列
关于该溶液的说法不正确的是
A.该溶液中溶质的物质的量浓度为1mol·L-1
B.该溶液中含有58.5gNaCl
C.该溶液中含有的Na+和Cl-的总数约为6.02×1023个
D.用量筒量取20mL该溶液时,俯视读数,所得溶液中Na+的物质的量小于0.02mol
4.(2024·广东广州·期中)已知:溶液呈电中性的原因是溶液中阴、阳离子所带的正、负电荷总数相等,
在KCl、 、 形成的混合溶液中, , ,
。计算分析判断,则 为
A. B. C. D.
5.(2024·湖南长沙·期末)现有1L浓度为 的盐酸,为使其浓度增大1倍,采取措施合理的是
A.将溶液加热浓缩到0.5L
B.通入22.4LHCl气体(标准状况下)
C.加入 的盐酸0.3L,再稀释至2L
D.加入0.5L 的盐酸,并充分混合均匀
题型二 配制一定物质的量浓度的溶液
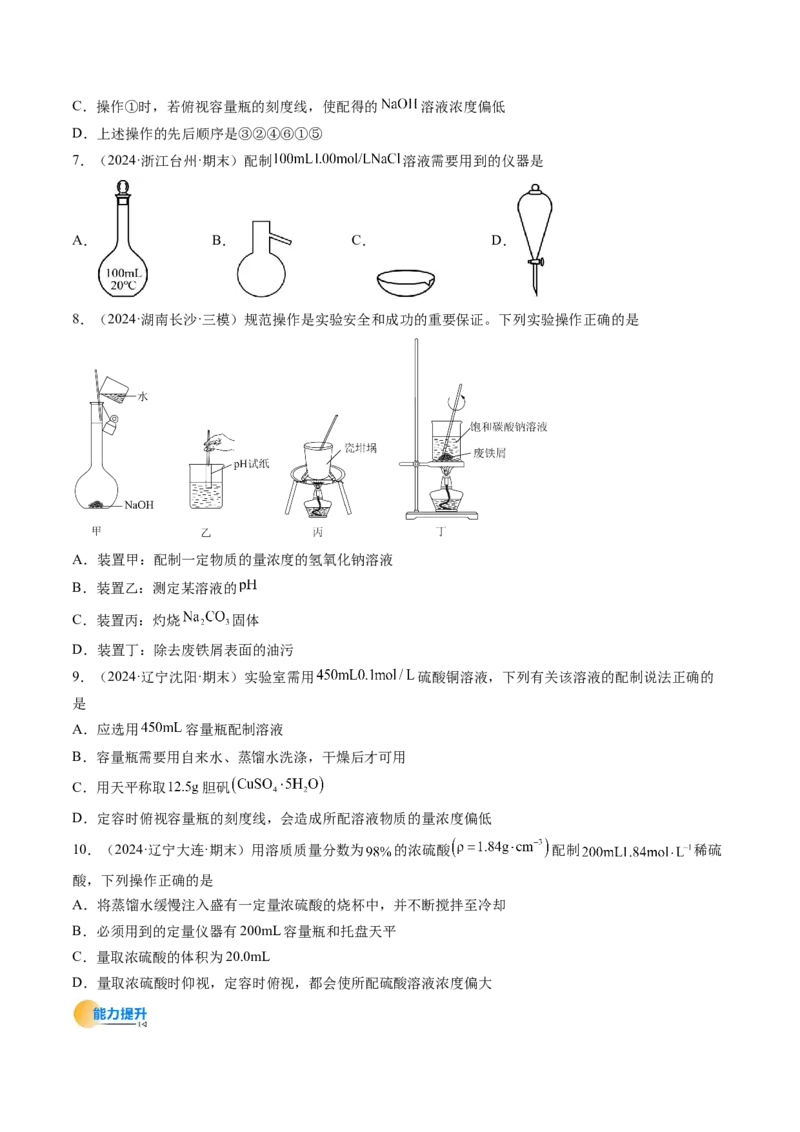
6.(2024·河北邯郸·期末)某实验需1 溶液90 ,配制该 溶液的几个关键实验步骤
和操作示意图如下:
下列说法正确的是
A.用托盘天平和滤纸称取3.6g氢氧化钠固体
B. 在烧杯中完全溶解,立即转移到容量瓶中C.操作①时,若俯视容量瓶的刻度线,使配得的 溶液浓度偏低
D.上述操作的先后顺序是③②④⑥①⑤
7.(2024·浙江台州·期末)配制 溶液需要用到的仪器是
A. B. C. D.
8.(2024·湖南长沙·三模)规范操作是实验安全和成功的重要保证。下列实验操作正确的是
A.装置甲:配制一定物质的量浓度的氢氧化钠溶液
B.装置乙:测定某溶液的
C.装置丙:灼烧 固体
D.装置丁:除去废铁屑表面的油污
9.(2024·辽宁沈阳·期末)实验室需用 硫酸铜溶液,下列有关该溶液的配制说法正确的
是
A.应选用 容量瓶配制溶液
B.容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
C.用天平称取 胆矾
D.定容时俯视容量瓶的刻度线,会造成所配溶液物质的量浓度偏低
10.(2024·辽宁大连·期末)用溶质质量分数为 的浓硫酸 配制 稀硫
酸,下列操作正确的是
A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却
B.必须用到的定量仪器有200mL容量瓶和托盘天平
C.量取浓硫酸的体积为20.0mL
D.量取浓硫酸时仰视,定容时俯视,都会使所配硫酸溶液浓度偏大11.(2024·山东济南·期末)实验室需要配制80mL2.2mol·L-1的稀硫酸,操作步骤如下:用100mL量筒量
取18.4mol·L-1的浓硫酸12.0mL,将浓硫酸沿烧杯内壁缓缓注入盛有蒸馏水的烧杯中,并不断用玻璃棒搅
拌。搅拌均匀后立即沿玻璃棒注入容量瓶中,用蒸馏水洗涤烧杯和玻璃棒,洗涤液转移至容量瓶中,重复
操作2~3次,继续用烧杯向容量瓶中加入蒸馏水,使溶液的凹液面恰好与刻度线相切,盖上瓶塞后摇匀,
装入试剂瓶中。实验操作中存在的错误有几处?
A.2处 B.3处 C.4处 D.5处
12.(2024·广东深圳·期末)把300mL含有BaCl 、MgCl 、Mg(NO) 的混合溶液分成3等份,分别逐滴加
2 2 3 2
入NaSO 溶液、AgNO 溶液、NaOH溶液,直至不再产生沉淀,此时消耗amolNa SO 、bmolAgNO、
2 4 3 2 4 3
cmolNaOH,则该混合溶液中 的浓度为
A. mol/L B.10(2a-b+c)mol/L
C.10(2a﹣b+2c)mol/L D. mol/L
13.(2024·湖南长沙·模拟)下列关于物质的量浓度表述中正确的是
A.0.3 mol·L-1 Na SO 溶液中含有Na+和SO 的总物质的量为0.9 mol
2 4
B.当1 L水吸收22.4 L氨气(NH )时所得氨水的浓度不是1 mol·L-1,只有当22.4 L氨气溶于水制得1 L氨
3
水时,其浓度才是1 mol·L-1
C.在KSO 和NaCl的中性混合水溶液中,如果Na+和SO 的物质的量浓度相等,则K+和Cl-的物质的量
2 4
浓度之比为1∶2
D.10 ℃时0.35 mol·L-1的KCl饱和溶液100 mL,蒸发掉5 g水,冷却到10 ℃时,其体积小于100 mL,它
的物质的量浓度仍为0.35 mol·L-1
14.(2024·山东烟台·期中)t℃时,A的溶解度是S g/100g水,其饱和溶液密度为d g·cm-3,物质的量浓
度为c mol·L-1,溶液的质量分数为w,摩尔质量为M g·mol-1,实验测得向一定量含A的溶液中加入m g
无水A或蒸发掉n g水后恢复到t℃,均为饱和溶液,下列关系式正确的是
A. B. C. D.
15.(2024·黑龙江·联考)相对分子质量为Mr的气态化合物V L(标准状况)溶于m g水中,得到溶液的质
量分数为w%,物质的量浓度为c mol·L-1,密度为ρ g·cm-3,则下列说法正确的是
A.溶液密度ρ可表示为 B.物质的量浓度c可表示为
C.溶液的质量分数w%可表示为 D.相对分子质量Mr可表示为
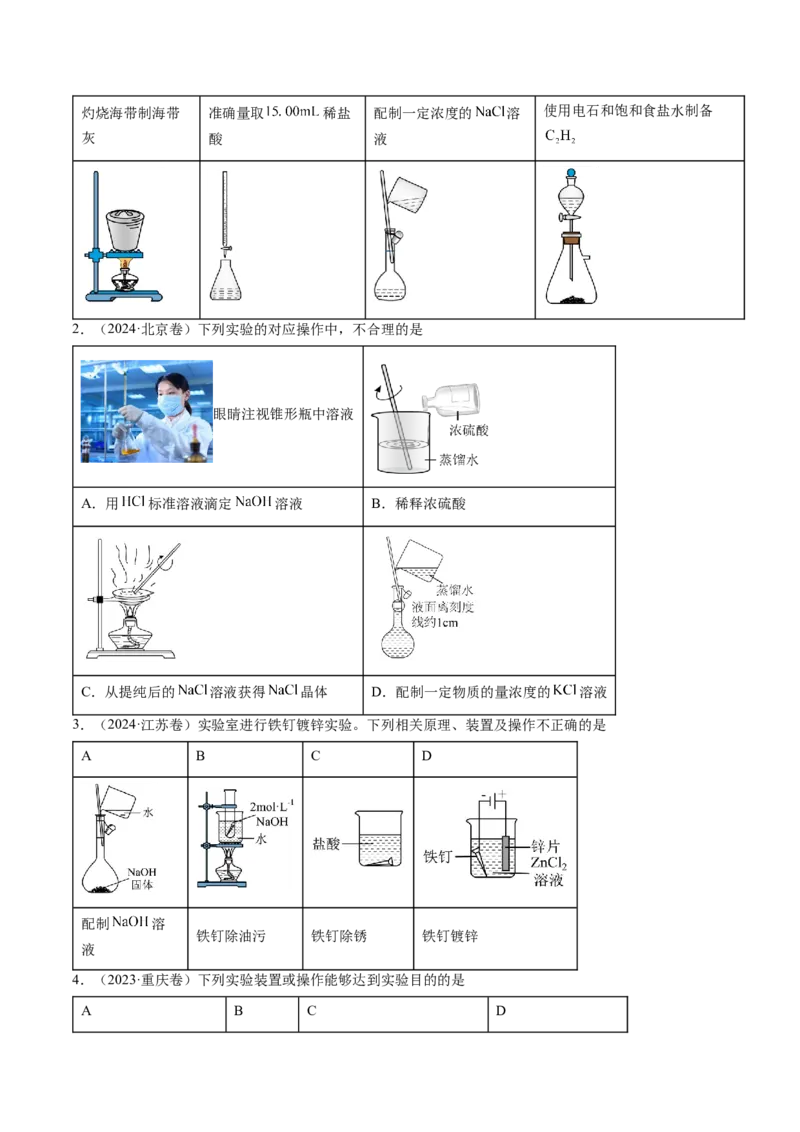
1.(2024·甘肃卷)下列实验操作对应的装置不正确的是
A B C D灼烧海带制海带 准确量取 稀盐 配制一定浓度的 溶 使用电石和饱和食盐水制备
灰 酸 液
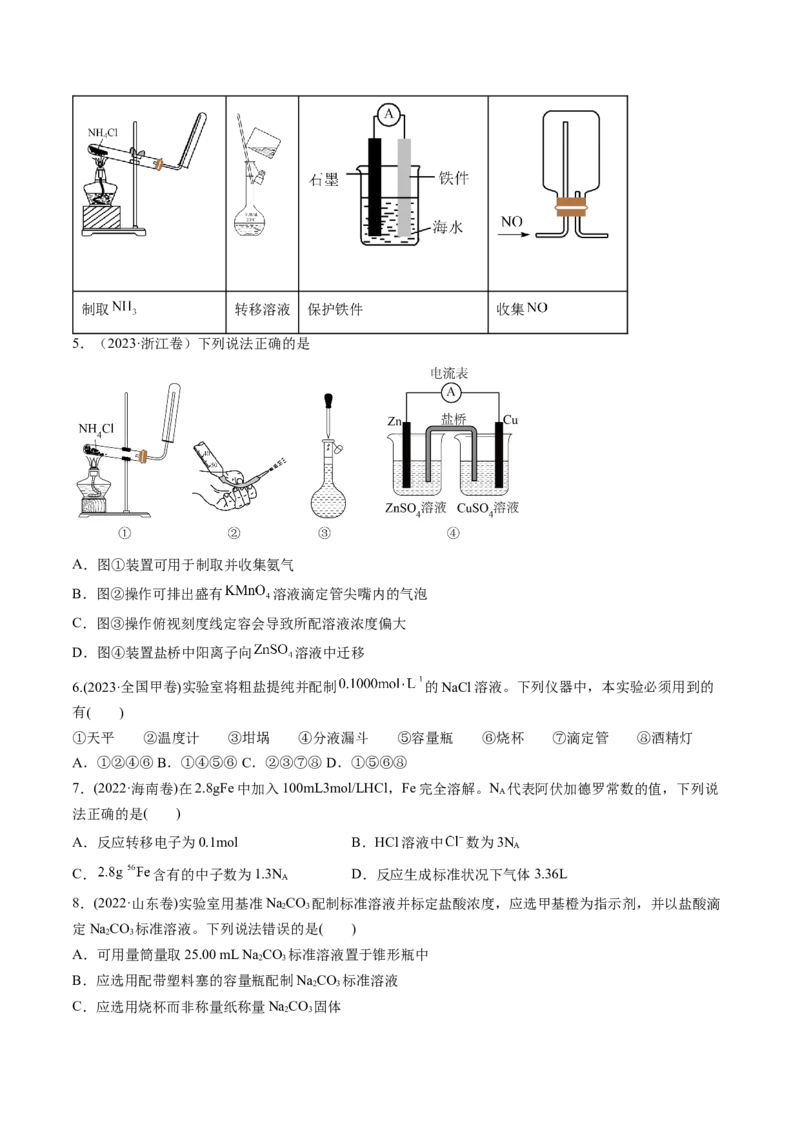
2.(2024·北京卷)下列实验的对应操作中,不合理的是
眼睛注视锥形瓶中溶液
A.用 标准溶液滴定 溶液 B.稀释浓硫酸
C.从提纯后的 溶液获得 晶体 D.配制一定物质的量浓度的 溶液
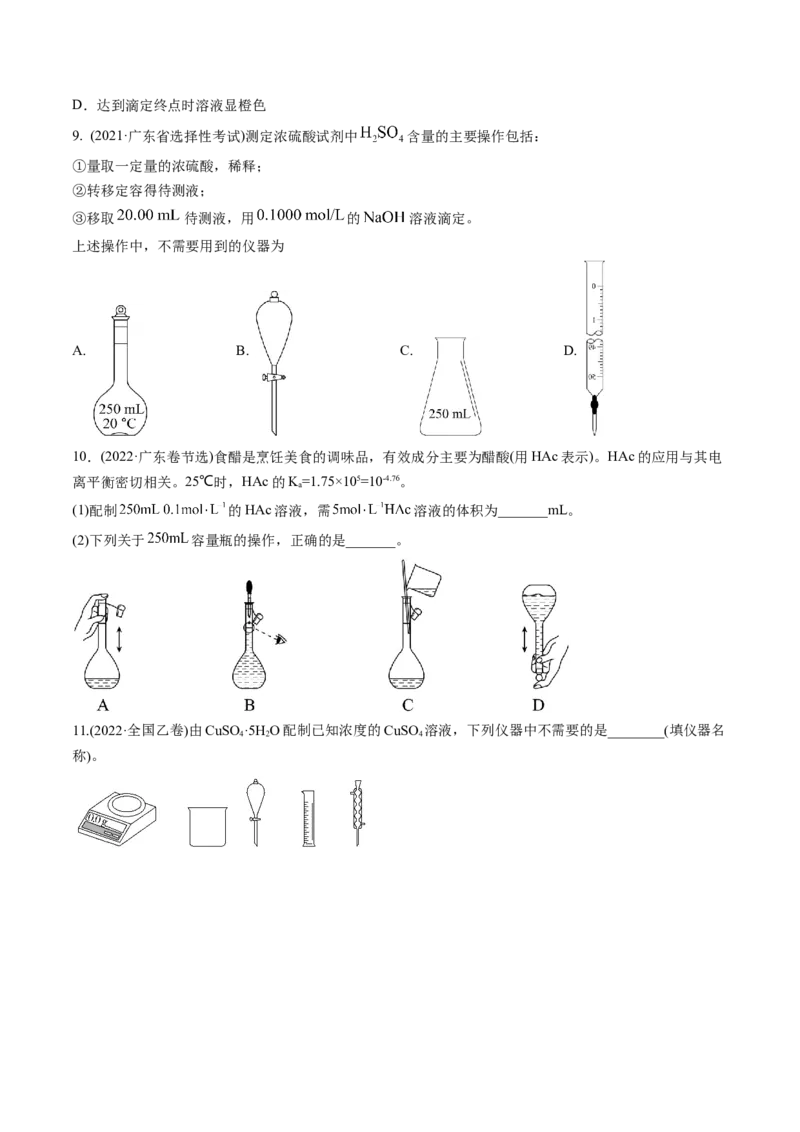
3.(2024·江苏卷)实验室进行铁钉镀锌实验。下列相关原理、装置及操作不正确的是
A B C D
配制 溶
铁钉除油污 铁钉除锈 铁钉镀锌
液
4.(2023·重庆卷)下列实验装置或操作能够达到实验目的的是
A B C D制取 转移溶液 保护铁件 收集
5.(2023·浙江卷)下列说法正确的是
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向 溶液中迁移
6.(2023·全国甲卷)实验室将粗盐提纯并配制 的NaCl溶液。下列仪器中,本实验必须用到的
有( )
①天平 ②温度计 ③坩埚 ④分液漏斗 ⑤容量瓶 ⑥烧杯 ⑦滴定管 ⑧酒精灯
A.①②④⑥B.①④⑤⑥ C.②③⑦⑧ D.①⑤⑥⑧
7.(2022·海南卷)在2.8gFe中加入100mL3mol/LHCl,Fe完全溶解。N 代表阿伏加德罗常数的值,下列说
A
法正确的是( )
A.反应转移电子为0.1mol B.HCl溶液中 数为3N
A
C. 含有的中子数为1.3N D.反应生成标准状况下气体3.36L
A
8.(2022·山东卷)实验室用基准NaCO 配制标准溶液并标定盐酸浓度,应选甲基橙为指示剂,并以盐酸滴
2 3
定NaCO 标准溶液。下列说法错误的是( )
2 3
A.可用量筒量取25.00 mL Na CO 标准溶液置于锥形瓶中
2 3
B.应选用配带塑料塞的容量瓶配制NaCO 标准溶液
2 3
C.应选用烧杯而非称量纸称量NaCO 固体
2 3D.达到滴定终点时溶液显橙色
9. (2021·广东省选择性考试)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
上述操作中,不需要用到的仪器为
A. B. C. D.
10.(2022·广东卷节选)食醋是烹饪美食的调味品,有效成分主要为醋酸(用HAc表示)。HAc的应用与其电
离平衡密切相关。25℃时,HAc的K=1.75×105=10-4.76。
a
(1)配制 的HAc溶液,需 溶液的体积为_______mL。
(2)下列关于 容量瓶的操作,正确的是_______。
11.(2022·全国乙卷)由CuSO ·5HO配制已知浓度的CuSO 溶液,下列仪器中不需要的是________(填仪器名
4 2 4
称)。