文档内容
高频考点 31 酸碱中和滴定及其拓展
题点(一)酸碱中和滴定
1.(2021·广东)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
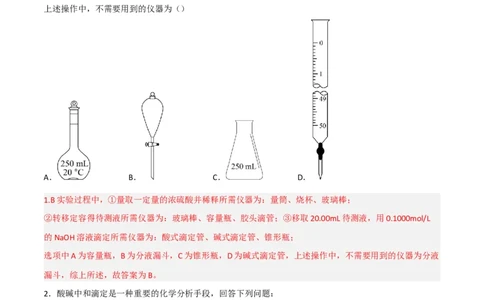
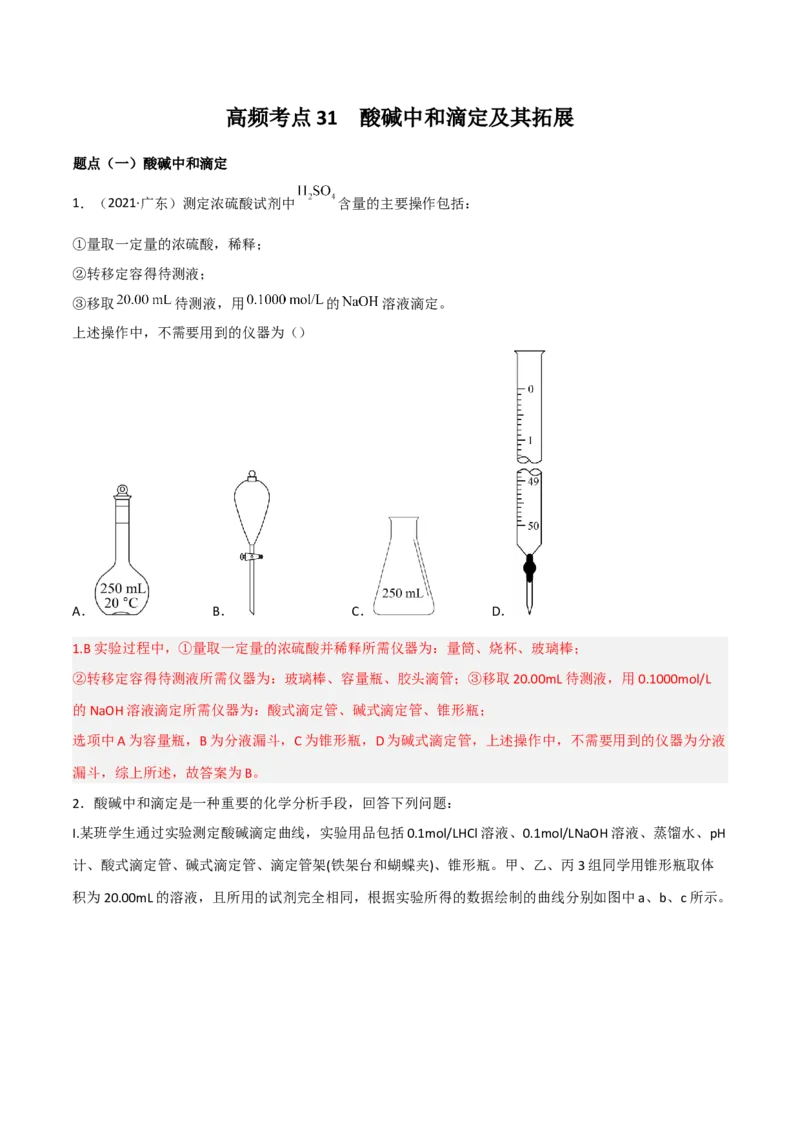
上述操作中,不需要用到的仪器为()
A. B. C. D.
1.B实验过程中,①量取一定量的浓硫酸并稀释所需仪器为:量筒、烧杯、玻璃棒;
②转移定容得待测液所需仪器为:玻璃棒、容量瓶、胶头滴管;③移取20.00mL待测液,用0.1000mol/L
的NaOH溶液滴定所需仪器为:酸式滴定管、碱式滴定管、锥形瓶;
选项中A为容量瓶,B为分液漏斗,C为锥形瓶,D为碱式滴定管,上述操作中,不需要用到的仪器为分液
漏斗,综上所述,故答案为B。
2.酸碱中和滴定是一种重要的化学分析手段,回答下列问题:
I.某班学生通过实验测定酸碱滴定曲线,实验用品包括0.1mol/LHCl溶液、0.1mol/LNaOH溶液、蒸馏水、pH
计、酸式滴定管、碱式滴定管、滴定管架(铁架台和蝴蝶夹)、锥形瓶。甲、乙、丙3组同学用锥形瓶取体
积为20.00mL的溶液,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示。(1)滴定时选用的滴定管为____(选填“酸式”或“碱式”)滴定管,在装入标准溶液前需要对滴定管进行的
操作为____。
(2)在图中的三条滴定曲线中,较为准确的是____。
II.在实际操作过程中,由于甲基橙指示剂的变色不敏锐,难以判断滴定终点,需在其中加入少量的“惰性
染料”靛蓝二磺酸钠,其固定颜色与甲基橙的可变颜色进行叠加(变色范围不变),形成“酸色”为紫色、
过渡色为浅灰色、“碱色”为绿色的混合指示剂。已知室温下0.10mol/LNH Cl溶液的,若以甲基橙-靛蓝
4
二磺酸钠为指示剂,用0.20mol/L盐酸滴定20.00mL同浓度的氨水,则:
(3)NH Cl溶液显酸性的原因是____(用离子方程式表示)。
4
(4)判断滴定终点的现象是____。
(5)若多组实验中所用盐酸的体积均略大于20.00mL,原因是____。
2. (1) 碱式 检验是否漏水、使用蒸馏水清洗、使用标准溶液润洗
(2)a(3)NH ++H O NH •H O+H+
4 2 3 2
(4)滴入最后一滴盐酸时,锥形瓶中液体由绿色变为浅灰色,且30s内不褪色
(5)指示剂的变色点4.4略小于反应的终点5.1,滴入的盐酸总是稍微过量
解析:该实验用NaOH溶液滴定HCl溶液,则锥形瓶内装的是HCl溶液,则滴定管装的是NaOH溶液,实验
开始前需对碱式滴定管检漏以及润洗;
(1)由图可知起点溶液pH<7,说明锥形瓶内装的是HCl溶液,则滴定管装的是NaOH溶液,所用的滴定
管应为碱式滴定管,在装入标准溶液前需要对滴定管进行的操作为检验是否漏水、使用蒸馏水清洗、使用
标准溶液润洗,故答案为:碱式;检验是否漏水、使用蒸馏水清洗、使用标准溶液润洗;
(2)NaOH溶液滴定HCl溶液,到达滴定终点时溶液pH发生突变,均为一元强电解质,则到达滴定终点
时消耗NaOH溶液体积为20.00mL,此时pH=7,图a符合滴定曲线,故答案为:a;
(3)NH Cl溶液中铵根发生水解反应使溶液显酸性,水解方程式为: ;
4
(4)甲基橙-靛蓝二磺酸钠为指示剂在碱性溶液中呈绿色,在酸性溶液中为紫色,过渡色为浅灰色,用
盐酸滴定同浓度的氨水,则判断滴定终点的现象是:滴入最后一滴盐酸时,锥形瓶中液体由绿色变为浅灰色,且30s内不褪色;
(5)甲基橙-靛蓝二磺酸钠为指示剂的变色点为pH=4.4,而盐酸与氨水在滴定终点时pH=5.1,因此需多
加稀盐酸,则多组实验中所用盐酸的体积均略大于20.00mL,原因是指示剂的变色点4.4略小于反应的终点
5.1,滴入的盐酸总是稍微过量。
题点(二)氧化还原反应滴定
3.(2021·山东卷节选)利用碘量法测定WCl 产品纯度,实验如下:
6
(1)称量:将足量CS (易挥发)加入干燥的称量瓶中,盖紧称重为m g;开盖并计时1分钟,盖紧称重为
2 1
m g;再开盖加入待测样品并计时1分钟,盖紧称重为m g,则样品质量为___g(不考虑空气中水蒸气的干
2 3
扰)。
(2)滴定:先将WCl 转化为可溶的Na WO ,通过IO 离子交换柱发生反应:WO +Ba(IO ) =BaWO +2IO ;
6 2 4 3 2 4
交换结束后,向所得含IO 的溶液中加入适量酸化的KI溶液,发生反应:IO +5I-+6H+=3I +3H O;反应完全
2 2
后,用Na S O 标准溶液滴定,发生反应:I +2S O =2I-+S O 。滴定达终点时消耗cmol•L-1的Na S O 溶液
2 2 3 2 2 4 2 2 3
VmL,则样品中WCl (摩尔质量为Mg•mol-1)的质量分数为___。称量时,若加入待测样品后,开盖时间超过
6
1分钟,则滴定时消耗Na S O 溶液的体积将___(填“偏大”“偏小”或“不变”),样品中WCl 质量分数
2 2 3 6
的测定值将___(填“偏大”“偏小”或“不变”)。
3. (1) ( m +m -2m ) (2) % 不变 偏大
3 1 2
解析:(1)根据分析,称量时加入足量的CS ,盖紧称重为m g,由于CS 易挥发,开盖时要挥发出来,称量
2 1 2
的质量要减少,开盖并计时1分钟,盖紧称重m g,则挥发出的CS 的质量为(m - m )g,再开盖加入待测样
2 2 1 2
品并计时1分钟,又挥发出(m - m )g的CS ,盖紧称重为m g,则样品质量为:m g-m g+2(m - m )g=( m +m -
1 2 2 3 3 1 1 2 3 1
2m )g,故答案为:( m +m - 2m );
2 3 1 2
(2)滴定时,根据关系式:WO ~2IO ~6I ~12 S O ,样品中n(WCl )=n(WO )= n(S O )= cV 10-3mol,
2 2 6 2
m(WCl )= cV 10-3mol Mg/mol= g,则样品中WCl 的质量分数为: 100%=
6 6%;根据测定原理,称量时,若加入待测样品后,开盖时间超过1分钟,挥发的CS 的质
2
量增大,m 偏小,但WCl 的质量不变,则滴定时消耗Na S O 溶液的体积将不变,样品中WCl 质量分数的
3 6 2 2 3 6
测定值将偏大,故答案为: %;不变;偏大。
4.(2022·山东·乳山市银滩高级中学高三期末)焦亚硫酸钠含量的测定
工业焦亚硫酸钠(Na S O )优质品要求质量分数 %。通过下列实验检测焦亚硫酸钠样品是否达到优质
2 2 5
品标准。实验检测原理为:
(未配平)
准确称取 样品,快速置于预先加入 碘标准液及 水的 碘量瓶中,
加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置 ;用
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na S O 溶
2 2 3
液 。
(1)滴定终点现象是___________。
(2)通过计算判断该样品是否为优质品。(写出计算过程)___________。
4.(1)溶液由蓝色变为无色,且半分钟内不再复原
(2)是
解析:(1)由题意可知,溶液中的碘与硫代硫酸钠溶液完全反应时,滴入最后一滴硫代硫酸钠溶液,溶
液由蓝色变为无色,则当溶液由蓝色变为无色,且半分钟内不再复原说明滴定达到滴定终点,故答案为:
溶液由蓝色变为无色,且半分钟内不再复原;
(2)由题意可知,滴定消耗20.00mL 0.1000mol/L硫代硫酸钠溶液,则与焦亚硫酸钠反应的碘的物质的量
为0.1000mol/L×0.03000L —0.1000mol/L×0.02000L× =0.002mol,由得失电子数目守可得如下关系:Na S O
2 2 5
—2I ,由消耗碘的物质的量可知,样品中焦亚硫酸钠的质量分数为 ×100%≈97.44%>
296.5%,则该样品是为优质品,故答案为:是。
5.(2022·河北唐山·高三开学考试) 是制备金属钛及其化合物的重要中间体。已知反应:
,在耐高温陶瓷管内加入 粉末和碳粉制备 。装置如图(夹持装置
略去)。
已知:
① 的熔、沸点分别为 、 ,遇潮湿空气产生白色烟雾;
② 的熔、沸点分别为 、 ,与 互溶。
请回答下列问题:
(1)装置A中反应的离子反应方程式为_______,
(2)装置C中所盛试剂为_______,装置D仪器名称_______。
(3)装置E中碱石灰的作用是_______。装置F中生成了金属单质和两种酸性气体,写出其反应的化学方程式
为_______。
(4)制备 时副反应生成 。实验结束后提纯 的操作是_______(填操作名称)。
(5)测定产品纯度:测定产品密度为 。准确量取 产品,溶于盛有足量盐酸的 容
量瓶中。摇至无烟雾后加水稀释至刻度线,摇匀得到含 溶液。取 配好的溶液加入过量金属铝,
将 全部转化为 。再加适量盐酸待过量金属铝完全溶解并冷却后得无色溶液,加入指示剂,用
标准溶液滴定至终点,将 氧化为 。记录消耗标准溶液的体积。重复操作2~3次,消耗标准溶液平均体积为 。
①滴定时所用的指示剂为_______(填标号)。
a.酚酞溶液 b.甲基橙 c. 溶液 d. 溶液
②滴定到达终点的现象是_______。
③产品中 的纯度为_______。
5.(1)2MnO + 16H+ + 10Cl-=2Mn2+ +5Cl ↑+8H O
2 2
(2) 浓硫酸 直形冷凝管
(3) 防止水蒸气进入,影响产品纯度;吸收未反应的氯气,防止污染空气
PdCl +CO+H O=Pd+CO +2HCl
2 2 2
(4)蒸馏
(5) c 滴入最后半滴硫酸铁铵标准溶液,锥形瓶内溶液由无色变红色且半分钟不褪色 98.8%
解析:(1)装置A中是高锰酸钾和浓盐酸制备氯气,离子方程式为:2MnO + 16H+ + 10Cl-=2Mn2+
+5Cl ↑+8H O;
2 2
(2)装置A制备的氯气中含有氯化氢和水蒸气,装置C可以除去其中的水蒸汽,其中的试剂为:浓硫酸;
由图可知,装置D仪器名称为直形冷凝管;
(3)由图可知,装置E中的为碱石灰,可以吸收水蒸气,另外,反应过程中使用了氯气,氯气有毒,氯气
可以和碱石灰反应;由题干信息客户自,在制备 的过程中会产生一氧化碳,一氧化碳在装置F中和氯
化铅以及水反应生成单质铅和二氧化碳,故答案为:防止水蒸气进入,影响产品纯度;吸收未反应的氯气,
防止污染空气;PdCl +CO+H O=Pd+CO +2HCl;
2 2 2
(4)由题干信息可知 和 沸点相差较大,故提纯的时候可以采用蒸馏的方法分离;
(5)①标准溶液是 其中的三价铁遇到硫氰化钾显示红色,故答案为:c;
②滴定终点时三价铁和硫氰根离子相遇显示红色,故答案为:滴入最后半滴硫酸铁铵标准溶液,锥形瓶内
溶液由无色变红色且半分钟不褪色;
③由题意可得如下关系:TiO —Ti3+—Fe3+,滴定消耗0.08650mol/L标准溶液的平均体积为10.40mL,则样品
2中二氧化钛的纯度为 。
题点(三)沉淀滴定
6.(2022·陕西省高三模拟)用沉淀滴定法快速测定NaI等碘化物溶液中 ,实验过程包括准备标准溶
液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取 (0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备
用。
b.配制并标定100mL 标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL 溶液(过量),使 完全转化为AgI沉淀。
c.加入 溶液作指示剂。
d.用 溶液滴定过量的 ,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,
停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
消耗 标准溶液体积/mL 10.24 10.02 9.98
f.数据处理。回答下列问题:
(1)滴定应在 的条件下进行,其原因是______。
(2)b和c两步操作不能颠倒,说明理由______。
(3)计算 ______ 。(4)判断下列操作对 测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制 标准溶液时,烧杯中的溶液有少量溅出,则测定结果______。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果______。
6.(1)防止因 的水解而影响滴定终点的判断(或抑制 的水解)
(2)若颠倒, 与 反应,指示剂耗尽,无法判断滴定终点
(3)0.0600
(4) 偏高 偏高
解析:用沉淀滴定法快速测定 等碘化物溶液中 ,根据 计算氢离子浓
度和进行误差分析。
(1)实验中用 溶液作指示剂,利用Fe3+与SCN-作用溶液变血红色判断滴定终点,滴定应在
pH<0.5的条件下进行,其原因是抑制Fe3+的水解。。
(2)b和c两步操作不能颠倒,说明理由:若颠倒, 与 反应2Fe3++2I-=2Fe2++I ,指示剂耗尽,无法判
2
断滴定终点。
(3)由于第1次实验误差较大,第1次实验数据略去,两次实验消耗NH SCN标准溶液体积的平均值为
4
=10.00mL,n(AgNO ) =n(NH SCN)=0.1mol/L 0.01L=0.001mol,与I-反应的AgNO 物质的
3 过量 4 3
量为0.1mol/L 0.025L-0.001mol=0.0015mol,n(I-)=0.0015mol, = =0.0600mol/L。。
(4)反应的原理为c(AgNO )×V(AgNO )=c(NH SCN)×V(NH SCN)+c(I−)×V(I−),①若在配制AgNO 标准溶液时,
3 3 4 4 3
烧杯中的溶液有少量溅出,配得的AgNO 溶液浓度偏小,导致滴定时消耗NH SCN标准溶液的体积偏小,
3 4
测定结果偏高。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,消耗NH SCN标准溶液的体积偏小,测定结果偏高。
4
7.碱式氯化铜[ ]是重要的无机杀菌剂,是一种墨绿色结晶性粉末,难溶于水,溶于稀盐酸和
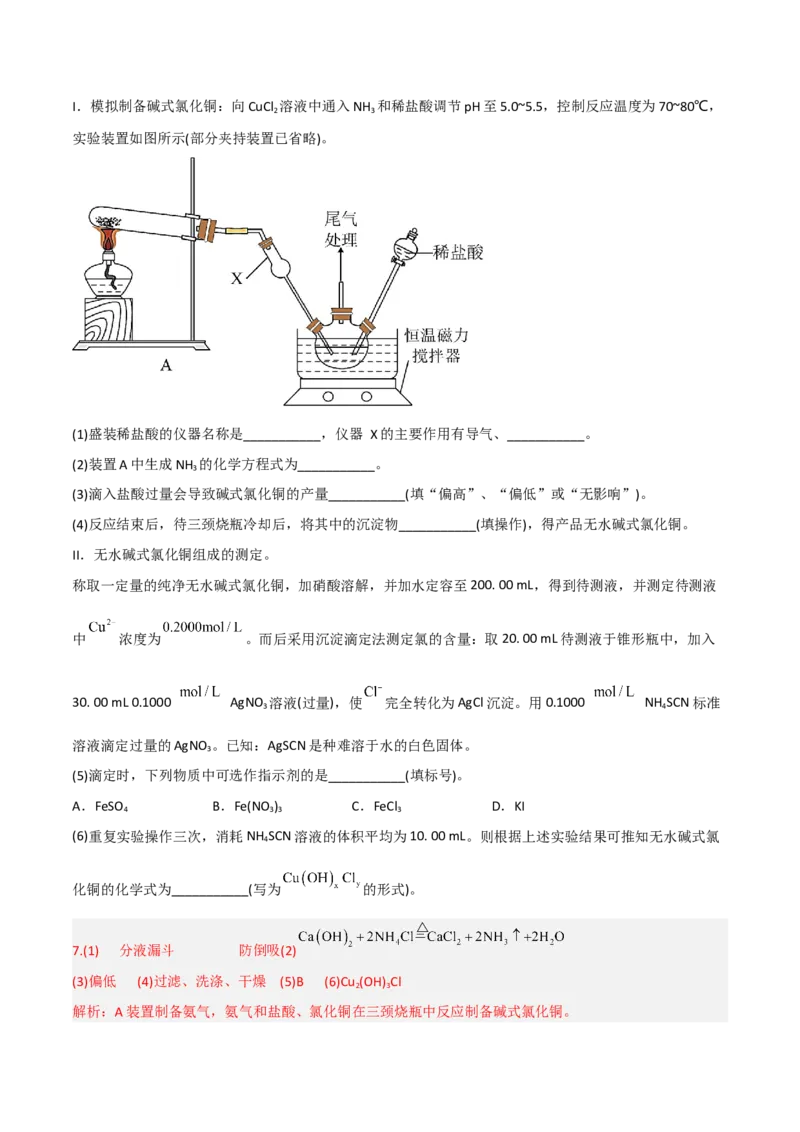
氨水,在空气中十分稳定。I.模拟制备碱式氯化铜:向CuCl 溶液中通入NH 和稀盐酸调节pH至5.0~5.5,控制反应温度为70~80℃,
2 3
实验装置如图所示(部分夹持装置已省略)。
(1)盛装稀盐酸的仪器名称是___________,仪器 X的主要作用有导气、___________。
(2)装置A中生成NH 的化学方程式为___________。
3
(3)滴入盐酸过量会导致碱式氯化铜的产量___________(填“偏高”、“偏低”或“无影响”)。
(4)反应结束后,待三颈烧瓶冷却后,将其中的沉淀物___________(填操作),得产品无水碱式氯化铜。
II.无水碱式氯化铜组成的测定。
称取一定量的纯净无水碱式氯化铜,加硝酸溶解,并加水定容至200. 00 mL,得到待测液,并测定待测液
中 浓度为 。而后采用沉淀滴定法测定氯的含量:取20. 00 mL待测液于锥形瓶中,加入
30. 00 mL 0.1000 AgNO 溶液(过量),使 完全转化为AgCl沉淀。用0.1000 NH SCN标准
3 4
溶液滴定过量的AgNO 。已知:AgSCN是种难溶于水的白色固体。
3
(5)滴定时,下列物质中可选作指示剂的是___________(填标号)。
A.FeSO B.Fe(NO ) C.FeCl D.KI
4 3 3 3
(6)重复实验操作三次,消耗NH SCN溶液的体积平均为10. 00 mL。则根据上述实验结果可推知无水碱式氯
4
化铜的化学式为___________(写为 的形式)。
7.(1) 分液漏斗 防倒吸(2)
(3)偏低 (4)过滤、洗涤、干燥 (5)B (6)Cu (OH) Cl
2 3
解析:A装置制备氨气,氨气和盐酸、氯化铜在三颈烧瓶中反应制备碱式氯化铜。(1)根据仪器特点判断盛装稀盐酸的仪器是分液漏斗;仪器X球型干燥管连接A装置,A中是制取氨气的
装置,氨气极易溶于水,故X管的作用是导气、防止倒吸, 故答案为:分液漏斗;防止倒吸;
(2)A是大试管,试管口略向下倾斜,故是固体或固体混合物加热制取气体的装置,根据题目需要制氨气,
故A中发生的化学方程式为: ;
(3)当滴入稀盐酸过量会导致溶液碱性减弱,酸性增强,不利用生成碱式氯化铜,故碱式氯化铜的的产
量偏低,故答案为:偏低;
(4)反应结束后,待三颈烧瓶冷却后,将其中的沉淀物过滤、洗涤、干燥,得产品无水碱式氯化铜;
(5)NH SCN标准溶液滴定过量的硝酸银,生成AgSCN沉淀,当溶液中的Ag+被消耗完时,再滴入NH SCN
4 4
溶液,溶液中的指示剂应和NH SCN反应有明显现象,故应选择三价铁做指示剂,因为SCN-可与三价铁反
4
应有血红色现象产生,为不干扰检验,故应该加入硝酸铁,故选答案b;
(6)根据Cu2+浓度为0. 2000 mol·L-1及配制溶液的总体积为200.00mL可计算出铜离子的物质量为
n(Cu2+)=c⋅V =0.04mol;滴定过量的AgNO ,用去0.1000 mol· L-1 NH SCN标准溶液为10.00 mL,故NH SCN
3 4 4
的物质的量为1×10-3mol,根据AgSCN判断剩余银离子的物质的量为0.001mol,则生成氯化银的氯离子的物
质的量为30. 00 mL×10-3× 0.1000 mol·L-1-0.001mol=0.002mol;则Cu2+和Cl-的物质的量之比为2:1,根据正负
化合价代数和为0,铜离子、氢氧根离子、氯离子三种微粒的物质的量之比为2:3:1,故化学式为:
Cu (OH) Cl;故答案为:Cu (OH) Cl。
2 3 2 3
题点(四)其他形式的滴定
8.(2021·湖南卷)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,
并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. 的制备
步骤Ⅱ.产品中 含量测定
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸 ;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终点),
又消耗盐酸 ;
④平行测定三次, 平均值为22.45, 平均值为23.51。
已知:(i)当温度超过35℃时, 开始分解。
(ii)相关盐在不同温度下的溶解度表
温度/ 0 10 20 30 40 50 60
35.7 35.8 36.0 36.3 36.6 37.0 37.3
11.9 15.8 21.0 27.0
6.9 8.2 9.6 11.1 12.7 14.5 16.4
29.4 33.3 37.2 41.4 45.8 50.4 55.2
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是_______;
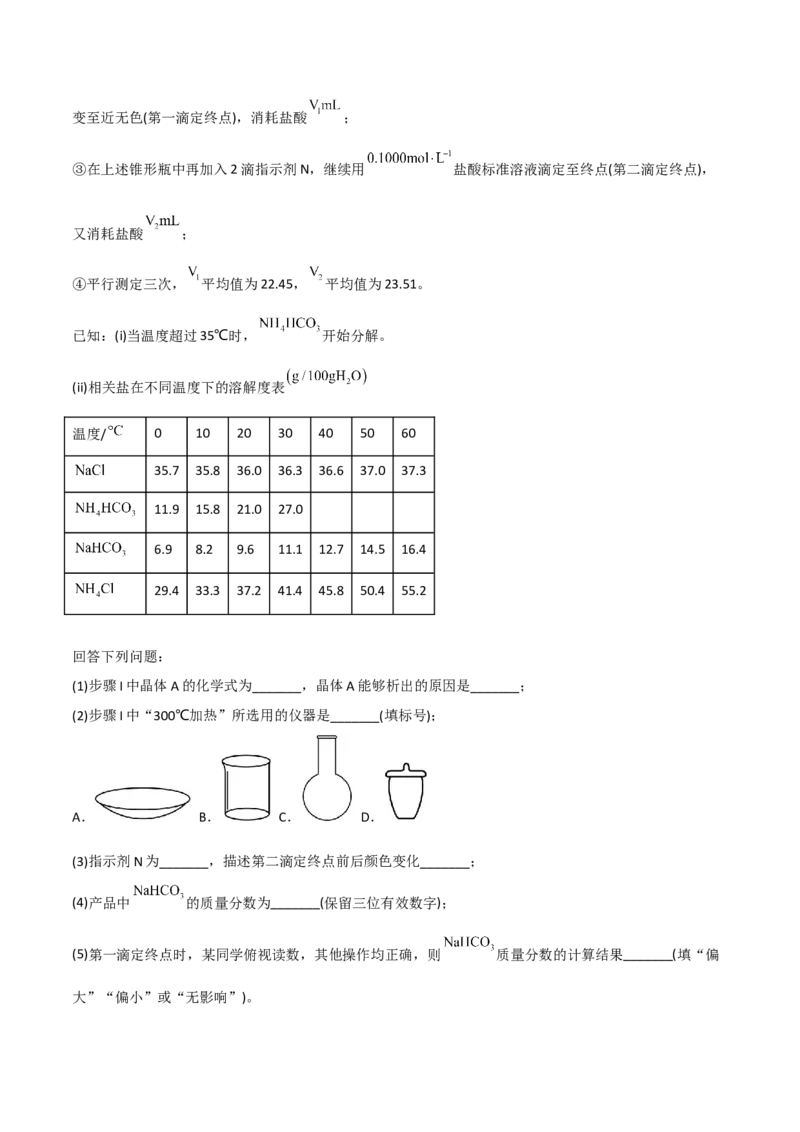
(2)步骤I中“300℃加热”所选用的仪器是_______(填标号);
A. B. C. D.
(3)指示剂N为_______,描述第二滴定终点前后颜色变化_______;
(4)产品中 的质量分数为_______(保留三位有效数字);
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则 质量分数的计算结果_______(填“偏
大”“偏小”或“无影响”)。8. (1)NaHCO 在30-35 C时NaHCO 的溶解度最小(意思合理即可) (2) D (3)
3 3
甲基橙 由黄色变橙色,且半分钟内不褪色 (4) 3.56% (5) 偏大
解析:根据上述分析可知,
(1)根据题给信息中盐在不同温度下的溶解度不难看出,控制温度在30-35 C,目的是为了时NH HCO 不发
4 3
生分解,同时析出NaHCO 固体,得到晶体A,因为在30-35 C时,NaHCO 的溶解度最小,故答案为:
3 3
NaHCO ;在30-35 C时NaHCO 的溶解度最小;
3 3
(2)300 C加热抽干后的NaHCO 固体,需用坩埚、泥三角、三脚架进行操作,所以符合题意的为D项,故
3
答案为:D;
(3)根据上述分析可知,第二次滴定时,使用的指示剂N为甲基橙试液,滴定到终点前溶液的溶质为碳酸氢
钠和氯化钠,滴定达到终点后溶液的溶质为氯化钠和碳酸(溶解的CO ),所以溶液的颜色变化为:由黄
2
色变为橙色,且半分钟内不褪色;
(4) 第一次滴定发生的反应是:Na CO +HCl=NaHCO +NaCl,则n(Na CO )=n (NaHCO )=n(HCl)=0.1000mol/L
2 3 3 2 3 生成 3
22.45 10-3L=2.245 10-3mol,第二次滴定消耗的盐酸的体积V =23.51mL,则根据方程式
2
NaHCO +HCl=NaCl+H O+CO ↑可知,消耗的NaHCO 的物质的量n (NaHCO )= 0.1000mol/L 23.51 10-
3 2 2 3 总 3
3L=2.351 10-3mol,则原溶液中的NaHCO 的物质的量n(NaHCO )= n (NaHCO )- n (NaHCO )= 2.351 10-
3 3 总 3 生成 3
3mol-2.245 10-3mol=1.06 10-4mol,则原产品中NaHCO 的物质的量为 =1.06 10-
3
3mol,故产品中NaHCO 的质量分数为 ,故答案为:
3
3.56%;
(5)若该同学第一次滴定时,其他操作均正确的情况下,俯视读数,则会使标准液盐酸的体积偏小,即测得
V 偏小,所以原产品中NaHCO 的物质的量会偏大,最终导致其质量分数会偏大,故答案为:偏大。
1 3
9.(2022·山东淄博第一中学高三期中)氮化铬(CrN)是一种耐磨性良好的新型材料,难溶于水。探究小组
同学用如图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。已知:实验室中常用NH Cl溶液与NaNO 溶液反应制取N ;CrCl 能溶于水和乙醇,高温下能被氧气氧化。
4 2 2 3
回答下列问题:
(1)实验装置中盛放饱和氯化铵溶液的仪器名称是_______,实验准备就绪后,装置A和装置E应先加热的
是_______(填“装置A”或“装置E”),原因是_______。
(2)写出装置E中发生反应的化学方程式_______。实验过程中需间歇性微热b处导管的目的是_______。
(3)为了测所得CrN纯度,把7.0g所得产品中加入足量NaOH溶液,然后通入水蒸气将NH 全部蒸出,将
3
NH 用60mL1lmol·L-1H SO 溶液完全吸收,剩余的H SO 用2mol·L-1NaOH滴定,消耗NaOH溶液10mL。
3 2 4 2 4
①滴定管使用的正确的操作顺序为:蒸馏水洗涤→标准液润洗→_______→洗净→放回滴定管架(填字母)。
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②所得产品中CrN的质量分数为_______(用百分数表示,保留一位小数)。
9.(1) 恒压滴液漏斗 装置A 用N 排尽装置中的空气,防止CrCl 与氧气反应
2 3
(2) 防止NH 与HCl反应生成NH Cl固体堵塞导管造成危险
3 4
(3) c→b→a→d 94.3%
解析:(1)由图可知,实验装置中盛放饱和氯化铵溶液的仪器是恒压滴液漏斗;实验准备就绪后,应先加热
A装置生成氮气,N 排尽装置中的空气,防止CrCl 与氧气反应,故答案为:恒压滴液漏斗;装置A;用N
2 3 2
排尽装置中的空气,防止CrCl 与氧气反应;
3
(2)装置E中CrCl 与氨气反应生成CrN和HCl,反应的化学方程式为 ;氨气与HCl遇
3
冷易化合生成NH Cl,因此实验过程中需间歇性微热b处导管,防止NH 与HCl反应生成NH Cl固体堵塞导
4 3 4管造成危险,故答案为: ;防止NH 与HCl反应生成NH Cl固体堵塞导管造成危险;
3 4
(3)①滴定管使用时应先用蒸馏水洗涤,为防止稀释标准液,再用标准液润洗,然后装入标准液并排净尖
嘴处的气泡,并调节液面至0刻度或0刻度略靠下,记录刻度,然后开始滴定,滴定结束后,记录刻度,
将未滴定完的标准液回收,再洗净滴定管放回管架,因此操作顺序为c→b→a→d,故答案为:
c→b→a→d;
②向7.0g所得CrN中加入足量NaOH溶液,然后通入水蒸气将NH 全部蒸出,将NH 用60mL1mol/LH SO 溶
3 3 2 4
液完全吸收,剩余的H SO 用10mL2mol/LNaOH溶液恰好中和,则有 ,
2 4
,则
, ,故所得产品中CrN的
质量分数为 ,故答案为:94.3%。