文档内容
高频考点 31 酸碱中和滴定及其拓展
题点(一)酸碱中和滴定
1.(2021·广东)测定浓硫酸试剂中 含量的主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取 待测液,用 的 溶液滴定。
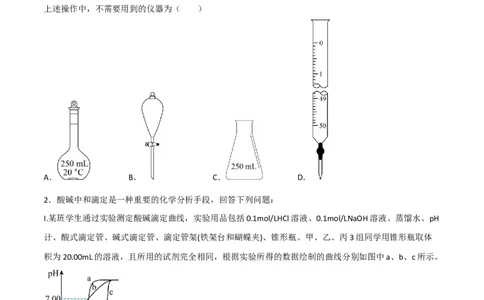
上述操作中,不需要用到的仪器为( )
A. B. C. D.
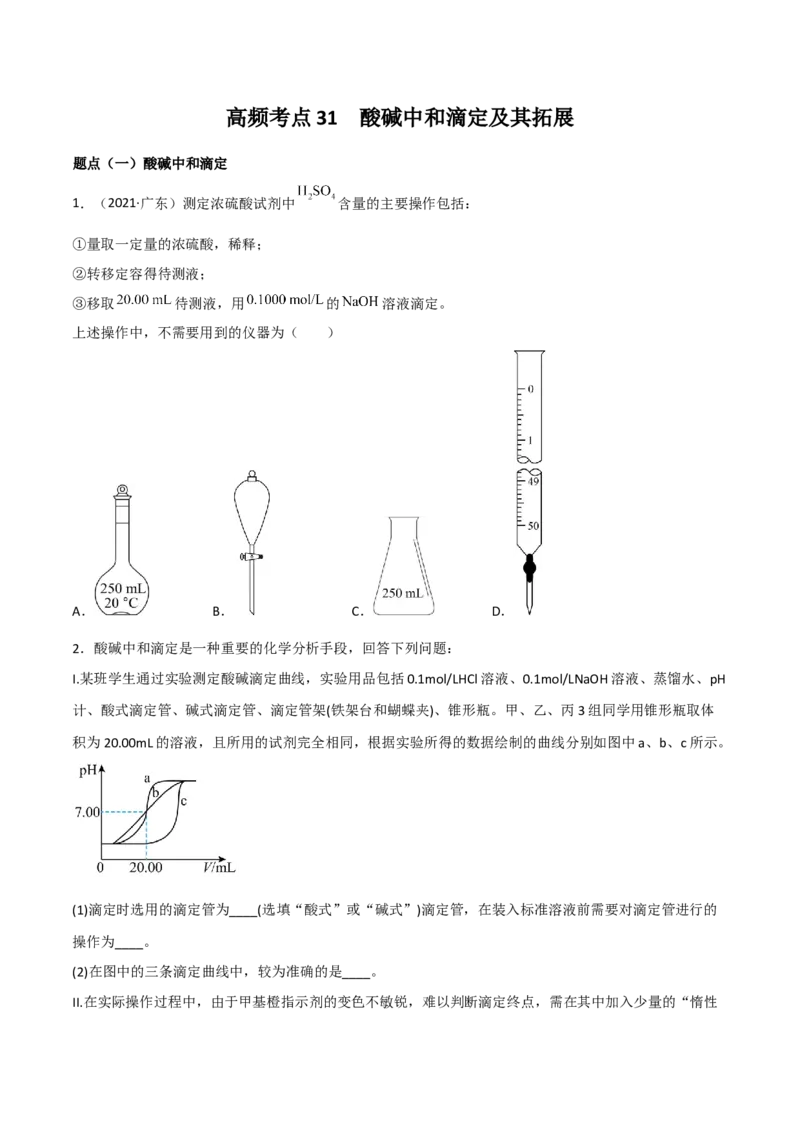
2.酸碱中和滴定是一种重要的化学分析手段,回答下列问题:
I.某班学生通过实验测定酸碱滴定曲线,实验用品包括0.1mol/LHCl溶液、0.1mol/LNaOH溶液、蒸馏水、pH
计、酸式滴定管、碱式滴定管、滴定管架(铁架台和蝴蝶夹)、锥形瓶。甲、乙、丙3组同学用锥形瓶取体
积为20.00mL的溶液,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示。
(1)滴定时选用的滴定管为____(选填“酸式”或“碱式”)滴定管,在装入标准溶液前需要对滴定管进行的
操作为____。
(2)在图中的三条滴定曲线中,较为准确的是____。
II.在实际操作过程中,由于甲基橙指示剂的变色不敏锐,难以判断滴定终点,需在其中加入少量的“惰性染料”靛蓝二磺酸钠,其固定颜色与甲基橙的可变颜色进行叠加(变色范围不变),形成“酸色”为紫色、
过渡色为浅灰色、“碱色”为绿色的混合指示剂。已知室温下0.10mol/LNH Cl溶液的,若以甲基橙-靛蓝
4
二磺酸钠为指示剂,用0.20mol/L盐酸滴定20.00mL同浓度的氨水,则:
(3)NH Cl溶液显酸性的原因是____(用离子方程式表示)。
4
(4)判断滴定终点的现象是____。
(5)若多组实验中所用盐酸的体积均略大于20.00mL,原因是____。
题点(二)氧化还原反应滴定
3.(2021·山东卷节选)利用碘量法测定WCl 产品纯度,实验如下:
6
(1)称量:将足量CS (易挥发)加入干燥的称量瓶中,盖紧称重为m g;开盖并计时1分钟,盖紧称重为
2 1
m g;再开盖加入待测样品并计时1分钟,盖紧称重为m g,则样品质量为___g(不考虑空气中水蒸气的干
2 3
扰)。
(2)滴定:先将WCl 转化为可溶的Na WO ,通过IO 离子交换柱发生反应:WO +Ba(IO ) =BaWO +2IO ;
6 2 4 3 2 4
交换结束后,向所得含IO 的溶液中加入适量酸化的KI溶液,发生反应:IO +5I-+6H+=3I +3H O;反应完全
2 2
后,用Na S O 标准溶液滴定,发生反应:I +2S O =2I-+S O 。滴定达终点时消耗cmol•L-1的Na S O 溶液
2 2 3 2 2 4 2 2 3
VmL,则样品中WCl (摩尔质量为Mg•mol-1)的质量分数为___。称量时,若加入待测样品后,开盖时间超过
6
1分钟,则滴定时消耗Na S O 溶液的体积将___(填“偏大”“偏小”或“不变”),样品中WCl 质量分数
2 2 3 6
的测定值将___(填“偏大”“偏小”或“不变”)。
4.(2022·山东·乳山市银滩高级中学高三期末)焦亚硫酸钠含量的测定
工业焦亚硫酸钠(Na S O )优质品要求质量分数 %。通过下列实验检测焦亚硫酸钠样品是否达到优质
2 2 5
品标准。实验检测原理为:
(未配平)
准确称取 样品,快速置于预先加入 碘标准液及 水的 碘量瓶中,
加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置 ;用
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na S O 溶
2 2 3
液 。(1)滴定终点现象是___________。
(2)通过计算判断该样品是否为优质品。(写出计算过程)___________。
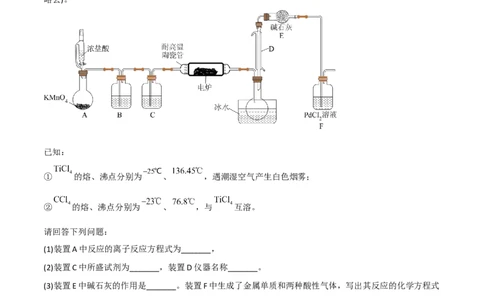
5.(2022·河北唐山·高三开学考试) 是制备金属钛及其化合物的重要中间体。已知反应:
,在耐高温陶瓷管内加入 粉末和碳粉制备 。装置如图(夹持装置
略去)。
已知:
① 的熔、沸点分别为 、 ,遇潮湿空气产生白色烟雾;
② 的熔、沸点分别为 、 ,与 互溶。
请回答下列问题:
(1)装置A中反应的离子反应方程式为_______,
(2)装置C中所盛试剂为_______,装置D仪器名称_______。
(3)装置E中碱石灰的作用是_______。装置F中生成了金属单质和两种酸性气体,写出其反应的化学方程式
为_______。
(4)制备 时副反应生成 。实验结束后提纯 的操作是_______(填操作名称)。
(5)测定产品纯度:测定产品密度为 。准确量取 产品,溶于盛有足量盐酸的 容
量瓶中。摇至无烟雾后加水稀释至刻度线,摇匀得到含 溶液。取 配好的溶液加入过量金属铝,
将 全部转化为 。再加适量盐酸待过量金属铝完全溶解并冷却后得无色溶液,加入指示剂,用标准溶液滴定至终点,将 氧化为 。记录消耗标准溶液的体积。重复操
作2~3次,消耗标准溶液平均体积为 。
①滴定时所用的指示剂为_______(填标号)。
a.酚酞溶液 b.甲基橙 c. 溶液 d. 溶液
②滴定到达终点的现象是_______。
③产品中 的纯度为_______。
题点(三)沉淀滴定
6.(2022·陕西省高三模拟)用沉淀滴定法快速测定NaI等碘化物溶液中 ,实验过程包括准备标准溶
液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取 (0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备
用。
b.配制并标定100mL 标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL 溶液(过量),使 完全转化为AgI沉淀。
c.加入 溶液作指示剂。
d.用 溶液滴定过量的 ,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,
停止滴定。
e.重复上述操作两次。三次测定数据如下表:
实验序号 1 2 3
消耗 标准溶液体积/mL 10.24 10.02 9.98
f.数据处理。回答下列问题:(1)滴定应在 的条件下进行,其原因是______。
(2)b和c两步操作不能颠倒,说明理由______。
(3)计算 ______ 。
(4)判断下列操作对 测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制 标准溶液时,烧杯中的溶液有少量溅出,则测定结果______。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果______。
7.碱式氯化铜[ ]是重要的无机杀菌剂,是一种墨绿色结晶性粉末,难溶于水,溶于稀盐酸和
氨水,在空气中十分稳定。
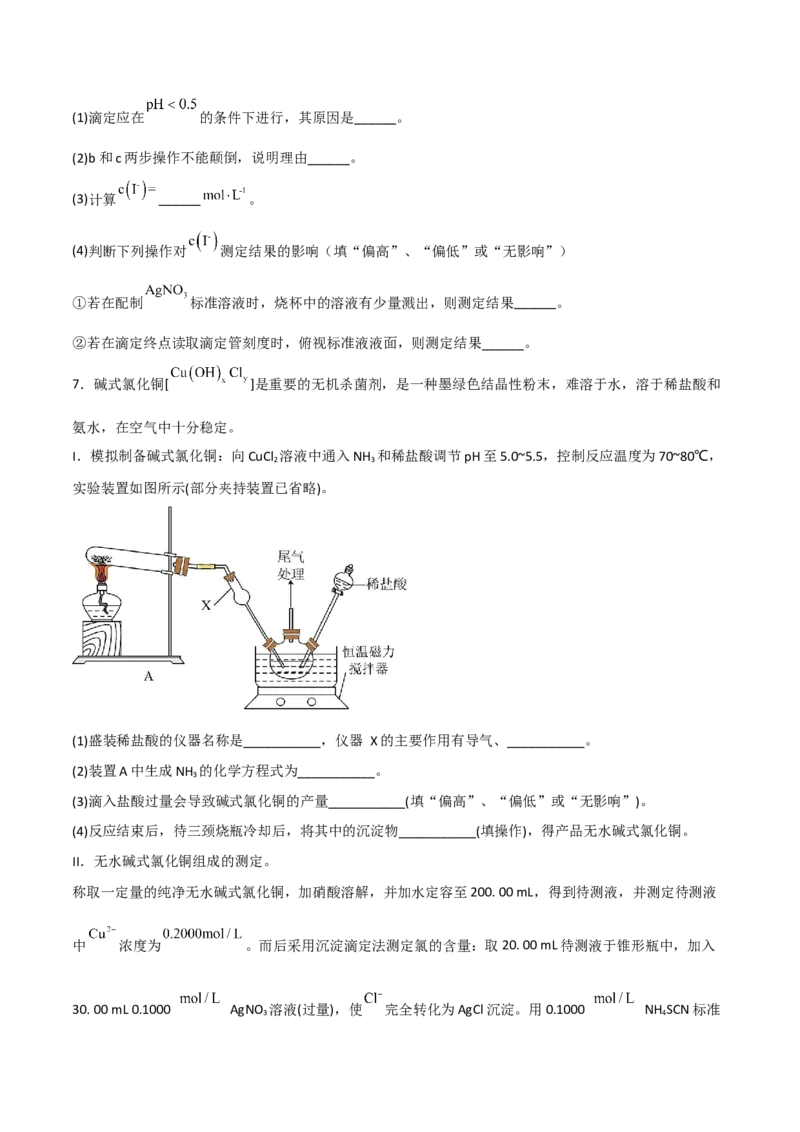
I.模拟制备碱式氯化铜:向CuCl 溶液中通入NH 和稀盐酸调节pH至5.0~5.5,控制反应温度为70~80℃,
2 3
实验装置如图所示(部分夹持装置已省略)。
(1)盛装稀盐酸的仪器名称是___________,仪器 X的主要作用有导气、___________。
(2)装置A中生成NH 的化学方程式为___________。
3
(3)滴入盐酸过量会导致碱式氯化铜的产量___________(填“偏高”、“偏低”或“无影响”)。
(4)反应结束后,待三颈烧瓶冷却后,将其中的沉淀物___________(填操作),得产品无水碱式氯化铜。
II.无水碱式氯化铜组成的测定。
称取一定量的纯净无水碱式氯化铜,加硝酸溶解,并加水定容至200. 00 mL,得到待测液,并测定待测液
中 浓度为 。而后采用沉淀滴定法测定氯的含量:取20. 00 mL待测液于锥形瓶中,加入
30. 00 mL 0.1000 AgNO 溶液(过量),使 完全转化为AgCl沉淀。用0.1000 NH SCN标准
3 4溶液滴定过量的AgNO 。已知:AgSCN是种难溶于水的白色固体。
3
(5)滴定时,下列物质中可选作指示剂的是___________(填标号)。
A.FeSO B.Fe(NO ) C.FeCl D.KI
4 3 3 3
(6)重复实验操作三次,消耗NH SCN溶液的体积平均为10. 00 mL。则根据上述实验结果可推知无水碱式氯
4
化铜的化学式为___________(写为 的形式)。
题点(四)其他形式的滴定
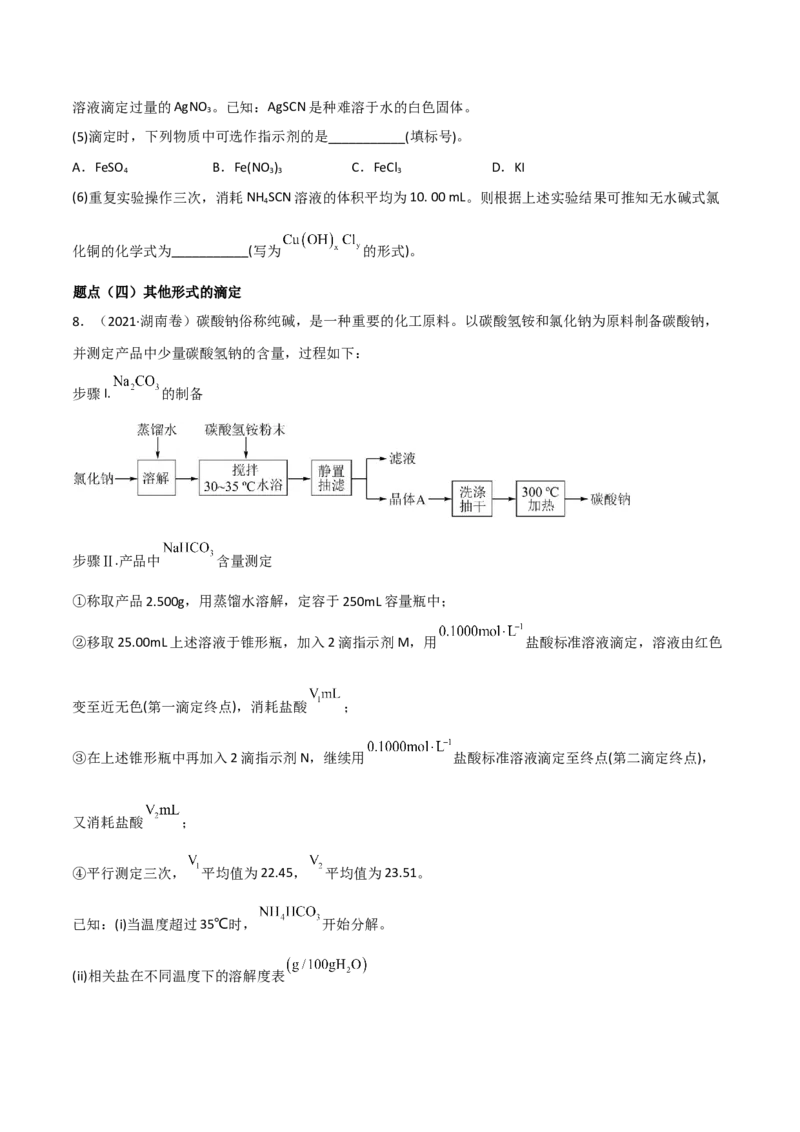
8.(2021·湖南卷)碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,
并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. 的制备
步骤Ⅱ.产品中 含量测定
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定,溶液由红色
变至近无色(第一滴定终点),消耗盐酸 ;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终点),
又消耗盐酸 ;
④平行测定三次, 平均值为22.45, 平均值为23.51。
已知:(i)当温度超过35℃时, 开始分解。
(ii)相关盐在不同温度下的溶解度表温度/ 0 10 20 30 40 50 60
35.7 35.8 36.0 36.3 36.6 37.0 37.3
11.9 15.8 21.0 27.0
6.9 8.2 9.6 11.1 12.7 14.5 16.4
29.4 33.3 37.2 41.4 45.8 50.4 55.2
回答下列问题:
(1)步骤I中晶体A的化学式为_______,晶体A能够析出的原因是_______;
(2)步骤I中“300℃加热”所选用的仪器是_______(填标号);
A. B. C. D.
(3)指示剂N为_______,描述第二滴定终点前后颜色变化_______;
(4)产品中 的质量分数为_______(保留三位有效数字);
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则 质量分数的计算结果_______(填“偏
大”“偏小”或“无影响”)。
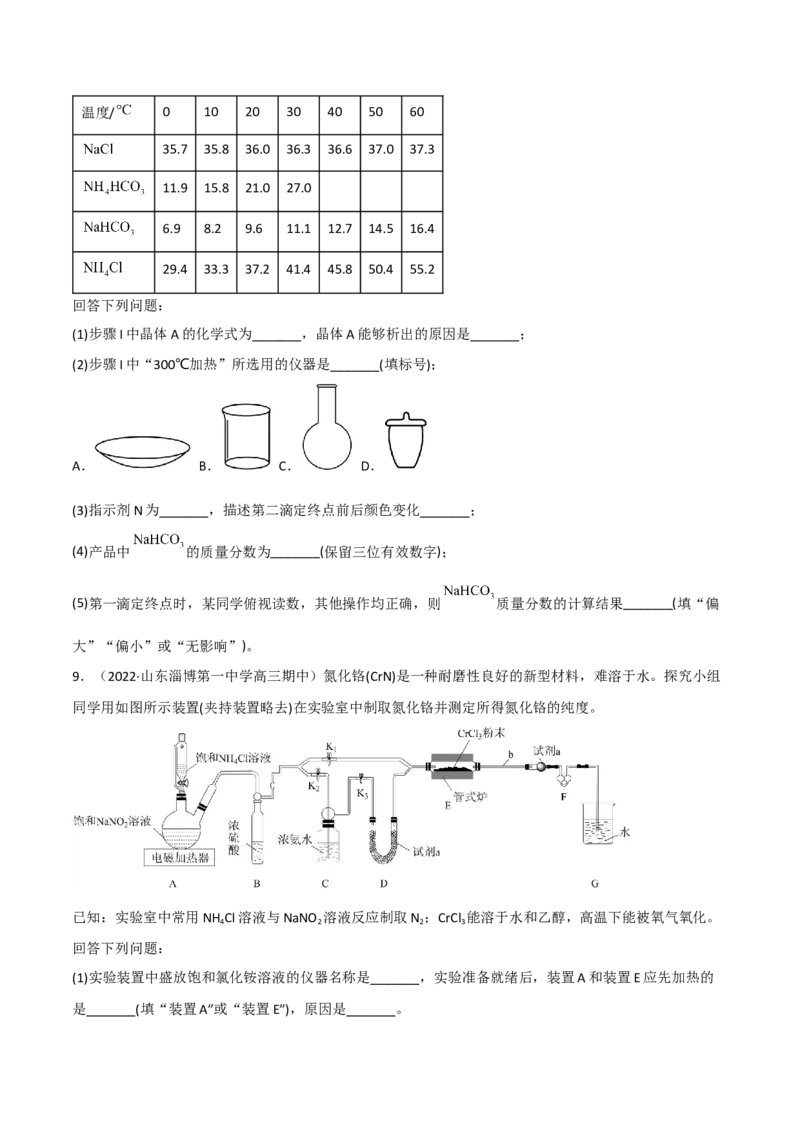
9.(2022·山东淄博第一中学高三期中)氮化铬(CrN)是一种耐磨性良好的新型材料,难溶于水。探究小组
同学用如图所示装置(夹持装置略去)在实验室中制取氮化铬并测定所得氮化铬的纯度。
已知:实验室中常用NH Cl溶液与NaNO 溶液反应制取N ;CrCl 能溶于水和乙醇,高温下能被氧气氧化。
4 2 2 3
回答下列问题:
(1)实验装置中盛放饱和氯化铵溶液的仪器名称是_______,实验准备就绪后,装置A和装置E应先加热的
是_______(填“装置A”或“装置E”),原因是_______。(2)写出装置E中发生反应的化学方程式_______。实验过程中需间歇性微热b处导管的目的是_______。
(3)为了测所得CrN纯度,把7.0g所得产品中加入足量NaOH溶液,然后通入水蒸气将NH 全部蒸出,将
3
NH 用60mL1lmol·L-1H SO 溶液完全吸收,剩余的H SO 用2mol·L-1NaOH滴定,消耗NaOH溶液10mL。
3 2 4 2 4
①滴定管使用的正确的操作顺序为:蒸馏水洗涤→标准液润洗→_______→洗净→放回滴定管架(填字母)。
a.滴定结束后,记录刻度
b.调节液面至0刻度或0刻度略靠下,记录刻度
c.装入标准液并排净尖嘴处的气泡
d.将未滴定完的标准液回收
②所得产品中CrN的质量分数为_______(用百分数表示,保留一位小数)。