文档内容
高频考点 33 离子浓度大小的比较
1.(2022·浙江卷) 时,向 浓度均为 的盐酸和醋酸的混合溶液中逐滴加入 的
溶液(酷酸的 ;用 的 溶液滴定 等浓度的盐酸,滴定终点的 突
跃范围4.3~9.7)。下列说法不正确的是( )
A.恰好中和时,溶液呈碱性
B.滴加 溶液至 的过程中,发生反应的离子方程式为:
C.滴定过程中,
D. 时,
1.B A.恰好中和时,生成氯化钠溶液和醋酸钠溶液,其中醋酸根离子会水解,溶液显碱性,A正确;B.
滴加 溶液至 的过程中,若只发生反应的离子方程式: ,则滴加NaOH溶液的
体积为20mL,则根据电离常数, 的醋酸中,c(H+)≈c(CH COO-)= =
3
= >1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子方程
式为:H++OH-=H O和CH COOH+OH-=CH COO-+H O,B错误;C.滴定前盐酸和醋酸的浓度相同,故滴定过
2 3 3 2
程中,根据物料守恒可知: ,C正确;D.向 浓度均为
的盐酸和醋酸的混合溶液中逐滴加入 的 溶液,当盐酸的体积为20ml时,溶液为氯化钠和
醋酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH溶液的体积为30mL时,溶液为
NaCl和等浓度的CH COONa、CH COOH,根据Ka=1.8×10-5>Kh= 可知,此时溶液仍然呈酸性,
3 3需继续滴加NaOH溶液,故有 ,D正确;故答案为:B。
2.(2021·湖南卷)常温下,用 的盐酸分别滴定20.00mL浓度均为 三种一
元弱酸的钠盐 溶液,滴定曲线如图所示。下列判断错误的是( )
A.该 溶液中:
B.三种一元弱酸的电离常数:
C.当 时,三种溶液中:
D.分别滴加20.00mL盐酸后,再将三种溶液混合:
2. C A.NaX为强碱弱酸盐,在溶液中水解使溶液呈碱性,则溶液中离子浓度的大小顺序为c(Na+)>c(X-)
>c(OH-)>c(H+),故A正确;B.弱酸的酸性越弱,电离常数越小,由分析可知,HX、HY、HZ三种一元弱
酸的酸性依次减弱,则三种一元弱酸的电离常数的大小顺序为K(HX)>K (HY)>K(HZ),故B正确;C.当
a a a
溶液pH为7时,酸越弱,向盐溶液中加入盐酸的体积越大,酸根离子的浓度越小,则三种盐溶液中酸根
的浓度大小顺序为c(X-)>c(Y-)>c(Z-),故C错误;D.向三种盐溶液中分别滴加20.00mL盐酸,三种盐都完
全反应,溶液中钠离子浓度等于氯离子浓度,将三种溶液混合后溶液中存在电荷守恒关系c(Na+)+ c(H+)=
c(X-)+c(Y-)+c(Z-)+ c(Cl-)+ c(OH-),由c(Na+)= c(Cl-)可得:c(X-)+c(Y-)+c(Z-)= c(H+)—c(OH-),故D正确;故选C。
3.(2021·天津卷)常温下,下列有关电解质溶液的叙述正确的是( )
A.在 溶液中
B.在 溶液中C.在 溶液中
D.氨水和NH Cl溶液混合,形成pH=9的溶液中
4
3. A A.由于磷酸为多元酸,第一步电离大于第二步电离大于第三步电离,所以在 溶液
中,离子浓度大小为: ,故A正确;B.在 溶液
中,根据电荷守恒得到 ,故B错误;C.在 溶液中,
根据物料守恒得到 ,故C错误;D.氨水和NH Cl溶液混合,形成
4
pH=9的溶液,则 ,根据电荷守恒 ,则 ,故D错
误;故选A。
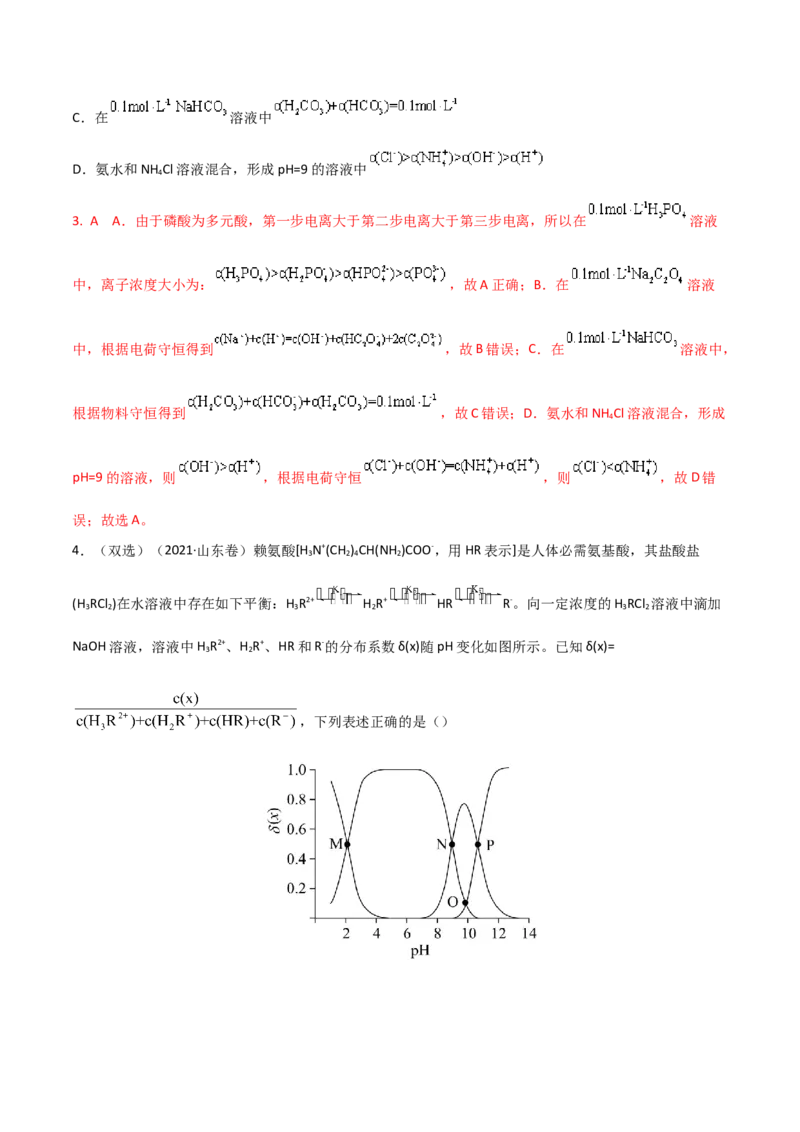
4.(双选)(2021·山东卷)赖氨酸[H N+(CH ) CH(NH )COO-,用HR表示]是人体必需氨基酸,其盐酸盐
3 2 4 2
(H RCl )在水溶液中存在如下平衡:H R2+ H R+ HR R-。向一定浓度的H RCl 溶液中滴加
3 2 3 2 3 2
NaOH溶液,溶液中H R2+、H R+、HR和R-的分布系数δ(x)随pH变化如图所示。已知δ(x)=
3 2
,下列表述正确的是()A. >
B.M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C.O点,pH=
D.P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
4.CD A. , ,因此 ,故A错误;
B.M点存在电荷守恒: ,此时
,因此 ,故B错误;
C.O点 ,因此 ,即 ,
因此 ,溶液 ,故C正确;D.P点溶质为NaCl、HR、
NaR,此时溶液呈碱性,因此 ,溶质浓度大于水解和电离所产生微粒浓度,因此
,故D正确;综上所述,正确的是CD,故答案为CD。
5.(2022·河南·焦作市第一中学模拟预测)常温下,一元碱 的 。在某体系中,
与 等离子不能穿过膜,未电离的 可自由穿过该膜(如图所示)。设溶液中 ,当达到平衡时,下列叙次正确的是( )
A.溶液Ⅰ中仅含有三种阴阳离子
B.溶液Ⅱ中的
C. 的电离度 :溶液Ⅰ<溶液Ⅱ
D.溶液Ⅰ中 大约是溶液Ⅱ中 的1668倍
5.D A.溶液Ⅰ中pH=7,所以存在 , ,故溶液Ⅰ中不仅
含有三种阴阳离子,A错误;B.常温下溶液Ⅱ中pH=11,溶液中 ,
, ,则 ,
解得 ,B错误;C.溶液Ⅰ中pH=7,所以存在 ,
, , ,则电离度为
,溶液Ⅱ中pH=11,溶液中 , ,则电离度为 ,溶液Ⅰ>溶液Ⅱ,C错误;D.溶液Ⅰ中 ,
, , ,
解得 ,溶液Ⅱ中 , ,
, ,解得 ,未电离的
可自由穿过该膜,故溶液Ⅰ和溶液Ⅱ中的 相等,溶液Ⅰ和Ⅱ中 之比为
,故溶液Ⅰ中 大约是溶液Ⅱ中 的1668倍,D正确;故答案选
D。
6.(2022·广东深圳·一模)常温下,将 溶液滴加到20mL 二元弱酸 溶液中,
混合溶液的pH随NaOH溶液滴入量的关系如图所示。下列叙述不正确的是( )
A.
B.b点时溶液中存在C.c点时溶液中存在
D.溶液中水的电离程度:c>b>a
6.C 滴定至a点时,溶液成分为NaHA和H A,滴定至b点时,溶液全为NaHA,滴定至c点时溶液成分为
2
NaHA和 Na A。A.a点时pH≈3,加入10mLNaOH溶液,此时c(H A)=c(NaHA),可知,
2 2
,A项正确;B. ,由c点pH=9.5可知
K (H A)=10-9.5,b点时溶液为NaHA,则HA-的电离程度大于水解程度,溶液中c(HA-) >c(A2-) >c(H A),B项正
a2 2 2
确;C.由电荷守恒可知,c点时溶液中c(Na+)+c(H+)= c(HA-)+ c(OH-)+2 c(A2-),C项错误;D.a点为H A与
2
NaHA混合溶液,b点为NaHA,c点为NaHA与Na A混合溶液,溶液中水的电离程度:c>b>a,D项正确;
2
故选C。
7.(2022·湖北·高三开学考试)常温下,向一定浓度的H X溶液中滴加NaOH溶液,混合溶液的pH与离子
2
浓度变化的关系如图所示。下列叙述错误的是( )
A.H X的电离常数K 的数量级为10-2
2 a1
B.水电离的(H+):N点c(X²-)>c(HX-)>c(H+)=c(OH-)
7.B A.由分析可知 ,A正确;B.直线n表示pH与 的关系, ,N点
=0,则c(H+)=1×10-4.3, HX-电离出氢离子使溶液呈酸性,则M点氢离子浓度更大,氢离子抑制水的电离,故水的电离程度N点>M点,B错误;
C.N点存在电荷守恒,c(Na+)+ c(H+)=2c(X2-)+c(HX-)+c(OH-),由图可知N点时c(X2-)=c(HX-),由选项B分析可知,
此时溶液显酸性,c(H+)>c(OH-),则c(Na+)<3c(X2-),C正确;
D.当混合溶液呈中性时 , ,所以c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-),D正确;
故选B。
8.(2022·烟台高三模拟)25℃时, 水溶液中含砷物种的分布分数(平衡时某物种的浓度占各物种
浓度之和的分数)随溶液的 变化如图所示。下列说法错误的是( )
A. 的电离常数
B. 时,溶液中
C. 时,溶液中
D.以酚酞为指示剂用 溶液滴定 溶液,终点时
8.D A.由图可知, 时, , ,
选项A正确;B.由图可知, 时,溶液中存在较多的 ,几乎不存在 ,选项B正确;
C.由图可知, 时, ,选项C正确;D.酚酞试剂的变色范围为8.2~10.0,由图可知,此时 ,选项D错误;答案选D。
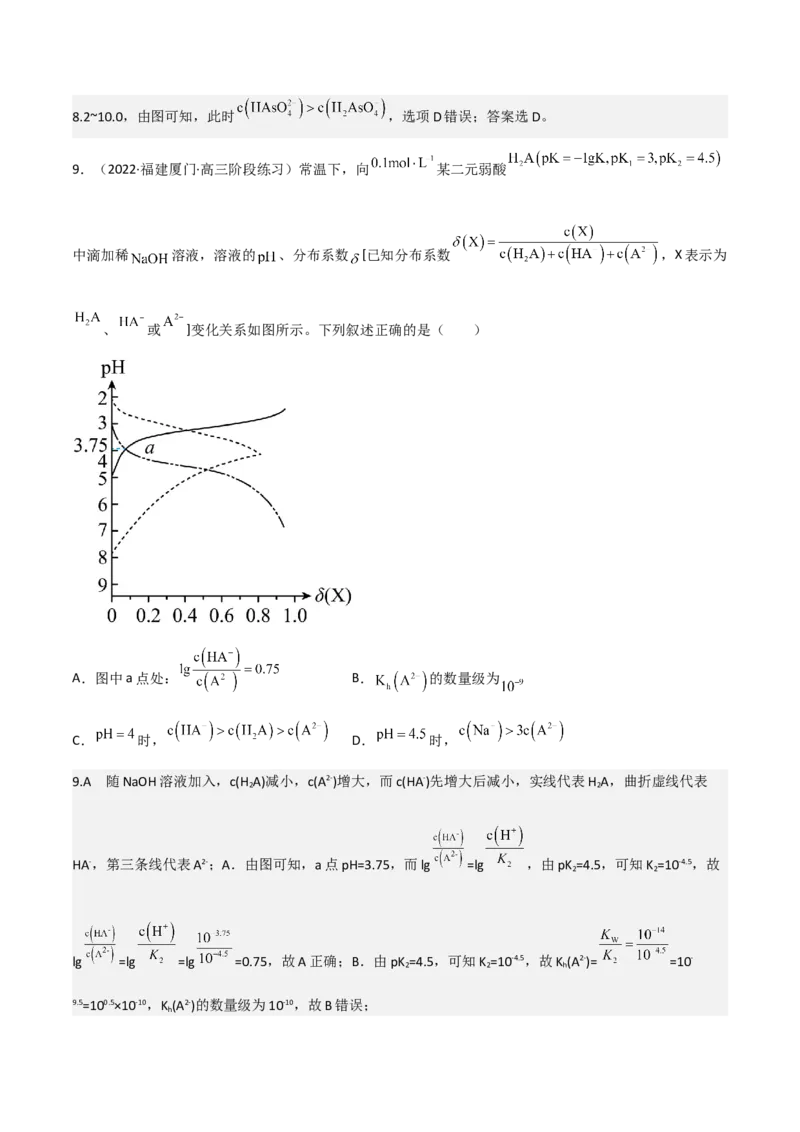
9.(2022·福建厦门·高三阶段练习)常温下,向 某二元弱酸
中滴加稀 溶液,溶液的 、分布系数 [已知分布系数 ,X表示为
、 或 ]变化关系如图所示。下列叙述正确的是( )
A.图中a点处: B. 的数量级为
C. 时, D. 时,
9.A 随NaOH溶液加入,c(H A)减小,c(A2-)增大,而c(HA-)先增大后减小,实线代表H A,曲折虚线代表
2 2
HA-,第三条线代表A2-;A.由图可知,a点pH=3.75,而lg =lg ,由pK =4.5,可知K =10-4.5,故
2 2
lg =lg =lg =0.75,故A正确;B.由pK =4.5,可知K =10-4.5,故K (A2-)= =10-
2 2 h
9.5=100.5×10-10,K (A2-)的数量级为10-10,故B错误;
hC.pH=4时,由图可知,δ(HA-)>δ(A2-)>δ(H A),故c(HA-)>c(A2-)>c(H A),故C错误;
2 2
D.pH=4.5时,c(OH-)<c(H+),由图可知,δ(HA-)=δ(A2-),即c(HA-)=c(A2-),根据电荷守恒有c(Na+)+c(H+)=c(HA-)
+2c(A2-)+c(OH-),则有c(Na+)=3c(A2-)+c(OH-)-c(H+),而c(OH-)-c(H+)<0,故c(Na+)<3c(A2-),故D错误;故选:
A。