文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(江苏专用)
黄金卷04·参考答案
(考试时间:75分钟 试卷满分:100分)
第 I 卷(选择题)
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1 2 3 4 5 6 7 8 9 10 11 12 13
D D C B C A B C D C D D D
第Ⅱ卷(非选择题)
二、非选择题:共4题,共61分。
14.(15分)(1)2Fe2++ClO-+5HO===2Fe(OH) ↓+Cl-+4H+
2 3
(2)在酸性溶液中加入氟化铵,氟离子和氢离子会生成氢氟酸,氢氟酸会和玻璃中的二氧化硅反应,腐
蚀玻璃;
(3)除去溶液中的Zn2+
(4)1.6×10-10
(5)3 温度升高,反应速率加快,镍浸出率增加
(6)4NiCO+2Li CO+O 4LiNiO +6CO
3 2 3 2 2 2
15.(15分)(1)加成反应
(2)3
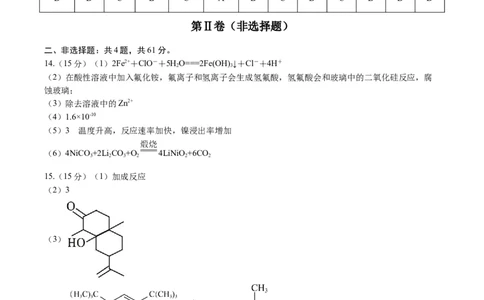
(3)
(4) 或(5)
16.(15分)(1)4Fe(CrO )+ 10Na CO+ 7 O 8NaCrO+ 4NaFeO + 10CO
2 2 2 3 2 2 4 2 2
(2)防止酸性太强,Cr O 氧化性增强,后续步骤中氧化Cl—
2
(3)NaSO
2 4
(4)94.08%
(5)向KCr O 溶液中加入6mol·L-1的KOH溶液,至pH略小于7.2,加热溶液至沸腾,先加入一滴0.5
2 2 7
mol·L-1 Pb(NO ) 溶液搅拌片刻产生少量沉淀,继续滴加至不再产生沉淀【解析】由题给流程可知,铬铁矿
3 2
与碳酸钠、氧气高温条件下反应生成NaCrO、NaFeO ,冷却后,向熔渣中加入水,使NaFeO 水解转化为
2 4 2 2
氢氧化铁沉淀,过滤、洗涤得到NaCrO 溶液;向NaCrO 溶液加入稀硫酸,将NaCrO 转化为NaCr O,
2 4 2 4 2 4 2 2 7
将酸化后的溶液蒸发结晶、过滤、洗涤得到含有硫酸钠的滤渣和NaCr O 溶液;向NaCr O 溶液中加入氯
2 2 7 2 2 7
化钾固体,将蒸发浓缩、冷却结晶、洗涤、过滤、干燥得到KCr O。(1)由分析可知,步骤I中发生的
2 2 7
反应为铬铁矿与碳酸钠、氧气高温条件下反应生成NaCrO、NaFeO 和二氧化碳,反应的化学方程式为。
2 4 2
(2)若步骤III中加入硫酸不宜过多,加入氯化钾固体时,酸性条件下重铬酸根离子会将氯离子氧化,造
成重铬酸钾的产率降低。(3)由分析可知,步骤IV所得滤渣的主要成分是硫酸钠。(4)由得失电子数
目守恒可得如下关系式:KCr O~3I ~6Na SO,滴定消耗20.00mL0.1200mol/L硫代硫酸钠溶液,则2.5g
2 2 7 2 2 2 3
样品中重铬酸钾的纯度为 ×100%=94.08%。 (5)由六价铬与pH
关系图知,在碱性条件下,主要以铬酸根存在,但是氢氧化铅在pH为7.2时开始沉淀,所以溶液pH不能
超过7.2,铬酸根与铅离子在沸腾时会生成铬酸铅沉淀,所以制备铬酸铅沉淀的实验方案为向KCr O 溶液
2 2 7
中加入6mol·L-1的KOH溶液,至pH略小于7.2,加热溶液至沸腾,先加入一滴0.5 mol·L-1 Pb(NO ) 溶液
3 2
搅拌片刻产生少量沉淀,继续滴加至不再产生沉淀。
17.(16分)(1)①
② 段, ,c(H+)基本保特不变
段, ,c(H+)增大
(2)① 大量汽化与催化剂的接触更好,产生更多的 , 浓度越大,与 反应速率越快
② 后, 分解速率加快,高于 催化分解生成 的速率,导致 浓度减小, 的脱除
率下降
(3) 在阴极得电子生成低价态的铁或0价铁,低价态的铁与 反应生成 和
, 在该过程中起催化作用
【解析】(1)①25℃,pH=8.5时, 恰好沉淀完全 ,可以计算出c(OH-)=10-(14-8.5)mol/L=10-5.5 mol/L,则Ksp(Fe(OH) )=10-5×(10-5.5)2=10-16,则当pH为6.0时,c(OH-)=10-(14-6)mol/L=10-8
2
mol/L,溶液中残留 浓度为c(Fe2+)= =1.0mol/L;② 时段,溶液pH几乎不变, 时段,
溶液pH明显降低,原因是 段,发生反应: ,c(H+)基本保特不变,
段,发生反应: ,c(H+)增大。(2)①根据题目已知条件: 在
催化剂 的表面上,分解产生 , 较 和 更易与烟气中的 发生反应生成 ,且
温度升高,过氧化氢汽化,增大了反应接触面积,所以, 时,随着温度升高 的脱除效率显著
提高的原因是: 大量汽化与催化剂的接触更好,产生更多的 , 浓度越大,与 反应速率越
快;②温度过高,过氧化氢分解速率加快,所以,温度高于 的脱除效率降低的原因是:
分解速率加快,高于 催化分解生成 的速率,导致 浓度减小, 的脱除率下降。(3)该电
解装置中,阴阳极均为惰性电极,电解质溶液中有OH-, 在阴极得电子生成低价态的铁或0价
铁,低价态的铁与 反应生成 和 , 在该过程中起催化作用,所以
在阴极参与反应,电解前后 的质量不变(催化剂参与反应,但反应前后质量不变)。