文档内容
2019 年福建省初中毕业及高中阶段各类学校招生考试(化学)试题
第Ⅰ卷
本卷共 10 小题,每小题 3 分,共 30 分。
1. 十一世纪,中国就用“卓筒井”凿井技术获取食盐。食盐的主要成分是( )
A. NaHCO B. NaCO C. NaCl D. NaOH
3 2 3
2. 下列应用只涉及物质的物理性质的是( )
A. 煤用作燃料 B. 干冰用于人工降雨
C. 熟石灰用于改良酸性土壤 D. 生石灰用作干燥剂
3. 《化学通讯》报道:“人造肉汉堡”的研制被称为突破性技术,可以减轻畜牧业生产造成的环境污染。“人
造肉”的营养价值接近真实肉类,它可以为人体补充的最重要的营养素 是 ( )
A. 蛋白质 B. 糖类 C. 维生素 D. 无机盐
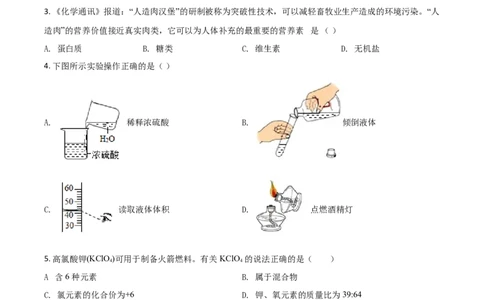
4. 下图所示实验操作正确的是( )
A. 稀释浓硫酸 B. 倾倒液体
C. 读取液体体积 D. 点燃酒精灯
5. 高氯酸钾(KClO)可用于制备火箭燃料。有关 KClO 的说法正确的是( )
4 4
.
A 含 6 种元素 B. 属于混合物
C. 氯元素的化合价为+6 D. 钾、氧元素的质量比为 39:64
6. 化学与生产、生活息息相关,下列说法错误的是( )
A. 油锅着火,可用锅盖盖灭
B. 港珠澳大桥使用的吊绳所含的聚乙烯纤维,属于有机合成材料
C. 洗洁精有乳化作用,可用来清洗油污
D. 为延迟食品的保质期,可用福尔马林(甲醛的水溶液)作防腐剂
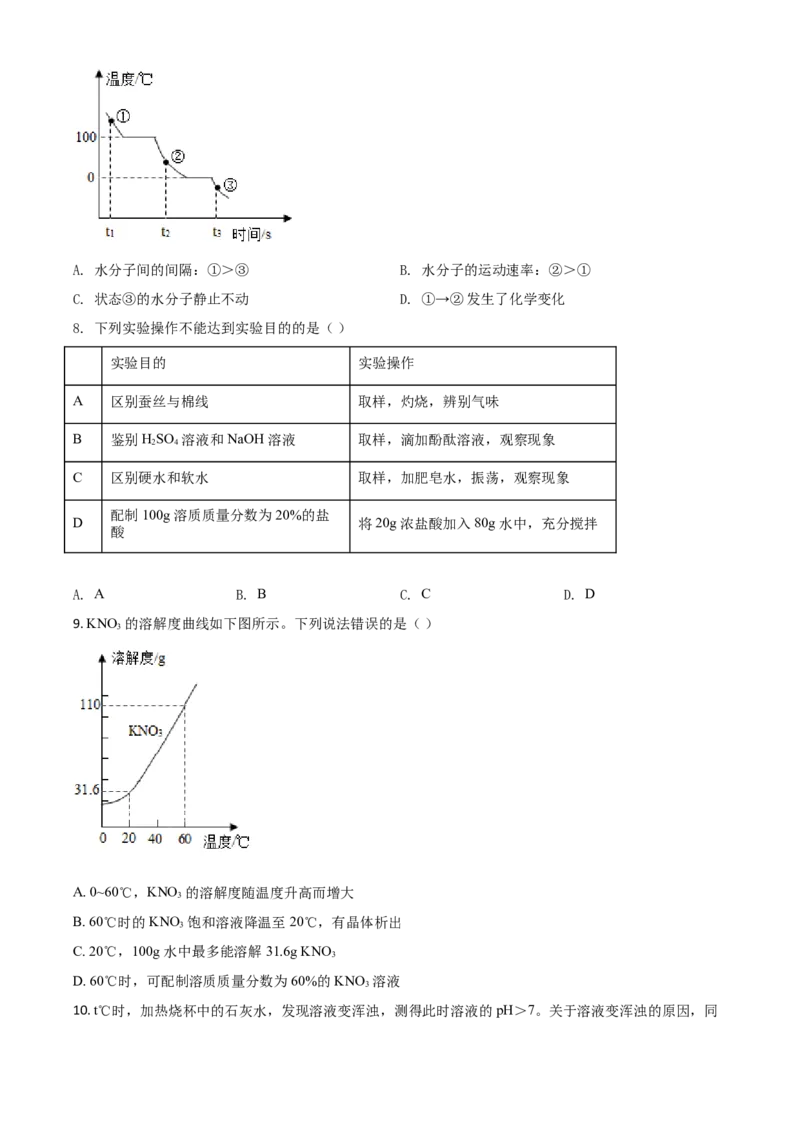
7. 一定条件下,水在密闭容器里的冷却过程中,温度和时间的关系如下图所示。①、②、③表示水在不同
时刻的存在状态,下列有关判断正确的是( )A. 水分子间的间隔:①>③ B. 水分子的运动速率:②>①
C. 状态③的水分子静止不动 D. ①→②发生了化学变化
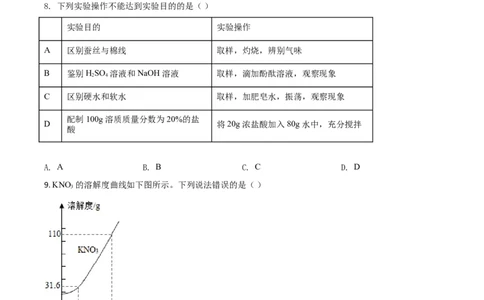
8. 下列实验操作不能达到实验目的的是( )
实验目的 实验操作
A 区别蚕丝与棉线 取样,灼烧,辨别气味
B 鉴别 HSO 溶液和 NaOH 溶液 取样,滴加酚酞溶液,观察现象
2 4
C 区别硬水和软水 取样,加肥皂水,振荡,观察现象
配制 100g 溶质质量分数为 20%的盐
D 将 20g 浓盐酸加入 80g 水中,充分搅拌
酸
A. A B. B C. C D. D
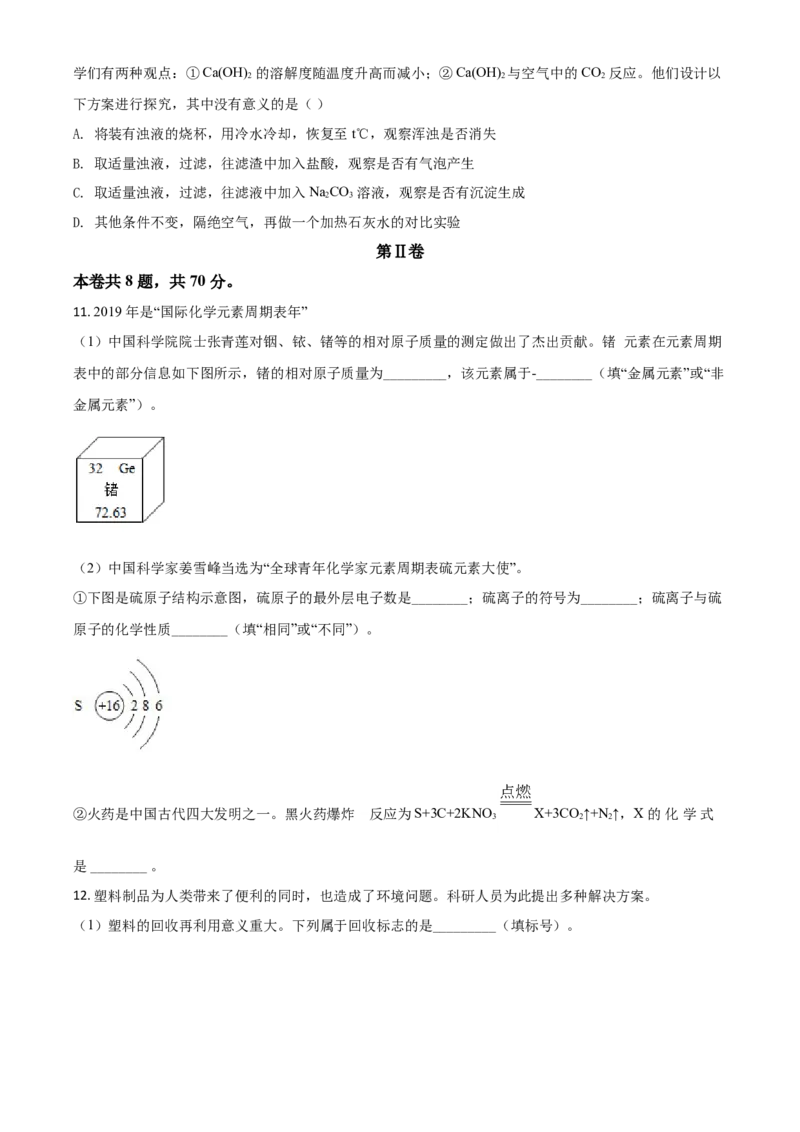
9. KNO 的溶解度曲线如下图所示。下列说法错误的是( )
3
A. 0~60℃,KNO 的溶解度随温度升高而增大
3
B. 60℃时的 KNO 饱和溶液降温至 20℃,有晶体析出
3
C. 20℃,100g 水中最多能溶解 31.6g KNO
3
D. 60℃时,可配制溶质质量分数为 60%的 KNO 溶液
3
10. t℃时,加热烧杯中的石灰水,发现溶液变浑浊,测得此时溶液的 pH>7。关于溶液变浑浊的原因,同学们有两种观点:①Ca(OH) 的溶解度随温度升高而减小;②Ca(OH) 与空气中的 CO 反应。他们设计以
2 2 2
下方案进行探究,其中没有意义的是( )
A. 将装有浊液的烧杯,用冷水冷却,恢复至 t℃,观察浑浊是否消失
B. 取适量浊液,过滤,往滤渣中加入盐酸,观察是否有气泡产生
C. 取适量浊液,过滤,往滤液中加入 NaCO 溶液,观察是否有沉淀生成
2 3
D. 其他条件不变,隔绝空气,再做一个加热石灰水的对比实验
第Ⅱ卷
本卷共 8 题,共 70 分。
11. 2019 年是“国际化学元素周期表年”
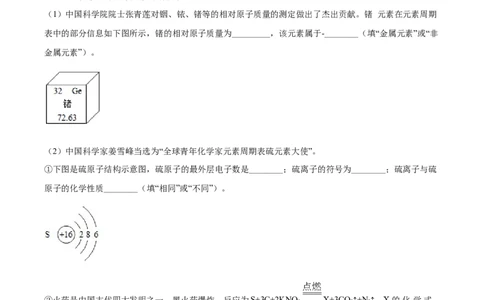
(1)中国科学院院士张青莲对铟、铱、锗等的相对原子质量的测定做出了杰出贡献。锗 元素在元素周期
表中的部分信息如下图所示,锗的相对原子质量为_________,该元素属于-________(填“金属元素”或“非
金属元素”)。
(2)中国科学家姜雪峰当选为“全球青年化学家元素周期表硫元素大使”。
①下图是硫原子结构示意图,硫原子的最外层电子数是________;硫离子的符号为________;硫离子与硫
原子的化学性质________(填“相同”或“不同”)。
②火药是中国古代四大发明之一。黑火药爆炸 反应为S+3C+2KNO X+3CO↑+N ↑,X 的 化 学 式
的3 2 2
是 ________ 。
12. 塑料制品为人类带来了便利的同时,也造成了环境问题。科研人员为此提出多种解决方案。
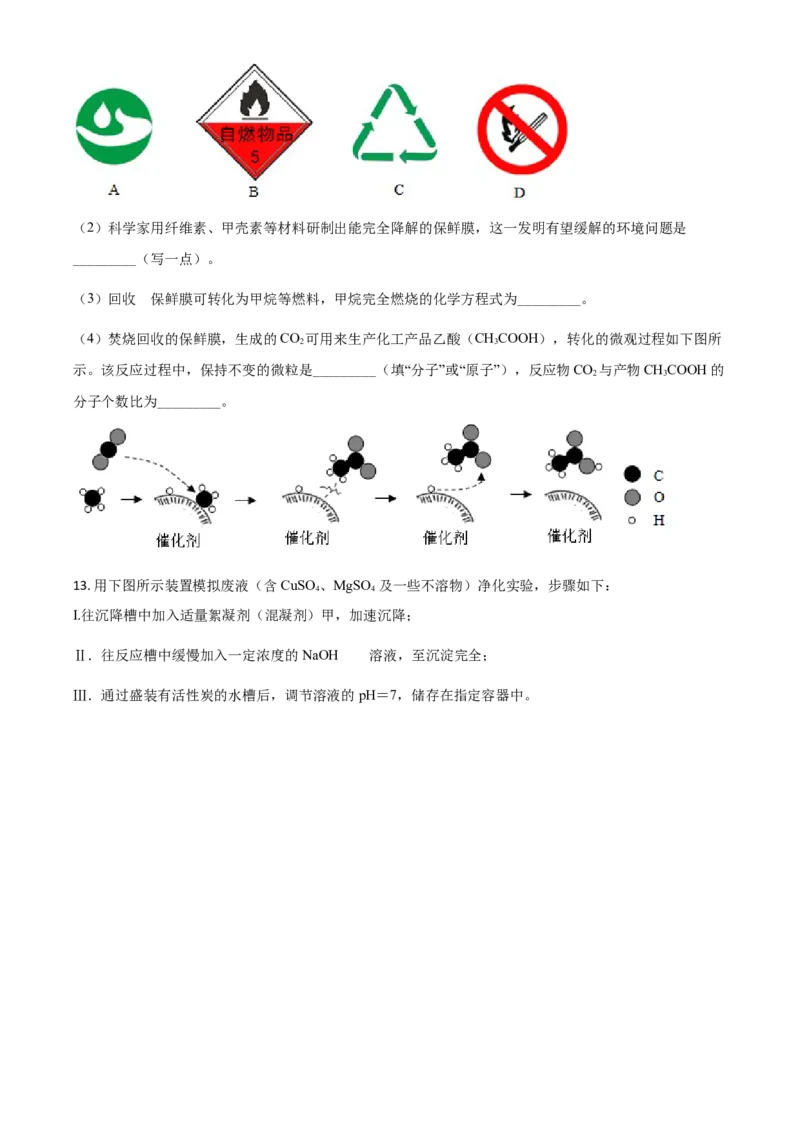
(1)塑料的回收再利用意义重大。下列属于回收标志的是_________(填标号)。(2)科学家用纤维素、甲壳素等材料研制出能完全降解的保鲜膜,这一发明有望缓解的环境问题是
_________(写一点)。
的
(3)回收 保鲜膜可转化为甲烷等燃料,甲烷完全燃烧的化学方程式为_________。
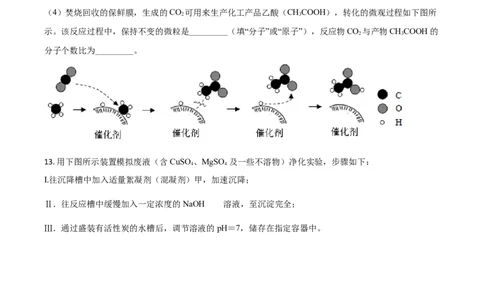
(4)焚烧回收的保鲜膜,生成的CO 可用来生产化工产品乙酸(CHCOOH),转化的微观过程如下图所
2 3
示。该反应过程中,保持不变的微粒是_________(填“分子”或“原子”),反应物CO 与产物CHCOOH的
2 3
分子个数比为_________。
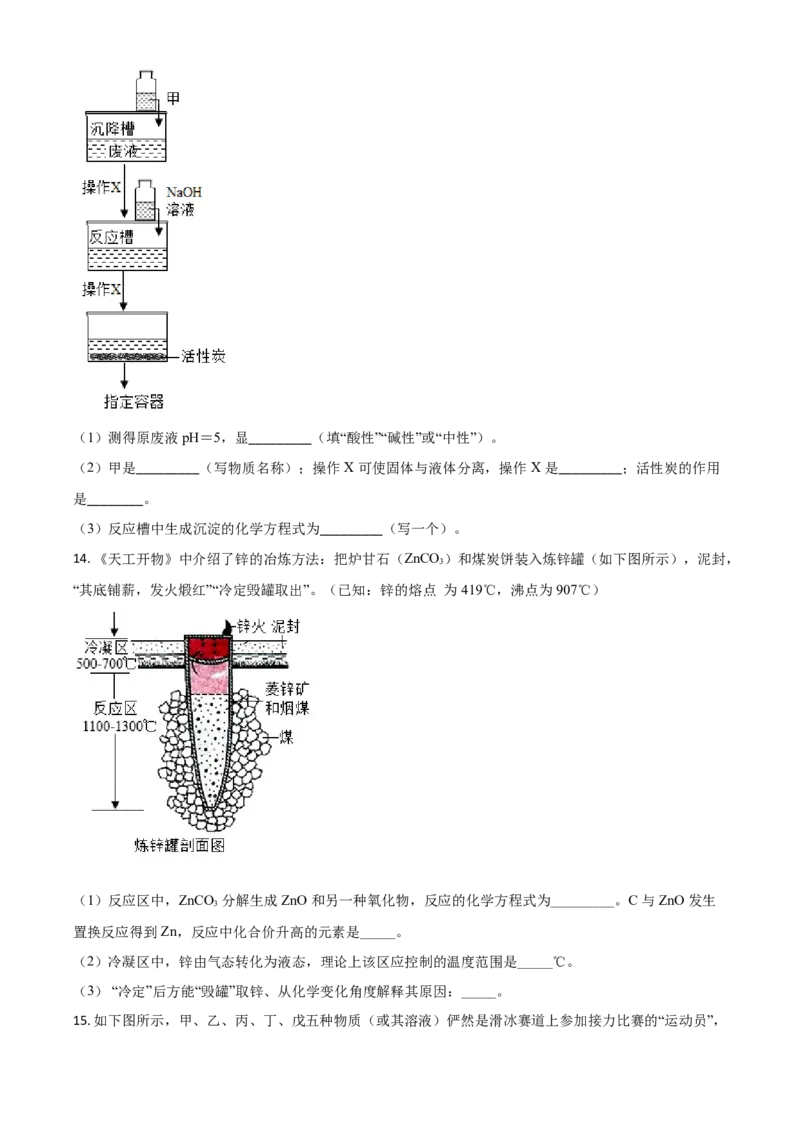
13. 用下图所示装置模拟废液(含 CuSO 、MgSO 及一些不溶物)净化实验,步骤如下:
4 4
I.往沉降槽中加入适量絮凝剂(混凝剂)甲,加速沉降;
Ⅱ.往反应槽中缓慢加入一定浓度的 NaOH 溶液,至沉淀完全;
Ⅲ.通过盛装有活性炭的水槽后,调节溶液的 pH=7,储存在指定容器中。(1)测得原废液 pH=5,显_________(填“酸性”“碱性”或“中性”)。
(2)甲是_________(写物质名称);操作 X 可使固体与液体分离,操作 X 是_________;活性炭的作用
是________。
(3)反应槽中生成沉淀的化学方程式为_________(写一个)。
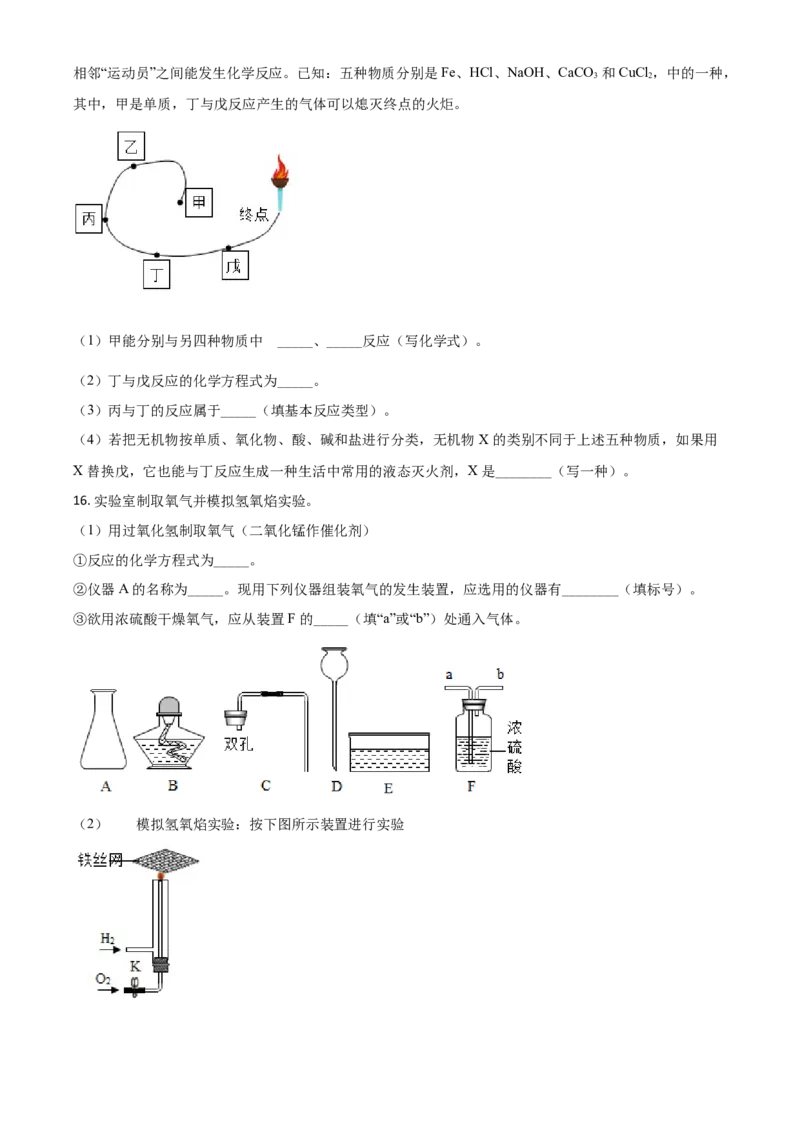
14. 《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO )和煤炭饼装入炼锌罐(如下图所示),泥封,
3
“其底铺薪,发火煅红”“冷定毁罐取出”。(已知:锌的熔点 为 419℃,沸点为 907℃)
(1)反应区中,ZnCO 分解生成 ZnO 和另一种氧化物,反应的化学方程式为_________。C 与 ZnO 发生
3
置换反应得到 Zn,反应中化合价升高的元素是_____。
(2)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是_____℃。
(3) “冷定”后方能“毁罐”取锌、从化学变化角度解释其原因:_____。
15. 如下图所示,甲、乙、丙、丁、戊五种物质(或其溶液)俨然是滑冰赛道上参加接力比赛的“运动员”,相邻“运动员”之间能发生化学反应。已知:五种物质分别是 Fe、HCl、NaOH、CaCO 和 CuCl ,中的一种,
3 2
其中,甲是单质,丁与戊反应产生的气体可以熄灭终点的火炬。
的
(1)甲能分别与另四种物质中 _____、_____反应(写化学式)。
(2)丁与戊反应的化学方程式为_____。
(3)丙与丁的反应属于_____(填基本反应类型)。
(4)若把无机物按单质、氧化物、酸、碱和盐进行分类,无机物 X 的类别不同于上述五种物质,如果用
X 替换戊,它也能与丁反应生成一种生活中常用的液态灭火剂,X 是________(写一种)。
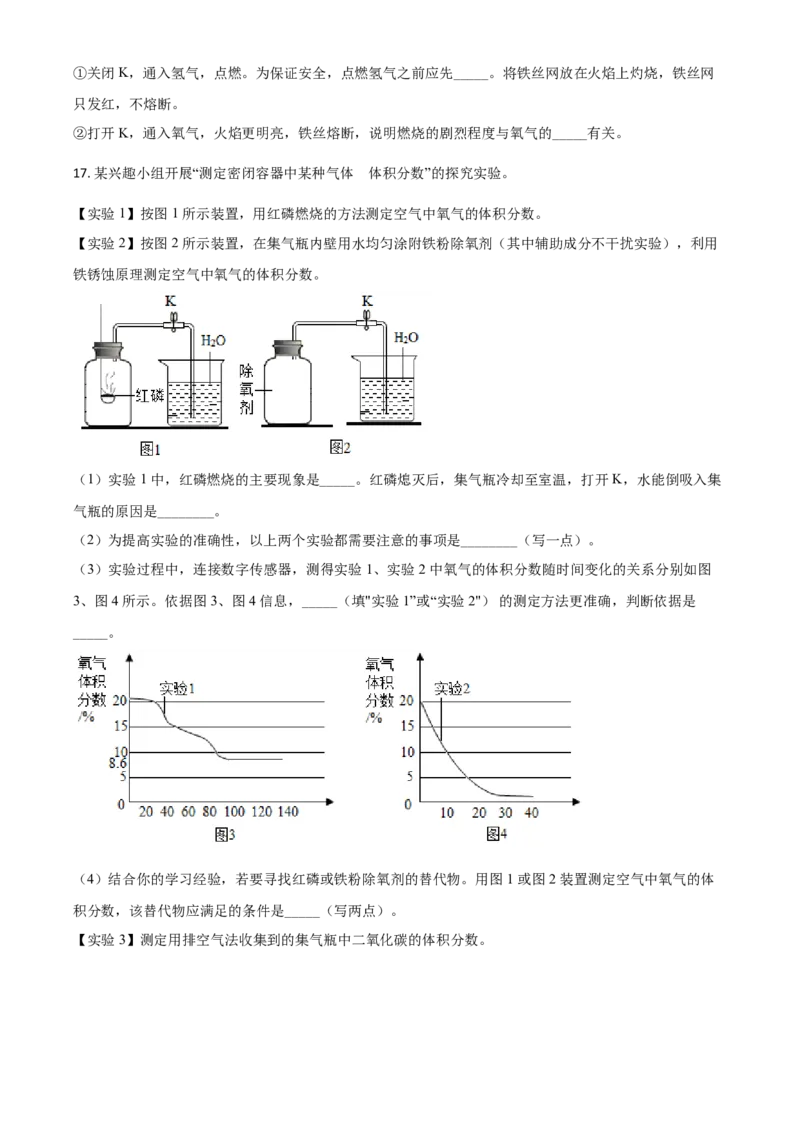
16. 实验室制取氧气并模拟氢氧焰实验。
(1)用过氧化氢制取氧气(二氧化锰作催化剂)
①反应的化学方程式为_____。
②仪器 A 的名称为_____。现用下列仪器组装氧气的发生装置,应选用的仪器有________(填标号)。
③欲用浓硫酸干燥氧气,应从装置 F 的_____(填“a”或“b”)处通入气体。
(2) 模拟氢氧焰实验:按下图所示装置进行实验①关闭 K,通入氢气,点燃。为保证安全,点燃氢气之前应先_____。将铁丝网放在火焰上灼烧,铁丝网
只发红,不熔断。
②打开 K,通入氧气,火焰更明亮,铁丝熔断,说明燃烧的剧烈程度与氧气的_____有关。
的
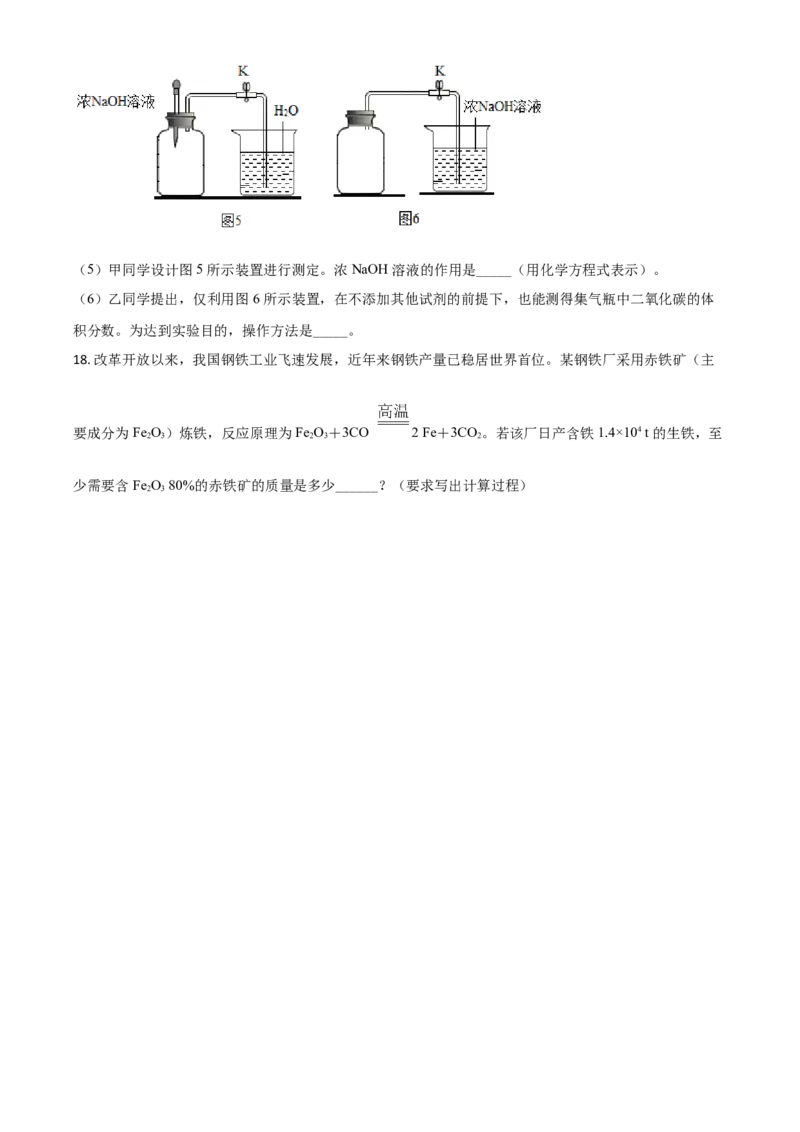
17. 某兴趣小组开展“测定密闭容器中某种气体 体积分数”的探究实验。
【实验 1】按图 1 所示装置,用红磷燃烧的方法测定空气中氧气的体积分数。
【实验 2】按图 2 所示装置,在集气瓶内壁用水均匀涂附铁粉除氧剂(其中辅助成分不干扰实验),利用
铁锈蚀原理测定空气中氧气的体积分数。
(1)实验 1 中,红磷燃烧的主要现象是_____。红磷熄灭后,集气瓶冷却至室温,打开 K,水能倒吸入集
气瓶的原因是________。
(2)为提高实验的准确性,以上两个实验都需要注意的事项是________(写一点)。
(3)实验过程中,连接数字传感器,测得实验 1、实验 2 中氧气的体积分数随时间变化的关系分别如图
3、图 4 所示。依据图 3、图 4 信息,_____(填"实验 1”或“实验 2") 的测定方法更准确,判断依据是
_____。
(4)结合你的学习经验,若要寻找红磷或铁粉除氧剂的替代物。用图 1 或图 2 装置测定空气中氧气的体
积分数,该替代物应满足的条件是_____(写两点)。
【实验 3】测定用排空气法收集到的集气瓶中二氧化碳的体积分数。(5)甲同学设计图 5 所示装置进行测定。浓 NaOH 溶液的作用是_____(用化学方程式表示)。
(6)乙同学提出,仅利用图 6 所示装置,在不添加其他试剂的前提下,也能测得集气瓶中二氧化碳的体
积分数。为达到实验目的,操作方法是_____。
18. 改革开放以来,我国钢铁工业飞速发展,近年来钢铁产量已稳居世界首位。某钢铁厂采用赤铁矿(主
要成分为 Fe O)炼铁,反应原理为 Fe O+3CO 2 Fe+3CO。若该厂日产含铁 1.4×104 t 的生铁,至
2 3 2 3 2
少需要含 Fe O 80%的赤铁矿的质量是多少______?(要求写出计算过程)
2 3