文档内容
专练 22 化学工艺流程题
授课提示:对应学生用书43页
1.[2023·辽宁卷]某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、
Fe3+、Mg2+和Mn2+)。实现镍、钴、镁元素的回收。
已知:
物质 Fe(OH) Co(OH) Ni(OH) Mg(OH)
3 2 2 2
K 10-37.4 10-14.7 10-14.7 10-10.8
sp
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为 (答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸
(HSO ),1 mol H SO 中过氧键的数目为 。
2 5 2 5
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,该反应的离子
2 5 2
方程式为 (HSO 的电离第一步完全,第二步微弱);滤渣的成分为 MnO 、
2 5 2
(填化学式)。
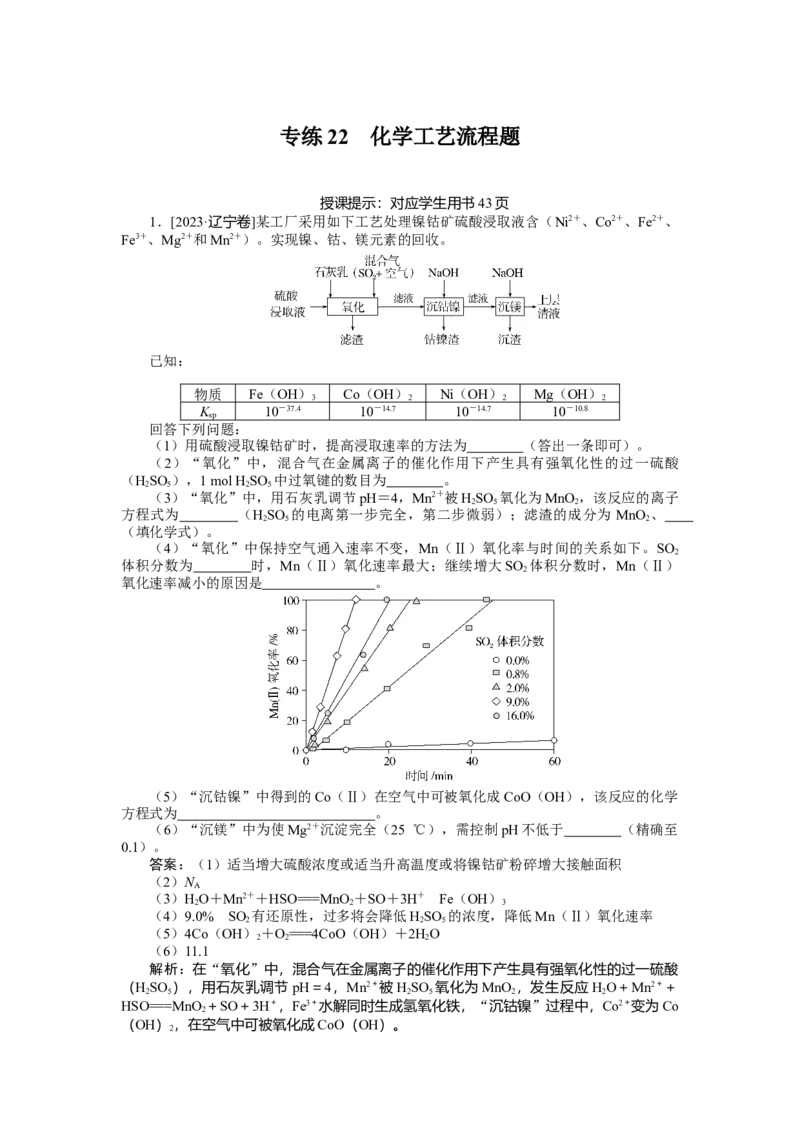
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如下。SO
2
体积分数为 时,Mn(Ⅱ)氧化速率最大;继续增大SO 体积分数时,Mn(Ⅱ)
2
氧化速率减小的原因是 。
(5)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学
方程式为 。
(6)“沉镁”中为使Mg2+沉淀完全(25 ℃),需控制pH不低于 (精确至
0.1)。
答案:(1)适当增大硫酸浓度或适当升高温度或将镍钴矿粉碎增大接触面积
(2)N
A
(3)HO+Mn2++HSO===MnO+SO+3H+ Fe(OH)
2 2 3
(4)9.0% SO 有还原性,过多将会降低HSO 的浓度,降低Mn(Ⅱ)氧化速率
2 2 5
(5)4Co(OH)+O===4CoO(OH)+2HO
2 2 2
(6)11.1
解析:在“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸
(HSO ),用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,发生反应HO+Mn2++
2 5 2 5 2 2
HSO===MnO +SO+3H+,Fe3+水解同时生成氢氧化铁,“沉钴镍”过程中,Co2+变为Co
2
(OH),在空气中可被氧化成CoO(OH)。
2(1)用硫酸浸取镍钴矿时,为提高浸取速率可适当增大硫酸浓度、升高温度或将镍钴
矿粉碎增大接触面积。
(2)(HSO )的结构简式为 ,所以1 mol H SO 中过氧键的数目为
2 5 2 5
N 。
A
(3)用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,该反应的离子方程式为:
2 5 2
HO+Mn2++HSO===MnO +SO+3H+;氢氧化铁的K =10-37.4,当铁离子完全沉淀时,
2 2 sp
溶液中c(Fe3+)=10-5 mol·L-1,K =c3(OH-)×c(Fe3+)=c3(OH-)×10-5=10-
sp
37.4,c(OH-)=10-10.8 mol·L-1,根据K =10-14,pH=3.2,此时溶液的pH=4,则铁离
w
子完全水解,生成氢氧化铁沉淀,故滤渣还有氢氧化铁;
(4)根据图示可知SO 的体积分数为0.9%时,Mn(Ⅱ)氧化速率最大;继续增大
2
SO 体积分数时,由于SO 有还原性,过多将会降低HSO 的浓度,降低Mn(Ⅱ)氧化速
2 2 2 5
率;
(5)“沉钴镍”中得到的Co(OH) ,在空气中可被氧化成CoO(OH),该反应的
2
化学方程式为:4Co(OH)+O===4CoO(OH)+2HO;
2 2 2
(6)氢氧化镁的K =10-10.8, 当镁离子完全沉淀时,c(Mg2+)=10-5 mol·L-1,根据
sp
K 可计算c(OH-)=10-2.9 mol·L-1,根据K =10-14,c(H+)=10-11.1 mol·L-1,所以
sp w
溶液的pH=11.1。
2.[2024·吉林卷]中国是世界上最早利用细菌冶金的国家。已知金属硫化物在“细菌氧
化”时转化为硫酸盐,某工厂用细菌冶金技术处理载金硫化矿粉(其中细小的 Au颗粒被
FeS、FeAsS包裹),以提高金的浸出率并冶炼金,工艺流程如下:
2
回答下列问题:
(1)北宋时期我国就有多处矿场利用细菌氧化形成的天然“胆水”冶炼铜,“胆水”
的主要溶质为 (填化学式)。
(2)“细菌氧化”中,FeS 发生反应的离子方程式为
2
________________________________________________________________________
________________________________________________________________________。
(3)“沉铁砷”时需加碱调节pH,生成 (填化学式)胶体起絮凝作用,
促进了含As微粒的沉降。
(4)“焙烧氧化”也可提高“浸金”效率,相比“焙烧氧化”,“细菌氧化”的优势
为 (填标号)。
A.无需控温
B.可减少有害气体产生
C.设备无需耐高温
D.不产生废液废渣
(5)“真金不怕火炼”表明Au难被O 氧化,“浸金”中NaCN的作用为
2
________________________________________________________________________
________________________________________________________________________。
(6)“沉金”中Zn的作用为
________________________________________________________________________
________________________________________________________________________。
(7)滤液②经HSO 酸化,[Zn(CN)]2-转化为ZnSO 和HCN的化学方程式为
2 4 4 4
________________________________________________________________________
________________________________________________________________________。
用碱中和HCN可生成 (填溶质化学式)溶液,从而实现循环利用。答案:(1)CuSO
4
(2)4FeS+15O+2HO===4Fe3++8SO+4H+
2 2 2
(3)Fe(OH)
3
(4)BC
(5)与Au+结合形成[Au(CN)]-,提高Au的还原性
2
(6)将浸出液中的[Au(CN)]-还原为Au
2
(7)Na[Zn(CN)]+2HSO ===Na SO +ZnSO+4HCN NaCN
2 4 2 4 2 4 4
解析:(1)利用“胆水”冶炼铜为湿法炼铜,利用了铁和硫酸铜溶液的置换反应:Fe
+CuSO ===FeSO +Cu,故“胆水”的主要溶质为CuSO 。(2)金属硫化物在“细菌氧
4 4 4
化”时转化为硫酸盐,则“细菌氧化”中空气中的氧气将FeS 氧化为Fe3+和SO,1 mol
2
FeS 失15 mol电子,1 mol氧气得4 mol电子,根据得失电子守恒、电荷守恒和原子守恒,
2
配平离子方程式为4FeS +15O +2HO===4Fe3++8SO+4H+。(3)“沉铁砷”时加碱调
2 2 2
节pH,Fe3+转化为Fe(OH) 胶体起絮凝作用,促进了含As微粒的沉降。(4)高温时细
3
菌可能会失活,故“细菌氧化”也要控制温度,A错误;“焙烧氧化”时有SO 产生,
2
“细菌氧化”无SO 产生,故B正确;“焙烧氧化”时温度高,设备需耐高温,而“细菌
2
氧化”设备无需耐高温,C正确;由题图知,“细菌氧化”也有废液废渣产生,故D错误。
(5)“浸金”中发生反应:4Au+O+8CN-+2HO===4[Au(CN)]-+4OH-,NaCN作
2 2 2
络合剂与 Au+结合形成[Au(CN) ]-,使 Au 的还原性增强,促进其与 O 反应。
2 2
(6)“沉金”时发生反应:2[Au(CN) ]-+Zn===2Au+[Zn(CN) ]2-,Zn的作用是作
2 4
还原剂,将浸出液中的[Au(CN) ]-还原为Au。(7)滤液②中[Zn(CN) ]2-转化为
2 4
ZnSO 和HCN,发生非氧化还原反应,根据原子守恒配平化学方程式为Na[Zn(CN) ]+
4 2 4
2HSO ===Na SO +ZnSO +4HCN。根据流程中所加物质知,用碱中和HCN生成NaCN,
2 4 2 4 4
从而循环到“浸金”环节被利用。
3.MnSO ·H O是一种重要的饲料添加剂,一种以软锰矿(主要成分是 MnO ,还有
4 2 2
CaO、Al O、Fe O、SiO 等杂质)为原料制备MnSO ·H O的工艺流程如图1所示。
2 3 2 3 2 4 2
已知:①25℃时,K (CaF )=1.5×10-10、K (MnF )=4.5×10-3。
sp 2 sp 2
②该工艺条件下,有关金属离子沉淀的pH范围如表所示。
金属离子 Fe3+ Fe2+ Al3+ Mn2+
开始沉淀的pH 1.9 7.0 3.4 8.1
4.7(>9.8
沉淀完全的pH 3.2 9.0 10.1
时开始溶解)
回答下列问题:
(1)“酸浸”得到的滤渣Ⅰ需要进行二次酸浸,然后将浸出液合并。二次酸浸的目的
为 。
(2)“酸浸”时,MnO 被Fe2+还原,该反应的离子方程式是 。
2
(3)“氧化”时,加热温度不宜过高的原因是 。
(4)“除铁铝”时,应调节溶液pH的范围是 。
(5)“除钙”时,加入MnF 发生反应的离子方程式是
2
在25℃时该反应的平衡常数K= 。
(6)硫酸锰在不同温度下的溶解度S和一定温度内析出晶体的组成如图2所示。“一
系列操作”包括将所得滤液控制温度在80~90℃之间蒸发结晶、 、 、真
空干燥,最后得到MnSO ·H O。
4 2(7)用BaCl 标准溶液测定样品中MnSO ·H O的质量分数时,发现样品纯度大于
2 4 2
100% ( 测 定 过 程 中 产 生 的 误 差 可 以 忽 略 ) , 可 能 的 原 因 是
(写出一种)。
答案:(1)提高Mn元素的浸出率(或Mn元素的利用率)
(2)MnO +2Fe2++4H+===Mn2++2Fe3++2HO
2 2
(3)防止温度过高HO 分解
2 2
(4)4.7≤pH<8.1
(5)MnF
2
+Ca2+ ⇌CaF
2
+Mn2+ 3×107
(6)趁热过滤 用80~90℃的蒸馏水洗涤2~3次
(7)部分晶体失去结晶水(或混有硫酸盐杂质)(合理即可)
解析:
(1)第一次酸浸可能无法完全提取目标物质,故需将滤渣Ⅰ进行二次酸浸,以提高
Mn元素的浸出率或Mn元素的利用率。
(2)MnO 被Fe2+还原为Mn2+,该反应的离子方程式为MnO +2Fe2++4H+===Mn2+
2 2
+2Fe3++2HO。
2
(3)HO 受热易分解,因此“氧化”时,加热温度不宜过高。
2 2
(4)“除铁铝”时,要保证Fe3+和Al3+完全沉淀,Mn2+不能沉淀,故应调节溶液pH
的范围是4.7≤pH<8.1。
(5)“除钙”时,加入MnF 除钙的原理是沉淀的转化,反应的离子方程式为MnF +
2 2
Ca2+ ⇌CaF
2
+Mn2+,在25℃时该反应的平衡常数K=====3×107。
(6)根据题图2中硫酸锰在不同温度下的溶解度曲线可知,要从硫酸锰溶液中得到
MnSO ·H O,应将所得滤液控制温度在80~90℃之间蒸发结晶、趁热过滤、用80~ 90℃
4 2
的蒸馏水洗涤2~3次、真空干燥。
(7)用BaCl 标准溶液测定样品中MnSO ·H O的质量分数时,可能有部分晶体失去
2 4 2
结晶水或样品中混有硫酸盐杂质,导致相同质量的样品中SO含量比理论上更高,故消耗
的BaCl 标准溶液更多,导致最终样品纯度的测定结果大于100%。
2
4.[2022·河北卷]以焙烧黄铁矿FeS (杂质为石英等)产生的红渣为原料制备铵铁蓝
2
FeFe(CN) 颜料。工艺流程如下:
6回答下列问题:
(1)红渣的主要成分为 (填化学式),滤渣①的主要成分为 (填化学
式)。
(2)黄铁矿研细的目的是
________________________________________________________________________
________________________________________________________________________。
(3)还原工序中,不生成S单质的反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(4)工序①的名称为___________________________________,所得母液循环使用。
(5)沉铁工序产生的白色沉淀Fe Fe(CN) 中Fe的化合价为 ,氧化工序发
2 6
生反应的离子方程式为_________________________________________________
________________________________________________________________________。
(6)若用还原工序得到的滤液制备 Fe O·xHO 和(NH ) SO ,所加试剂为
2 3 2 4 2 4
和 (填化学式,不引入杂质)。
答案:(1)Fe O、SiO SiO
2 3 2 2
(2)增大反应物的接触面积,加快反应速率,提高黄铁矿的利用率
(3)7Fe (SO )+FeS+8HO===15FeSO+8HSO
2 4 3 2 2 4 2 4
(4)蒸发浓缩、冷却结晶、过滤洗涤
(5)+2 6Fe(NH ) Fe(CN) +ClO+=====6Fe(NH )Fe(CN) +Cl-+3HO
4 2 6 4 6 2
+6NH ↑
3
(6)O NH ·H O
2 3 2
解析:以熔烧黄铁矿产生的红渣为原料制备铵铁蓝颜料的工艺流程
(1)黄铁矿含 FeS 、石英(主要成分为 SiO ),焙烧时 FeS 发生反应:4FeS +
2 2 2 2
11O=====2Fe O +8SO ,石英不反应,因此红渣的主要成分为Fe O 、SiO 。“酸浸”时
2 2 3 2 2 3 2
Fe O 和硫酸反应生成Fe (SO ) 和水,SiO 与硫酸不反应,因此滤渣①的主要成分为
2 3 2 4 3 2
SiO 。(3)还原工序中,FeS 与Fe (SO ) 溶液反应,若不生成S单质,则FeS 中硫元
2 2 2 4 3 2
素被氧化为SO,Fe (SO ) 被还原为FeSO ,FeS→2SO失14e-、Fe (SO ) →2FeSO
2 4 3 4 2 2 4 3 4
得2e-,根据得失电子守恒,FeS 、Fe (SO ) 的化学计量数分别为1、7,再根据原子守
2 2 4 3
恒配平化学方程式即可。(4)由流程图知,通过工序①获得了FeSO 晶体,则工序①为蒸
4
发浓缩、冷却结晶、过滤,所得母液为硫酸,可以返回“酸浸”循环利用。(5)根据离子
式NH、CN-及化合物中正负化合价代数和为0,可知该物质中Fe的化合价为+2。氧化工序中NaClO 在酸性条件下将Fe(NH ) Fe(CN) 氧化为Fe(NH )Fe(CN) ,NaClO
3 4 2 6 4 6 3
被还原为NaCl,Fe(NH ) Fe(CN) →Fe(NH )Fe(CN) 失e-,ClO→Cl-得6e-,
4 2 6 4 6
根据得失电子守恒,Fe(NH ) Fe(CN) 、ClO的化学计量数分别为6、1,再根据电荷
4 2 6
守恒和原子守恒配平离子方程式即可。(6)“还原”工序得到的滤液为FeSO 和HSO 的
4 2 4
混合溶液,用其制备Fe O·xHO和(NH ) SO 的过程中铁元素被氧化,为了不引入杂质,
2 3 2 4 2 4
结合元素守恒知,所加试剂为O(或HO)和NH ·H O(或NH )。
2 2 2 3 2 3