文档内容
专练 6 离子反应与离子共存
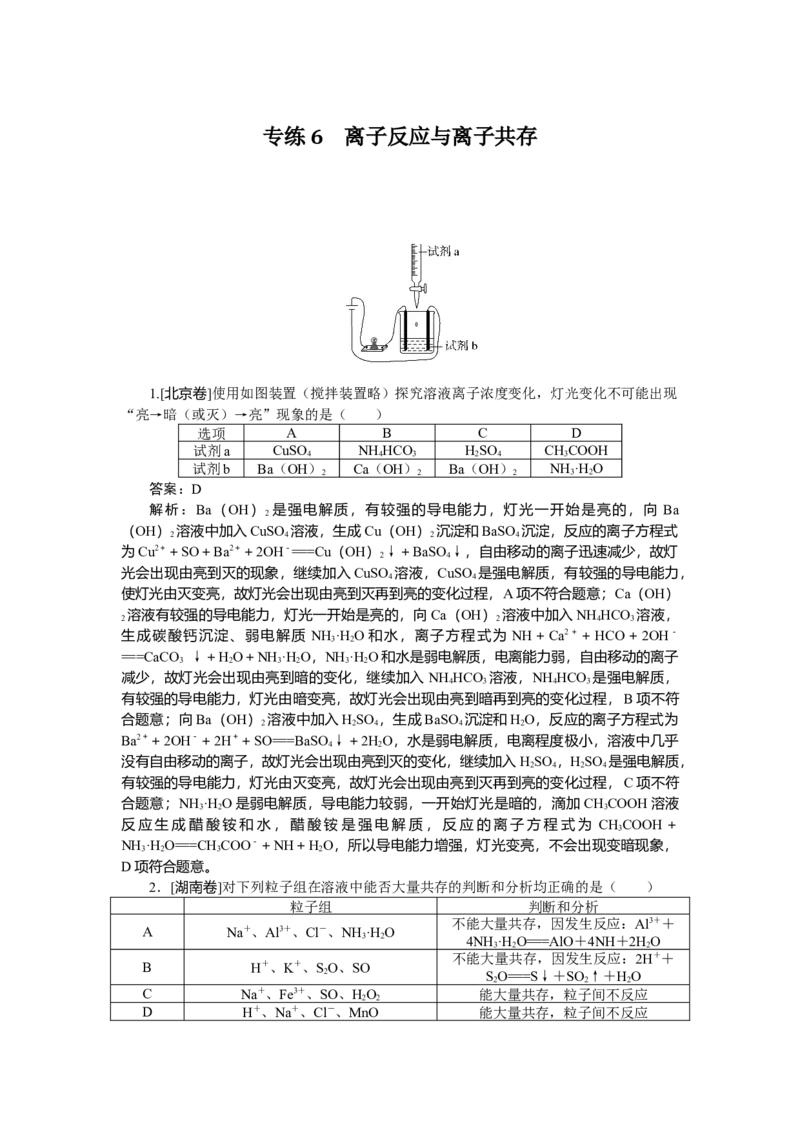
1.[北京卷]使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现
“亮→暗(或灭)→亮”现象的是( )
选项 A B C D
试剂a CuSO NH HCO HSO CHCOOH
4 4 3 2 4 3
试剂b Ba(OH) Ca(OH) Ba(OH) NH ·H O
2 2 2 3 2
答案:D
解析:Ba(OH) 是强电解质,有较强的导电能力,灯光一开始是亮的,向 Ba
2
(OH) 溶液中加入CuSO 溶液,生成Cu(OH) 沉淀和BaSO 沉淀,反应的离子方程式
2 4 2 4
为Cu2++SO+Ba2++2OH-===Cu(OH) ↓+BaSO↓,自由移动的离子迅速减少,故灯
2 4
光会出现由亮到灭的现象,继续加入CuSO 溶液,CuSO 是强电解质,有较强的导电能力,
4 4
使灯光由灭变亮,故灯光会出现由亮到灭再到亮的变化过程,A项不符合题意;Ca(OH)
溶液有较强的导电能力,灯光一开始是亮的,向Ca(OH) 溶液中加入NH HCO 溶液,
2 2 4 3
生成碳酸钙沉淀、弱电解质 NH ·H O 和水,离子方程式为 NH+Ca2++HCO+2OH-
3 2
===CaCO ↓+HO+NH ·H O,NH ·H O和水是弱电解质,电离能力弱,自由移动的离子
3 2 3 2 3 2
减少,故灯光会出现由亮到暗的变化,继续加入 NH HCO 溶液,NH HCO 是强电解质,
4 3 4 3
有较强的导电能力,灯光由暗变亮,故灯光会出现由亮到暗再到亮的变化过程,B项不符
合题意;向Ba(OH) 溶液中加入HSO ,生成BaSO 沉淀和HO,反应的离子方程式为
2 2 4 4 2
Ba2++2OH-+2H++SO===BaSO ↓+2HO,水是弱电解质,电离程度极小,溶液中几乎
4 2
没有自由移动的离子,故灯光会出现由亮到灭的变化,继续加入HSO ,HSO 是强电解质,
2 4 2 4
有较强的导电能力,灯光由灭变亮,故灯光会出现由亮到灭再到亮的变化过程,C项不符
合题意;NH ·H O是弱电解质,导电能力较弱,一开始灯光是暗的,滴加 CHCOOH溶液
3 2 3
反应生成醋酸铵和水,醋酸铵是强电解质,反应的离子方程式为 CHCOOH+
3
NH ·H O===CH COO-+NH+HO,所以导电能力增强,灯光变亮,不会出现变暗现象,
3 2 3 2
D项符合题意。
2.[湖南卷]对下列粒子组在溶液中能否大量共存的判断和分析均正确的是( )
粒子组 判断和分析
不能大量共存,因发生反应:Al3++
A Na+、Al3+、Cl-、NH ·H O
3 2 4NH ·H O===AlO+4NH+2HO
3 2 2
不能大量共存,因发生反应:2H++
B H+、K+、SO、SO
2 SO===S↓+SO ↑+HO
2 2 2
C Na+、Fe3+、SO、HO 能大量共存,粒子间不反应
2 2
D H+、Na+、Cl-、MnO 能大量共存,粒子间不反应答案:B
解析:Al3+与NH ·H O反应产生Al(OH) 沉淀,不产生AlO,A错误;H+与SO不
3 2 3 2
能共存,发生反应的离子方程式为2H++SO===S↓+SO ↑+HO,B正确;Fe3+可催化
2 2 2
HO 分解,不能大量共存,C错误;酸性条件下,MnO可将Cl-氧化为Cl,D错误。
2 2 2
3.[2022·湖北卷]下列各组离子在给定溶液中能大量共存的是( )
A.在0.1 mol·L-1氨水中:Ag+、Cu2+、NO、SO
B.在0.1 mol·L-1氯化钠溶液中:Fe3+、I-、Ba2+、HCO
C.在0.1 mol·L-1醋酸溶液中:SO、NH、Br-、H+
D.在0.1 mol·L-1硝酸银溶液中:K+、Cl-、Na+、CO
答案:C
解析:氨水呈碱性,Ag+、Cu2+不能大量存在,且Ag+、Cu2+均与SO发生反应生成沉
淀,A项错误;在中性溶液中,Fe3+不能大量存在,且Fe3+与I-、HCO均能反应而不能大
量共存,B项错误;AgNO 溶液中不能大量存在CO、Cl-,D项错误。
3
4.下列实验操作、现象与结论均正确的是( )
选项 实验目的 实验操作 现象与结论
取待测液少许,加入过量的Fe 液体分层,向上层清液中
检验Cl-、I-混合溶 (NO ) 溶液,再加CCl 振 加入硝酸酸化的AgNO 溶
A 3 3 4 3
液中的Cl- 荡、静置;取上层清液,向其 液有白色沉淀产生,则溶
中加入硝酸酸化的AgNO 溶液 液中含Cl-
3
取待测液少许,加入盐酸,有
检验某溶液中是否含 澄清石灰水变浑浊,则含
B 气体放出,将气体通入澄清石
有CO CO
灰水中
检验溶液中是否含有 取待测液少许,先通入氯气, 溶液变为血红色,则含
C
Fe2+ 再加KSCN溶液 Fe2+
检验食盐中是否含有 取少量食盐溶于水中,加少量
D 溶液变蓝色则含KIO
KIO 淀粉 3
3
答案:A
解析:检验氯离子用硝酸酸化的硝酸银溶液,但碘离子的存在对氯离子的检验有干扰,
因此用Fe(NO ) 将碘离子氧化为碘单质并用CCl 萃取,此时上层清液中不含碘离子,取
3 3 4
上层清液加硝酸酸化的硝酸银溶液,有白色沉淀产生,则表明溶液中含有氯离子,故A正
确;CO、SO、HCO、HSO均可与盐酸反应,生成能使澄清石灰水变浑浊的气体,故B错
误;检验亚铁离子应先加KSCN溶液,溶液未变血红色,再通入氯气,溶液变为血红色,
证明含有Fe2+,故C错误;能使淀粉变蓝色的碘单质,而不是碘酸钾,故D错误。
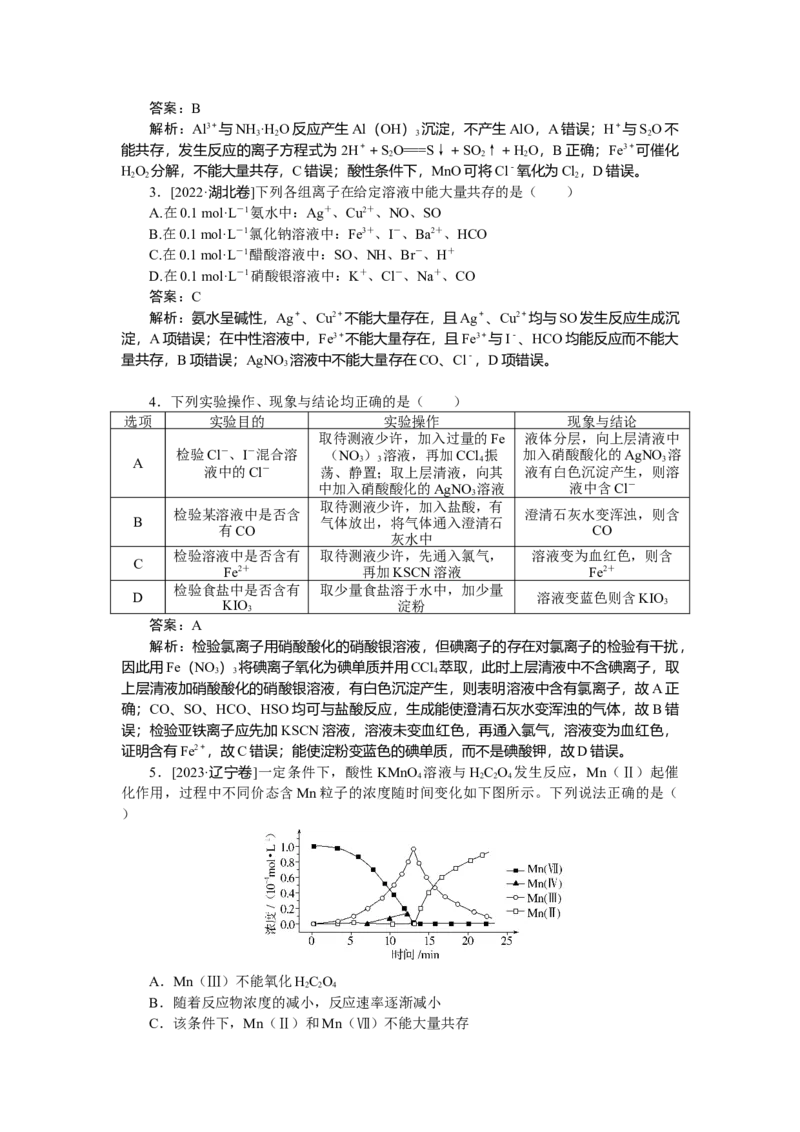
5.[2023·辽宁卷]一定条件下,酸性KMnO 溶液与HC O 发生反应,Mn(Ⅱ)起催
4 2 2 4
化作用,过程中不同价态含Mn粒子的浓度随时间变化如下图所示。下列说法正确的是(
)
A.Mn(Ⅲ)不能氧化HC O
2 2 4
B.随着反应物浓度的减小,反应速率逐渐减小
C.该条件下,Mn(Ⅱ)和Mn(Ⅶ)不能大量共存D.总反应为:2MnO+5C O+16H+===2Mn2++10CO↑+8HO
2 2 2
答案:C
解析:开始一段时间(大约13 min前)随着时间的推移Mn(Ⅶ)浓度减小直至为0,
Mn(Ⅲ)浓度增大直至达到最大值,结合图像,此时间段主要生成Mn(Ⅲ),同时先生
成少量Mn(Ⅳ)后Mn(Ⅳ)被消耗;后来(大约13 min后)随着时间的推移Mn(Ⅲ)
浓度减少,Mn(Ⅱ)的浓度增大;据此作答。
由图像可知,随着时间的推移Mn(Ⅲ)的浓度先增大后减小,说明开始反应生成Mn
(Ⅲ),后Mn(Ⅲ)被消耗生成Mn(Ⅱ),Mn(Ⅲ)能氧化HC O ,A项错误;随着
2 2 4
反应物浓度的减小,到大约13 min时开始生成Mn(Ⅱ),Mn(Ⅱ)对反应起催化作用,
13 min后反应速率会增大,B项错误;由图像可知,Mn(Ⅶ)的浓度为0后才开始生成
Mn(Ⅱ),该条件下Mn(Ⅱ)和Mn(Ⅶ)不能大量共存,C项正确;HC O 为弱酸,在
2 2 4
离子方程式中应以化学式保留,总反应为 2MnO+5HC O +6H+===2Mn2++10CO↑+
2 2 4 2
8HO,D项错误;答案选C。
2
6.[2024·哈尔滨师大附中高三月考]常温下,下列各组离子在指定溶液中能大量共存的
是( )
A.无色透明的溶液中:Fe3+、Mg2+、SCN-、Cl-
B.=1×10-12的溶液中:K+、Na+、CO、NO
C.c(Fe2+)=1 mol·L-1的溶液中:K+、NH、MnO、SO
D.能使甲基橙变红的溶液中:Na+、NH、SO、HCO
答案:B
解析:Fe3+和SCN-会发生反应生成血红色的配合物,A错误;根据K 可以求出c
w
(OH-)=0.1 mol·L-1,溶液显碱性,这4种离子可以大量共存,B正确;Fe2+还原性较强,
MnO氧化性较强,两者因发生氧化还原反应而不能大量共存,C错误;使甲基橙变红的溶
液显酸性,HCO不能在酸性溶液中大量共存,D错误。
7.下列有关NaClO和NaCl混合溶液(已知该混合溶液呈碱性)的叙述正确的是(
)
A.该溶液中, H+、NH、SO、Br-可以大量共存
B.该溶液中, Ag+、K+、NO可以大量共存
C.向该溶液中滴入少量FeSO 溶液,反应的离子方程式为:2Fe2++ClO-+2H+===Cl
4
-+2Fe3++HO
2
D.向该溶液中加入浓盐酸,每产生1 mol Cl ,转移电子约为6.02×1023个
2
答案:D
解析:H+与ClO-不能大量共存,且在酸性条件下, Br-可被ClO-氧化,A项错误;
Ag+与Cl-不能大量共存,B项错误; NaClO和NaCl的混合溶液呈碱性,反应物中不应出
现H+,C项错误;该反应是ClO-与Cl-在酸性条件下发生的归中反应,D项正确。
8.制备(NH ) Fe(SO ) ·6H O的实验中,需对过滤出产品的母液(pH<1)进行
4 2 4 2 2
处理。常温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的离子组合
正确的是( )
A.通入过量Cl:Fe3+、H+、NH、Cl-、SO
2
B.加入过量NaClO溶液:NH、Fe2+、H+、SO、ClO-
C.加入过量NaClO溶液:Na+、SO、Cl-、ClO-、H+
D.加入过量NaOH溶液:Na+、Fe2+、NH、SO、OH-
答案:A
解析:根据信息可知,母液中主要存在的离子有NH、Fe2+、H+、SO。通入过量Cl,
2Cl 具有较强的氧化性,能将Fe2+氧化成Fe3+,同时得到Cl-,反应后溶液中的离子可共存
2
故A正确;加入过量NaClO溶液,ClO-在酸性条件下,能将Fe2+氧化成Fe3+,同时生成
Cl-,所以反应后的溶液中不存在Fe2+,故B错误;加入过量NaClO溶液,过量的ClO-部
分水解生成次氯酸和OH-,OH-消耗NH和H+,结合B项中的分析,反应后的溶液中存
在Na+、SO、Cl-、ClO-、OH-,故C错误;加入过量NaOH溶液,Fe2+与OH-反应生成
氢氧化亚铁沉淀,NH与OH-反应生成一水合氨,则Fe2+、NH不存在,故D错误。
9.下列离子或分子组中,在相应的环境中一定能大量共存的是( )
选项 环境要求 离子或分子
A Al (SO ) 溶液中 K+、AlO、Cl-、NO
2 4 3
B 滴加石蕊溶液显蓝色的溶液中 Na+、K+、SO、S2-
C 水电离产生的c(OH-)=10-12 mol·L-1的溶液 ClO-、CO、NH、K+
D 氯气中 O、NH 、CO、HCl
2 3 2
答案:B
解析:Al (SO ) 溶液中,AlO与Al3+发生相互促进水解反应,在溶液中不能大量共
2 4 3
存,故A错误;S2-、SO在碱性溶液中不发生氧化还原反应,在溶液中能大量共存,故 B
正确;水电离产生的c(OH-)=10-12 mol·L-1的溶液中存在大量H+或OH-,CO、ClO-
均与H+反应,NH与OH-反应,在溶液中不能大量共存,故C错误;NH 与HCl相遇立即
3
生成NH Cl,且在常温下NH 也能被Cl 氧化为N,故D错误。
4 3 2 2
10.某强碱性溶液中,只含有K+、NH、Al3+、AlO、CO、SiO、Cl-中的某几种离子,
现进行如下实验:①取少量溶液用硝酸酸化后,该溶液无沉淀生成;②另取一定量原溶液
逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,而后产生一种气体,最
后沉淀逐渐减少至全部溶解。③另取一定量的原溶液,加入5 mL 0.2 mol·L-1盐酸,沉淀会
完全消失,再继续加入足量的硝酸银溶液可得到沉淀 0.287 g。下列说法一定正确的是(
)
A.原溶液中含有Al3+、CO、Cl-
B.无法确定原溶液中是否含有Cl-和K+
C.原溶液中含有Al3+、CO、Cl-
D.原溶液中一定不含Al3+、NH
答案:D
解析:通过信息①判断出溶液中不含SiO,通过信息②判断出溶液中含有AlO、CO,
则溶液中一定不含 Al3+,通过信息③判断出:盐酸提供的 n(Cl-)=0.001 mol,n
(AgCl)=mol=0.002 mol,所以原溶液中含有Cl-,D正确。
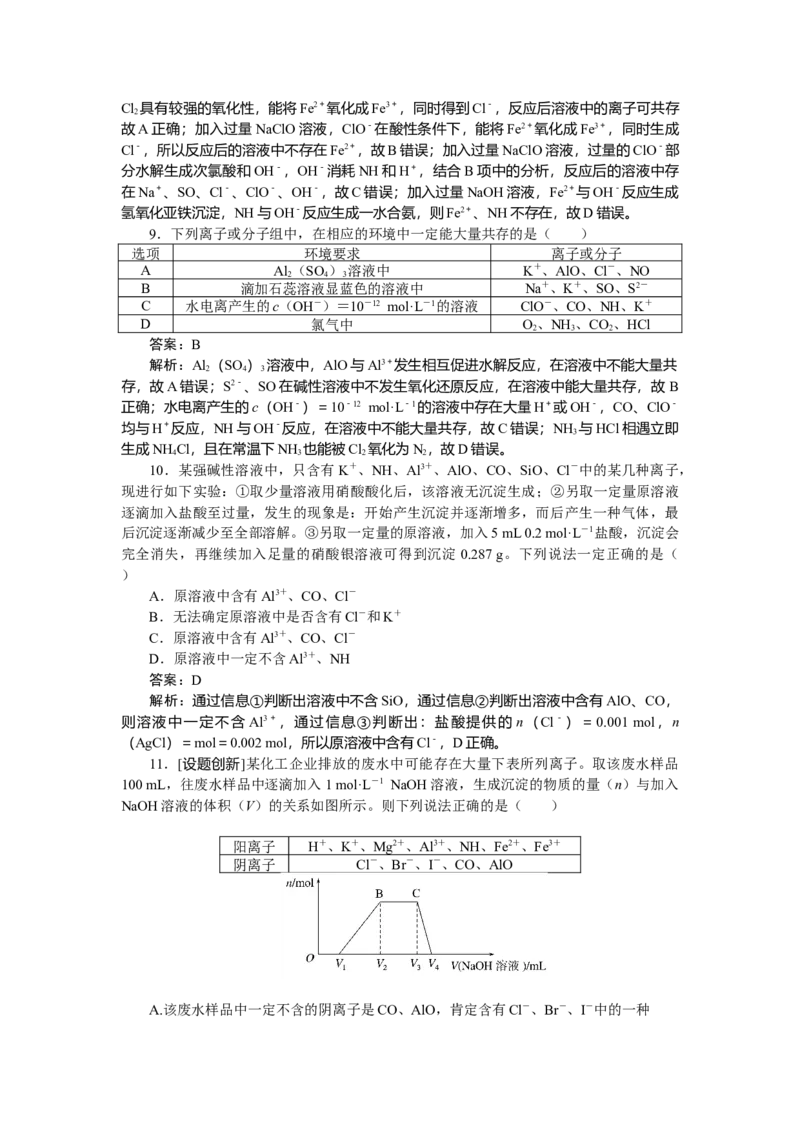
11.[设题创新]某化工企业排放的废水中可能存在大量下表所列离子。取该废水样品
100 mL,往废水样品中逐滴加入1 mol·L-1 NaOH溶液,生成沉淀的物质的量(n)与加入
NaOH溶液的体积(V)的关系如图所示。则下列说法正确的是( )
阳离子 H+、K+、Mg2+、Al3+、NH、Fe2+、Fe3+
阴离子 Cl-、Br-、I-、CO、AlO
A.该废水样品中一定不含的阴离子是CO、AlO,肯定含有Cl-、Br-、I-中的一种B.该废水样品中一定含有的阳离子是Al3+、H+、NH、Mg2+、Fe2+、Fe3+,可能含有
K+
C.该废水样品中n(H+)∶n(NH)∶n(Al3+)=V∶(V-V)∶(V-V)
1 3 2 2 1
D.若V =10、V =40、V =70,则废水样品中n(H+)∶n(NH)∶n(Al3+)=
1 2 4
1∶3∶1
答案:A
解析:向废水样品中不断加入NaOH溶液的过程中,开始时无沉淀产生,然后沉淀逐
渐增多,BC段沉淀量不变,最后沉淀全部溶解,说明溶液中存在H+、NH、Al3+,肯定不
存在CO、AlO、Fe2+、Fe3+、Mg2+,根据溶液呈电中性原则知,废水中至少含有Cl-、Br
-、I-中的一种。根据图中沉淀变化曲线知,n(H+)∶n(NH)∶n(Al3+)=V∶(V -
1 3
V)∶,若V=10,V=40,V=70,则有n(H+)∶n(NH)∶n(Al3+)=1∶2∶1。
2 1 2 4
12.[2024·湖北恩施月考]某溶液中可能存在Na+、Al3+、Fe2+、NH、NO、CO、SO中
的若干种离子,且各离子的物质的量相同。取该溶液进行如下实验:
下列判断正确的是( )
A.A是CO,B是NH
2 3
B.白色沉淀一定是Al(OH)
3
C.溶液中一定存在Al3+、Fe2+、NO、NH
D.溶液中一定不存在Na+
答案:D
解析:向溶液中加入过量稀盐酸生成气体A,溶液中可能存在CO或同时存在Fe2+和
NO,二者发生氧化还原反应生成NO,溶液Ⅰ中加入过量氢氧化钡生成气体B,应为氨气,
则原溶液中存在NH,有白色沉淀产生,应为氢氧化铁,则原溶液中含有Fe2+、NO,不存
在CO,气体A应是NO;存在的各离子具有相同的物质的量,根据溶液呈电中性可知,溶
液中还存在SO,不含Na+、Al3+;由以上分析可知,A为NO,A错误;溶液Ⅱ呈碱性,
生成的白色沉淀应为碳酸钡,B错误;溶液中不存在Al3+,C错误;溶液中不含Na+、Al3
+,D正确。