文档内容
《化学》三色速记手册
1.物态:
在常温下,C~C 的烷烃是气体,C~C 为液体C 以上为固体。直链烷烃随分子量增大而发
1 4 5 17 18
生物态变化。
2.(1)分子结构相似(同系列中的同系物)随分子量的增大(或C原子增多);分子间作
用力增大,熔沸点增高。
(2)分子式相同的烃,支链越多,熔沸点越低(如戊烷的3种同分异构体的沸点:正戊烷>
异戊烷>新戊烷)C原子5个以上的烷烃唯独新戊烷为气态
(五)烷烃的化学性质
1.取代反应
烷烃能与卤素在高温或光照条件下发生取代反应。
2.氧化反应(加氧去氢)
氧化:在有机分子中加入氧或去氢。
还原:在有机分子中加入氢或去掉氧。
①完全氧化:
CH+2O→CO+HO
4 2 2 2
应用:烷烃因为燃烧相对缓和,而常被用作燃料。
②不完全氧化
3.热裂反应
热裂反应:在高温及没有氧气的条件下发生键断裂的反应。
烷烃在800-1100°C的热裂产物主要是乙烯,其次为丙烯,丁烯,丁二烯和氢。
热裂反应相当复杂,热裂的同时,还有转变为较大分子的反应。
(六)甲烷
1.存在形式
甲烷是天然气、沼气、油田气和煤矿坑道气的主要成分。海底存在的“可燃冰”主要是天然
气水合物(CH4·nH2O)
2.甲烷的用途
是一种重要的燃料和化工原料(是合成氨和合成甲醇、汽油等工业的原料),甲烷分解生成
的炭黑是橡胶工业的原料。
3.甲烷的物理性质
是一种没有颜色、没有气味的气体,密度是0.717g/L(标准状况),极难溶于水。
4.甲烷的分子结构
二、不饱和烃
分子中含有碳碳双键或碳碳三键的开链烃,称为不饱和开链烃。不饱和开链烃分为烯烃和炔
烃。
第 38 页《化学》三色速记手册
(一)烯烃
1.烯烃定义
分子中含有碳碳双键的链烃称为烯烃,简称烯
通式:CH
n 2n
官能团:碳碳双键(C=C)
2.烯烃的理化性质
(1)物理性质
①沸点:直链α-烯烃的沸点随着分子中碳原子数的增多而升高。
②相对密度:都小于1,随着分子中碳原子数的增多,直链α-烯烃的相对密度逐渐增大。
③不溶于水,能溶解于非极性和弱极性的有机溶剂(相似相溶原理)
(3)化学性质
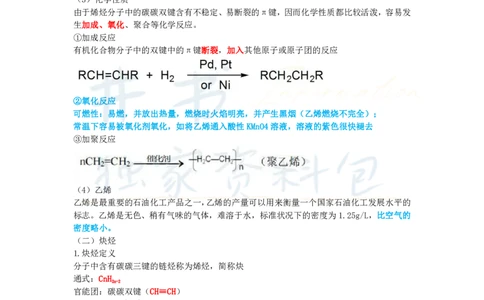
由于烯烃分子中的碳碳双键含有不稳定、易断裂的π键,因而化学性质都比较活泼,容易发
生加成、氧化、聚合等化学反应。
①加成反应
有机化合物分子中的双键中的π键断裂,加入其他原子或原子团的反应
②氧化反应
可燃性:易燃,并放出热量,燃烧时火焰明亮,并产生黑烟(乙烯燃烧不完全);
常温下容易被氧化剂氧化,如将乙烯通入酸性KMnO4溶液,溶液的紫色很快褪去
③加聚反应
(4)乙烯
乙烯是最重要的石油化工产品之一,乙烯的产量可以用来衡量一个国家石油化工发展水平的
标志。乙烯是无色、稍有气味的气体,难溶于水,标准状况下的密度为1.25g/L,比空气的
密度略小。
(二)炔烃
1.炔烃定义
分子中含有碳碳三键的链烃称为烯烃,简称炔
通式:CnH
2n-2
官能团:碳碳双键(CH≡CH)
2.炔烃的物理性质
3.化学性质
由于炔烃分子中的碳碳三键含有不稳定、易断裂的π键,因而化学性质活泼,容易发生加成、
氧化、聚合等化学反应
(1)加成反应
(2)氧化反应
①点燃
燃烧时火焰明亮且带有浓烈的黑烟,燃烧时放出大量的热,产生温度很高的氧炔焰,可用来
切割金属。
②不饱和烃分子的双键或三键中,由于含有不稳定的π键,很容易被氧化。
第 39 页《化学》三色速记手册
例如:把乙炔通入高锰酸钾溶液中,溶液的紫色就会很快褪去,因此可以用炔烃的定性鉴定。
三、芳香烃
(一)定义
芳香烃,也称为芳烃,一般是指分子中含苯环结构的碳氢化合物
(二)苯的同系物
苯的同系物:只含有一个苯环且苯环侧链上所连接的取代基为饱和烷烃基。其通式为CnH
2n-6
(n≥6)。
(三)苯的物理性质
苯是无色带有特殊气味的液体,有毒,不溶于水,密度比水小,熔点5.5℃,沸点80.1℃。
当温度低于5.5℃时,苯就会凝结成无色晶体。
(四)苯的化学性质
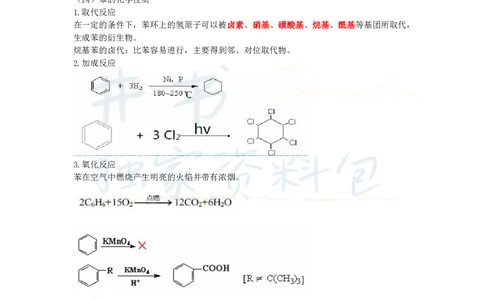
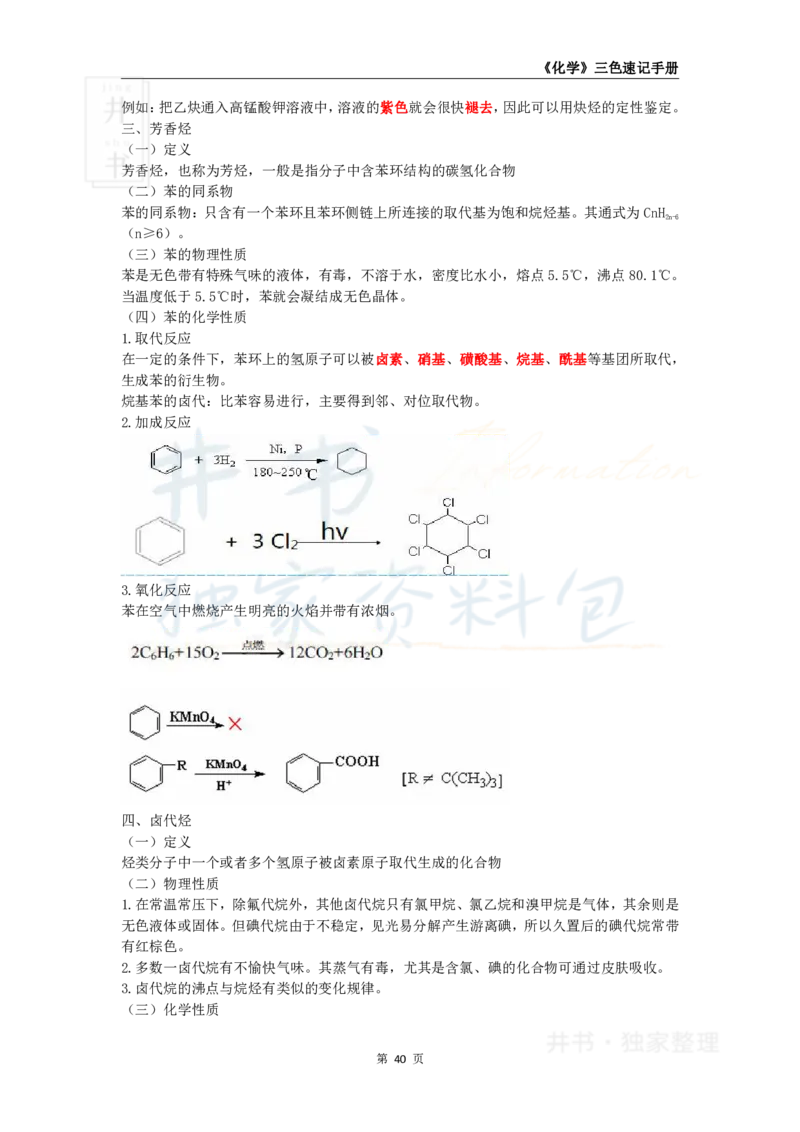
1.取代反应
在一定的条件下,苯环上的氢原子可以被卤素、硝基、磺酸基、烷基、酰基等基团所取代,
生成苯的衍生物。
烷基苯的卤代:比苯容易进行,主要得到邻、对位取代物。
2.加成反应
3.氧化反应
苯在空气中燃烧产生明亮的火焰并带有浓烟。
四、卤代烃
(一)定义
烃类分子中一个或者多个氢原子被卤素原子取代生成的化合物
(二)物理性质
1.在常温常压下,除氟代烷外,其他卤代烷只有氯甲烷、氯乙烷和溴甲烷是气体,其余则是
无色液体或固体。但碘代烷由于不稳定,见光易分解产生游离碘,所以久置后的碘代烷常带
有红棕色。
2.多数一卤代烷有不愉快气味。其蒸气有毒,尤其是含氯、碘的化合物可通过皮肤吸收。
3.卤代烷的沸点与烷烃有类似的变化规律。
(三)化学性质
第 40 页《化学》三色速记手册
1.取代反应
水解反应
卤代烷和NaOH或KOH的水溶液共热,生成相应的醇。
卤素被-OH取代
2.消除反应
从分子中脱去一个简单分子生成不饱和键的反应称为消除反应
扎依采夫规则:仲卤代烷和叔卤代烷脱HX时,主要从含氢较少的β-碳原子脱去氢原子,这
一经验称为扎依采夫规则。
伯卤代烷与强碱的稀水溶液共热时主要发生取代反应,
与强碱的醇溶液共热时发生消除反应。
【考点五】、醇、酚、醚
(一)醇
1.定义
脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基取代后的化合物称为醇,羟基是醇的
官能团。
2.物理性质
形态:低级的一元饱和醇为无色中性液体,具有特殊的气味和辛辣味道。水与醇均具有羟
基,彼此可以形成氢键,甲醇、乙醇和丙醇可与水以任何比例相溶;4-11个碳的醇为油状
液体,仅可部分地溶于水;高级醇为无臭、无味的固体,不溶于水。
密度:随着相对分子质量的增大烷基对整个分子的影响越来越大,从而使高级醇的物理性
质与烷烃近似。一元饱和醇的密度虽比相应的烷烃密度大,但仍比水轻;
沸点:醇的沸点随相对分子质量的增大而升高,在同系列中,少于10个碳原子的相邻两个
醇的沸点差为18~20℃,高于10个碳原子者,沸点差较小。支链醇的沸点总比相同碳原子
数的直链醇的沸点低。
(三)化学性质
1.与活泼金属的反应
钠与水反应剧烈,单位时间内放出的热量大,使钠粒熔化,说明钠的熔点低。反应生成氢气,
说明水分子中的氢原子相对较活泼。
钠与乙醇反应缓慢,生成氢气,说明乙醇分子里羟基中的氢原子相对不活泼;
2.氧化反应
(1)燃烧
第 41 页《化学》三色速记手册
(2)催化氧化
乙醇在加热和有催化剂(Cu或Ag)存在的条件下,被空气中氧气氧化成乙醛。
3.酯化反应
醇与有机酸或无机酸反应,生成酯称为酯化反应。
4.脱水反应
(二)酚
1.定义
羟基直接连在苯环上的化合物称作酚
通式:ArOH
2.苯酚的物理性质
纯净的苯酚是无色晶体(露置在空气里会因小部分被氧化而呈粉红色)。苯酚具有特殊的气
味,熔点43℃,在水中的溶解度不大,当温度高于65℃时,则能与水混溶。苯酚易溶于乙
醇等有机溶剂。苯酚有毒,其稀溶液可直接用作防腐剂和消毒剂。其浓溶液对皮肤有强烈的
腐蚀性,若不慎沾上,应立即用酒精清洗。
3.苯酚的化学性质
(1)酸性
苯酚具有酸性,俗称石炭酸,酚的酸性比醇强,但比碳酸弱。
(2)取代反应
苯酚与浓溴水反应,生成2,4,6-三溴苯酚白色沉淀:
此反应十分灵敏,常用于苯酚的定性检验和定性测定。
(3)显色反应
酚能与三氯化铁发生显色反应,不同酚产生不同的颜色,酚类物质的特征反应
苯酚跟FeCl 溶液作用显紫色,利用这一反应可以检验苯酚的存在。
3
(4)氧化反应
酚类物质很容易被氧化
(三)醚
1.定义
醚可以看作是水分子中的2个氢被烃基取代的化合物,也可以看作醇或酚中羟基上氢的被烃
基取代的产物,
通式:R一0-R或R一O-Ar,
官能团:-O-
2.物理性质
第 42 页《化学》三色速记手册
(1)多数醚是易挥发、易燃的液体。
(2)与醇不同,醚分子间不能形成氢键,所以醚的沸点比相对分子质量相近的醇低得多,
醚分子中的氧可与水形成氢键,所以醚在水中的溶解比烷烃大
(3)醚常用作有机溶剂
【考点二】醛酮
(一)定义
碳原子与氧原子用双键相连的基团称为羰基。羰基碳与氢和烃基相连的化合物称为醛。羰基
碳与两个烃基相连的化合物称为酮
(二)物理性质
沸点:由于羰基的偶极矩增加了分子间的作用力,因此醛、酮的沸点比相应相对分子质量
的烷烃高,但比醇低。
溶解性:酮的氧原子可以与水形成氢键,因此低级醛、酮可以与水混溶,随着相对分子质量
的增加,在水中溶解度或微溶或不溶
密度:脂肪族醛、酮相对密度小于1,芳香族醛、酮大于1。
(三)化学性质
1.加成反应
(1)与氢氰酸的加成(增长碳链)
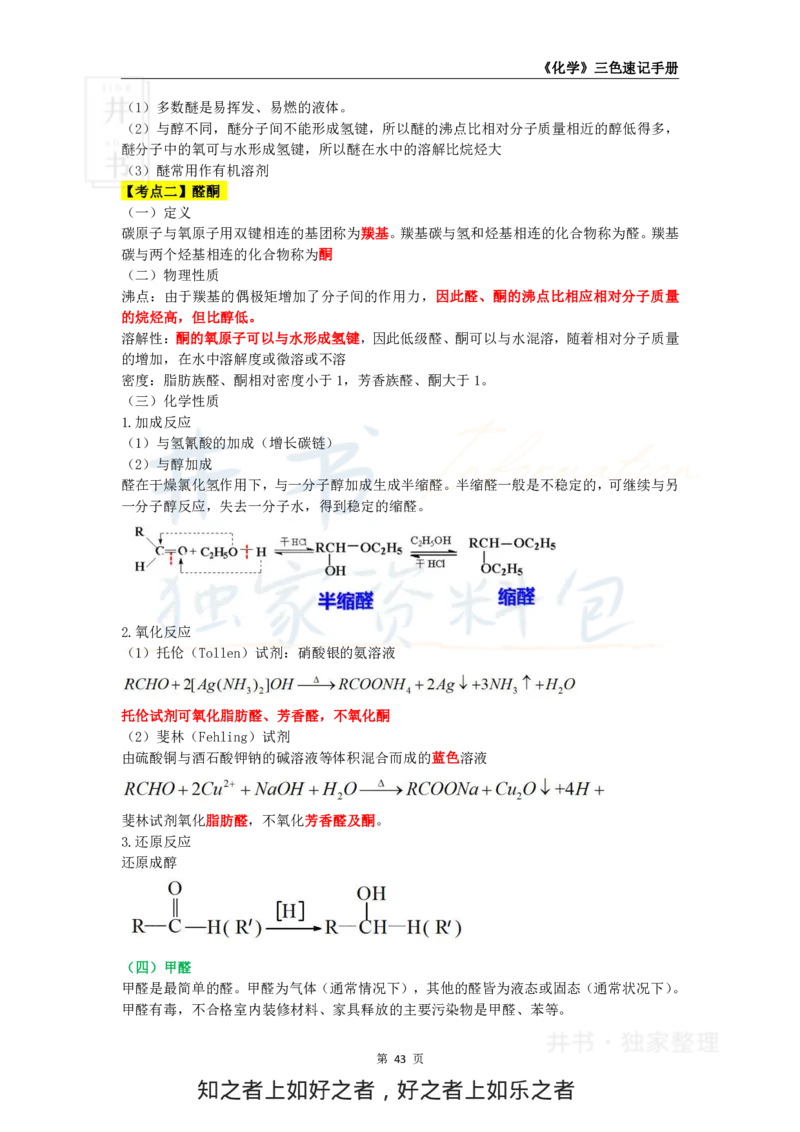
(2)与醇加成
醛在干燥氯化氢作用下,与一分子醇加成生成半缩醛。半缩醛一般是不稳定的,可继续与另
一分子醇反应,失去一分子水,得到稳定的缩醛。
2.氧化反应
(1)托伦(Tollen)试剂:硝酸银的氨溶液
托伦试剂可氧化脂肪醛、芳香醛,不氧化酮
(2)斐林(Fehling)试剂
由硫酸铜与酒石酸钾钠的碱溶液等体积混合而成的蓝色溶液
斐林试剂氧化脂肪醛,不氧化芳香醛及酮。
3.还原反应
还原成醇
(四)甲醛
甲醛是最简单的醛。甲醛为气体(通常情况下),其他的醛皆为液态或固态(通常状况下)。
甲醛有毒,不合格室内装修材料、家具释放的主要污染物是甲醛、苯等。
第 43 页