文档内容
秘密★启用前
2008 年广州市初中毕业生学业考试
化 学
本试卷分为选择题和非选择题两部分;第一部分1至4页,第二部分5至8页,共8页,满分
100分。考试时间80分钟。
注意事项:
1.答卷前,考生务必在答题卡第1面和第3面上用黑色字迹的钢笔或签字笔填写自己的考
生号、姓名;同时填写考场试室号、座位号,再用2B铅笔把对应这两个号码的标号涂黑。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号;不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内
的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出指
定的区域;不准使用铅笔、圆珠笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束时,将本试卷和答题卡一并交回。
5.全卷共三大题29小题,请考生检查题数。
可能用到的相对原子质量:H 1 O 16 Mg 24 S 32
第一部分 选择题
(共40分)
一、选择题(本题包括20小题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选错、
不选、多选或涂改不清的,均不给分。
1.下列过程中发生了化学变化的是
A.水通电后分解成氢气和氧气
B. 湿衣服晾晒后变干
C.玻璃敲击后变碎
D. 冷水加热后沸腾
2. 下列关于空气的说法正确的是
化学试卷 第1页 (共8页)A.空气由空气分子组成
B.空气中的氮气没有任何用途
C.空气中二氧化碳含量的增加对环境没有任何影响
D.空气中含有氮气、氧气、二氧化碳等分子
3. 在原子的原子核里,质子数等于
A.核外电子数 B.中子数
C.中子数和电子数之差 D.中子数和电子数之和
4.下列原子属于非金属元素的是
A. B.
+17
+11
C. D. +12
5.如图所示的实验中,小烧杯①盛的是紫色石蕊溶液,②盛的是浓盐酸。
片刻后,可以观察到烧杯①中液体的颜色是
A.紫色
B.红色
① ②
C.无色
D.蓝色
6. 下列事实与液态二氧化碳的灭火原理无关的是
A.液态二氧化碳气化时能降低其周围的温度
B.二氧化碳的密度比空气大,能将燃烧物与空气隔绝
C.二氧化碳是无色无味的气体
D.二氧化碳不能燃烧,也不支持燃烧
7.分析下表数据,下列关于广东省城市降水酸碱性的说法正确的是
年度 2005年 2006年
化学试卷 第2页 (共8页)广东省城市降水pH均值 4.66 4.80
A.2006年和2005年降水总体都偏显碱性
B.2005年降水的碱性比2006年更强
C.2006年酸雨污染程度比2005年减缓
D. 2006年酸雨污染程度比2005年严重
8.下列物质能与CuCl 溶液发生置换反应的是
2
A.H SO B.NaOH C. Ag D. Fe
2 4
9. 俗话说“酒香不怕巷子深”,从化学的角度来解释是由于
A.分子在不断地运动 B.分子间有间隔
C.分子是由原子构成的 D. 分子在化学变化中发生了变化
10.下列图示实验操作正确的是
A B C D
11. 从2008年6月1日开始,超市禁止为顾客无偿提供塑料袋,目的是减少废弃塑
料带来的“白色污染”。下列措施不能用于解决“白色污染”的是
A.用布袋代替塑料袋 B.重复使用某些塑料制品
C.回收利用各种废弃塑料 D.将废弃塑料集中到野外焚烧
12. 人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是
A.铁是由钢冶炼成的
B.生铁是含有碳的铁合金
C.炼铁的过程是把铁矿石变成纯净的氧化铁
D.被腐蚀后的铁制品属于不可回收垃圾
13. 下列有关木炭、一氧化碳、甲烷燃烧的说法正确的是
A.燃烧时发生的都是化合反应 B.燃烧时都有蓝色火焰
化学试卷 第3页 (共8页)C.燃烧后都有CO 生成 D.点燃前都要检验纯度
2
14.下列关于金刚石和石墨的说法正确的是
A.组成元素都相同 B.原子排列方式都相同
C.都能导电 D.硬度都很大
15.下列说法符合事实的是
A.铁丝伸入盛有氧气的集气瓶中会剧烈燃烧
B.木炭粉与黑色的氧化铜粉末混合后可看到红色粉末
C.铝放置在空气中不与氧气反应
D.硫燃烧后生成有刺激性气味的气体
16. 下列物质不能导电的是
A.澄清石灰水 B.氢氧化钠溶液
C.稀硫酸 D.乙醇
17. 下列各组溶液,相互能发生反应的是
A. 碳酸钾和硝酸钡 B. 硝酸钡和盐酸
C.氢氧化钠和碳酸钾 D.硫酸钠和碳酸钾
18. 下列方法能够将石灰水和氢氧化钠溶液区别开的是
A.分别滴加紫色石蕊溶液 B.分别通入CO
2
C.分别滴加氯化钠溶液 D.分别滴加稀盐酸
19. 氧化镁(MgO)中,镁元素的质量分数是
A.30% B. 40% C.60% D. 70%
20. 下列操作可以达到实验目的的是
A.用灼烧的方法除去铜粉中混有的木炭粉
B.用测定溶液pH的方法区别食盐水和蒸馏水
C.加入氧化镁除去硫酸镁溶液中含有的少量硫酸
D.通入澄清石灰水除去气体中含有的一氧化碳
第二部分 非选择题 (共60分)
化学试卷 第4页 (共8页)二、本题包括5小题,共36分
21.(4分)用化学用语表示下列物质:
(1)氧化钙 ,氯化钡溶于水电离出的离子 ;
(2)1个氮分子 ;
(3)某氮的氧化物中氮元素的化合价为+1价,该氧化物是 ;
22.(4分)现有下列物质:①甲烷 ②氧气 ③硝酸钾 ④碳酸氢钠 ⑤一氧化碳
⑥二氧化碳 ⑦乙醇 ⑧铁。
(1)属于有机化合物的是(填编号,下同) ;
(2)属于单质的是 ;
(3)属于氧化物的是 ;属于盐的是 。
23.( 8分)选择“CO”、“CO ”或“稀HCl”填空,并写出有关反应的化学方程
2
式。
(1)能够与氢氧化钠反应的是 ,
反应的化学方程式是 ;
(2)能够把铁从铁矿石(Fe O )里还原出来的是 ,
2 3
反应的化学方程式是 ;
(3)能够除去铁制品表面的铁锈(Fe O )的是 ,
2 3
反应的化学方程式是 ;
24.(10分)在当今社会,人类需要的大部分能量都是由化学反应产生的。
(1)下列物质属于化石燃料的是(填写字母编号) 。
A.乙醇 B.石油 C.氢气 D.煤
(2)氢气是一种清洁能源,氢气燃烧的化学方程式为 ,在
实验室里可以通过置换反应来制取氢气,写出其中一个化学方程式:
。
(3)煤中含有的硫在燃烧时会以二氧化硫的形式排放,污染大气。某工厂有含硫
0.8%的煤5000t,回答下列问题:
①5000t含硫0.8%的煤中,所含硫的质量是 t;
化学试卷 第5页 (共8页)②二氧化硫的相对分子质量为 ,上述煤如果不经处理直接完全
燃烧,产生二氧化硫的质量是 t;
③二氧化硫可用于生产硫酸,化学方程式为2SO +O +2H O=2H SO 。参加反应
2 2 2 2 4
的SO 与生成的H SO 的质量比是 ,如果将上述SO 全部转化
2 2 4 2
可得到H SO 的质量为 t(精确到0.1)。
2 4
25. (10分)某制碱厂以岩盐水为主要原料生产纯碱(碳酸钠)和其他副产品。
(一)原料岩盐水主要是含氯化钠,此外还含有较多硫酸钠,以及少量氯化钙和
氯化镁。上述几种物质在不同温度时的溶解度数据如下表:
温度/℃ 0 10 20 30 40
溶 氯化钠 35.7 35.8 36.0 36.3 36.6
解
硫酸钠 4.5 9.6 20.2 40.8 48.4
度
/g 氯化钙 59.5 65.0 74.5 100 116
氯化镁 52.9 53.8 54.8 56.0 58.0
(1)根据所提供的溶解度数据,画出硫酸钠的溶解度曲线。
(2)10℃时由100g水配制得到的饱和硫酸钠溶液中溶质的质量是 g,溶
质的质量分数是 (精确到0.1%)。
(二)岩盐水初步处理后,经净化、精制得到生产碳酸钠所需要的食盐水,同时制
取副产品A晶体,其主要流程如下:
过量 Ca(OH) 2 适量Na 2 CO 3 适量HCl
初步处理后
的 ( 岩 室 盐 温 水 ) 降温 操作Ⅰ 盐 精 水 制Ⅰ 盐 精 水 制Ⅱ 过滤 调 pH 节 食盐水
A晶体 滤渣
(3)“降温”的目的是析出副产品“A晶体”,A的化学式是 。
(4)“操作Ⅰ”中的操作是 ,若在实验室进行该操作,需要
用到的玻璃仪器除烧杯、玻璃棒外,还有 。
(5)“盐水精制Ⅰ”是除去盐水中的少量氯化镁,反应的化学方程式是
。
化学试卷 第6页 (共8页)(6)“盐水精制Ⅱ”是除去盐水中的其他杂质,反应的化学方程式 是
。
三、本题包括4小题,共24 分。
请写出他在操作中的两个错误:
26.(2分)右图是某同学在加热试管里的液体时的操作。
错误1 ;
错误2 。
27. (7分)实验室可用下列A或B装置制取O ,用C装置收集O 。
2 2
a
b
C
A B
(1)写出C装置中仪器的名称:a ,b 。
(2)如果选用B、C装置制取并收集O ,回答下列问题:
2
①装入药品前,先应检查装置 ;
②试管中装入的药品是 (填化学式);
③当观察到C装置中 时,开始收集O ;
2
④实验结束停止加热时,要先 ,然后再熄灭酒精灯。
28.(6分)有三瓶无色透明的液体,分别是碳酸钠溶液、氢氧化钠溶液和水。请设计
一个实验方案把这三瓶液体区分开来,并将实验操作、预期现象和结论填写在下表
中。
提示:碳酸钠俗称“纯碱”,其水溶液显碱性。
实验操作 预期现象与结论
1、
2、
29.(9分)金属在生产、生活中有着广泛的用途。
化学试卷 第7页 (共8页)(1)指出金属铝的一个性质及其对应的用途
性质 ,对应用途 ;
(2)黄铜是铜锌合金,其硬度比纯铜 (填“大”、“小”或“相同”)。
(3)长期露置于空气中的金属M 表面会被锈蚀。经检测,锈蚀物中除含有M外,
还含有C、H、O 三种元素。根据质量守恒定律,推测与金属M发生反应生
成锈蚀物的物质。
推测Ⅰ:锈蚀物中的H 来自空气中的 (填化学式,下同),C 来
自空气中的 ,因此这两种物质肯定参加了反应。
推测Ⅱ:锈蚀物中的O 有多种来源,因此不能确定空气中的O 是否参加了
2
反应。
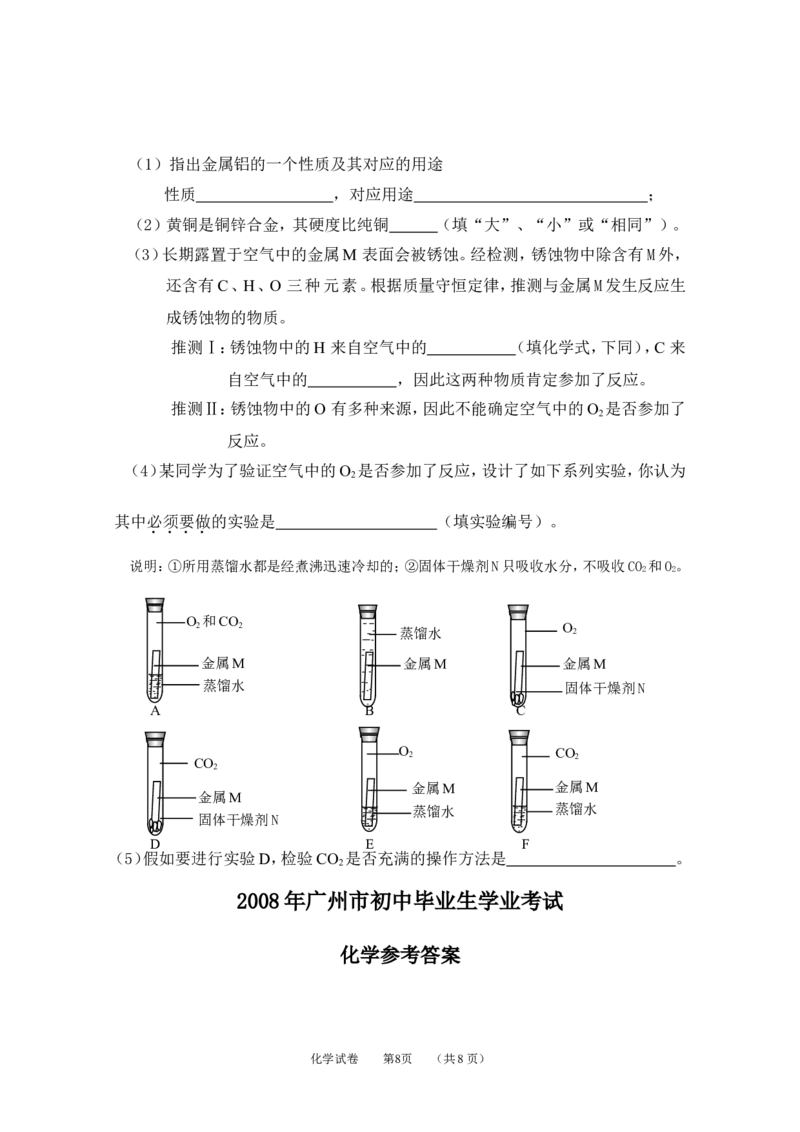
(4)某同学为了验证空气中的O 是否参加了反应,设计了如下系列实验,你认为
2
其中必须要做的实验是 (填实验编号)。
说明:①所用蒸馏水都是经煮沸迅速冷却的;②固体干燥剂N只吸收水分,不吸收CO 和O。
2 2
O 和CO
2 2 O
蒸馏水 2
金属M 金属M 金属M
蒸馏水 固体干燥剂N
A B C
O 2 CO 2
CO
2
金属M 金属M
金属M
蒸馏水 蒸馏水
固体干燥剂N
D E F
(5)假如要进行实验D,检验CO 是否充满的操作方法是 。
2
2008 年广州市初中毕业生学业考试
化学参考答案
化学试卷 第8页 (共8页)第一部分 选择题
(共40分)
一、选择题(本题包括20小题,每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 A D A B B C C D A B
题号 11 12 13 14 15 16 17 18 19 20
答案 D B C A D D A B C C
二、本题包括5小题,共36分
21.(1)CaO,Ba2+、Cl-; (2)N ,(3)N O (4分)
2 2
22.(1)①⑦;(2)②⑧;(3)⑤⑥,③④ (4分)
23.(8分)
(1)CO 、稀HCl
2
CO +2NaOH==Na CO + H O HCl+NaOH==NaCl+H O
2 2 3 2 2
(2)CO, 3CO+Fe O ==高=温=2Fe+3CO ;
2 3 2
(3)稀HCl,6HCl+Fe O ==2FeCl +3H O;
2 3 3 2
24.(10分)
(1)B、D(各1分,共2分)
(2)2H 60 +O == 点 = 燃 =2H O, Zn+H SO(稀)==ZnSO +H ↑(或其它合理答案)
2 2 2 2 4 4 2
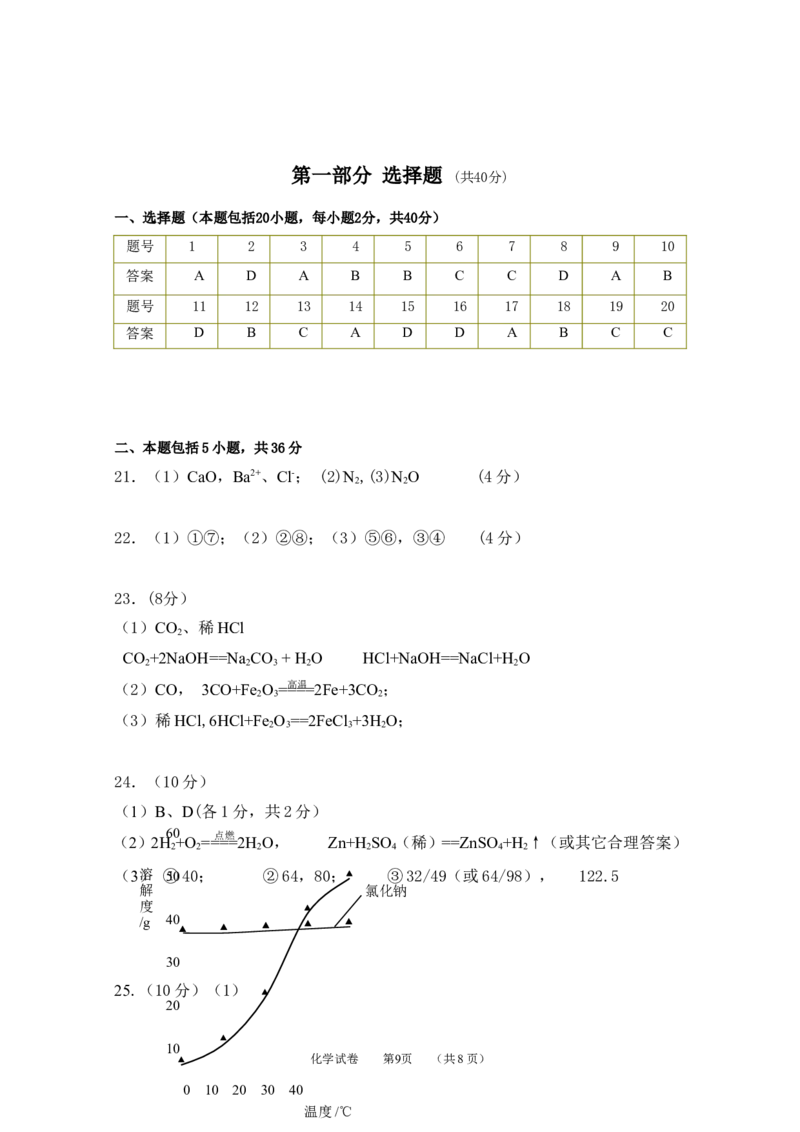
(3)溶 ①5040; ②64,80;▲ ③32/49(或64/98), 122.5
解 氯化钠
度
▲
/g 40 ▲ ▲ ▲ ▲ ▲
30
25.(10分)(1)
▲
20
▲
10
▲ 化学试卷 第9页 (共8页)
0 10 20 30 40
温度/℃(2)①9.6,②8.8%;
(3)Na SO
2 4
(4)过滤,漏斗
(5)Ca(OH) +MgCl =Mg(OH) +CaCl
2 2 2 2
(6) CaCl +Na CO =CaCO ↓+2NaCl
2 2 3 3
Ca(OH) +Na CO =CaCO ↓+2NaOH
2 2 3 3
三、本题包括4小题,共24分。
26.(2分)
错误1:用手拿试管加热(或“不能用手拿试管加热”、“没有用试管夹夹住试管
加热”)
错误2:试管口垂直向上加热(或“管口应该向上倾斜加热”)
(画出正确操作的图也可得分)
27. (7分)
(1)集气瓶,水槽
(2)①气密性;
②KClO 和MnO ;(答“KMnO ”也可给分)
3 2 4
化学试卷 第10页 (共8页)③导管口气泡连续地并比较均匀地冒出(或导管口有连续气泡冒出)
④把C装置中的导管移出水面
28. (6分)
实验操作 现象与结论
1、分别取少量液体于三支试管中,然 有气泡产生的是碳酸钠溶液,没有明显
后滴加稀盐酸。 现象的是氢氧化钠溶液和水
2、分别取尚未区分的两种液体于两 溶液由无色变红色的是氢氧化钠溶液;
支试管中,再滴入酚酞溶液。 没有明显现象的是水。
(其它合理答案也可得分)
29.(9分)
(1)导电性优良,做导线(其它合理答案都可得分)
(2)较大
(3)H O,CO
2 2
(4)A、F
(5)用燃着的木条放在试管口,如果木条熄灭,说明试管中已充满CO 。
2
化学试卷 第11页 (共8页)