文档内容
准考证号:_ 姓名:
(在此卷上答题无效)
2025—2026学年第一学期初中毕业班期末考试
化 学
本试卷共8页。满分100分。
注意事项:
1.答题前,考生务必在试题卷、答题卡规定位置填写本人准考证号、姓名等信息。核对答
题卡上粘贴的条形码的“准考证号、姓名”与本人准考证号、姓名是否一致。
2.选择题每题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,
用橡皮擦干净后,再选涂其他答案标号。非选择题答案用0.5毫米黑色签字笔在答题
卡上相应位置书写作答,在试题卷上答题无效。
可能用到的相对原子质量:H1 C12 016 Na 23 S32 Ca40 Hg 201
一、选择题:本大题共10题,每题3分,共30分。在每题给出的四个选项中,只有一项是符合
题目要求的。
1.科技新成果是发展新质生产力的重要体现。下列研究属于化学研究范畴的是
A.开发DeepSeek智能大模型 B.制备大面积二维金属材料
C.侵入式脑机接口临床试验 D.构建超导量子计算原型机
2.用大理石和稀盐酸制备二氧化碳,下列实验及操作正确的是
CO?-
CO?-
紫色
石蕊
d 溶液
A.加入大理石 B.取用稀盐酸 C.收集并验满 D.检验气体
“玲珑一号”“麒麟一号”都是我国独立研发的先进核反应堆。“麒麟一号”设计中使用了
铅铋合金作为冷却剂,替代传统钠钾合金,以提升安全和效率。已知铋的金属活动性介于铅、
铜之间。结合信息完成第3~4题:
3.铀可作为核燃料。铀元素在元素周期表中部分信息及原子结构示意图如下图,下列说法
错误的是
A.铀是一种金属元素
B.铀的相对原子质量为238.0g
92 U X
C.X=92 818322192
铀
D.铀原子最外层电子数为2
238.0
4.下列有关铅铋合金的说法错误的是
A.铅铋合金属于金属材料
B.铅铋合金的熔点比纯铅和纯铋的熔点都高
C.相比于钠钾合金,铅铋合金化学性质更稳定
D.铅铋合金作为冷却剂,主要利用其优良的导热性
化学试题 第1页(共8页)5.《天工开物》记载了银朱的制备过程如下图。下列说法错误的是
二斤石亭脂(S)
研磨 密封 加热、蘸水擦盛 银朱(HgS)
一斤水银(Hg)— 泥罐
A.“研磨”的目的是使水银与石亭脂充分接触
B.“密封”的目的是防止有毒水银蒸气泄漏
C.“蘸水擦盏”是为了让泥罐外壁降温,银朱凝华贴于内壁
D.“一斤水银”与“二斤石亭脂”能恰好完全反应
氢能被公认为是最理想的“绿色能源”之一,氢能的研究与应用已成为全球能源转型的重
要方向。氢气的存储是制约氢能应用的一大难题,常见有物理储氢和化学储氢。化学储氢可
通过催化反应将氢气储存于液态物质中,实现常温常压储氢。结合信息完成第6~7题:
6.氢气经加压储存在专用无缝高压钢瓶中,关于该过程的说法正确的是
A.氢分子质量变小 B.氢分子间间隔变小
C.氢分子停止运动 D.氢分子化学性质改变
7.利用苯(C?H?)和环己烷(C?H??)之间的转化可实现加氢和脱氢,原理如下:
C.H?+3H?高温△C?H?。下列说法正确的是
A.苯是一种单质 B.一个环己烷分子中含有12个原子
C.环己烷中氢元素质量分数比苯高 D.参加反应的苯与氢气质量比为39:1
8.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 除去CO?中的少量CO 将气体点燃
B 除去炭粉中的少量氧化铜 在空气中灼烧
C 鉴别H?O和C?H?OH 观察颜色
D 鉴别O?、CO?和空气 将燃着的木条分别伸人集气瓶中
9.某兴趣小组利用暖宝宝贴测定空气中氧气的含量(主要利用铁粉生锈的原理,不考虑其他
反应),实验装置如下图。已知实验开始后温度计的读数变大,实验数据如下表(导管中残
留的水及瓶塞、暖宝宝贴所占的体积忽略不计,实验过程中试剂足量)。下列说法错误的是
温度计-
弹簧夹
实验前 实验后
空气 100 广口瓶容积/mL量简内水的体积/mL量简内水的体积/mL
80
60
暖宝宝贴-
20mL水- 4 20 0 250 100.0 60.0
容积为250 mL的广口瓶
A.待装置恢复至室温,打开弹簧夹,等液面稳定后读数
B.实验过程中,该反应将化学能转化为热能
C.实验中,暖宝宝贴增加的质量等于消耗氧气的质量
D.根据表中数据,计算出空气中氧气的体积分数约为17.4%
化学试题 第2页(共8页)10.过氧化钙(CnO?)在水产、农业等领域应用广泛。过氧化钙工业产品中常含有CaO(其他杂
质忽略不计)。实验室对某过氧化钙样品进行成分分析,取10.0g样品用热分析仪对其进
:2CaO?—2CaO+0?1),残留固体质量随温度的变化如下图。下列
行热分解实验(已知:
说法正确的是
固体质量/g10.0
A.反应过程中钙元素的质量变大
B.样品中CaO的质量为5.6g 8.4
C.样品中氧元素的质量为1.6g
D.样品中钙元素的质量分数为60% 温度/℃
二、非选择题(本大题共7题,共70分)
11.(9分)兴趣小组开展“调查人类取火方式变迁”的主题实践活动。
燃芯 o 小 竹帽 金属防风罩
0
孔
压电陶瓷
氯酸钾、
竹筒- 二氧化锰、
液态丁烷
硫等
红磷等可燃物
图1 图2 图3 图4
(1)木燧取火。3万年前,山顶洞人使用钻木取火(如图1)。从燃烧的条件分析,“钻木”
的主要目的是_____。
(2)火折子取火。火折子(如图2)是古代的一种取火用具,燃芯含有硫、硝酸钾、薯藤和棉
花等。
①火折子使用时发生的化学反应之一:2KNO,—2X+0?↑,x的化学式是_____;
②取火时,打开竹帽,吹气后燃芯上的火星就会复燃,其原因是___。
(3)火柴取火。19世纪末,安全火柴(如图3)问世。
①已知在二氧化锰催化作用下,氯酸钾受热生成氯化钾和氧气。该变化的基本反应类
型是______;
②火柴使用时会闻到刺激性气味,主要原因是____(用化学方程式表示)。
(4)打火机取火。20世纪中后期,打火机(如图4)逐渐普及。点火时,按压陶瓷开关形成
电火花,同时丁烷汽化喷出,产生稳定火焰。
①转动打火机出气阀可以调节火焰大小的原理是_______;
②若保存不当,打火机易发生爆炸。写出一条妥善保存打火机的措施:_____。
(5)结合以上内容,梳理人类取火方式变迁的趋势:________(写一点)。
化学试题 第3页(共8页)12.(6分)研究小组开展“微型空气质量检测站的设计与组装”项目式学习活动。
PM?,/PM?
传感器
数据显示器
SO,传感器□ 过滤材料
CO传感器
臭氧
传感器
扩展板
进风口 出风口
主控板
图1 图2
活动一:设计微型空气质量“检测站”
小组同学查阅资料并设计微型空气质量“检测站”的结构如图1所示。
(1)为测量空气中其他污染物,图1中还应放置的传感器是________(选填标号)。
A.氧气传感器 B.氮气传感器 C.二氧化氮传感器
(2)已知含SO?的空气通过SO?传感器的透气膜,在电极上转化为SO,2并形成电流,经
电路处理转化为读数。该过程中硫元素的化合价________(选填“升高”“降低”或
“不变”)。
(3)小组同学制作微型新风机(如图2)去除可吸入颗粒物,改善室内空气质量。该装置具
有一定净化效果但效率不高,为提升净化效率,请给出一条装置改进建议:_____。
活动二:测量校园空气质量
小组同学利用微型空气质量“检测站”于某周周一至周五上午测量校园教室、操场、食
堂附近的空气质量,5天所测的部分数据(取均值)如下表:
检测地点 PM?s浓度(μg·m?3) SO?浓度(ppm)
教室(上课中) 40 0.00
操场(课间活动) 60 0.00
食堂附近(午餐时) 73 0.02
(4)课间活动时操场PM?,浓度较高的可能原因是____(写一条,下同);为降低食
堂附近SO?浓度,可以采取的措施是_____。
(5)有同学提出该小组数据采集方案不科学,请你提出改进建议:_______。
化学试题 第4页(共8页)13.(9分)研究小组开展“制作模型并认识物质的组成、结构与变化”主题学习活动。
主题一:史料梳理与模型初建
资料一:1803年道尔顿在原子论中提出,元素由微小的不可分的原子组成;不同元素的原子以
简单数目比形成不可再分的原子—“复杂原子”。道尔顿采用的部分元素符
号如图所示: ◎○①● 道尔顿认为氢气可用“◎”表示,氧气可用“〇”表示。
氢氧 氮 碳°
资料二:1809年盖·吕萨克提出,在同温同压下,相同体积的不同气体中含有相同数目的
原子(包括“复杂原子”)。
研究小组同学结合以上资料展开讨论。
(1)部分同学的观点:盖·吕萨克通过实验发现2体积氢气和1体积氧气反应生成2.体积
水蒸气。结合资料,可推导出氢气和氧气反应生成水的微观示意图如下,说明道尔顿
的原子论具有局限性。理由是_____。
◎◎+〇 ◎ o
(2)另一部分同学的观点:资料一中“原子不可分”的说法也有其合理性。理由是_____。
主题二:学说完善与模型修正
资料三:1811年阿伏加德罗提出分子学说,认为分子是由原子构成的,在化学变化中构成
分子的原子重新结合。
(3)用“O”表示氢原子、用“”表示氧原子、用“●"表示氮原子,下列模型能说明“同一分
子中含有不同原子,但不同分子中原子总数相同”的两组模型是_______和_
(选填标号)。
c.
A. B. D. E.
(4)已知1体积的氢气和1体积的氯气在点燃条件下生成2体积的氯化氢气体(在同温同
压下)。请结合以上相关信息,将该反应的微观示意图补充完整(在方框中画出)。
O氢原子
0+
氯原子
主题三:现代应用与模型迁移
2025年诺贝尔化学奖授予开发金属有机框架(MOFs)的科学家。MOFs材料被称为
“分子乐高”,由金属离子和有机碳基分子构成。MOFs材料可用于净化含NO?的废气,废
气中的NO?先转化为N?O?,经MOFs材料吸附、催化,进一步转化为HNO?,示意图如下:
清洁空气 H?O、0,
吸附
MOFs材料 N?O.
图例
再生 HNO,
含NO?的废气
(5)NO?与N?O?的元素含量相同但性质不同的原因是_____。
(6)根据以上示意图,写出生成HNO?的化学方程式:___。
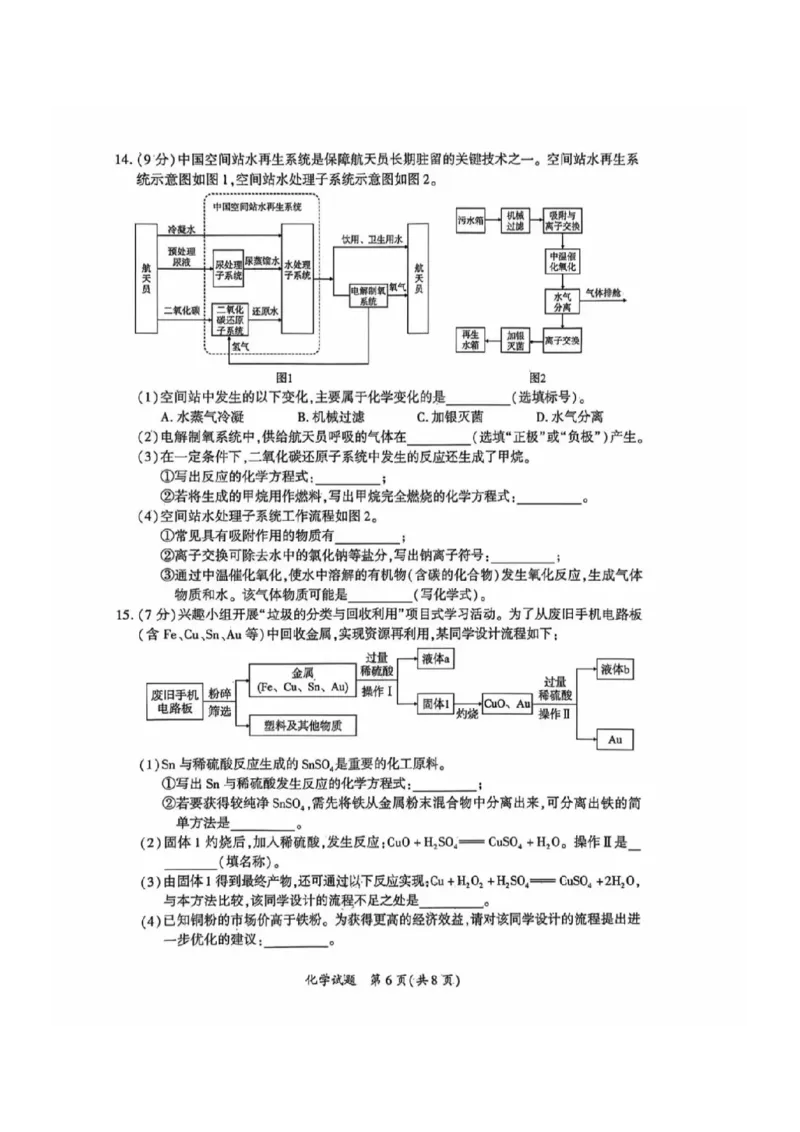
化学试题 第5页(共8页)14.(9分)中国空间站水再生系统是保障航天员长期驻留的关键技术之一。空间站水再生系
统示意图如图1,空间站水处理子系统示意图如图2。
中国空间站水再生系统
机械 吸附与
污水箱
冷凝水 过滤 离子交换
饮用、卫生用水
预处理
航天员 尿液 尿处理 尿蒸馏水水处理 航天员 化 中 氧 温 化 催
子系统 子系统
电解制氧 氧气 水气 气体排舱
系统
二氧化碳 二氧化 还原水 分离
碳还原
子系统 再生 加银
氯气 水箱 灭菌 离子交换
图1 图2
(1)空间站中发生的以下变化,主要属于化学变化的是________(选填标号)。
A.水蒸气冷凝 B.机械过滤 C.加银灭菌 D.水气分离
(2)电解制氧系统中,供给航天员呼吸的气体在_______(选填“正极”或“负极”)产生。
(3)在一定条件下,二氧化碳还原子系统中发生的反应还生成了甲烷。
①写出反应的化学方程式:_____;
②若将生成的甲烷用作燃料,写出甲烷完全燃烧的化学方程式:_______。
(4)空间站水处理子系统工作流程如图2。
①常见具有吸附作用的物质有_______;
②离子交换可除去水中的氯化钠等盐分,写出钠离子符号:____;
③通过中温催化氧化,使水中溶解的有机物(含碳的化合物)发生氧化反应,生成气体
物质和水。该气体物质可能是______(写化学式)。
15.(7分)兴趣小组开展“垃圾的分类与回收利用”项目式学习活动。为了从废旧手机电路板
(含Fe、Cu、Sn、Au等)中回收金属,实现资源再利用,某同学设计流程如下:
过量 液体a
金属 稀硫酸 液体b
过量
废旧手机粉碎 (Fe、Cu、Sn、Au) 操作I CuO、Au-稀硫酸
固体1
电路板 筛选 灼烧 操作Ⅱ
塑料及其他物质
Au
(1)Sn与稀硫酸反应生成的SnSO?是重要的化工原料。
①写出Sn与稀硫酸发生反应的化学方程式:_____;
②若要获得较纯净SnSO?,需先将铁从金属粉末混合物中分离出来,可分离出铁的简
单方法是___。
(2)固体1灼烧后,加入稀硫酸,发生反应:Cu0+H?SO.=CuSO?+H?O。操作Ⅱ是_
____(填名称)。
(3)由固体1得到最终产物,还可通过以下反应实现;Cu+H?O?+H?SO,=CuSO?+2H?O,
与本方法比较,该同学设计的流程不足之处是______。
(4)已知铜粉的市场价高于铁粉。为获得更高的经济效益,请对该同学设计的流程提出进
一步优化的建议:________。
化学试题 第6页(共8页)16.(10分)基于化学吸收法的DAC(Direct Air Capture,直接空气捕集)工艺技术,通过吸收、
解吸、再生等步骤,实现CO?的高效捕集与资源化利用。
(1)固体DAC技术可用钙基捕集,其中一种工艺流程如下:
A B
烟气
碳化炉 CaCO? 煅烧炉
(含CO?)
CaO
①在加热条件下,碳化炉中发生化合反应。写出反应的化学方程式:_______;
②图中CO?浓度较高的是____(选填“A”或“B”)。
(2)液体DAC技术可用氨法捕集,其中一种工艺流程如下:
CO,含量低的净化气
高纯度
CO?
Q NH,HCO
喷淋 溶液 再生塔
吸收剂
富含CO,
吸收塔
工厂烟道- 的废气 分离器 NH,HCO,
废气
固体
除尘净化装置
①吸收塔中吸收剂采用喷淋方式的优点是______;
②已知再生塔内NH?HCO?受热分解生成NH?、H?0和CO?,则吸收塔内发生主要反应
的化学方程式是_______;
③吸收塔内需保持低温的原因是_____(写一条)。
(3)DAC技术应用
①捕集所得的CO?,可用于___(写一条);
②假设你是一名环保工程师,请将DAC技术与校园实际相结合,设计一个校园CO?
捕集实验方案:_____。
17.(20分)鱼缸中常出现鱼缺氧浮头、水草生长缓慢等问题。为解决这些问题,兴趣小组开
展“鱼缸生态气体补给”跨学科实践活动。
输液袋
任务一:设计鱼缸简易供氧器
水
(1)利用过氧化氢和二氧化锰反应提供氧气
导管
流量
调节器 连接鱼缸
过碳酸钠、
二氧化锰
图1 图2
①写出反应的化学方程式:____;
②用图1装置制取氧气,写出检查装置气密性的方法:___。
化学试题 第7页(共8页)(2)家庭常用过碳酸钠固体(2Na?CO?·3H?O?)作为供氧剂。过碳酸钠溶于水发生反应:
2(2Na?CO?·3H?O?)—4Na?CO?+6H?O+30?↑。
①与过氧化氢供氧相比,用过碳酸钠作为供氧剂的优点是_____
②用图2装置供氧,输液袋上导管的作用是____;
③常温常压下若需150mL的氧气,计算需要过碳酸钠的质量(写出计算过程,结果保留
一位小数。已知常温常压下氧气密度约为1.4 g·L?1,过碳酸钠相对分子质量为314)。
任务二:设计水草培育所需气肥补充器
(3)为研究鱼缸水中的溶解氧含量,小组同学在两个500mL锥形瓶中按要求放入水草、小鱼、
水等。控制其他条件相同,将第I组放置在12W光线下,第Ⅱ组放置在黑暗环境中。
4小时后分别测定水中的溶解氧含量,如图3所示。结果如下表: 溶解氧传感器
第I组 第Ⅱ组
条件 光照 避光
8.24 1.15
水中溶解氧含量/mg·L?1
①本实验需控制的变量是______(写一个);
图图33
②为确保实验严谨,还需做的补充实验是______;
③结合表中数据,对解决鱼缺氧浮头、水草生长缓慢 调调节节阀阀
单单向向阀阀33
等问题提出建议:________。
气气球球
(4)为促进鱼缸中水草光合作用,小组用图4装置为鱼缸
型型料料瓶瓶AA 简简阀阀 塑塑料料瓶瓶BB
中水草供给CO?(已知小苏打溶液能与醋酸溶液反应
22
生成CO?)。
ll ①①
①往装置中装人适量试剂,为启动反应产生CO?,需
进行的操作是______; 小小苏苏打打溶溶液液 醋醋酸酸溶溶液液 鱼鱼缸缸
图图44
②气球的作用是___;单向阀2的作用是____。
化学试题 第8页(共8页)2025—2026学年第一学期初中毕业班期末考试
化学试题参考答案及评分标准
1.除化学方程式及特别说明外每空各1分,开放性题目答案参考以下答案及标准给分。
2.化学方程式评分说明:每个化学方程式2分,所有化学式都正确1分,其他都正确再给1分。
一、选择题(共10题,每题3分,共30分)
序号 1 2 3 4 5 6 7 8 9 10
答案 B C B B D B C D C D
二、非选择题(共7题,共70分)
11.(9分)
(1)钻木生热使温度升高,达到木柴着火点
(2)①KNO? ②提供更多氧气
②S+o?点燃so?
(3)①分解反应
(4)①调节气阀控制可燃物的流出量 ②远离火源(或其他合理答案)
(5)更便捷(或更环保、更安全等其他合理答案)
12.(6分)
(1)C (2)升高
(3)增加过滤材料厚度(或增添进风口的数量等其他合理答案)
(4)学生活动引发扬尘,导致空气中PM?s增大 使用更清洁能源(或其他合理答案)
(5)增加采集时段,涵盖上、下午及夜间(或增加其他时间段采样等其他合理答案)
13.(9分)
(1)根据实验事实推导得到氧原子要被分割成半个原子,道尔顿“原子不可再分”无法解释实验事实。
(2)在化学变化时,原子不可分
(3)C D(两个都正确得2分)
(4) o (2分)
(5)分子的构成不同
MOFs4HNO?(或4NO?+2H?O+o?MOFs4HNO?)
(6)2N?O?+2H?O+O?
14.(9分)
(1)C (2)正极
②CH?+202点燃CO?+2H?O
(3)①4H?+CO?一定条件2H?O+CH
(4)①活性炭(或其他合理答案) ②Na ③CO?(或CO等其他合理答案)
第1页共2页15.(7分)
(1)①Sn+H?SO?=SnSO?+H?↑ ②用磁铁吸引
(2)过滤 (3)灼烧需消耗能源
(4)往液体b中加入从金属混合物中回收的铁粉,充分反应后回收铜粉 (2分)
16.(10分)
(1)①CaO+co?CaCo?
②B
(2)①增大反应物间的接触面,使反应更充分
②CO?+NH?+H?O=NH?HCO?
③防止NH?HCO?分解(或其他合理答案)
(3)①制作碳酸饮料(或其他合理答案)
②通过抽气装置把空气通入石灰水中(或其他合理答案) (2分)
17.(20分)
(1)①2H?O?MnO2 2H?O+O?↑
②打开止水夹,加水至浸没漏斗下端管口。在止水夹控制下往漏斗里加水至形成一段水柱,关闭
止水夹一段时间后,漏斗内液面不发生变化,则装置气密性良好 (2分)
(2)①储存运输更安全方便(或使用更便捷可控等其他合理答案)
②平衡袋内外压强,确保液体顺利流下
③解:设需要过碳酸钠的质量为m (6分)
氧气的质量=0.15L×1.4gL1=0.21g
2(2Na?COs:3H?O?)4Na?COs+6H?O+30?1
2×314 3×32
m 0.21g
62二0218
m≈1.4g
答:需要过碳酸钠的质量约为1.4g。
(3)①水的量(或小鱼、水草数量及大小等其他合理答案)
②在瓶中放入和前面实验相同的水,不放水草和小鱼,控制其他条件相同,完成第1、Ⅱ组实验操作(2分)
③适当延长光照时间
(4)①挤压塑料瓶B,使醋酸溶液进入塑料瓶A与小苏打溶液混合
②缓冲瓶内气压
将塑料瓶A产生的部分CO?导入塑料瓶B中,持续挤压醋酸溶液,防止液体从该导管流出(2分)
第2页 共2页