文档内容
2 0 2 4 年 上 教 师 资 格 笔 试 · 化 学 学 科 知 识 与 教 学 能 力
理 论 精 讲 - 化 学 基 本 概 念 2
讲师:沈蕾
更多干货关注 粉笔教师教育 粉笔教师化学计量P8
(二)表示溶液组成的其他物理量
1.溶解度
(1)饱和溶液与不饱和溶液
一定温度下,在一定量溶剂里加入某种溶质,当溶质不能继续
溶解时,所得的溶液叫作这种溶质的饱和溶液。当溶质还能继续溶
解时,所得的溶液叫作这种溶质的不饱和溶液。
不饱和溶液和饱和溶液之间的转化(对大多数固体溶质):
增加溶质、蒸发溶剂或降低温度
不饱和溶液 饱和溶液
增加溶剂或升高温度P8
(2)溶解度
在一定温度下,某固体物质在100g溶剂里达到饱和状态时所溶
解的质量,叫作这种物质在这种溶剂里的溶解度。其单位为“g”。
m
S 质 100g
m
剂
影响溶解度大小的因素:
①内因:物质本身的属性(由结构决定)。
②外因:溶剂和温度,一般升温固体物质的溶解度增大,但少
数物质相反,如Ca(OH) 。
2P9
(3)气体的溶解度
通常指气体的压强为 101kPa 和一定温度时,在 1 体积水里溶
解达到饱和状态时的气体的体积,常记为 1:X 。
气体溶解度大小与温度和压强有关,温度升高,气体溶解度减
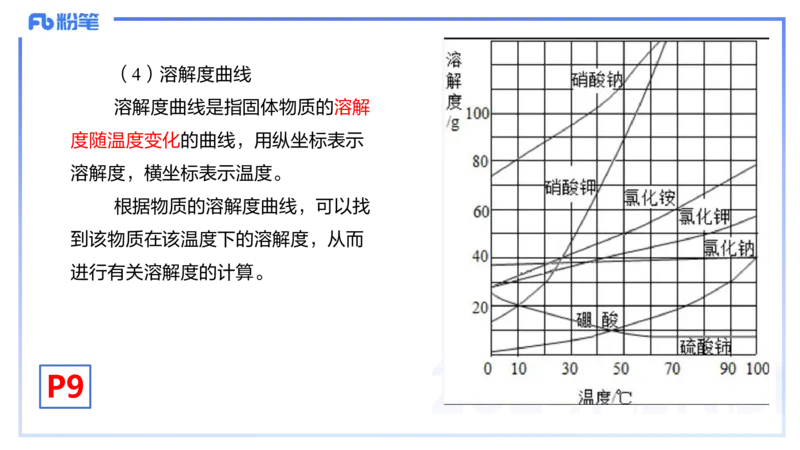
小;压强增大,气体溶解度增大。(4)溶解度曲线
溶解度曲线是指固体物质的溶解
度随温度变化的曲线,用纵坐标表示
溶解度,横坐标表示温度。
根据物质的溶解度曲线,可以找
到该物质在该温度下的溶解度,从而
进行有关溶解度的计算。
P9P9
2.溶质的质量分数
m
(1)溶液中溶质的质量分数: w 质 100%
m m
剂 质
S
(2)饱和溶液的质量分数:
w 100%
100g S
(3)溶质的质量分数、物质的量浓度及溶液密度之间的关系
(密度的单位为g/mL):
1000w
c
MP11
2. 向饱和的澄清石灰水中加入少量 CaC ,充分反应后,再恢复到原
2
来的温度,所得溶液中( )。
A. c(Ca2+ )、c(OH–) 均增大 B. c(OH–) 增大、c(H+) 减小
C. c(Ca2+ )、c(OH–) 均减小 D. c(Ca2+ )、c(OH–) 均保持不变P9
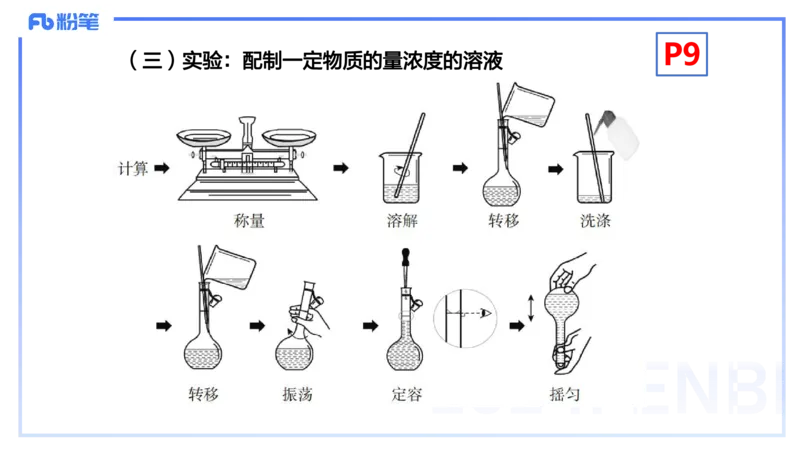
(三)实验:配制一定物质的量浓度的溶液P10
1.实验步骤:(以配制100 mL 1.00 mol/L的NaOH溶液为例)
(1)计算:配制 100mL 1.00mol/L 的 NaOH 溶液需要n(NaOH)=0.1mol,
则需m(NaOH)=4.0g。
(2)称量:4.0 gNaOH(保留一位小数)。
称量时遵循“左物右码”,一般托盘两边各放一张质量相同的称量纸,
但易腐蚀、易潮解的物质(如 NaOH)应放在玻璃器皿中称量。
(3)溶解:将称好的 NaOH 固体放入烧杯中,用适量蒸馏水溶解。
(4)转移:待烧杯中溶液冷却至室温后,转移至容量瓶,并用玻璃棒引
流。P10
(5)洗涤:用少量蒸馏水洗涤烧杯内壁及玻璃棒 2 ~ 3 次,并
将洗涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀。
(6)定容:将蒸馏水沿玻璃棒注入容量瓶,液面离容量瓶颈刻
度线下 1 ~ 2cm 时,改用胶头滴管滴加蒸馏水至凹液面最低处与刻
度线相切。若蒸馏水不慎超过刻度线,应重新配制。
(7)摇匀:盖好瓶塞,反复上下颠倒,摇匀。
(8)装瓶贴标签:标签上注明药品的名称、浓度。P10
2.实验仪器
托盘天平、药匙、烧杯、玻璃棒、
量筒、100ml容量瓶、胶头滴管。
3.容量瓶的使用
(1)容量瓶:只有一个刻度线,
标有温度和容量,只能配制容量瓶上
规定容量的溶液(另外标有温度和容
量的仪器还有滴定管、量筒)。P10
(2)常见容量瓶的规格:50mL、100mL、250mL、500mL、
1000mL。若要配制480mL 与 240mL 溶液,应分别使用 500mL 容量
瓶和 250mL 容量瓶。
(3)容量瓶使用之前必须查漏。
方法:向容量瓶中加适量水后,塞紧瓶塞,倒置,观察是否漏
水,若不漏水,将瓶正立,且将瓶塞旋转 180°,再次倒置看是否
漏水。物质的组成、分类及变化P13
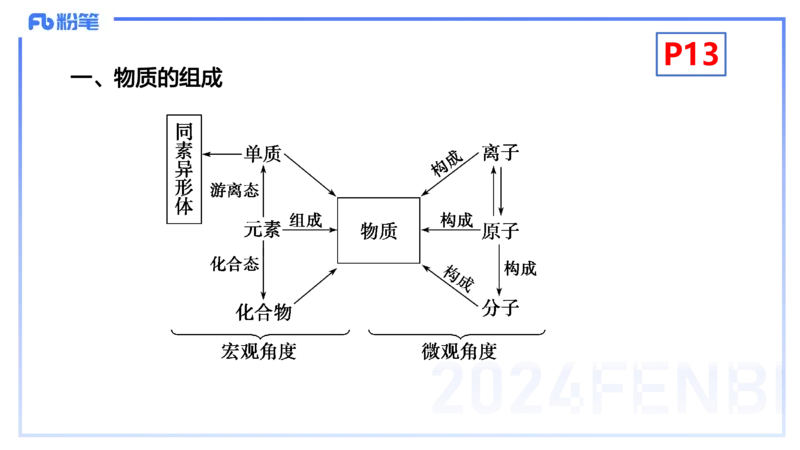
一、物质的组成P13
1.元素
(1)宏观上物质是由元素组成的,微观上物质是由分子、原子
或离子构成的。
(2)元素:具有相同核电荷数(质子数)的一类原子的总称。
注意:由同种元素组成的物质不一定是同种物质,如 O 和 O 。
2 3
(3)元素与物质的关系P14
2.分子和原子
分子 原子
定义 分子是保持物质化学性质的最小粒子 原子是化学变化中的最小粒子
性质 质量小、体积小;不断运动;有间隔
联系 分子是由原子构成的。分子、原子都是构成物质的微粒。
区别 在化学变化中,分子可以再分,而原子不可以再分
一种物质如果由分子构成,那么保持它化学性质的最小粒子是分子;
备注
如果由原子构成,那么保持它化学性质的最小粒子是原子。P14
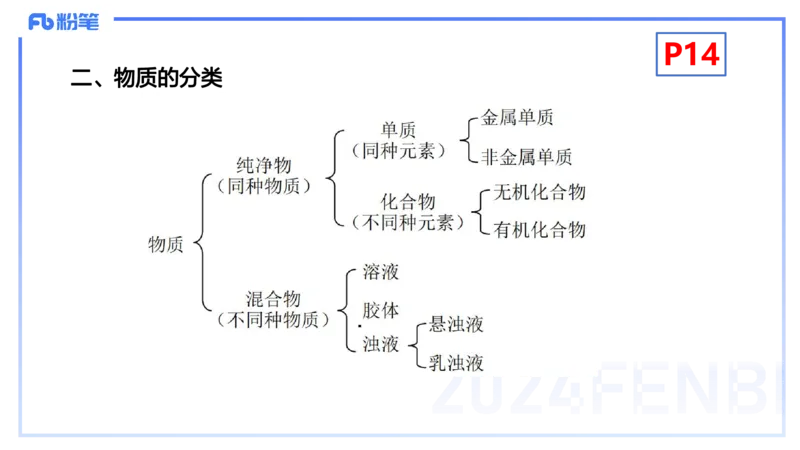
二、物质的分类P14
(一)纯净物
由同种物质组成的一类物质,可分为单质和化合物两类,具有固
定的物理、化学性质。
1.单质
定义:由同种元素组成的纯净物。
同素异形体:同种元素形成的不同单质叫同素异形体。
同素异形体的形成有两种方式:
(1)组成分子的原子个数不同:如 O 和 O ;
2 3
(2)晶体中原子的排列方式不同:如金刚石和石墨、白磷和红磷。P15
同素异形体之间的性质差异主要体现在物理性质上。
同素异形体在一定条件下可以相互转化,转化过程中破坏原有的
化学键,故同素异形体之间的转化属于化学变化。
同素异形体在纯氧中燃烧的产物是唯一的。P15
2.化合物
定义:由两种或两种以上元素组成的纯净物。
(1)有机物
含有碳元素的化合物,如甲烷、乙醇、葡萄糖、蛋白质等。
但是不包括碳的氧化物(一氧化碳、二氧化碳)、碳酸,碳酸盐、氰化物、
硫氰化物、氰酸盐、金属碳化物、部分简单含碳化合物(如SiC)等物质。
(2)无机物
无机物是无机化合物的简称,通常指不含碳元素的化合物。少数含碳的化
合物,如一氧化碳、二氧化碳、碳酸盐、氰化物等也属于无机物。
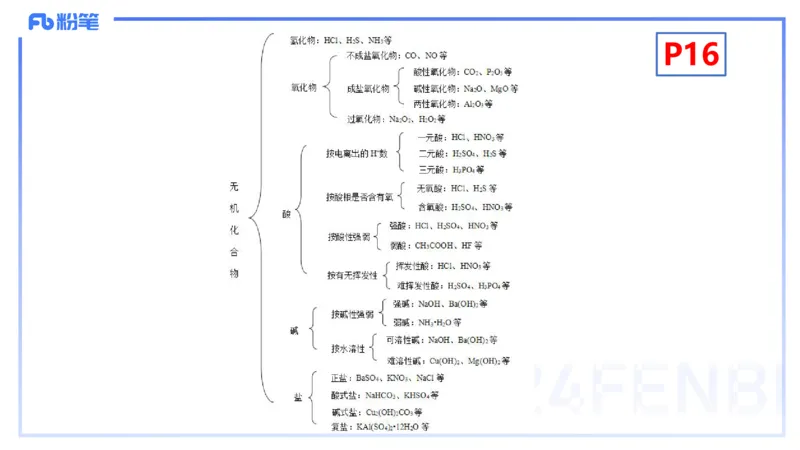
无机物常见分类如下:P16P16
氢化物:HCl、H S、NH 等
2 3
不成盐氧化物:CO、NO等
酸性氧化物:CO 、P O 等
2 2 5
氧化物 成盐氧化物 碱性氧化物:Na O、MgO等
2
两性氧化物:Al O 等
2 3
过氧化物:Na O 、H O 等
2 2 2 2P17
下面详细介绍一下氧化物中的成盐氧化物:
氧化物种类 概念 组成 性质
①与水反应生成对应的含氧酸;
凡能跟碱反应生成盐和 大多数是非金属
酸性氧化物 (SiO 除外)
2
水的氧化物 氧化物
②与可溶性碱反应生成盐和水
凡能跟酸反应生成盐和 ①与水反应生成可溶性碱;
碱性氧化物 都是金属氧化物
水的氧化物 ②与酸反应生成盐和水
既能和酸反应生成盐和
①与酸反应生成盐和水;
两性氧化物 水,又能和碱反应生成 例:Al O
2 3
②与碱反应生成盐和水
盐和水的氧化物。P16P16
强碱:NaOH、Ba(OH) 等
2
按碱性强弱
弱碱:NH ·H O等
3 2
碱
可溶性碱:NaOH、Ba(OH) 等
2
按水溶性
难溶性碱:Cu(OH) 、Mg(OH) 等
2 2P16
正盐:BaSO 、KNO 、NaCl等
4 3
盐 酸式盐:NaHCO 、KHSO 等
3 4
碱式盐:Cu (OH) CO 等
2 2 3
复盐:KAl(SO ) ·12H O等
4 2 2P17
(二)混合物
由两种或两种以上的物质混合而成的物质,没有固定的组成和性质。
常见混合物:
1. 同素异形体间的混合物。
2. 同分异构体间的混合物。
3. 分散系(溶液、胶体、浊液)。
4. 高分子化合物(蛋白质、淀粉、纤维素、聚合物)。P17
5. 其他:
(1)氨水(NH 水溶液)、氯水(Cl 水溶液)、王水(浓硝酸和浓盐酸)、天然水、
3 2
硬水、软水、水玻璃(Na SiO 溶液)、福尔马林(HCHO溶液)、盐酸、硫酸;
2 3
(2)水煤气(CO、H )、天然气(CH )、焦炉气(H 、CH )、高炉煤气(CO、
2 4 2 4
N )、石油气(CH )、裂解气(CH 、C ~C 烯烃)、空气;
2 4 4 2 5
(3)钢、生铁、普钙(Ca(H PO ) 、CaSO ·2H O)、漂白粉(CaCl 、Ca(ClO) )、
2 4 2 4 2 2 2
碱石灰(CaO、NaOH)、黑火药(KNO 、S、C)、铝热剂(Al、Fe O )、水泥(硅酸
3 2 3
盐)、铁触媒(Fe O )、玻璃(Na SiO 、CaSiO 、SiO )、煤;
3 4 2 3 3 2
(4)煤焦油(芳香族化合物)、石油及其各种馏分、植物油和动物油等。P17
三、分散系、胶体
(一)分散系
1.概念:一种物质(或几种物质)以粒子形式分散到另一种物
质里所形成的混合物。
分散质——分散成微粒的物质。
分散剂——微粒分布在其中的物质。
2.分类:溶液
分 散 系
胶体
浊液P18
3.三种分散系的比较:
溶液 胶体 浊液
分散质粒子直径
<1 nm 1 nm~100 nm >100 nm
大小(本质区分)
分散质粒子成分 离子或小分子 分子或离子的集合体 大量分子或离子的集合体
外观特征 均一、透明 均一、透明或半透明 浑浊、不均一、不透明
稳定性 稳定,静置无沉淀 一定条件下稳定存在(介稳体系) 不稳定
分散质粒子能否
能 不能 不能
透过半透膜
分散质粒子能否
能 能 不能
透过滤纸
Fe(OH) 胶体、肥皂水、血液、
3
实例 食盐水、蔗糖溶液 土壤胶体、硅酸胶体、淀粉胶体、 泥水
蛋白质胶体、雾、云、烟
鉴别 无丁达尔现象 有丁达尔现象 静置分层或沉淀