文档内容
2 0 2 4 年 上 物 理 教 师 资 格 证
大学热 学-第 一讲
讲师:余贞
更多干货关注 粉笔教师教育 粉笔教师一、基本概念
(一)平衡态
一个系统在不受外界影响的条件下,且其宏观性质不随时间变化,则该系统处于平衡态。
(二)弛豫时间
系统由非平衡态过渡到平衡态的过程称为弛豫,所需的时间称为弛豫时间。
(三)准静态过程
如果系统由非平衡态过渡到平衡态进行得十分缓慢,其中的每一步所经历的时间均比弛豫时间长得多,
则每一步都有充分的时间来建立新的平衡态,使过程中的每一中间状态均可以近似看作平衡态,这样
的过程称为准静态过程,反之就称为非准静态过程。
2024FENBI(四)自由度
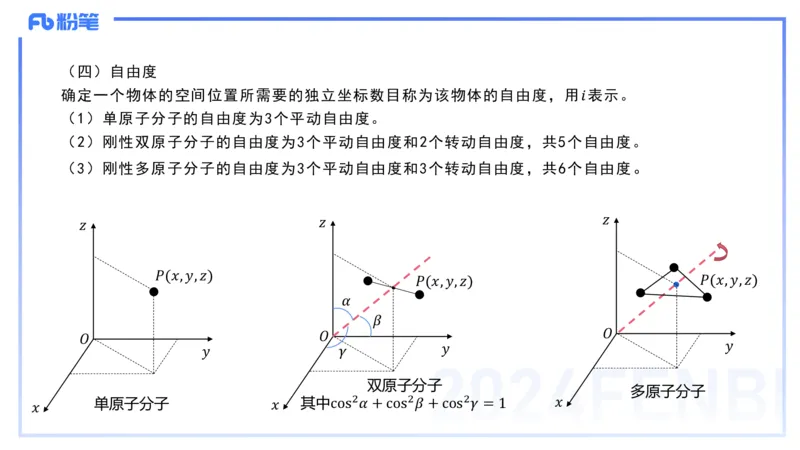
确定一个物体的空间位置所需要的独立坐标数目称为该物体的自由度,用𝑖表示。
(1)单原子分子的自由度为3个平动自由度。
(2)刚性双原子分子的自由度为3个平动自由度和2个转动自由度,共5个自由度。
(3)刚性多原子分子的自由度为3个平动自由度和3个转动自由度,共6个自由度。
𝑧
𝑧
𝑧
𝑃(𝑥, 𝑦, 𝑧)
𝑃(𝑥, 𝑦, 𝑧) 𝑃(𝑥, 𝑦, 𝑧)
𝛼
𝛽
𝑂
𝑂
𝑂
𝑦
𝑦 𝛾 𝑦
2024FENBI
双原子分子
多原子分子
单原子分子 𝑥 其中cos2𝛼 + cos2𝛽 + cos2𝛾 = 1 𝑥
𝑥理 想 气 体 状 态 方 程
𝑚
𝑝𝑉 = 𝑅𝑇 或 𝑝𝑉 = 𝑛𝑅𝑇
𝑀
式中,𝑀为气体的摩尔质量;𝑚为气体的质量;𝑛为气体物质的量;𝑅为摩尔气体常
数(又称通用、理想气体常数及普适气体常数等) ,国际单位制中𝑅 = 8.314J/
(mol ⋅ K);𝑝为气体压强;𝑇为气体的热力学温度;𝑉为气体分子的活动空间。
2024FENBI理 想 气 体 的 压 强 和 温 度 公 式
(一)理想气体压强公式
2
𝑝 = 𝑛𝜀
𝑘
3
𝑁 1
式中,𝑛为分子数密度(𝑛 = ),𝜀 = 𝑚𝑣2为分子的平均平动动能。
𝑘
𝑉 2
ഥ
𝑣2
注:速度分量的方均值与方均速率的关系𝑣 2 =
𝑥
3
(二)理想气体温度公式
3
𝜀 = 𝑘𝑇
𝑘
2
该公式表明:温度是气体分子平均平动动能大小的量度。
𝑅
式中,𝑘 = = 1.38 × 10−23J/K,为玻尔兹曼常数;𝑁 = 6.02 × 1023mol−1。
𝑁 2A 024FENBI
A5 3
【例1】一容器内贮有气体,温度为27℃。问(1)压强为1.013 × 10 𝑃𝑎时,在1𝑚
−5 3
中有多少个分子;(2)在高真空时,压强为1.33 × 10 𝑃𝑎,在1𝑚 中有多少个分子?
2024FENBI气 体 分 子 的 方 均 根 速 率
因为气体的温度是气体分子平均平动动能的量度,所以
1 3
𝜀 = 𝑚𝑣ഥ2 = 𝑘𝑇
𝑘
2 2
由此可以计算在任何温度下气体分子的方均根速率 𝑣2,它是气体分子速率的一种平均值
3𝐾𝑇 3𝑅𝑇
𝑣2 = =
𝑚 𝑀
0
注意:在相同温度时虽然各种分子的平均平动动能相等,但它们的方均根速率并不相等。
2024FENBI【例1】试求氮气分子的平均平动动能和方均根速率;(1)在温度𝑇 = 100℃时;
(2)在温度𝑇 = 0℃时;(3)在温度𝑇 = −150℃时。
2024FENBI理 想 气 体 的 内 能
理想气体分子间势能可忽略不计,故理想气体的内能仅是所有分子热运动动能的总
和,有
𝑖
𝑈 = 𝑛 𝑅𝑇
2
式中,𝑛为理想气体物质的量,𝑖为理想气体分子的自由度。
该公式为理想气体内能的表达式,表明理想气体的内能只与温度有关,仅是温度的
单值函数。
2024FENBI【例1】容器内贮有1mol的某种气体,今从外界输入𝑄热量,测得温度升高Δ𝑇,则该气
体分子的自由度为( )。
2𝑄 𝑅Δ𝑇 𝑄 2𝑅Δ𝑇
A. B. C. D.
𝑅Δ𝑇 2𝑄 2𝑅Δ𝑇 𝑄
2024FENBI热 力 学 基 础
一、热力学第一定律
(一)公式
在热力学过程中,系统吸收的热量𝑄与系统内能的增量∆𝑈 = 𝑈 − 𝑈 及系统对外做的功
2 1
𝐴之间的关系为
𝑄 = ∆𝑈 + 𝐴
该公式说明系统从外界吸收的热量,一部分用于增加内能,一部分用于对外做功。
在准静态过程中,d𝐴 = 𝐹d𝑙 = 𝑝𝑆d𝑙 = 𝑝d𝑉(补充),热力学第一定律可写为
𝑉
2
𝑄 =△ 𝑈 + න 𝑝d𝑉
2024FENBI
𝑉
1【例1】已知热力学系统在某一准静态过程中体积与压强之积保持常量。设初状态压强
为𝑝 ,初状态和末状态的体积各为𝑉 、𝑉 ,求过程中系统所做的功。
1 1 2
2024FENBI【例2】一定量的空气,吸收了1.71 × 10 3 𝐽的热量,并保持在1.0 × 10 5 𝑃𝑎下膨胀,体积从
1.0 × 10 −2 𝑚 3增加到1.5 × 10 −2 𝑚 3,问空气对外做功 ;它的内能改变了 。
2024FENBI(二)应用
1.等容过程
由于体积不变,故d𝑉 = 0,同时𝑝d𝑉 = 0,由热力学第一定律,有d𝑄 = d𝑈,即
𝑉
𝑄 = 𝑈 − 𝑈
𝑉 2 1
式中,下标“𝑉”表示体积不变。
2.等压过程
𝑄 = 𝑈 − 𝑈 + 𝑝 𝑉 − 𝑉
𝑝 2 1 2 1
3.等温过程
等温过程中理想气体的内能不变,Δ𝑈 = 0(此过程中压强变化)。有
𝑉 𝑉
2 2 𝑚 d𝑉 𝑉
2024FEN2 BI
𝑄 = ∫ d𝑄 = ∫ d𝑈 + d𝐴 = ∫ d𝐴 = න 𝑝d𝑉 = න 𝑅𝑇 = 𝑛𝑅𝑇ln
𝑇
𝑀 𝑉 𝑉
𝑉 𝑉 1
1 1理 想 气 体 的 摩 尔 热 容
系统在某一无限小过程中吸收热量d𝑄与温度变化d𝑇的比值称为系统在该过程的热容量,用
𝐶表示,即
d𝑄
𝐶 =
d𝑇
热容量表示在该过程中,温度升高1K时系统吸收的热量,单位是J/K。单位质量的热容量
称为比热容𝑐,单位为J/ K ⋅ kg ,其值由物质和过程决定。热容量与比热容的关系为𝐶 =
𝑀𝑐。
2024FENBI(一)摩尔定容热容
1mol理想气体在等容过程中吸收的热量d𝑄与温度的变化d𝑇之比称为摩尔定容热容,
即
d𝑄 d𝑈 + 𝑝d𝑉 d𝑈 d𝑈
𝐶 = = = =
𝑉,𝑚
d𝑇 d𝑇 d𝑇 d𝑇
𝑉 𝑉 𝑉
上式最后一个等号用到了“理想气体的内能只是温度的单值函数、与体积无关”的结
论。
𝑖
1mol理想气体的内能为𝑈 = 𝑅𝑇,代入上式得
𝑚
2
𝑖
d 𝑅𝑇
d𝑈 2 𝑖
𝐶 = = 2=0𝑅 24FENBI
𝑉,𝑚
d𝑇 d𝑇 2
式中,𝑖是理想气体分子的自由度。(二)摩尔定压热容
1mol理想气体在等压过程中吸收的热量d𝑄与温度的变化d𝑇之比称为摩尔定压热容,
即
d𝑄 d𝑈 + 𝑝d𝑉 𝜕𝑈 𝜕𝑉 d𝑈 𝜕𝑉
𝐶 = = = + 𝑝 = + 𝑝
𝑝,𝑚
d𝑇 d𝑇 𝜕𝑇 𝜕𝑇 d𝑇 𝜕𝑇
𝑝 𝑝 𝑝 𝑝 𝑝
上式最后一个等号用到了“理想气体内能只是温度的函数、与压强无关”的结论。
𝜕𝑉 𝜕𝑉 𝑅
把1mol理想气体的状态方程𝑝𝑉 = 𝑅𝑇带入 求导,得 = ,有
𝜕𝑇 𝜕𝑇 𝑝
𝑝 𝑝
𝐶 = 𝐶 + 𝑅
𝑝,𝑚 𝑉,𝑚
上式称为迈耶方程。
𝑖 𝑖+2
由于𝐶 = 𝑅,得𝐶 = 𝑅。 2024FENBI
𝑉,𝑚 𝑝,𝑚
2 2(三)比热容比
摩尔定压热容与摩尔定容热容之比称为系统的比热容比,用𝛾表示,即
𝐶
𝑝,𝑚
𝛾 =
𝐶
𝑉,𝑚
𝑖 𝑖+2
对于理想气体,𝐶 = 𝑅,𝐶 = 𝑅,则
𝑉,𝑚 𝑝,𝑚
2 2
𝑖 + 2
𝛾 =
𝑖
由上式可以看出,𝛾 > 1,工程上称𝛾为绝热系数。
2024FENBI绝 热 过 程
1.绝热过程方程
(1)定义
如果气体在变化过程中不与外界交换热量,这样的过程称为绝热过程。
(2)方程
绝热过程中d𝑄 = 0,由热力学第一定律得𝑑𝑈 = −𝑝d𝑉,对于理想气体,有d𝑈 = 𝐶 d𝑇,所以
𝑉,𝑚
𝐶 d𝑇 = −𝑝d𝑉。
𝑉,𝑚
由1mol理想气体的状态方程 𝑝𝑉 = 𝑅𝑇 ,可得 𝑝d𝑉 + 𝑉d𝑝 = 𝑅d𝑇 ,联立 𝐶 d𝑇 = −𝑝d𝑉 消去 d𝑇 ,
𝑉,𝑚
𝐶 d𝑉 d𝑝
𝑝,𝑚
有 𝐶 + 𝑅 𝑝d𝑉 + 𝐶 𝑉d𝑝 = 0,因为𝐶 + 𝑅 = 𝐶 ,𝛾 = ,得𝛾 + = 0,积分得
𝑉,𝑚 𝑉,𝑚 𝑉,𝑚 𝑝,𝑚
𝐶 𝑉 𝑝
𝑉,𝑚
𝛾
𝑝𝑉 = 常数
2024FENBI
上式就是理想气体准静态绝热过程方程,还可以写为
𝛾−1 𝛾−1 −𝛾
𝑉 𝑇 = 常数,𝑝 𝑇 = 常数2.准静态绝热过程曲线
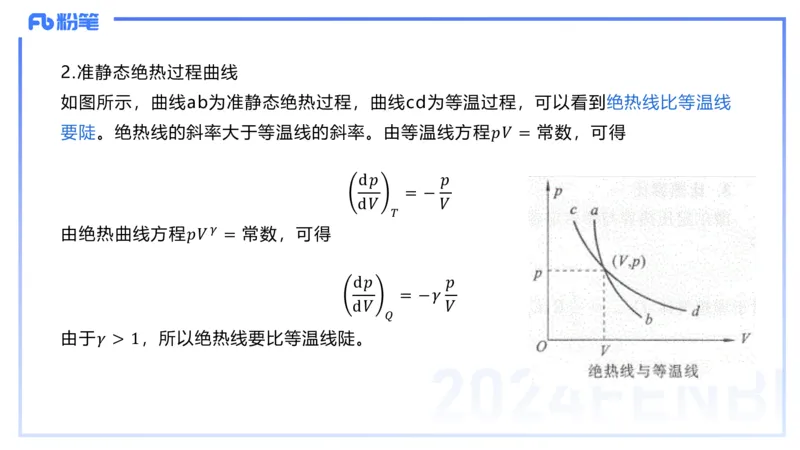
如图所示,曲线ab为准静态绝热过程,曲线cd为等温过程,可以看到绝热线比等温线
要陡。绝热线的斜率大于等温线的斜率。由等温线方程𝑝𝑉 = 常数,可得
d𝑝 𝑝
= −
d𝑉 𝑉
𝑇
𝛾
由绝热曲线方程𝑝𝑉 = 常数,可得
d𝑝 𝑝
= −𝛾
d𝑉 𝑉
𝑄
由于𝛾 > 1,所以绝热线要比等温线陡。
2024FENBI【例1】1𝑚𝑜𝑙单原子理想气体从300K加热到350K,(1)容积保持不变;(2)压强保持不变。
问在这两过程中各吸收了多少热量?增加了多少内能?对外做了多少功?
2024FENBI(一)循环过程
系统从一个状态出发,经过一些列的中间状态,又回到出发时的状态,称系统经历了一个循环过
程,简称循环。循环工作的物质系统称为工作物质,简称工质。
(二)循环过程的效率
1.正循环过程的效率为一个循环过程中系统对外所做的净功与吸收热量之比,即对外输出的净功
占吸收热量的百分比。正循环过程的效率用𝜂表示。设系统在一个循环中从高温热源吸收热量𝑄 ,向
1
低温热源放出热量𝑄 ,则
2
𝐴
净
𝜂 =
𝑄
1
循环过程应遵守热力学第一定律,𝑄 = Δ𝑈 + 𝐴 。一个循环后Δ𝑈 = 0,而𝑄 = 𝑄 − 𝑄 ,所以
净 1 2
𝐴 = 𝑄 − 𝑄 ,因此有
净 1 2
𝑄 − 𝑄 𝑄
1 2 2
𝜂 = = 1 −
2024FENBI
𝑄 𝑄
1 1
𝑄 和𝑄 都是绝对值。
1 22.逆循环过程的制冷系数为从低温物体吸收的热量与外界对系统所做净功之比。逆
循环过程的制冷系数用𝜔表示。设系统从低温热源吸收热量𝑄 ,向高温热源放出热量
2
′
𝑄 ,外界对系统做净功𝐴 ,则
1
净
𝑄
2
𝜔 =
′
𝐴
净
逆循环过程应遵守热力学第一定律,𝑄 = Δ𝑈 − 𝐴 ′ 。一个循环后,Δ𝑈 = 0,则𝐴 ′ = −𝑄 = 𝑄 − 𝑄 ,
净 净 1 2
有
𝑄
2
𝜔 =
𝑄 − 𝑄
1 2
𝑄 和𝑄 都是绝对值。
1 2
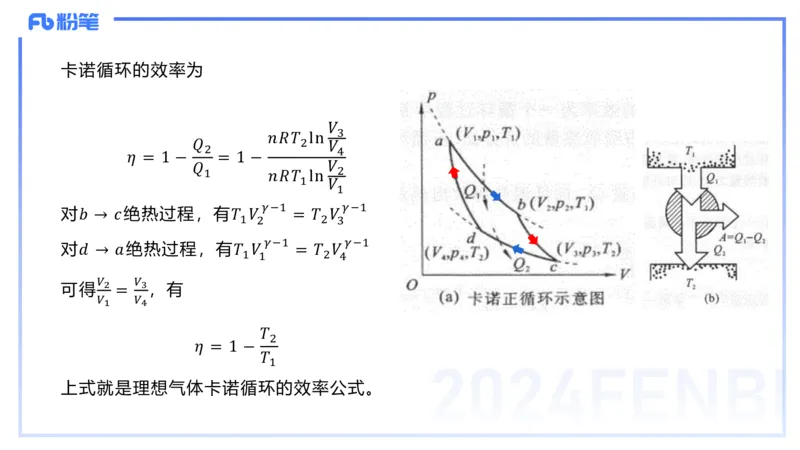
2024FENBI(三)卡诺循环
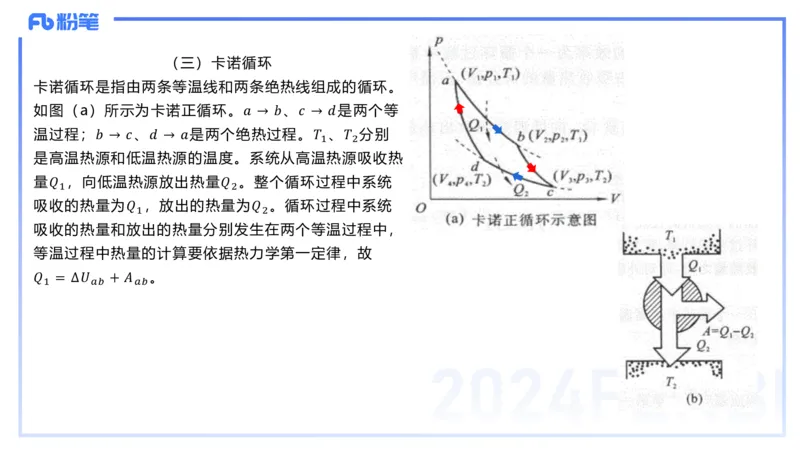
卡诺循环是指由两条等温线和两条绝热线组成的循环。
如图(a)所示为卡诺正循环。𝑎 → 𝑏、𝑐 → 𝑑是两个等
温过程;𝑏 → 𝑐、𝑑 → 𝑎是两个绝热过程。𝑇 、𝑇 分别
1 2
是高温热源和低温热源的温度。系统从高温热源吸收热
量𝑄 ,向低温热源放出热量𝑄 。整个循环过程中系统
1 2
吸收的热量为𝑄 ,放出的热量为𝑄 。循环过程中系统
1 2
吸收的热量和放出的热量分别发生在两个等温过程中,
等温过程中热量的计算要依据热力学第一定律,故
𝑄 = ∆𝑈 + 𝐴 。
1 𝑎𝑏 𝑎𝑏
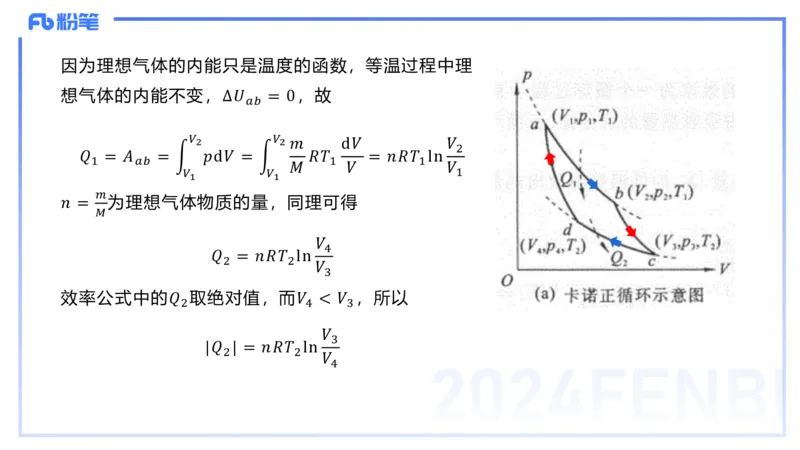
2024FENBI因为理想气体的内能只是温度的函数,等温过程中理
想气体的内能不变,∆𝑈 = 0,故
𝑎𝑏
𝑉 𝑉
2 2 𝑚 d𝑉 𝑉
2
𝑄 = 𝐴 = න 𝑝d𝑉 = න 𝑅𝑇 = 𝑛𝑅𝑇 ln
1 𝑎𝑏 1 1
𝑀 𝑉 𝑉
𝑉 𝑉 1
1 1
𝑚
𝑛 = 为理想气体物质的量,同理可得
𝑀
𝑉
4
𝑄 = 𝑛𝑅𝑇 ln
2 2
𝑉
3
效率公式中的𝑄 取绝对值,而𝑉 < 𝑉 ,所以
2 4 3
𝑉
3
|𝑄 | = 𝑛𝑅𝑇 ln
2 2
𝑉
4
2024FENBI卡诺循环的效率为
𝑉
3
𝑛𝑅𝑇 ln
𝑄 2 𝑉
2 4
𝜂 = 1 − = 1 −
𝑄 𝑉
1 𝑛𝑅𝑇 ln 2
1 𝑉
1
𝛾−1 𝛾−1
对𝑏 → 𝑐绝热过程,有𝑇 𝑉 = 𝑇 𝑉
1 2 2 3
𝛾−1 𝛾−1
对𝑑 → 𝑎绝热过程,有𝑇 𝑉 = 𝑇 𝑉
1 1 2 4
𝑉 𝑉
可得 2 = 3 ,有
𝑉 𝑉
1 4
𝑇
2
𝜂 = 1 −
𝑇
1
2024FENBI
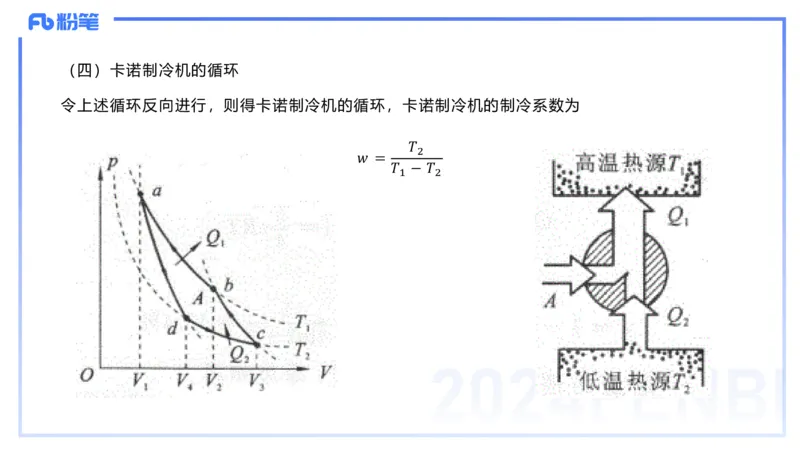
上式就是理想气体卡诺循环的效率公式。(四)卡诺制冷机的循环
令上述循环反向进行,则得卡诺制冷机的循环,卡诺制冷机的制冷系数为
𝑇
2
𝑤 =
𝑇 − 𝑇
1 2
2024FENBI(真题2019上高中)在图所示的理想气体循环中,若𝑇 , 𝑇 , 𝑇 , 𝑇 和𝛾已知,其中𝛾 =
𝑎 𝑏 𝑐 𝑑
𝐶
𝑝
,则其效率𝜂为( )
𝐶
𝑉
𝑇 −𝑇 𝑇 −𝑇
A.1 − 𝛾 𝑑 𝑎 B.1 − 𝛾 𝑐 𝑏
𝑇 −𝑇 𝑇 −𝑇
𝑐 𝑏 𝑑 𝑎
𝑇 −𝑇 𝑇 −𝑇
C.1 − 𝛾 𝑎 𝑑 D.1 − 𝛾 𝑏 𝑐
𝑇 −𝑇 𝑇 −𝑇
𝑐 𝑏 𝑑 𝑎
2024FENBI【例1】一定量的理想气体,经历如图所示的循环过程,𝐴𝐵、𝐶𝐷是等压过程,𝐵𝐶、𝐷𝐴为绝
热过程。已知𝑇 = 300𝐾,𝑇 = 400𝐾,求热机效率和制冷系数。
𝐶 𝐵
2024FENBI