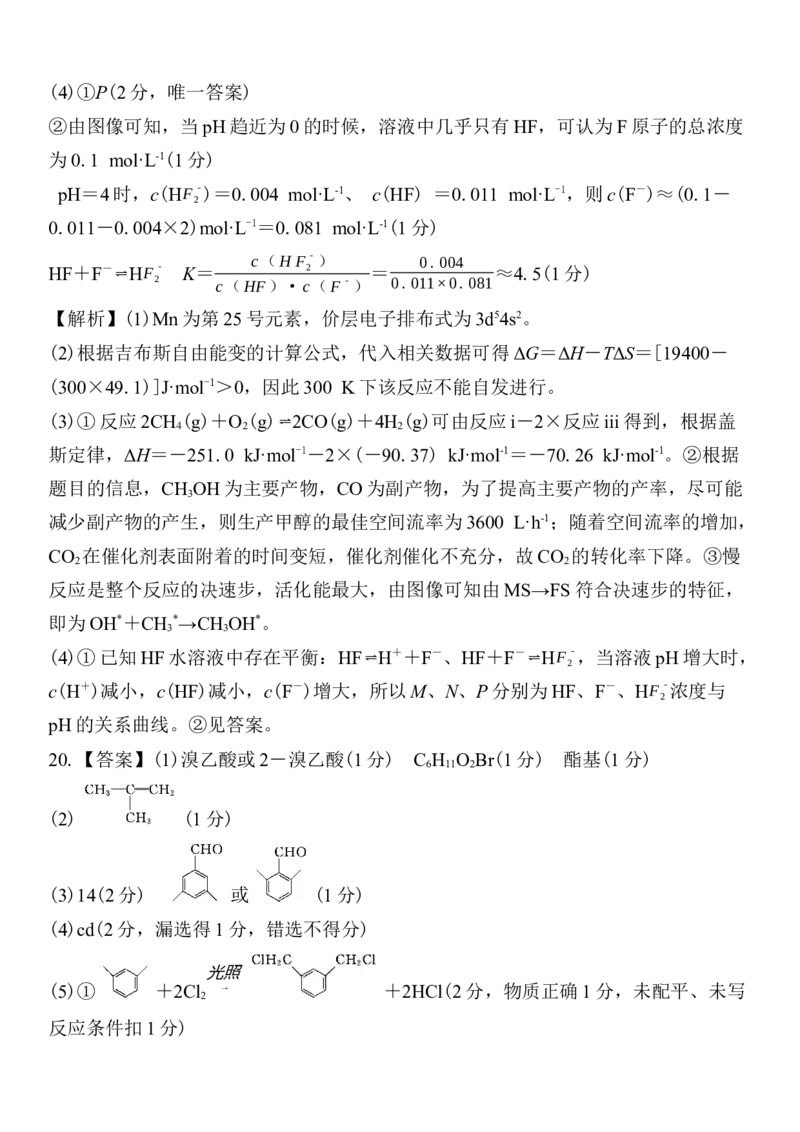
文档内容
广东省2025—2026学年领航高中联盟高三毕业班模拟考试
化学参考答案及评分细则
1.【答案】C
【解析】斑铜孔雀的主要成分属于金属材料,A项不符合题意;香云纱、牛皮皮影的
主要成分是蛋白质,属于有机高分子材料,B、D项不符合题意;陶瓷胚体属于无机
非金属材料,C项符合题意。
2.【答案】D
【解析】基态Al原子的价层电子排布式为3s23p1,故Al位于元素周期表p区,A项错
误;碳纤维属于无机物,B项错误;电镀过程中电能转化为化学能,C项错误;偏二
甲肼[(CH ) NNH ]的结构简式为 ,(CH ) NNH 分子中C、N原子均采
3 2 2 3 2 2
用sp3杂化,D项正确。
3.【答案】B
【解析】分子中的极性键为C—N、 C—H和N—H 键,A项正确;分子式为
C H N,分子中共有21个氢原子,B项错误;分子中含有苯环,苯环中存在大π键,
32 21
C项正确;该分子可以与氢气在催化剂条件下发生加成反应和还原反应,D项正确。
4.【答案】A
【解析】检测奶粉中碳酸钙的含量是基于化学定量分析方法,与碳酸钙的溶解度(S<
0.01 g)无直接关联,A项符合题意;秸秆中含纤维素,纤维素水解可生成葡萄糖,
葡萄糖可发酵转化为乙醇,B项不符合题意;聚乳酸在自然环境中可降解,因此用其
生产气球符合环保要求,C项不符合题意;ClO 具有氧化性,能杀菌消毒,D项不符
2
合题意。
5.【答案】B
【解析】纳米级TiO 为纯净物,不属于分散系,A项错误;碳纳米管与石墨烯均为碳
2
单质,但结构不同,二者互为同素异形体,B项正确;Si N 晶体的硬度大,属于共价
3 4
晶体,C项错误;晶态与非晶态的转换过程中没有新物质生成,属于物理变化,D项
错误。
6.【答案】D【解析】加热NH Cl时,NH 和HCl会在试管口遇冷重新化合生成NH Cl,无法制备
4 3 4
NH ,A项不符合题意;无水CaCl 会与NH 反应生成 CaCl ·8NH ,不能用于干燥
3 2 3 2 3
NH ,B项不符合题意;收集装置没有排空气导管,C项不符合题意;NH 难溶于
3 3
CCl ,将导管插入CCl 层可防止倒吸,从而能安全吸收NH ,D项符合题意。
4 4 3
7.【答案】C
【解析】Y为Na时,b为Na O或Na O ,c为NaCl,应电解熔融的NaCl制备Na,A
2 2 2
项不符合题意;Y为Fe时,铁的氧化物b与盐酸的反应不是氧化还原反应,B项不符
合题意;Y为S时,b为SO ,SO 能使酸性高锰酸钾溶液褪色,C项符合题意;Y为
2 2
N时,b为无色的NO,D项不符合题意。
8.【答案】A
【解析】葡萄糖为多羟基醛,醛基能与新制Cu(OH) 在加热条件下反应生成砖红色沉
2
淀,A项符合题意;氨水中的NH ·H O为弱碱,反应原理为Al3++3NH ·H O
3 2 3 2
Al(OH) ↓+3NH+,B项不符合题意;CuSO 能与H S反应生成黑色
3 4 4 2
沉淀CuS,是因为K (CuS)很小,二者的酸性与该反应的发生无关,且H SO 酸性强
sp 2 4
于H S,C项不符合题意;向溴水中滴加苯,单质Br 在苯中的溶解度大于在水中的溶
2 2
解度,水层褪色,有机层为橙色,该过程为萃取,D项不符合题意。
9.【答案】D
【解析】每个NH 分子中含有3个N—H键,4个NH 分子中含有12个N—H键,
3 3
Cu2+与4个NH 分子形成4个配位键,总计16个共价键,则1 mol [Cu(NH ) ]2+中含
3 3 4
有共价键的数目为16N ,A项错误;溶液中H O分子也可电离出OH-,故溶液中OH
A 2
-的数目无法计算,B项错误;NH 溶于水后,溶液中应同时存在NH+、NH 和
3 4 3
NH ·H O三种微粒,故N(NH+)+N(NH ·H O)<0.1N ,C项错误;基态Cu2+的简化
3 2 4 3 2 A
电子排布式为[Ar]3d9,1 mol基态Cu2+d轨道上的电子数目为9N ,D项正确。
A
10.【答案】D
【解析】CeH 发生反应生成CeH ,故A极发生了氧化反应,A项错误;放电的总反
2 3
应为3NaAlH +6CeH Na AlH +2Al+6CeH ,NaAlH 反应生成了Al,
4 2 3 6 3 4
Al元素的化合价降低,B极为正极,则A极为负极,H-往负极移动,B项错误;放电时,H-嵌入负极,负极质量增加,C项错误;根据总反应方程式可知,正极的电极反
应式为3NaAlH +6e- Na AlH +2Al+6H-,D项正确。
4 3 6
11.【答案】B
【解析】依据横、纵坐标分析,可知a~g依次为第二周期Li~F元素,h、i、j、k依
次为Na、Mg、Si、Cl。第一电离能:Be>B>Li,即b>c>a,A项错误;简单离子
半径:Cl->Na+>Mg2+,B项正确;O 为极性分子,C项错误;SiH 、H O、NH 的中
3 4 2 3
心原子杂化类型相同,孤电子对数越多,键角越小,故键角:SiH >NH >H O,D项
4 3 2
错误。
12.【答案】D
【解析】MnO 与浓盐酸的反应中氧化剂与还原剂的物质的量之比为1:2,A项错误;
2
湿润的有色纸条褪色,干燥的有色纸条不褪色,说明Cl 与H O生成的HClO具有漂
2 2
白性,B项错误;该实验不能比较Br 与I 的氧化性强弱,不能说明氧化性:Cl >Br
2 2 2 2
>I ,C项错误;反应停止后,④中NaOH溶液吸收过量的Cl 生成NaClO,向④中滴
2 2
加浓盐酸后,NaClO可与HCl反应生成Cl ,D项正确。
2
13.【答案】C
【解析】溶液中还含有Cl-,电荷不守恒,A项错误;NaCl溶液浓度很小时,[FeCl ]-
4
浓度会减小,B项错误;加入少量AgNO 固体,Ag+与Cl-反应生成AgCl沉淀,
3
c(Cl-) 减小,平衡Fe3++4Cl-
⇌
[FeCl
4
]-逆向移动,[FeCl
4
]-浓度一定减小,C项正确;
[FeCl ]-为配离子,难以解离,不能拆分为Fe3+和Cl-,D项错误。
4
14.【答案】B
【解析】NH 中的N元素电负性适中且N原子含有孤电子对,易形成配位键,故NH
3 3
是常见的配体,A项不符合题意;甲苯易发生苯环上邻、对位的取代反应是甲基对苯
环的影响,与甲苯中苯环使甲基活化无关,B项符合题意;晶体的自范性是晶体中粒
子在微观空间里呈现周期性有序排列的宏观表象,晶体的某些物理性质的各向异性同
样可以反映晶体内部质点排列的有序性,C项不符合题意;离子液体属于离子化合物,
其沸点高于由分子构成的传统有机溶剂,故C H NH NO 相比于传统有机溶剂沸点更
2 5 3 3
高,难挥发,D项不符合题意。
15.【答案】C【解析】由图可知①②③过程中均不存在非极性键的断裂, 是上述过程生成
的催化剂,A、B项正确; 与Cs CO 反应生成 和
2 3
CsHCO ,体现了 的酸性,C项错误;若R为H,则最终生成的有机物为
3
,根据已知信息可知CH CH —的吸电子能力弱于 ,故
3 2
的酸性强于CH CH COOH,D项正确。
3 2
16.【答案】D
【解析】电极 b 上产生H ,发生还原反应,为阴极,连接外电源的负极,A项正确;
2
结合示意图与溶液环境可知,物质转化关系正确,转移电子数目正确,守恒关系正确
(原子守恒、电荷守恒),B项正确;若隔膜M为阴离子交换膜,则Ⅱ室中n(K+)不变,
但Ⅱ室中存在电极反应:2H O+2e- H ↑+2OH-,反应消耗水,故
2 2
1000×3.66×10-3
c(K+)变大,C项正确;n[Sb(Ⅲ)]= mol=0.03 mol,依据得失电子
122
0.03×2
守恒,n(FeO2-)= mol=0.02 mol,故消耗m(Fe)=0.02×56 g=1.12 g,D
4 3
项错误。
17.【答案】(1)三颈(口)烧瓶(1分)
(2)酸性、(强)氧化性(2分,1个1分)
(3)①3BaSO +2H++2NO- 2NO↑+3BaSO +H O(2分,物质正确1分,
3 3 4 2
未配平、未写“↑”扣1分)
②稀硝酸可能被溶解在溶液中的SO 或H SO 还原(1分)
2 2 3
③装置A中的硫酸以酸雾的形式进入装置B中与Ba2+反应生成BaSO (2分)
4
(4)①1.68(2分)
②6.0×10-8(2分)
③1.2×10-8(2分)
【解析】(1)仪器X的名称为三颈(口)烧瓶。△
(2)装置A中发生反应:Cu+2H SO (浓) CuSO +2H O+SO ↑,浓硫酸体现
2 4 4 2 2
了酸性和强氧化性。
(3)①BaSO 与稀硝酸反应的离子方程式为3BaSO +2H++2NO- 2NO↑
3 3 3
+3BaSO +H O。②SO 易溶于水,有较多的SO 会溶解在BaCl 溶液中,SO 和
4 2 2 2 2 2
H SO 也能还原稀硝酸。③实验过程中,装置A中有白雾产生,白雾是硫酸酸雾,会
2 3
进入装置B中与Ba2+反应生成BaSO 。
4
K (H SO )×K (H SO )
(4)①Ba2++H
2
SO 3⇌BaSO
3
+2H+的化学平衡常数K= a 1 2
K
3
(BaSO
a 2
)
2 3 =
sp 3
1.4×10-2×6.0×10-8
=1.68。②由于H SO 的K ≫K ,说明溶液中c(SO2-)与H SO
5.0×10-10 2 3 a 1 a 2 3 2 3
的初始浓度几乎无关,c(SO2-)与H SO 的K 有关,且可近似认为c(H+)≈c(HSO-),
3 2 3 a 2 3
因此c(SO2-)≈K =6.0×10-8 mol·L-1。③将新制的饱和H SO 溶液与浓度为0.4
3 a 2 2 3
mol·L-1的BaCl 溶液等体积混合瞬间,c(Ba2+)=0.2 mol·L-1,由②可知c(SO2-
2 3
)≈6.0×10-8 mol·L-1,则此时溶液中离子积Q(BaSO )≈0.2×6.0×10-8=1.2×10-
3
8。
18.【答案】(1)将废渣粉碎、适当升温、适当增加硫酸用量等(1分,答对一条即可)
(2)CaSO (1分)
4
(3)钪与萃取剂中的O原子形成配位键生成稳定的配合物(1分);配合物中存在长链烷
烃基,具有疏水性(1分,合理表述即可)
(4)6Fe3++2Na++6CO2-+4SO2-+6H O Na Fe (SO ) (OH) ↓+
3 4 2 2 6 4 4 12
6CO ↑(2分,物质正确1分,未配平、未写“↑、↓”扣1分) pH过高Fe3+会水解生
2
成胶状或絮状的Fe(OH) ,不利于过滤分离(1分);pH过低,不利于生成
3
Na Fe (SO ) (OH) (1分,类似表述均可,多答pH过高,钴和镍会沉淀不扣分)
2 6 4 4 12
(5)H SO (1分)
2 4
(59×4+28×8)×1021
(6)8(2分,写八不扣分) C(1分) 4 3 (2分,无论化简至哪一步,
N ×( a)
A ❑√3
没有错误均不扣分,数量级错误扣1分)【解析】(1)“焙烧”中为了使废渣充分反应,可采取的措施有将废渣粉碎、适当升
温、适当增加硫酸用量等。
(2)废渣中含有的石英(SiO )、石膏(CaSO ·2H O)最终以浸出渣的形式分离出来,故
2 4 2
所得浸出渣的主要成分为SiO 、CaSO 。
2 4
(3)从钪与萃取剂形成的配合物的结构可知,钪能从水溶液中被萃取进入有机相的原
因是钪能与萃取剂中的O原子形成配位键生成稳定的配合物,且配合物中存在长链烷
烃基,具有疏水性。
(4)铁元素经过“氧化”生成Fe3+,“除铁”中,溶液pH为4.0~4.5,CO2-转化为
3
气体CO ,故该反应的离子方程式为6Fe3++2Na++6CO2-+4SO2-+6H O
2 3 4 2
Na Fe (SO ) (OH) ↓+6CO ↑。pH过高Fe3+会水解生成胶状或絮状的Fe(OH) ,不利
2 6 4 4 12 2 3
于过滤分离;pH过低,不利于生成Na Fe (SO ) (OH) ,导致除铁效果不佳。
2 6 4 4 12
(5)由“已知②”分析,“一系列操作”为先加入稀硫酸、后加入氨水调节pH,得到
的含Sc3+的溶液主要溶质为Sc (SO ) ,“沉钪”中加入草酸后,滤液中含有硫酸,
2 4 3
可在“酸浸”中循环利用。
(6)已知Si原子填充在Co原子形成的正四面体中心,故Co原子在晶胞的顶点与面心,
Si原子在立方晶胞体内,则1个晶胞中含有4个Co原子与8个Si原子,距离Co原子
最近且等距的Si原子有8个;沿着y轴方向的投影图要注意不能忽略面心的Co原子,
C项符合题意。Si原子与Co原子之间的最短距离为正四面体中Si原子与Co原子的距
(59×4+28×8)×1021
4
离,则晶胞参数为 a nm,故晶体密度ρ= 4 g·cm-3。
❑√3 N ×( a)3
A ❑√3
19.【答案】(1)3d54s2(1分)
(2)不能(1分)
(3)①-70.26(2分)
②3600(1分) 随着空间流率的增加,反应物与催化剂接触的时间变短,催化不充分
(2分)
③OH*+CH *→CH OH*(2分,物质正确1分,配平1分,“→”写成“
3 3
、 ”不扣分)
⇌(4)①P(2分,唯一答案)
②由图像可知,当pH趋近为0的时候,溶液中几乎只有HF,可认为F原子的总浓度
为0.1 mol·L-1(1分)
pH=4时,c(HF-)=0.004 mol·L-1、 c(HF) =0.011 mol·L-1,则c(F-)≈(0.1-
2
0.011-0.004×2)mol·L-1=0.081 mol·L-1(1分)
c(H F-) 0.004
HF+F- ⇌HF- K= 2 = ≈4.5(1分)
2 c(HF)·c(F-) 0.011×0.081
【解析】(1)Mn为第25号元素,价层电子排布式为3d54s2。
(2)根据吉布斯自由能变的计算公式,代入相关数据可得ΔG=ΔH-TΔS=[19400-
(300×49.1)]J·mol-1>0,因此300 K下该反应不能自发进行。
(3)①反应2CH
4
(g)+O
2
(g) ⇌2CO(g)+4H
2
(g)可由反应i-2×反应iii得到,根据盖
斯定律,ΔH=-251.0 kJ·mol-1-2×(-90.37) kJ·mol-1=-70.26 kJ·mol-1。②根据
题目的信息,CH OH为主要产物,CO为副产物,为了提高主要产物的产率,尽可能
3
减少副产物的产生,则生产甲醇的最佳空间流率为3600 L·h-1;随着空间流率的增加,
CO 在催化剂表面附着的时间变短,催化剂催化不充分,故CO 的转化率下降。③慢
2 2
反应是整个反应的决速步,活化能最大,由图像可知由MS→FS符合决速步的特征,
即为OH*+CH *→CH OH*。
3 3
(4)①已知HF水溶液中存在平衡:HF⇌H++F-、HF+F- ⇌HF-,当溶液pH增大时,
2
c(H+)减小,c(HF)减小,c(F-)增大,所以M、N、P分别为HF、F-、HF-浓度与
2
pH的关系曲线。②见答案。
20.【答案】(1)溴乙酸或2-溴乙酸(1分) C H O Br(1分) 酯基(1分)
6 11 2
(2) (1分)
(3)14(2分) 或 (1分)
(4)cd(2分,漏选得1分,错选不得分)
光照
(5)① +2Cl → +2HCl(2分,物质正确1分,未配平、未写
2
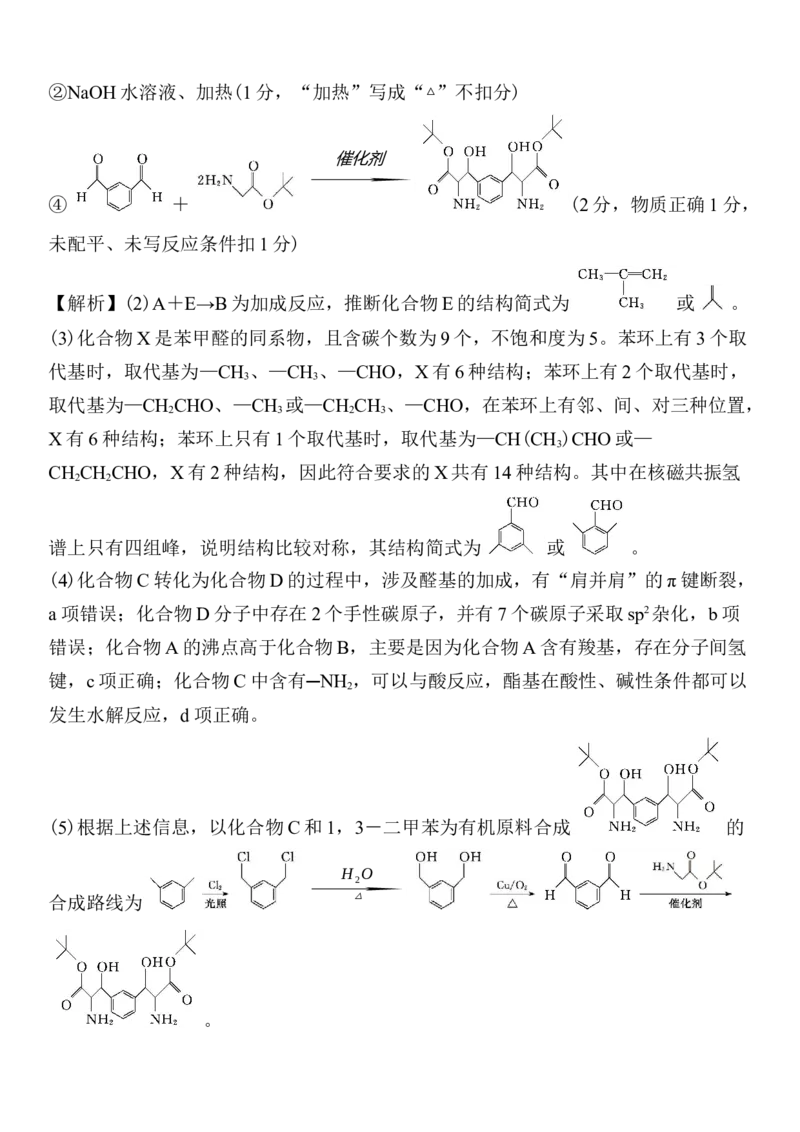
反应条件扣1分)②NaOH水溶液、加热(1分,“加热”写成“△”不扣分)
催化剂
⃗
④ + (2分,物质正确1分,
未配平、未写反应条件扣1分)
【解析】(2)A+E→B为加成反应,推断化合物E的结构简式为 或 。
(3)化合物X是苯甲醛的同系物,且含碳个数为9个,不饱和度为5。苯环上有3个取
代基时,取代基为—CH 、—CH 、—CHO,X有6种结构;苯环上有2个取代基时,
3 3
取代基为—CH CHO、—CH 或—CH CH 、—CHO,在苯环上有邻、间、对三种位置,
2 3 2 3
X有6种结构;苯环上只有1个取代基时,取代基为—CH(CH )CHO或—
3
CH CH CHO,X有2种结构,因此符合要求的X共有14种结构。其中在核磁共振氢
2 2
谱上只有四组峰,说明结构比较对称,其结构简式为 或 。
(4)化合物C转化为化合物D的过程中,涉及醛基的加成,有“肩并肩”的π键断裂,
a项错误;化合物D分子中存在2个手性碳原子,并有7个碳原子采取sp2杂化,b项
错误;化合物A的沸点高于化合物B,主要是因为化合物A含有羧基,存在分子间氢
键,c项正确;化合物C中含有─NH ,可以与酸反应,酯基在酸性、碱性条件都可以
2
发生水解反应,d项正确。
(5)根据上述信息,以化合物C和1,3-二甲苯为有机原料合成 的
H O
2
合成路线为 ⃗ △
。