文档内容
福建省漳州市 2025 届高三毕业班第四次教学质量检测
化学试题解析
一、选择题
1.A
【解析】B中碳量子点不是碳单质;C中碳量子点含有羟基、羧基等,可与H O形成分子间氢键,故水溶
2
性更好;D中碳量子点是纳米材料,但需要分散到分散剂中才能产生丁达尔效应。
2.C
【解析】A中含中子数目应为7N ;B中每个NO-中N含3对价层电子对;C中生成0.6molHN 时转移
A 2 3
1
电子为
3( )
0.6mol=2mol;D中HN
3
是弱酸,N-
3
会水解,数目小于0.1N
A
。
3
3.B
【解析】B中稀硝酸的还原产物为NO,故应为:3Ag+4H++NO-=3Ag++NO↑+2H O。
3 2
4.D
【解析】Z为第四周期元素,显-1价,Z为Br。W可与X、Y分别形成1个共价键,W为H,W、X和Y
的原子序数之和为14,且X可形成4个共价键,Y可形成3个共价键,由此可推X为C,Y为N。
A中N的原子半径小于Br,H-N键长更短,键能更大;B中NH Br为离子晶体,熔点更高,CBr
4 4
为分子晶体;C中电负性应为N>C>H;D中有机物CBr NH 中–CBr 为吸电子基团,导致N的电子云
3 2 3
密度降低,结合H+的能力减弱,CH NH 中–CH 为推电子基团,使N的电子云密度增大,结合H+的能
3 2 3
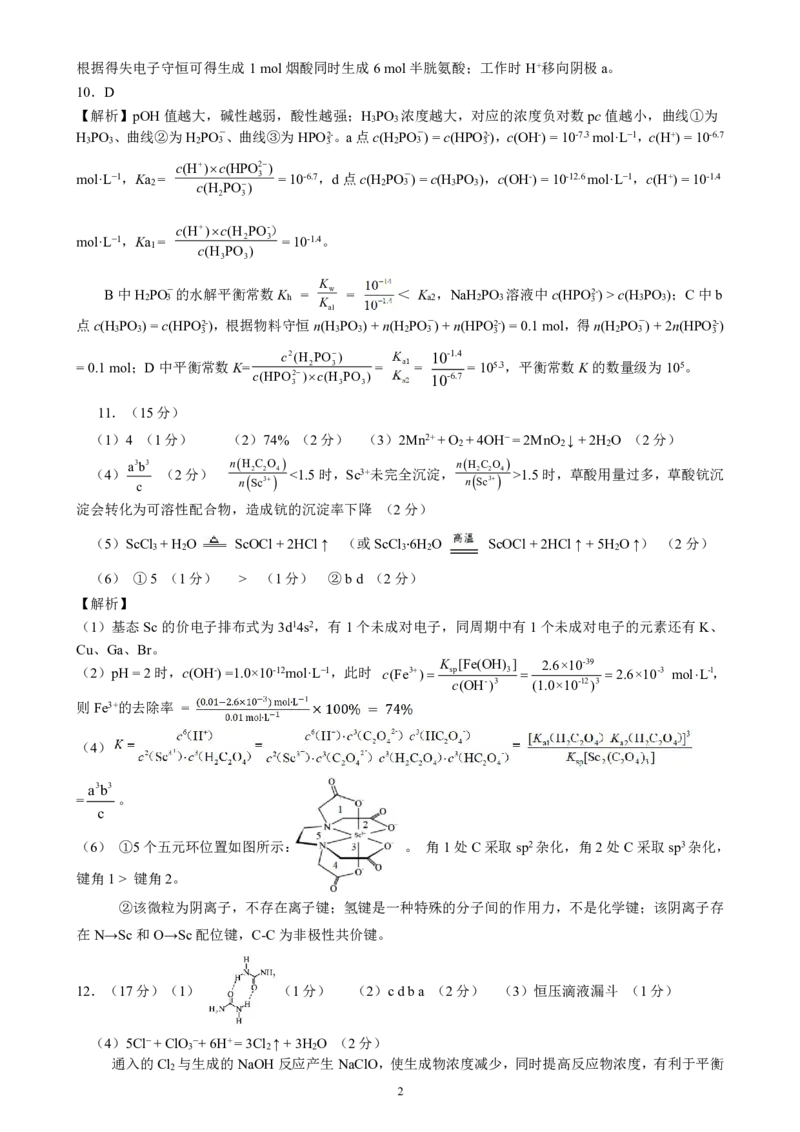
力增强,故碱性XZ YW c(H PO );C中b
2 3 h K a2 2 3 3 3 3
a1
点c(H PO )=c(HPO2-),根据物料守恒n(H PO )+n(H PO-)+n(HPO2-)=0.1mol,得n(H PO-)+2n(HPO2-)
3 3 3 3 3 2 3 3 2 3 3
c2(H PO) 10-1.4
=0.1mol;D中平衡常数K= 2 3 = = =105.3,平衡常数K的数量级为105。
c(HPO2)c(H PO ) 10-6.7
3 3 3
11.(15分)
(1)4 (1分) (2)74% (2分) (3)2Mn2++O +4OH−=2MnO ↓+2H O (2分)
2 2 2
a3b3 nH C O nH CO
(4)
c
(2分)
n S
2
c3
2
4 <1.5时,Sc3+未完全沉淀,
n S
2
c3
2
4 >1.5时,草酸用量过多,草酸钪沉
淀会转化为可溶性配合物,造成钪的沉淀率下降 (2分)
(5)ScCl +H O ScOCl+2HCl↑ (或ScCl ·6H O ScOCl+2HCl↑+5H O↑) (2分)
3 2 3 2 2
(6) ①5 (1分) > (1分) ②bd (2分)
【解析】
(1)基态Sc的价电子排布式为3d14s2,有1个未成对电子,同周期中有1个未成对电子的元素还有K、
Cu、Ga、Br。
K [Fe(OH) ] 2.6×10-39
(2)pH=2时,c(OH-)=1.0×10-12mol·L−1,此时 c(Fe3) sp 3 2.6×10-3 molL-1,
c(OH-)3 (1.0×10-12)3
则Fe3+的去除率 =
(4)
a3b3
= 。
c
(6) ①5个五元环位置如图所示: 。 角1处C采取sp2杂化,角2处C采取sp3杂化,
键角1> 键角2。
②该微粒为阴离子,不存在离子键;氢键是一种特殊的分子间的作用力,不是化学键;该阴离子存
在N→Sc和O→Sc配位键,C-C为非极性共价键。
12.(17分)(1) (1分) (2)cdba (2分) (3)恒压滴液漏斗 (1分)
(4)5Cl−+ClO −+6H+=3Cl ↑+3H O (2分)
3 2 2
通入的Cl 与生成的NaOH反应产生NaClO,使生成物浓度减少,同时提高反应物浓度,有利于平衡
2
2正向移动,提高产率 (2分)
(5)C H N O +9Cl +3H O=3NCl +3CO +9HCl (2分) (6)AgNO 溶液 (1分)
3 3 3 3 2 2 3 2 3
(7)用锥形瓶内壁将半滴溶液沾落,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁 (2分)
(8) (2分) (2分) (9)ac (2分)
【解析】
(2)各装置的作用为:A制取二氯异氰尿酸钠溶液;B除去Cl 中混有的HCl,避免HCl与NaOH溶液反
2
应,降低产率;C为干燥,但本题Cl 无需干燥;D尾气处理。
2
(3)恒压滴液漏斗可平衡压强,使液体顺利流下。
(6)过滤后,粗产品表面含有少量的NaCl杂质,判断是否洗涤干净,需检验洗涤液中是否含有Cl-
(8)根据得失电子守恒可知各物质所消耗量关系为C N O Cl −~2I ~4S O 2−,
3 3 3 2 2 2 3
1 1
n(C N O Cl Na)= n(Na S O )= ×cmol·L−1×V×10-3L=2.5×10-4cVmol,
3 3 3 2 4 2 2 3 4
2.5 ×10 -4 cVmol 100mL 220gmol 1
10.00mL 0.55cV
粗产品的纯度为 100% 100%
mg m
(9)b.滴定前有气泡,初始读数偏小,滴定后无气泡,终点读数不变,V偏大,结果偏高;
c.滴定管未润洗,消耗V偏大,结果偏高;d.滴定终点仰视刻度线,终点读数偏大,V偏大,结果偏高。
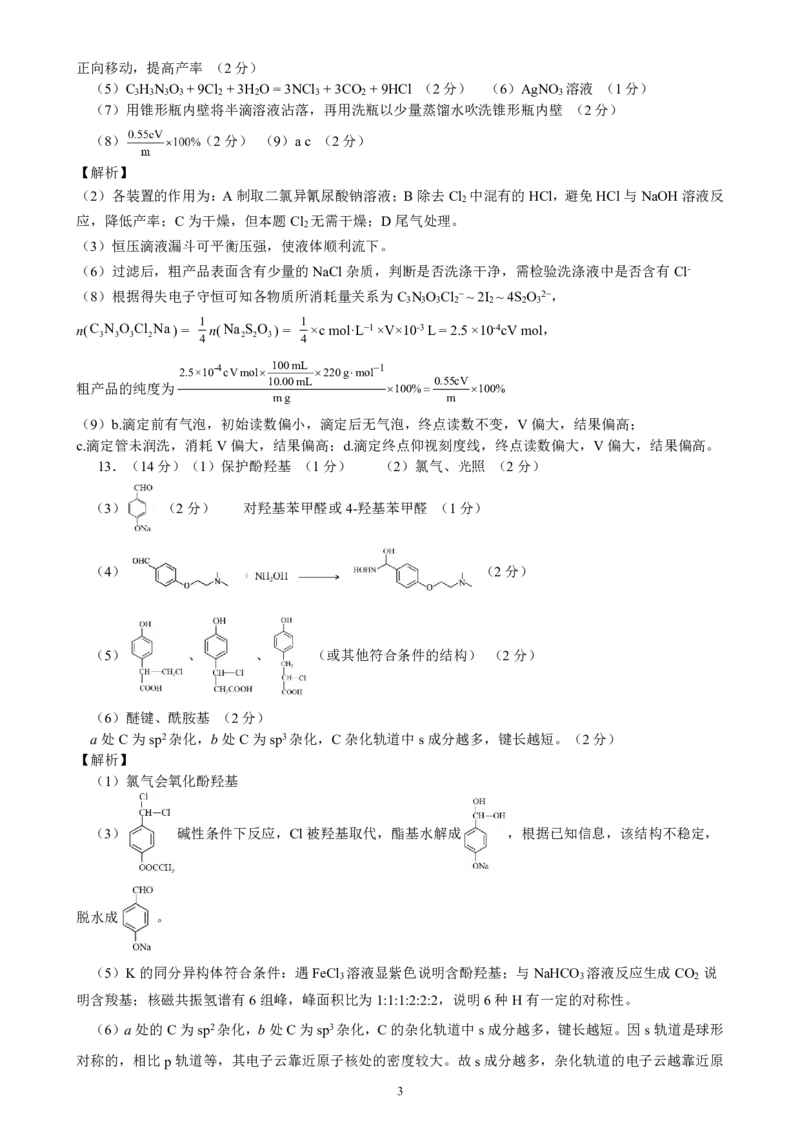
13.(14分)(1)保护酚羟基 (1分) (2)氯气、光照 (2分)
(3) (2分) 对羟基苯甲醛或4-羟基苯甲醛 (1分)
(4) (2分)
(5) 、 、 (或其他符合条件的结构) (2分)
(6)醚键、酰胺基 (2分)
a处C为sp2杂化,b处C为sp3杂化,C杂化轨道中s成分越多,键长越短。(2分)
【解析】
(1)氯气会氧化酚羟基
(3) 碱性条件下反应,Cl被羟基取代,酯基水解成 ,根据已知信息,该结构不稳定,
脱水成 。
(5)K的同分异构体符合条件:遇FeCl 溶液显紫色说明含酚羟基;与NaHCO 溶液反应生成CO 说
3 3 2
明含羧基;核磁共振氢谱有6组峰,峰面积比为1:1:1:2:2:2,说明6种H有一定的对称性。
(6)a处的C为sp2杂化,b处C为sp3杂化,C的杂化轨道中s成分越多,键长越短。因s轨道是球形
对称的,相比p轨道等,其电子云靠近原子核处的密度较大。故s成分越多,杂化轨道的电子云越靠近原
3子核,键长越短。
14.(14分)(1) (1分) (2) ①400 (1分)
+
②反应速率随温度升−高6增大,该温度范围内催化剂活性随温度升高而增强,反应速率增大,单位时间
内转化率增大 (2分)
③未达到 (1分) M点相同温度时,不同催化剂下氮氧化物转化率还能增大 (1分)
(3)①0.05 (2分) ② (2分)
(4)①12 (1分) N (1分) ② (2分)
【解析】(1)由盖斯定律可知:∆H=1(∆H +∆H )。
1 2
6
(3)方法一 :设反应ⅰ消耗NO的物质的量为6amol、反应ⅲ消耗的NO物质的量为8bmol,列三段式:
ⅰ:4NH (g)+6NO(g) 5N (g)+6H O(g)
3 2 2
起始n/(mol) 1 2 0 0
转化n/(mol) 4a 6a 5a 6a
平衡n/(mol) 1-4a-2b 2-6a-8b 5a 6a+3b
ⅲ:2NH (g)+8NO(g) 5N O(g)+3H O(g)
3 2 2
起始n/(mol) 1 2 0 0
转化n/(mol) 2b 8b 5b 3b
平衡n/(mol) 1-4a-2b 2-6a-8b 5b 6a+3b
因NO转化率为70%则有6a+8b=1.4mol;因N 选择性为50%则有 =0.5,解得a=0.1、b=0.1;
2
5
则平衡时:n(总)=n(NH )+n(NO)+n(N )+n(N O)+n(H O)=0.4mo5l ++50 .6mol+0.5mol+0.5mol+0.9
3 2 2 2
mol=2.9mol,反应ⅰ的平衡常数 。
方法二:由题意可知转化的NO物质的量为2×70%=1.4mol;设生成的N 的物质的量为xmol,因
2
N 的选择性为50%,则生成的n(N O)=xmol;转化的NH 分别为反应ⅰ:n(NH )=0.8xmol、反应ⅲ:n(NH )
2 2 3 3 3
=0.4xmol;根据N原子守恒:转化的n(NH )+n(NO)=2×[n(N )+n(N O)],即(0.8x+0.4x)+1.4=4x,解
3 2 2
得:x=0.5mol。故平衡时n(NH )=1-(0.8x+0.4x)=0.4mol;n(NO)=2-1.4=0.6mol;n(N )=n(N O)=
3 2 2
3
0.5mol。根据H原子守恒:平衡时n(H O)= 转化 =0.9mol。后续解法同上。
2
(NH3)
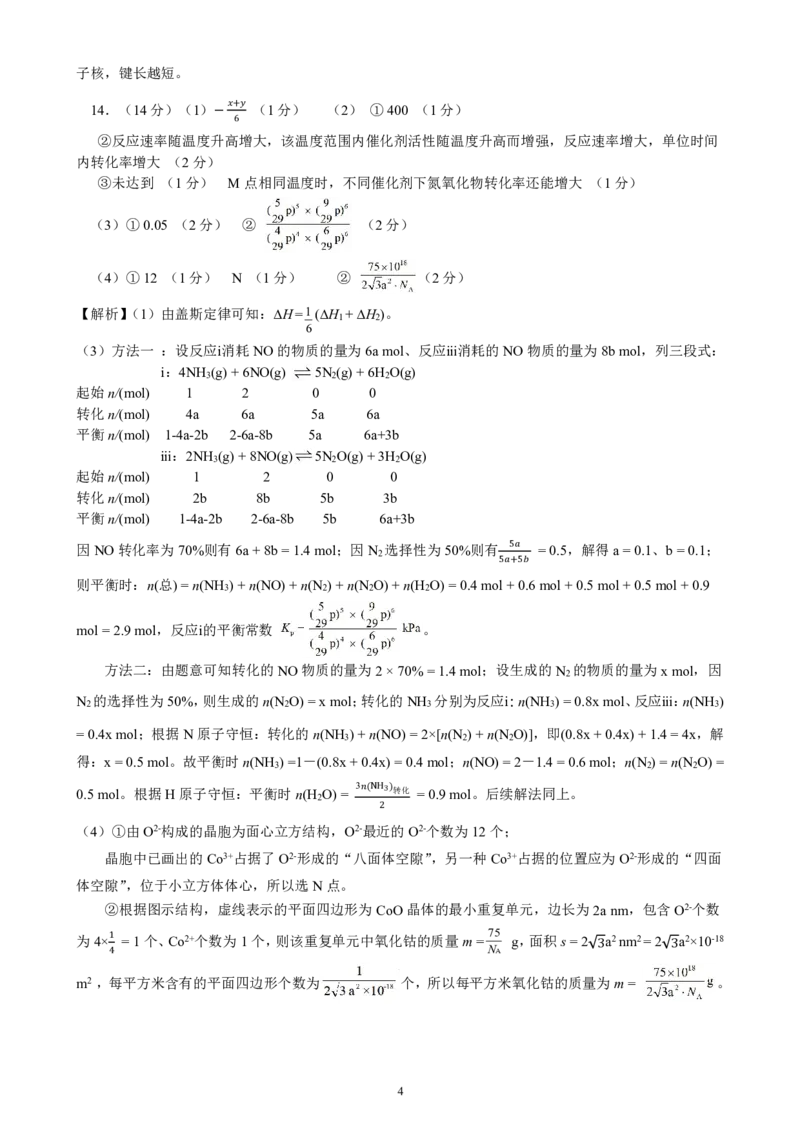
(4)①由O2-构成的晶胞为面心立方结构,O2-最近2 的O2-个数为12个;
晶胞中已画出的Co3+占据了O2-形成的“八面体空隙”,另一种Co3+占据的位置应为O2-形成的“四面
体空隙”,位于小立方体体心,所以选N点。
②根据图示结构,虚线表示的平面四边形为CoO晶体的最小重复单元,边长为2anm,包含O2-个数
75
为4× =1个、Co2+个数为1个,则该重复单元中氧化钴的质量m= g,面积s=2 a2nm2=2 a2×10-18
1
NA
4 3 3
m2 ,每平方米含有的平面四边形个数为 个,所以每平方米氧化钴的质量为m= 。
4