文档内容
高三化学参考答案
1 2 3 4 5 6 7
B A C D B B A
8 9 10 11 12 13 14
C B C C D C D
分 除标注外其它每空 分
15.(15 , 2 )
【答案】 分 分
(1)O>N>C>H (1 ) 6(1 )
恒压滴液漏斗 分 的 水浴加热
(2) (1 ) (70℃ )
防止 氧化
2+
(3) Fe
降低甘氨酸亚铁的溶解度 使其结晶析出
(4) ,
- 2+ + 3+ 2+
(5)①MnO4 +5Fe +8H 5Fe +Mn +4H2O
漏选且正确得 分
②AB( 1 ) ③40
分 除标注外其它每空 分
16.(14 , 2 )
【答案】 分 分
(1)f(1 ) (1 )
以增大固体与气体接触面积 增大氧气浓度 提高焙烧速率并且使反应更充分 合
(2) , , (
理即可
)
+ 3+
(3)2CeO2+6H +H2O22Ce +O2↑+4H2O
(4)9
或
-
(5)NaCl( Cl )
△ 条件有无加热都给分
(6)Ce(OH)4+6HNO3 H2Ce(NO3)6+4H2O( )
用玻璃棒向漏斗中引流入浓硝酸至固体全部浸没 待溶液自然流出 重复 次
(7) , , 2~3
合理即可
( )
分 每空 分
17.(14 , 2 )
【答案】
-1
(1)-166kJ·mol
t t t
(2)① 1< 2< 3
反应 是气体分子数减小的反应 增大压强 平衡正向移动 促进了反应 正向移
② ⅱ , , , ⅰ
动 因此温度一定 增大压强 的转化率增大 或总反应是气体分子数减小的反应
, , CO2 ( ,
增大压强 平衡正向移动 的转化率增大 解释合理即可
, ,CO2 , )
的体积比值小于 时 提高 浓度 促进反应 化学平衡正向移动 提高
③H2/CO2 2 , H2 , ⅰ ,
的转化率 比值高于 时 会促进 与 反应 生成甲烷 从而降低 选择性
CO2 ; 2 , CO H2 , , CO
解释合理即可
( )
-1 -1
(3)①CO2 ②0.012mol·L ·min ③0.57
高三化学参考答案 第 页(共 页)
1 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}分 除标注外其它每空 分
18.(15 , 2 )
【答案】 醚键 分 氰基 顺序可互换 分
(1) (1 ) ( ,1 )
对甲基苯酚 甲基苯酚
(2) (4- )
漏选且正确得 分
(3)①⑤( 1 )
吡啶具有碱性 中和反应 的生成物 促进反应正向进行 提高产率 答案合理
(4) , ⑥ HBr, , (
即可
)
(5)12
分
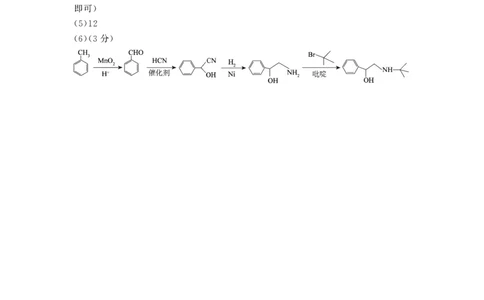
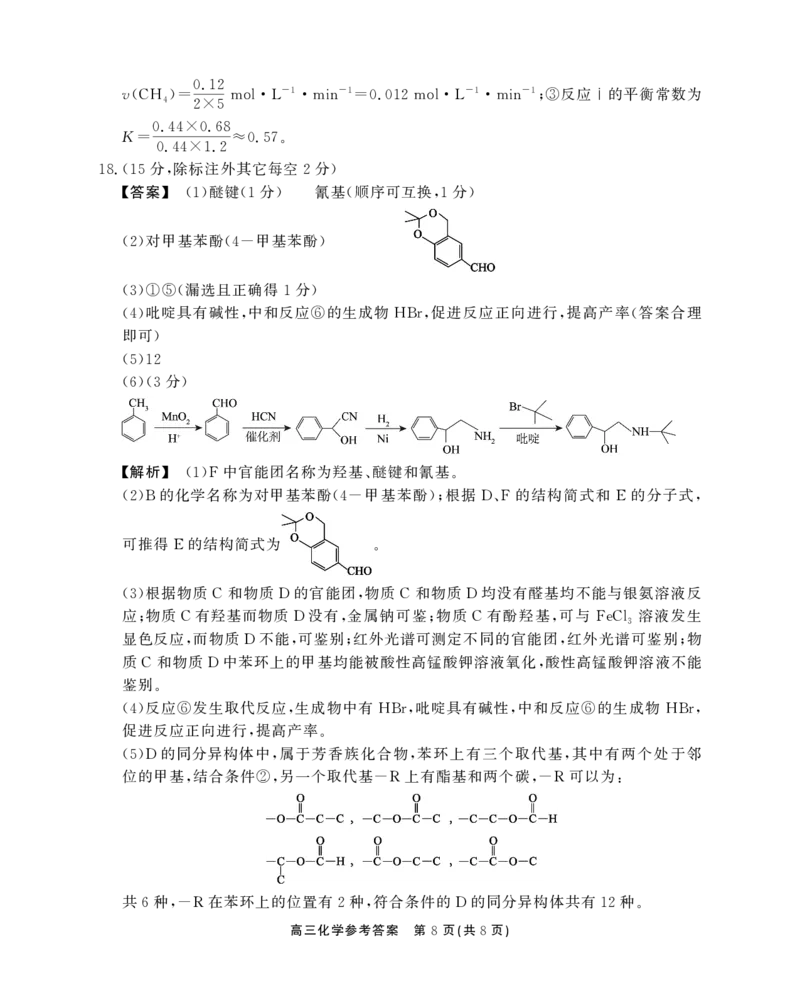
(6)(3 )
高三化学参考答案 第 页(共 页)
2 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}答案详解
【答案】
1. B
【解析】 氯乙烷常温下为气态 喷洒氯乙烷喷雾汽化时吸收热量 使运动员受伤部位起
, ,
到降温麻醉和镇痛作用 项正确 人体中没有水解纤维素的酶 在人体中纤维素的作
,A ; ,
用是促进胃肠蠕动 帮助消化 项错误 有机玻璃主要的化学成分是聚甲基丙烯酸甲
, ,B ;
酯 其结构简式为 项正确 生物柴油是由油脂转化而成的 含有
, : ,C ; , C、H、O
元素 项正确
,D 。
【答案】
2. A
【解析】 价层电子对数为 模型为四面体形 不是三角锥形 项错误
NH3 4,VSEPR , ,A ;
碳原子的电负性小于氧原子的电负性 碳氧成键时 共用电子对偏向氧 使氧相对显负
, , ,
项正确 晶态二氧化硅的 射线
电 醛基中碳氧双键上的电荷分布示意图
, : ,B ; X
衍射峰是锐峰 窄峰 而非晶态二氧化硅粉末的 射线衍射峰呈弥散状 项正确
( ), X ,C ;O2
分子中 键是由两个原子的 轨道 肩并肩 重叠形成的 形成示意图为
p-pπ p “ ” ,
项正确
,D 。
【答案】
3. C
【解析】 根据 和 的结构简式可知 发生取代反应生成 和 项正确 苯
E F ,E、F G HCl,A ;
环确定的平面与碳碳双键确定的平面绕单键旋转 所有碳原子可在同一平面上 项正
, ,B
确 化合物 分子中 原子均有孤对电子 故均能与盐酸反应生成盐酸盐 项错
; E、G N , ,C
误 存在顺反异构必须有碳碳双键 且双键两端的原子或原子团互不相同 化合物
; , , F、G
均符合 项正确
,D 。
【答案】
4. D
【解析】 根据题干信息和结构图可推得 元素 分别为 根
, W、X、Y、Z、R H、C、N、F、Al。
据同一周期第一电离能整体变化规律 可知 项错误 和 具有相同的
- 3+
, F>N>C,A ;F Al
核外电子排布 核电荷数大 离子半径小 项错误 和 分子间都存在氢
3+
,Al , ,B ;HF NH3
键 但 的电负性更大 形成的氢键更强 故 沸点更高 标况下为液态 项错误
, F , , HF , ,C ;Al
最外层只有 个电子 有空轨道 获得 个电子为 提供一对电子形成配位键 项
3 , ,F 1 Al ,D
正确
。
【答案】
5. B
【解析】 每个 分子中含有的价电子总数为 标准状况下 含有的价电子
B2H6 12, ,2.24L
总数为 N 项错误 每个 分子中含有的 键数为 即 含
1.2 A,A ; NH3BH3 σ 7,3.1g 0.1mol
有的 键数为 N 项正确 硼酸 是一元弱酸 -1 的
σ 0.7 A,B ; (H3BO3) ,1L0.1mol·L
溶液中 + 数小于 N 项错误 乙硼烷水解反应方程式为
H3BO3 H 0.1 A,C ; :B2H6+6H2O
高三化学参考答案 第 页(共 页)
3 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}中 价 和 中 价 发生归中反应 生成
2H3BO3+6H2↑,B2H6 -1 H H2O +1 H , 2g
转移的电子总数为N 项错误
H2 A,D 。
【答案】
6. B
【解析】 中 原子无孤对电子 而 中 原子有孤对电子 孤对电子对成
NH3BH3 N , NH3 N ,
键电子斥力大 故 键角 项错误 从立方氮化硼晶胞结构
, H-N-H :NH3BH3>NH3,A ;
可知 和 的配位数均为 故均为 杂化 项正确 中心原子 价层电子对
3
,N B 4, sp ,B ;BCl3 B
数为 无孤对电子 为 杂化 分子的空间结构为平面三角形 正负电荷重合故
2
3, , sp 。BCl3 ,
为非极性分子 项错误 从硼酸晶体二维平面结构可知 每个分子可形成 个氢键 每
,C ; , 6 ,
个氢键由两个分子共有 故 硼酸晶体中含有 氢键 项错误
, 1mol 3mol ,D 。
【答案】
7. A
【解析】 稀溶液存在 离子呈蓝色 加入足量 固体 生成黄绿
2+
CuSO4 [Cu(H2O)4] , NaCl ,
色的 说明存在 转化为 的平衡 项正确 酸性
2- 2+ 2-
[CuCl4] , [Cu(H2O)4] [CuCl4] ,A ;
溶液过量 不能褪色 实验方案设计不合理 项错误 溶液中含重金属
KMnO4 , , ,B ;CuSO4
离子 会使蛋白质变性 不可逆 项错误 终止反应 冷却后 应该把试管里的液体慢慢
, , ,C ; , ,
倒入盛有水的另一支试管里 实验操作不正确 项错误
, ,D 。
【答案】
8. C
【解析】 钴原子核外电子总数为 基态钴原子的价电子排布式为 项正确
7 2
27, :3d4s,A ;
中间产物 中 电子与钴形成了配位键 项正确 从中间产物 分子结构可知 与钴
b π ,B ; e ,H
形成了化学键 为正价 原子的化合价升高 故中间产物 与 反应过程中被氧
,Co ,Co , d H2
化 项错误 催化剂是降低了该反应的活化能 项正确
,C ; ,D 。
【答案】
9. B
【解析】 根据图中信息 乙醛比环氧乙烷的能量低 则乙醛更稳定 故 错误 根据乙烯
, , , A ;
与氧气反应可生成环氧乙烷和乙醛的两反应可得 H 增加氧气
, CH3CHO Δ <0,
浓度 的平衡常数不变 则平衡时环氧乙烷与乙醛的比例不变 故 正
, CH3CHO , , B
确 H 适当升高温度 平衡逆向移动 则平衡时环氧乙烷与乙醛
; CH3CHO Δ <0, , ,
的比例增大 故 错误 根据图中信息 由于生成环氧乙烷的活化能低 反应速率大 相
, C ; , , ,
对较短的反应时间内 可能生成的环氧乙烷更多 及时分离可获得高产率的环氧乙烷
, , ,
而生成乙醛的活化能高 反应速率小 相对较短的反应时间内生成乙醛的量较少 故
, , , D
错误
。
【答案】
10. C
【解析】 转化 为 和 反应生成 和 化
Ⅰ Na2SO4 NH3、H2O、CO2 NaHCO3 NH4 2SO4,
学方程式为 物质
Na2SO4+2NH3+2H2O+2CO2 2NaHCO3↓+ NH4 2SO4, M
为 故 项正确 操作 的步骤为蒸发浓缩 冷却结晶 过滤 洗涤 干燥 制得
NaHCO3, A ; a 、 、 、 、 ,
晶体 故 项正确 转化 为灼烧操作 加热时用到的仪
Na2SO4· NH4 2SO4·2H2O , B ; Ⅲ ,
器有泥三角 三脚架 酒精灯 玻璃棒 坩埚 坩埚钳 不能用蒸发皿 项错误 物质
、 、 、 、 、 , ,C ; N
高三化学参考答案 第 页(共 页)
4 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}为 可用于转化 循环利用 项正确
NH3, Ⅰ ,D 。
【答案】
11. C
【解析】 反应为气体分子数减小的反应 恒温条件下
PCl3 g +Cl2 g PCl5 g , ,
增大压强平衡正向移动 x 增大 故曲线 是等温过程的曲线 则曲线 为等压
,(PCl5) , Ⅰ , Ⅱ
过程的曲线 项错误 曲线 为等压过程的曲线 随着温度升高 x 减小 则该
,A ; Ⅱ , , (PCl5) ,
转化反应为放热反应 项错误 曲线 是等温过程的曲线 点对应的总压强
ΔH<0,B ; Ⅰ ,M
为
5
根据计算可得 的x 故 的分压为
4
3.0×10 Pa, PCl3 (PCl3)=25%, PCl3 7.5×10 Pa,
项正确 两点对应的温度均为 故平衡常数相等 项错误
C ;M、N 400℃, ,D 。
【答案】
12. D
【解析】 无膜微流体燃料电池工作时 燃料 发生失电子的反应 氧化剂
, CH3OH ,
发生得电子的反应 电极 为正极 电极 为负极 正极的电势高 故
K3[Fe(CN)6] , b , a , , A
错误 电解质溶液为 溶液 电极 上发生的反应为
- -
; NaOH , a CH3OH-6e +8OH
故 错误 电解质溶液为 溶液 已知电池工作过程中无固体析
2-
CO3 +6H2O, B ; NaOH ,
出 不会有 生成 电极 上发生的反应为 故
2+ 3- - 4-
, Fe , b [Fe(CN)6] +e [Fe(CN)6] ,
错误 根据电极反应式 电路上转移 电子 理论上消耗 故 正确
-
C ; , 6mol , 8molOH , D 。
【答案】
13. C
【解析】 原料溶液中含少量 故电荷守恒中应增加 使等式成立 项错误
3+ 3+
Fe , Fe ,A ;
c 2+ K
除铁 得 到 的 上 层 清 液 中 Mn sp [Mn(OH)2] c - 25.83
“ ” :c 3+ = K × OH =10 ×
Fe sp [Fe(OH)3]
c - 项错误 根据K -7 K -5
OH ,B ; a1(H2CO3)=4.2×10 , b(NH3·H2O)=1.8×10
知
-
的水解程度大于
+ -1
溶液中 故c
+
,HCO3 NH4 ,0.1mol·L NH4HCO3 , NH4 >
c - 项 正 确 沉 锰 后 的 滤 液 中 还 有 故 c +
HCO3 ,C ;“ ” (NH4)2SO4, NH4 +
c c - c c 2- 项错误
NH3·H2O > HCO3 + H2CO3 + CO3 ,D 。
【答案】
14. D
【解析】 该晶胞主要由 和 构成 观察晶胞结构图我们可以发现 位于晶胞
K SeBr6 , ,K
内部 一共有 个 分别位于顶点和面心 顶点处的 有 个 面心处的
, 8 K。SeBr6 , SeBr6 8 ,
有 个 所以一个晶胞中含有的 数目为 1 1 所以其化学式
SeBr6 6 , SeBr6 :8× +6× =4。
8 2
为 该离子化合物阳离子为 阴离子为 该离子化合物中 元素的
+ 2-
:K2SeBr6, K , SeBr6 , Se
化合价为 价 项错误 以 点 为例 位于相邻顶点和三个面心上的阴离子构成
+
+4 ,A ; 3 K ,
的四面体间隙中 项错误 从图 可以看出 两个 原子之间最短的距离为棱长的一
,B ; 2 , K
半 即相邻 + 之间的最短距离为 1 项错误 已知 点坐标参数为
, K : anm,C ; 1 (0,0,0),2
2
点为 则 点为 1 1 3 项正确
(1,1,1), 3 ( , , ),D 。
4 4 4
分 除标注外其它每空 分
15.(15 , 2 )
高三化学参考答案 第 页(共 页)
5 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}【答案】 分 分
(1)O>N>C>H (1 ) 6(1 )
恒压滴液漏斗 分 的 水浴加热
(2) (1 ) (70℃ )
防止 氧化
2+
(3) Fe
降低甘氨酸亚铁的溶解度 使其结晶析出
(4) ,
- 2+ + 3+ 2+
(5)①MnO4 +5Fe +8H 5Fe +Mn +4H2O
漏选且正确得 分
②AB( 1 ) ③40
【解析】 甘氨酸分子中各元素的电负性大小关系为 根据甘氨酸亚
(1) :O>N>C>H ;
铁的结构简式可知 的配位数为
2+
,Fe 6。
仪器 的名称是恒压滴液漏斗 根据反应原理 该反应的温度为 采用
(2) a ; , 70℃, (70℃
的 水浴加热
) 。
柠檬酸具有较强的还原性和酸性 加入柠檬酸促进 溶解并调节溶液 还
(3) , FeCO3 pH,
有的作用是防止 氧化
2+
Fe 。
甘氨酸易溶于水 微溶于乙醇 蒸发浓缩后加入无水乙醇的目的是降低甘氨酸亚铁
(4) , ,
的溶解度 使其结晶析出
, 。
- 2+ + 3+ 2+
(5)①MnO4 +5Fe +8H 5Fe +Mn +4H2O。
酸性高锰酸钾溶液应盛装在酸式滴定管中 滴定操作用到的仪器有 酸式滴定管 锥
② , : 、
形瓶
。
据图可得 其吸光度 为 甘氨酸亚铁的浓度为 产品中甘氨酸亚
③ , (A) 10.2, 0.04mol/L,
铁的物质的量为 根据 甘氨酸与过量的 反应 理
0.04mol, 200mL1.0mol/L FeCO3 ,
论上生成 甘氨酸亚铁 则产率为
0.1mol , 40%。
分 除标注外其它每空 分
16.(14 , 2 )
【答案】 分 分
(1)f(1 ) (1 )
以增大固体与气体接触面积 增大氧气浓度 提高焙烧速率并且使反应更充分 合
(2) , , (
理即可
)
+ 3+
(3)2CeO2+6H + H2O22Ce + O2↑ +4H2O
(4)9
或
-
(5)NaCl( Cl )
△ 条件有无加热都给分
(6)Ce(OH)4+6HNO3 H2Ce(NO3)6+4H2O( )
用玻璃棒向漏斗中引流入浓硝酸至固体全部浸没 待溶液自然流出 重复 次
(7) , , 2~3
合理即可
( )
【解析】 分析 本实验的目的是利用稀土氟化物制取硝酸铈铵 首
: [(NH4)2Ce(NO3)6],
先氟碳铈矿含 等 在空气中焙烧 酸浸 还原后生成 然后和
CeFCO3 , , 、 Ce2(SO4)3, NaOH
溶液反应得到 之后利用氯气氧化 得到 加入浓硝酸溶
Ce(OH)3, Ce(OH)3 Ce(OH)4,
解得到 然后再和 反应得到产品
H2[Ce(NO3)6], NH4NO3 。
铈 是镧系元素在元素周期表中属于 区 焙烧生成的气体为二氧化碳 其电子
(1) (Ce) f , ,
式为
。
高三化学参考答案 第 页(共 页)
6 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}焙烧 中常采用高压空气 逆流操作的目的是以增大固体接触面积 增大氧气浓
(2)“ ” 、 ,
度 提高焙烧速率并且使反应更充分
, 。
酸浸过程中 发生反应的离子方程式为
+ 3+
(3) CeO2 2CeO2+6H + H2O2 2Ce +
O2↑ +4H2O。
完 全 生 成 沉 淀 时 浓 度 小 于 依 据
3+ 3+ -5 -1
(4)Ce Ce(OH)3 ,Ce 10 mol·L ,
3
K -20c - 1.0×10
-20
-5 -1 则 大于
sp [Ce(OH)3]=1.0×10 , OH = -5 =10 mol·L , pH
10
时 完全生成 沉淀
3+
9 ,Ce Ce(OH)3 。
沉淀转化 的方程式为 该反
(5)“ ” 2Ce(OH)3+2NaOH+Cl2 2Ce(OH)4+2NaCl,
应的还原产物为
NaCl。
加热浆化 过程中生成了配合物 该反应的化学方程式为
(6)“ ” H2Ce(NO3)6, Ce(OH)4
△
+6HNO3 H2Ce(NO3)6+4H2O 。
洗涤产品用浓硝酸 洗涤操作的实验方法是 用玻璃棒向漏斗中引流入浓硝酸至固
(7) , ,
体全部浸没 待溶液自然流出 重复 次
, , 2~3 。
分 每空 分
17.(14 , 2 )
【答案】
-1
(1)-166kJ·mol
t t t
(2)① 1< 2< 3
反应 是气体分子数减小的反应 增大压强 平衡正向移动 促进了反应 正向移
② ⅱ , , , ⅰ
动 因此温度一定 增大压强 的转化率增大 或总反应是气体分子数减小的反应
, , CO2 ( ,
增大压强 平衡正向移动 的转化率增大 解释合理即可
, ,CO2 , )
的体积比值小于 时 提高 浓度 促进反应 化学平衡正向移动 提高
③H2/CO2 2 , H2 , ⅰ ,
的转化率 比值高于 时 会促进 与 反应 生成甲烷 从而降低 选择性
CO2 ; 2 , CO H2 , , CO
解释合理即可
( )
-1 -1
(3)①CO2 ②0.012mol·L ·min ③0.57
【解析】 根据盖斯定律 反应 反应 可得 H -1
(1) , ⅰ+ ⅱ Δ 3=-166kJ·mol 。
生成甲烷的反应为放热反应 升高温度甲烷的选择性降低 故t t t 反应
(2)① , , 1< 2< 3;②
是气体分子数减小的反应 增大压强 平衡正向移动 促进了反应 正向移动 因此
ⅱ , , , ⅰ ,
温度一定 增大压强 的转化率增大 解释合理即可 的体积比值小于
, CO2 ( );③H2/CO2 2
时 提高 浓度 促进反应 化学平衡正向移动 提高 的转化率 比值高于 时
, H2 , ⅰ , CO2 ; 2 ,
会促进 与 反应 生成甲烷 从而降低 选择性
CO H2 , , CO 。
由题干信息可知 升高温度 反应 正向移动 反应 逆向移动 则n 增大
(3) , , ⅰ , ⅱ , (CO) ,
n 减小 结合题干图像可知 表示 表示 则 表示 时
(CH4) , ,c CO、b CH4, a CO2。649℃ ,
n n n 初始加入的n 根据元
(H2)=1.2mol,(CO)= (CO2)=0.44mol, (CO2)=1mol,
素守恒可计算得 平衡时n n n n
, :(CH4)=0.12mol,(H2O)=0.68mol,(CO)= (CO2)
n 反应 达平衡 则反应 的化学反应速率为
=0.44mol, (H2)=1.2mol, 5min , ⅱ
高三化学参考答案 第 页(共 页)
7 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}v 0.12 -1 -1 -1 -1 反应 的平衡常数为
(CH4)= mol·L ·min =0.012mol·L ·min ;③ ⅰ
2×5
K 0.44×0.68
= ≈0.57。
0.44×1.2
分 除标注外其它每空 分
18.(15 , 2 )
【答案】 醚键 分 氰基 顺序可互换 分
(1) (1 ) ( ,1 )
对甲基苯酚 甲基苯酚
(2) (4- )
漏选且正确得 分
(3)①⑤( 1 )
吡啶具有碱性 中和反应 的生成物 促进反应正向进行 提高产率 答案合理
(4) , ⑥ HBr, , (
即可
)
(5)12
分
(6)(3 )
【解析】 中官能团名称为羟基 醚键和氰基
(1)F 、 。
的化学名称为对甲基苯酚 甲基苯酚 根据 的结构简式和 的分子式
(2)B (4- ); D、F E ,
可推得 的结构简式为
E 。
根据物质 和物质 的官能团 物质 和物质 均没有醛基均不能与银氨溶液反
(3) C D , C D
应 物质 有羟基而物质 没有 金属钠可鉴 物质 有酚羟基 可与 溶液发生
; C D , ; C , FeCl3
显色反应 而物质 不能 可鉴别 红外光谱可测定不同的官能团 红外光谱可鉴别 物
, D , ; , ;
质 和物质 中苯环上的甲基均能被酸性高锰酸钾溶液氧化 酸性高锰酸钾溶液不能
C D ,
鉴别
。
反应 发生取代反应 生成物中有 吡啶具有碱性 中和反应 的生成物
(4) ⑥ , HBr, , ⑥ HBr,
促进反应正向进行 提高产率
, 。
的同分异构体中 属于芳香族化合物 苯环上有三个取代基 其中有两个处于邻
(5)D , , ,
位的甲基 结合条件 另一个取代基 上有酯基和两个碳 可以为
, ②, -R ,-R :
共 种 在苯环上的位置有 种 符合条件的 的同分异构体共有 种
6 ,-R 2 , D 12 。
高三化学参考答案 第 页(共 页)
8 8
{#{QQABLQaowgAYgFTACZ5KAQUMCQgQsIAiLUoEwVCdqAwKAJFABIA=}#}