文档内容
专题22 金属有关的工艺流程
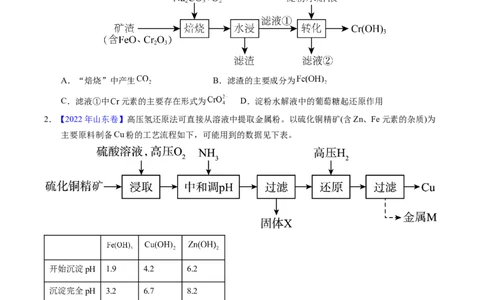
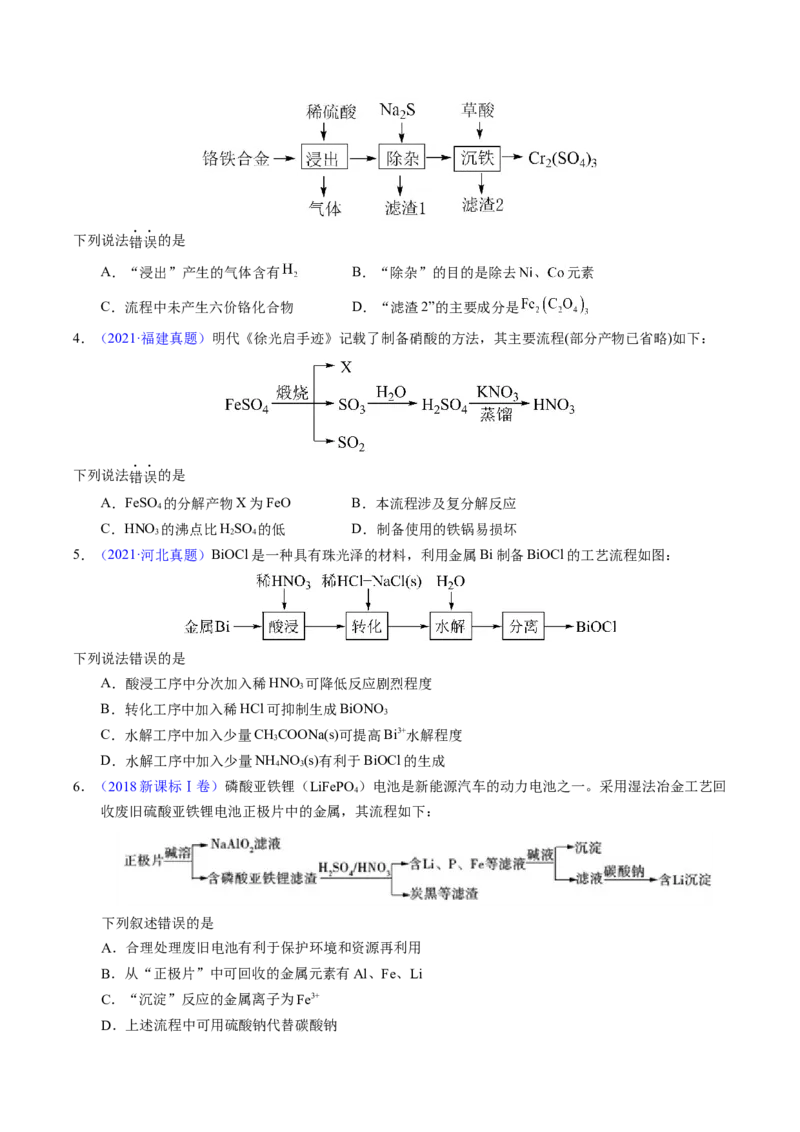
1.【2023年辽宁卷】某工厂采用如下工艺制备 ,已知焙烧后 元素以 价形式存在,下列说法
错误的是
A.“焙烧”中产生 B.滤渣的主要成分为
C.滤液①中 元素的主要存在形式为 D.淀粉水解液中的葡萄糖起还原作用
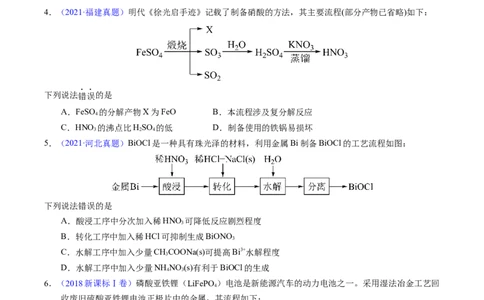
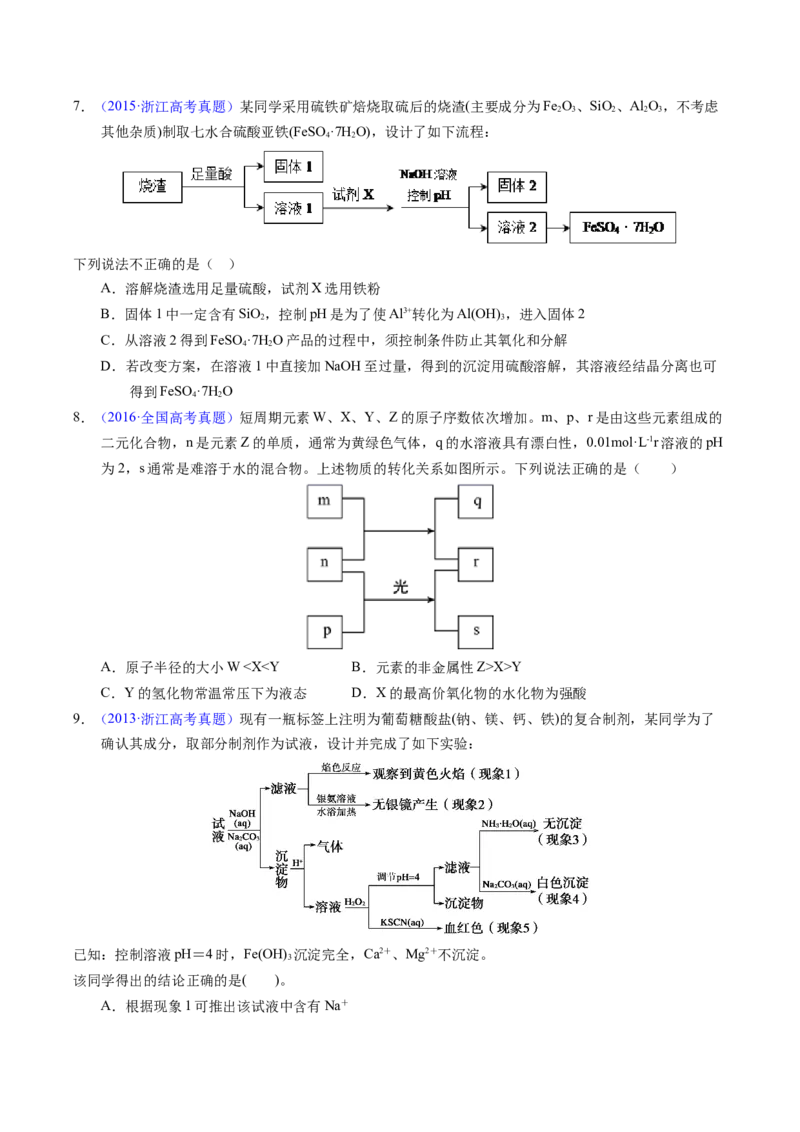
2.【2022年山东卷】高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为
主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是
A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
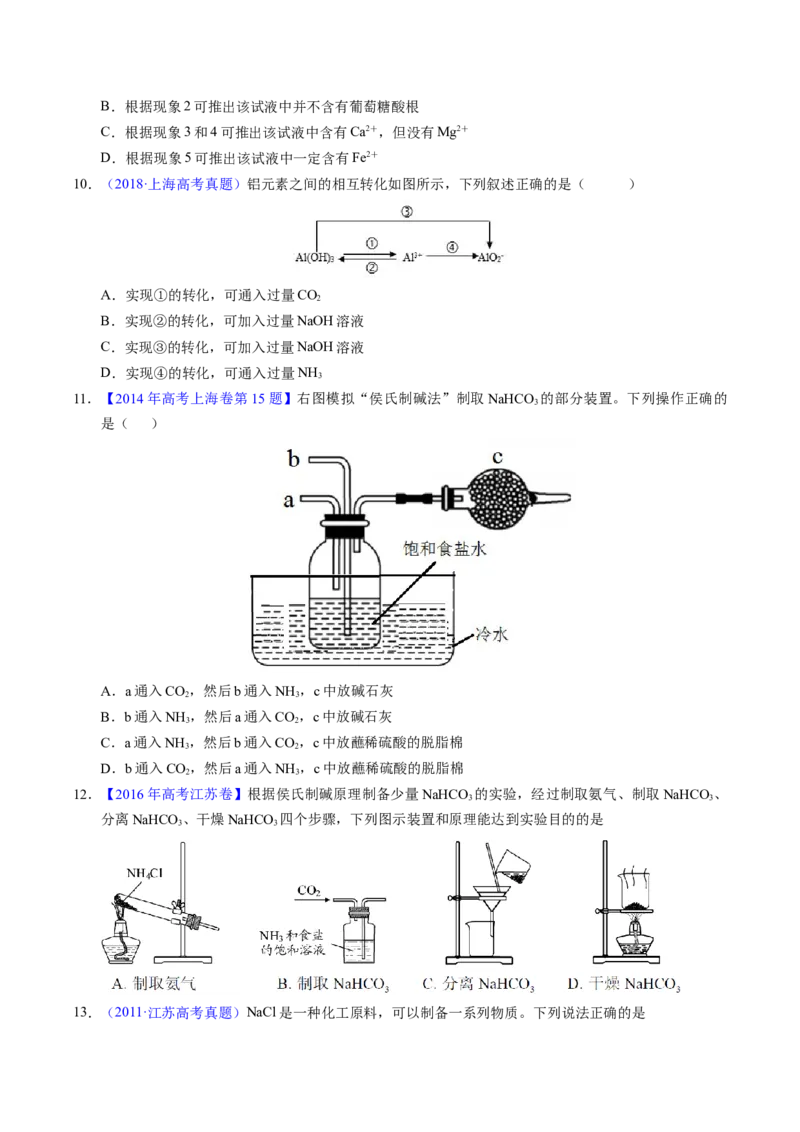
3.【2022年福建卷】用铬铁合金(含少量 单质)生产硫酸铬的工艺流程如下:下列说法错误的是
A.“浸出”产生的气体含有 B.“除杂”的目的是除去 元素
C.流程中未产生六价铬化合物 D.“滤渣2”的主要成分是
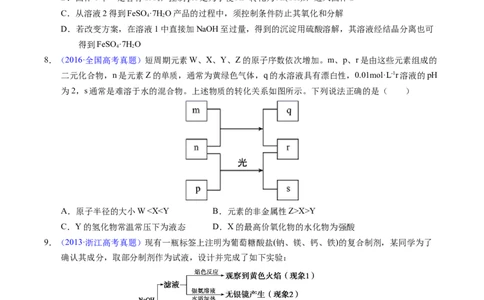
4.(2021·福建真题)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是
A.FeSO 的分解产物X为FeO B.本流程涉及复分解反应
4
C.HNO 的沸点比HSO 的低 D.制备使用的铁锅易损坏
3 2 4
5.(2021·河北真题)BiOCl是一种具有珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:
下列说法错误的是
A.酸浸工序中分次加入稀HNO 可降低反应剧烈程度
3
B.转化工序中加入稀HCl可抑制生成BiONO
3
C.水解工序中加入少量CHCOONa(s)可提高Bi3+水解程度
3
D.水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
6.(2018新课标Ⅰ卷)磷酸亚铁锂(LiFePO )电池是新能源汽车的动力电池之一。采用湿法冶金工艺回
4
收废旧硫酸亚铁锂电池正极片中的金属,其流程如下:
下列叙述错误的是
A.合理处理废旧电池有利于保护环境和资源再利用
B.从“正极片”中可回收的金属元素有Al、Fe、Li
C.“沉淀”反应的金属离子为Fe3+
D.上述流程中可用硫酸钠代替碳酸钠7.(2015·浙江高考真题)某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe O、SiO、Al O,不考虑
2 3 2 2 3
其他杂质)制取七水合硫酸亚铁(FeSO ·7H O),设计了如下流程:
4 2
下列说法不正确的是( )
A.溶解烧渣选用足量硫酸,试剂X选用铁粉
B.固体1中一定含有SiO,控制pH是为了使Al3+转化为Al(OH) ,进入固体2
2 3
C.从溶液2得到FeSO ·7H O产品的过程中,须控制条件防止其氧化和分解
4 2
D.若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可
得到FeSO ·7H O
4 2
8.(2016·全国高考真题)短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的
二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol·L-1r溶液的pH
为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
A.原子半径的大小W X>Y
C.Y的氢化物常温常压下为液态 D.X的最高价氧化物的水化物为强酸
9.(2013·浙江高考真题)现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了
确认其成分,取部分制剂作为试液,设计并完成了如下实验:
已知:控制溶液pH=4时,Fe(OH) 沉淀完全,Ca2+、Mg2+不沉淀。
3
该同学得出的结论正确的是( )。
A.根据现象1可推出该试液中含有Na+B.根据现象2可推出该试液中并不含有葡萄糖酸根
C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D.根据现象5可推出该试液中一定含有Fe2+
10.(2018·上海高考真题)铝元素之间的相互转化如图所示,下列叙述正确的是( )
A.实现①的转化,可通入过量CO
2
B.实现②的转化,可加入过量NaOH溶液
C.实现③的转化,可加入过量NaOH溶液
D.实现④的转化,可通入过量NH
3
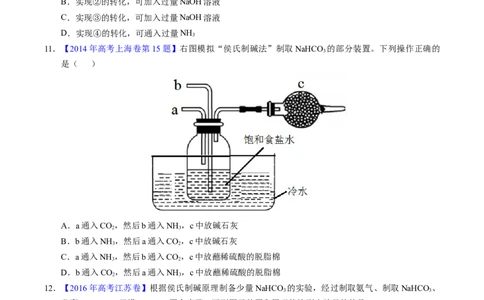
11.【2014年高考上海卷第15题】右图模拟“侯氏制碱法”制取NaHCO 的部分装置。下列操作正确的
3
是( )
A.a通入CO,然后b通入NH ,c中放碱石灰
2 3
B.b通入NH ,然后a通入CO,c中放碱石灰
3 2
C.a通入NH ,然后b通入CO,c中放蘸稀硫酸的脱脂棉
3 2
D.b通入CO,然后a通入NH ,c中放蘸稀硫酸的脱脂棉
2 3
12.【2016年高考江苏卷】根据侯氏制碱原理制备少量NaHCO 的实验,经过制取氨气、制取NaHCO 、
3 3
分离NaHCO 、干燥NaHCO 四个步骤,下列图示装置和原理能达到实验目的的是
3 3
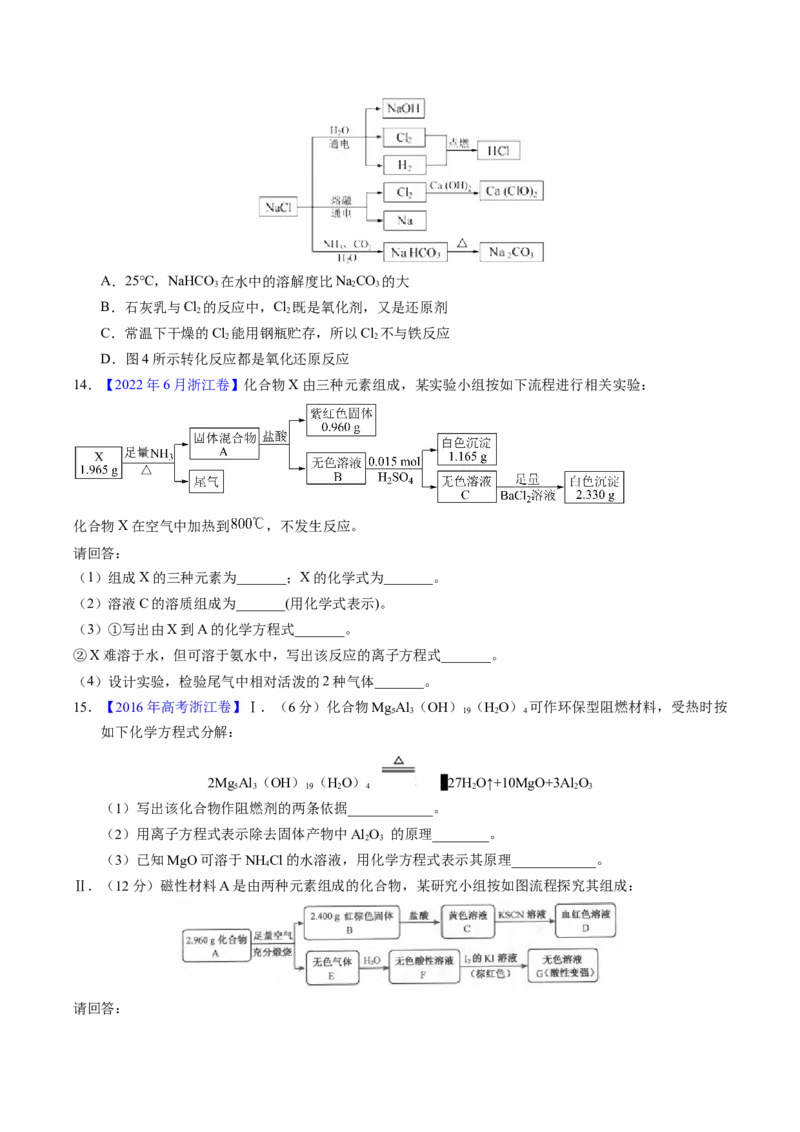
13.(2011·江苏高考真题)NaCl是一种化工原料,可以制备一系列物质。下列说法正确的是A.25℃,NaHCO 在水中的溶解度比NaCO 的大
3 2 3
B.石灰乳与Cl 的反应中,Cl 既是氧化剂,又是还原剂
2 2
C.常温下干燥的Cl 能用钢瓶贮存,所以Cl 不与铁反应
2 2
D.图4所示转化反应都是氧化还原反应
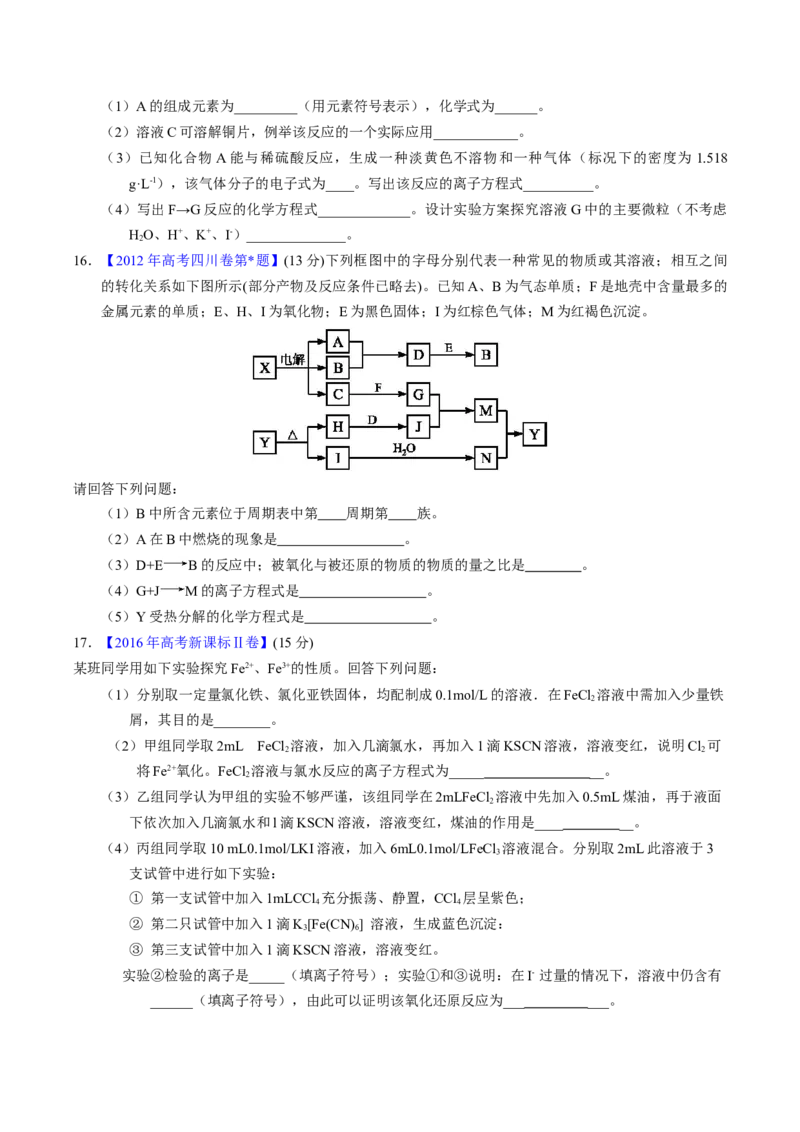
14.【2022年6月浙江卷】化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
15.【2016年高考浙江卷】Ⅰ.(6分)化合物MgAl (OH) (HO) 可作环保型阻燃材料,受热时按
5 3 19 2 4
如下化学方程式分解:
2MgAl (OH) (HO) 27HO↑+10MgO+3Al O
5 3 19 2 4 2 2 3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al O 的原理________。
2 3
(3)已知MgO可溶于NH Cl的水溶液,用化学方程式表示其原理____________。
4
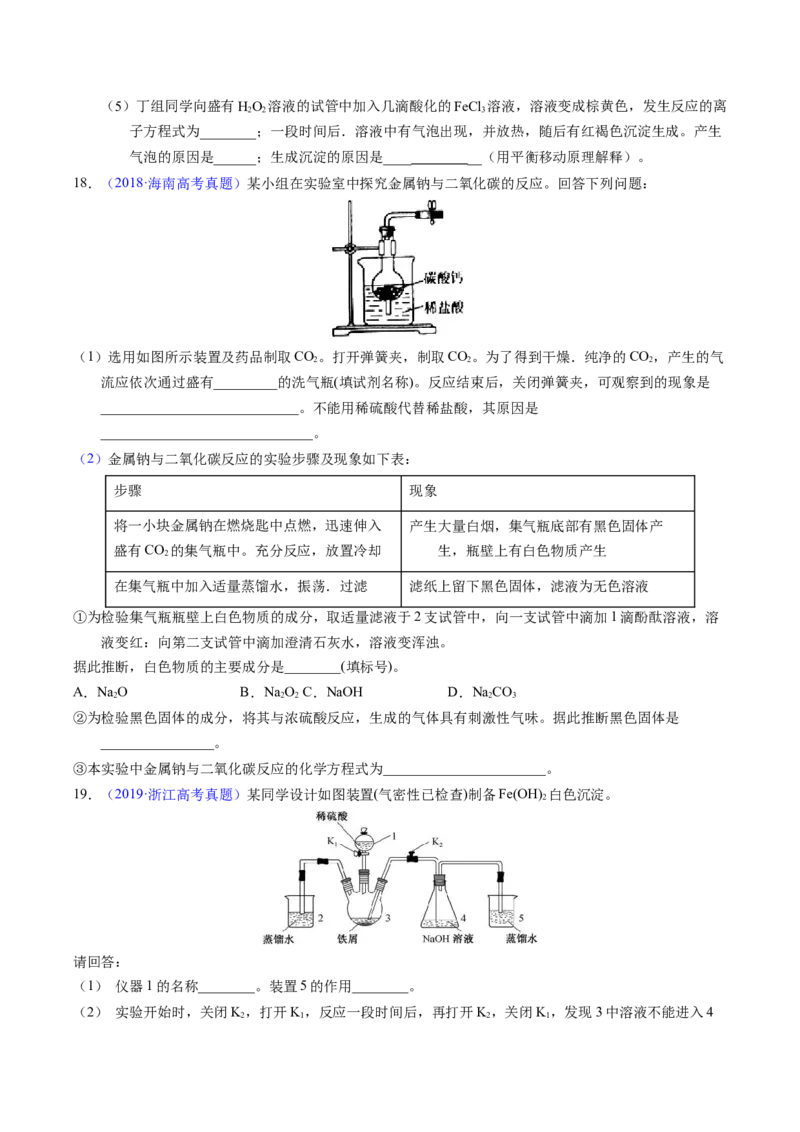
Ⅱ.(12分)磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
请回答:(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,例举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为 1.518
g·L-1),该气体分子的电子式为____。写出该反应的离子方程式__________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑
HO、H+、K+、I-)______________。
2
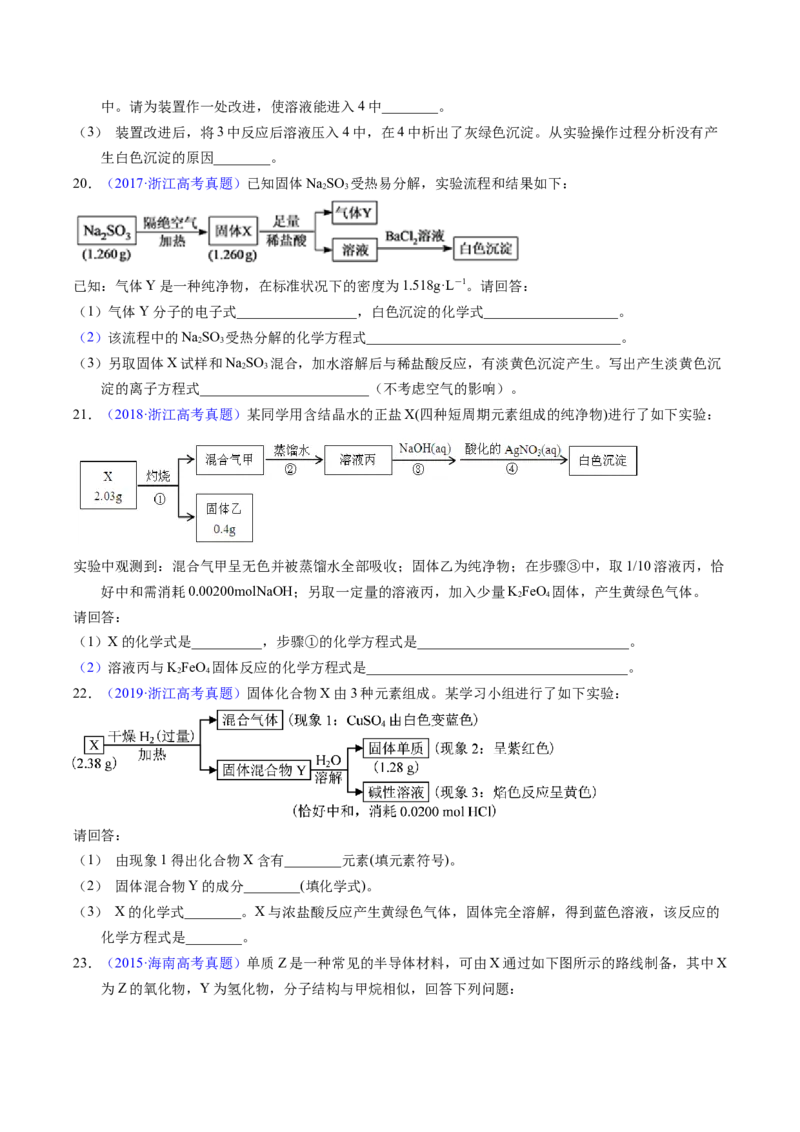
16.【2012年高考四川卷第*题】(13分)下列框图中的字母分别代表一种常见的物质或其溶液;相互之间
的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质;F是地壳中含量最多的
金属元素的单质;E、H、I为氧化物;E为黑色固体;I为红棕色气体;M为红褐色沉淀。
请回答下列问题:
(1)B中所含元素位于周期表中第 周期第 族。
(2)A在B中燃烧的现象是 。
(3)D+E B的反应中;被氧化与被还原的物质的物质的量之比是 。
(4)G+J M的离子方程式是 。
(5)Y受热分解的化学方程式是 。
17.【2016年高考新课标Ⅱ卷】(15分)
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl 溶液中需加入少量铁
2
屑,其目的是________。
(2)甲组同学取2mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl 可
2 2
将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为_____ __。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl 溶液中先加入0.5mL煤油,再于液面
2
下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是____ __。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl 溶液混合。分别取2mL此溶液于3
3
支试管中进行如下实验:
① 第一支试管中加入1mLCCl 充分振荡、静置,CCl 层呈紫色;
4 4
② 第二只试管中加入1滴K[Fe(CN) ] 溶液,生成蓝色沉淀:
3 6
③ 第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_____(填离子符号);实验①和③说明:在I- 过量的情况下,溶液中仍含有
______(填离子符号),由此可以证明该氧化还原反应为___ ___。(5)丁组同学向盛有HO 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄色,发生反应的离
2 2 3
子方程式为________;一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生
气泡的原因是______;生成沉淀的原因是____ __(用平衡移动原理解释)。
18.(2018·海南高考真题)某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:
(1)选用如图所示装置及药品制取CO。打开弹簧夹,制取CO。为了得到干燥.纯净的CO,产生的气
2 2 2
流应依次通过盛有_________的洗气瓶(填试剂名称)。反应结束后,关闭弹簧夹,可观察到的现象是
____________________________。不能用稀硫酸代替稀盐酸,其原因是
______________________________。
(2)金属钠与二氧化碳反应的实验步骤及现象如下表:
步骤 现象
将一小块金属钠在燃烧匙中点燃,迅速伸入 产生大量白烟,集气瓶底部有黑色固体产
盛有CO 的集气瓶中。充分反应,放置冷却 生,瓶壁上有白色物质产生
2
在集气瓶中加入适量蒸馏水,振荡.过滤 滤纸上留下黑色固体,滤液为无色溶液
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶
液变红:向第二支试管中滴加澄清石灰水,溶液变浑浊。
据此推断,白色物质的主要成分是________(填标号)。
A.NaO B.NaO C.NaOH D.NaCO
2 2 2 2 3
②为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是
________________。
③本实验中金属钠与二氧化碳反应的化学方程式为_______________________。
19.(2019·浙江高考真题)某同学设计如图装置(气密性已检查)制备Fe(OH) 白色沉淀。
2
请回答:
(1) 仪器1的名称________。装置5的作用________。
(2) 实验开始时,关闭K,打开K,反应一段时间后,再打开K,关闭K,发现3中溶液不能进入4
2 1 2 1中。请为装置作一处改进,使溶液能进入4中________。
(3) 装置改进后,将3中反应后溶液压入4中,在4中析出了灰绿色沉淀。从实验操作过程分析没有产
生白色沉淀的原因________。
20.(2017·浙江高考真题)已知固体NaSO 受热易分解,实验流程和结果如下:
2 3
已知:气体Y是一种纯净物,在标准状况下的密度为1.518g·L-1。请回答:
(1)气体Y分子的电子式_________________,白色沉淀的化学式___________________。
(2)该流程中的NaSO 受热分解的化学方程式____________________________________。
2 3
(3)另取固体X试样和NaSO 混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生。写出产生淡黄色沉
2 3
淀的离子方程式________________________(不考虑空气的影响)。
21.(2018·浙江高考真题)某同学用含结晶水的正盐X(四种短周期元素组成的纯净物)进行了如下实验:
实验中观测到:混合气甲呈无色并被蒸馏水全部吸收;固体乙为纯净物;在步骤③中,取1/10溶液丙,恰
好中和需消耗0.00200molNaOH;另取一定量的溶液丙,加入少量KFeO 固体,产生黄绿色气体。
2 4
请回答:
(1)X的化学式是__________,步骤①的化学方程式是______________________________。
(2)溶液丙与KFeO 固体反应的化学方程式是_____________________________________。
2 4
22.(2019·浙江高考真题)固体化合物X由3种元素组成。某学习小组进行了如下实验:
请回答:
(1) 由现象1得出化合物X含有________元素(填元素符号)。
(2) 固体混合物Y的成分________(填化学式)。
(3) X的化学式________。X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到蓝色溶液,该反应的
化学方程式是________。
23.(2015·海南高考真题)单质Z是一种常见的半导体材料,可由X通过如下图所示的路线制备,其中X
为Z的氧化物,Y为氢化物,分子结构与甲烷相似,回答下列问题:(1)能与X发生化学反应的酸是_________;由X制备MgZ的化学方程式为_________。
2
(2)由MgZ生成Y的化学反应方程式为_________,Y分子的电子式为_________。
2
(3)Z、X中共价键的类型分别是_________。
24.(2014·浙江高考真题)某研究小组为了探究一种无机矿物质X(仅含四种元素)的组成和性质,设计并
完成如下实验:
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1.请回答如下问题:
(1)画出白色沉淀1中金属元素的原子结构示意图_______,写出气体甲的电子式_______。
(2)X的化学式是______,在惰性气流中加热X至完全分解的化学反应方程式为_______。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是_______(用化学反应方程式表示)。
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式
_______,并设计实验方案验证该反应的产物_______。
25.(2016·江苏高考真题)实验室以一种工业废渣(主要成分为MgCO 、MgSiO 和少量Fe、Al的氧化
3 2 4
物)为原料制备MgCO ·3H O。实验过程如下:
3 2
(1)酸溶过程中主要反应的热化学方程式为
MgCO (s)+2H+(aq)=Mg2+(aq)+CO (g)+HO(l) ΔH=-50.4 kJ·mol-1
3 2 2
MgSiO(s)+4H+(aq)=2Mg2+(aq)+H SiO(s)+HO(l) ΔH=-225.4 kJ·mol-1
2 4 2 3 2
酸溶需加热的目的是______;所加HSO 不宜过量太多的原因是_______。
2 4
(2)加入HO 氧化时发生发应的离子方程式为___________。
2 2
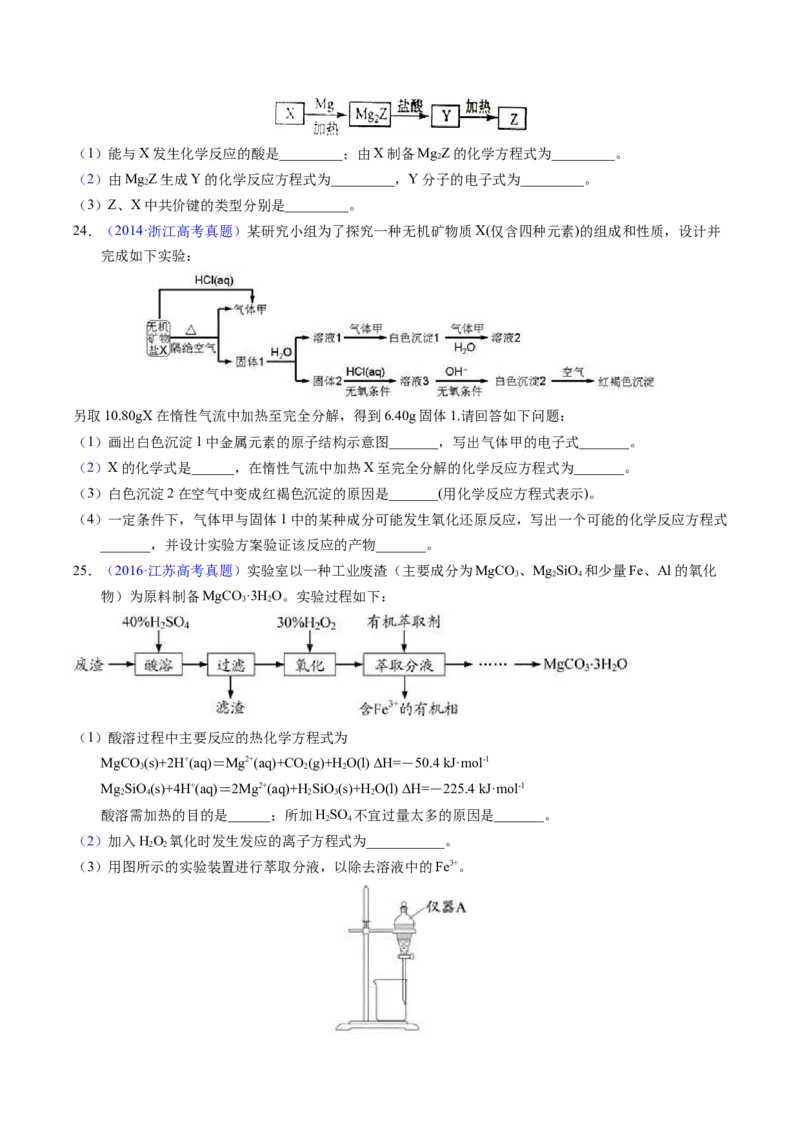
(3)用图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。①实验装置图中仪器A的名称为_______。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有
机萃取剂,______、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO ·3H O的实验方案:边搅拌边向溶液中滴加氨水,
3 2
______,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO ·3H O。
3 2
[已知该溶液中pH=8.5时Mg(OH) 开始沉淀;pH=5.0时Al(OH) 沉淀完全]。
2 3