文档内容
第2章 分子结构与性质
2.1 共价键
一.选择题(共12小题)
1.原子轨道在两核间以“肩并肩”方式重叠的键是
A.σ键 B.π键 C.氢键 D.离子键
2.下列说法不正确的是( )
A.π键是原子轨道以“肩并肩”方式相互重叠而形成的
B.2个原子形成的多重共价键中,只能有一个是σ键,而π键可以是一个或多个
C.s电子与s电子间形成的键是σ键,p电子与p电子间形成的键是π键
D.共价键一定有原子轨道的重叠
3.下列对分子中σ键重叠方式的分析不正确的是
A B C D
H HCl Cl ClF
2 2
两个氢原子的 氢原子的s轨道和氯 一个氯原子的s轨道和另一 氯原子的p轨道和氟原
s轨道重叠 原子的p轨道重叠 个氯原子的p轨道重叠 子的p轨道重叠
4.下列说法中不正确的是( )
A.双键、叁键都有π键
B.成键原子间原子轨道重叠越多,共价键越牢固
C.因每个原子未成对电子数是一定的,故配对原子个数也一定
D.所有原子轨道在空间都有自己的方向性
5.下列说法不正确的是( )
A.双键、叁键都含有π键
B.成键原子间原子轨道重叠愈多,共价键愈牢固
C.因每个原子未成对电子数是一定的,故配对原子个数也一定
D.每一个原子轨道在空间都具有自己的方向性
6.下列关于σ键和π键的理解不正确的是( )
A.σ键可以绕键轴旋转,π键不能绕键轴旋转
B.H 分子中的σ键是s-s σ键,HClO分子中的σ键都是p-p σ键
2
C.C H 分子和NH 中都是含有5个σ键
2 4 2 4
D.σ键以“头碰头”方式重叠,π键以“肩并肩”方式重叠
7.下列叙述中正确的是( )
A.两个原子间形成的共价键键能越大,键长越短,键越牢固B.两个原子半径之和就是所形成的共价键键长
C.两个原子间键长越长,键越牢固
D.键的强度与键长无关
8.关于键长、键能和键角,下列说法错误的是
A.键角是描述分子立体结构的重要参数 B.键长是形成共价键的两原子间的核间距
C.键能越大,键长越长,共价化合物越稳定 D.键角的大小与键长、键能的大小无关
9.根据键的成键特征,可判断出C=C键的键能与C-C键的键能的大小关系为( )
A.C=C键的键能等于C-C键键能的两倍
B.C=C键的键能大于C-C键键能的两倍
C.C=C键的键能小于C-C键键能的两倍
D.无法确定
10.从实验测得不同物质中O—O之间的键长和键能数据(如下表)。其中X、Y的键能数据尚未测定,但可根据
规律性推导键能的大小顺序为W>Z>Y>X。该规律性是( )
O—O键
O2- O- O O+
2 2 2 2
数据
键长/10-12m 149 128 121 112
键能/kJ·mol-1 X Y Z=494 W=628
A.电子数越多,键能越大
B.键长越长,键能越小
C.成键所用的电子数越少,键能越大
D.成键时电子对越偏移,键能越大
11.下列有关键角与分子空间构型的说法不正确的是( )
A.键角为180°的分子,空间构型是直线形
B.键角为120°的分子,空间构型是平面三角形
C.键角为109.5°的分子,空间构型是正四面体形
D.键角为90°~109.5°之间的分子,空间构型可能是V形
12.关于键长、键能和键角,下列说法不正确的是:
A.键角的大小与键长、键能的大小无关
B.键长的大小与成键原子的半径和成键数目有关
C.键能越大,键长越长,共价化合物越稳定
D.键角是描述分子立体结构的重要参数二、填空题
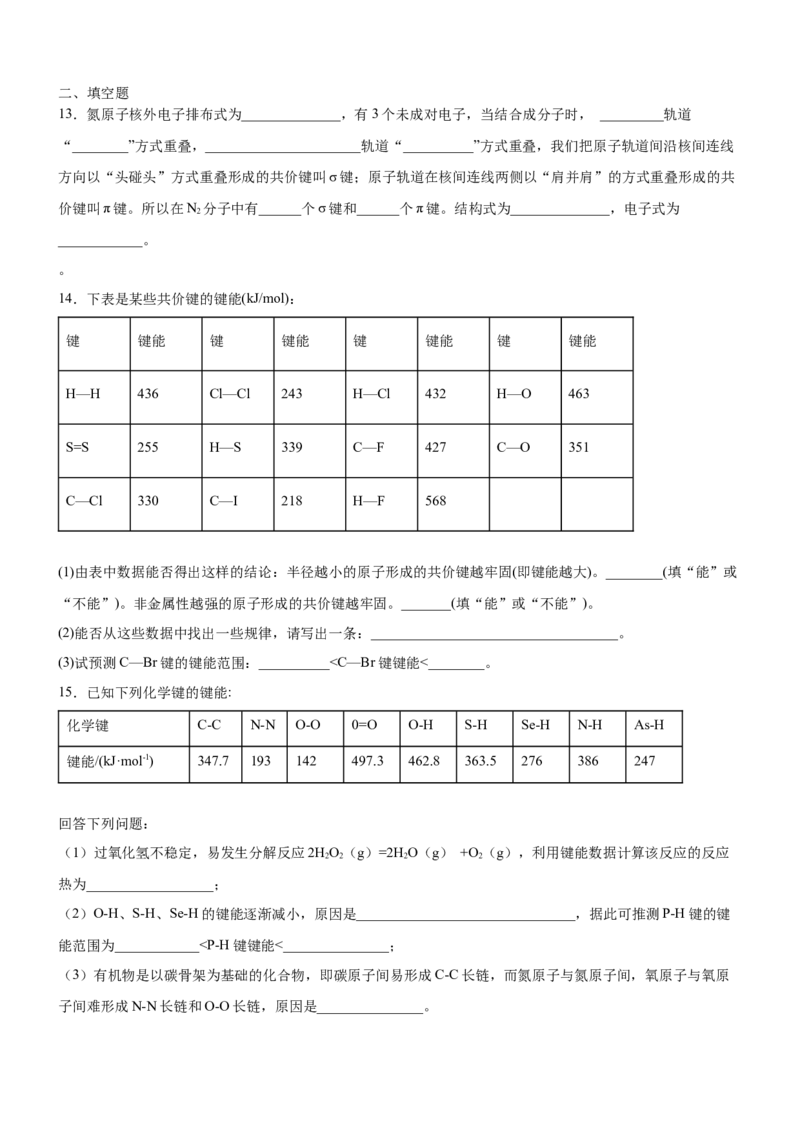
13.氮原子核外电子排布式为______________,有3个未成对电子,当结合成分子时, _________轨道
“________”方式重叠,______________________轨道“__________”方式重叠,我们把原子轨道间沿核间连线
方向以“头碰头”方式重叠形成的共价键叫σ键;原子轨道在核间连线两侧以“肩并肩”的方式重叠形成的共
价键叫π键。所以在N 分子中有______个σ键和______个π键。结构式为______________,电子式为
2
____________。
。
14.下表是某些共价键的键能(kJ/mol):
键 键能 键 键能 键 键能 键 键能
H—H 436 Cl—Cl 243 H—Cl 432 H—O 463
S=S 255 H—S 339 C—F 427 C—O 351
C—Cl 330 C—I 218 H—F 568
(1)由表中数据能否得出这样的结论:半径越小的原子形成的共价键越牢固(即键能越大)。________(填“能”或
“不能”)。非金属性越强的原子形成的共价键越牢固。_______(填“能”或“不能”)。
(2)能否从这些数据中找出一些规律,请写出一条:___________________________________。
(3)试预测C—Br键的键能范围:__________