文档内容
4.1.1 原电池的工作原理 练习(原卷版)
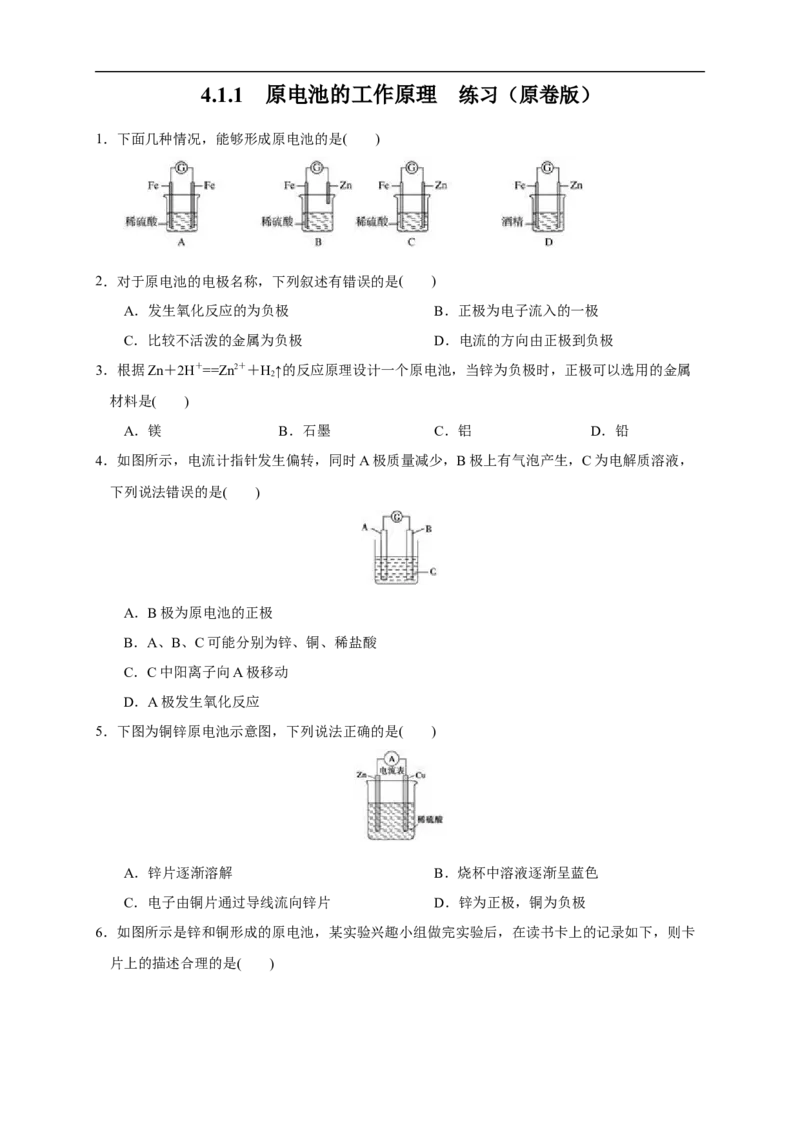
1.下面几种情况,能够形成原电池的是( )
2.对于原电池的电极名称,下列叙述有错误的是( )
A.发生氧化反应的为负极 B.正极为电子流入的一极
C.比较不活泼的金属为负极 D.电流的方向由正极到负极
3.根据Zn+2H+==Zn2++H↑的反应原理设计一个原电池,当锌为负极时,正极可以选用的金属
2
材料是( )
A.镁 B.石墨 C.铝 D.铅
4.如图所示,电流计指针发生偏转,同时A极质量减少,B极上有气泡产生,C为电解质溶液,
下列说法错误的是( )
A.B极为原电池的正极
B.A、B、C可能分别为锌、铜、稀盐酸
C.C中阳离子向A极移动
D.A极发生氧化反应
5.下图为铜锌原电池示意图,下列说法正确的是( )
A.锌片逐渐溶解 B.烧杯中溶液逐渐呈蓝色
C.电子由铜片通过导线流向锌片 D.锌为正极,铜为负极
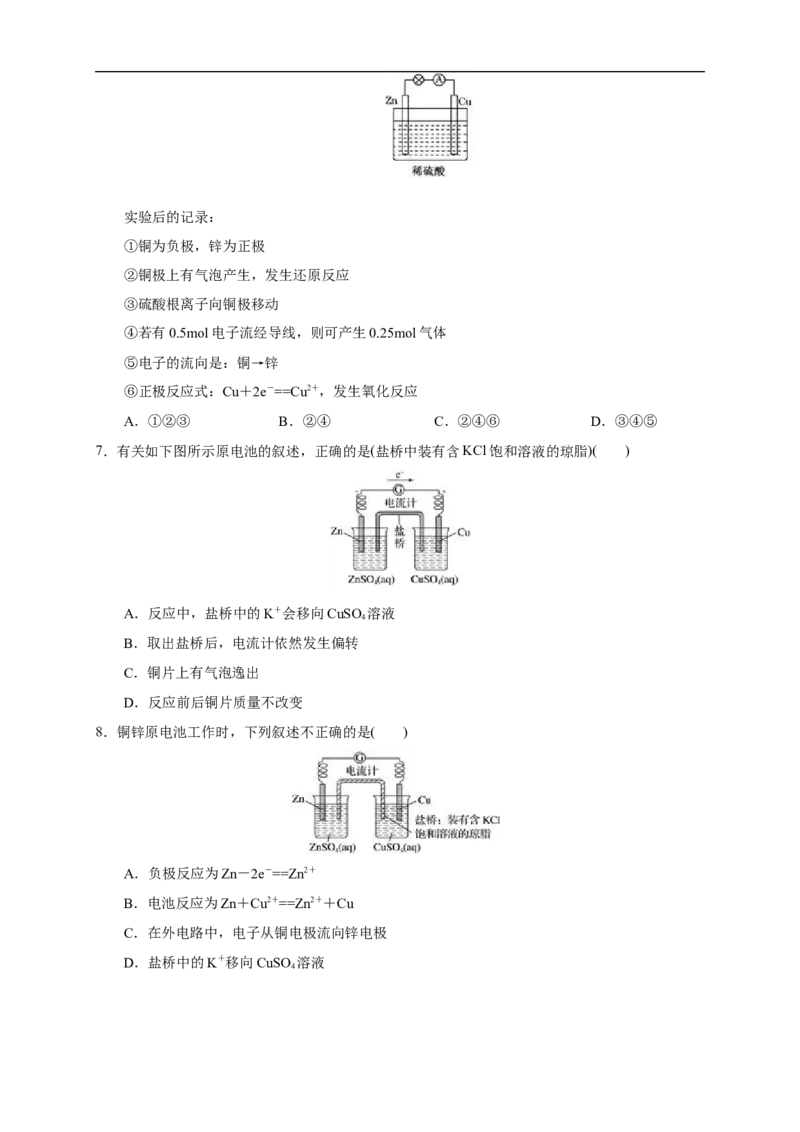
6.如图所示是锌和铜形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡
片上的描述合理的是( )实验后的记录:
①铜为负极,锌为正极
②铜极上有气泡产生,发生还原反应
③硫酸根离子向铜极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:铜→锌
⑥正极反应式:Cu+2e-==Cu2+,发生氧化反应
A.①②③ B.②④ C.②④⑥ D.③④⑤
7.有关如下图所示原电池的叙述,正确的是(盐桥中装有含KCl饱和溶液的琼脂)( )
A.反应中,盐桥中的K+会移向CuSO 溶液
4
B.取出盐桥后,电流计依然发生偏转
C.铜片上有气泡逸出
D.反应前后铜片质量不改变
8.铜锌原电池工作时,下列叙述不正确的是( )
A.负极反应为Zn-2e-==Zn2+
B.电池反应为Zn+Cu2+==Zn2++Cu
C.在外电路中,电子从铜电极流向锌电极
D.盐桥中的K+移向CuSO 溶液
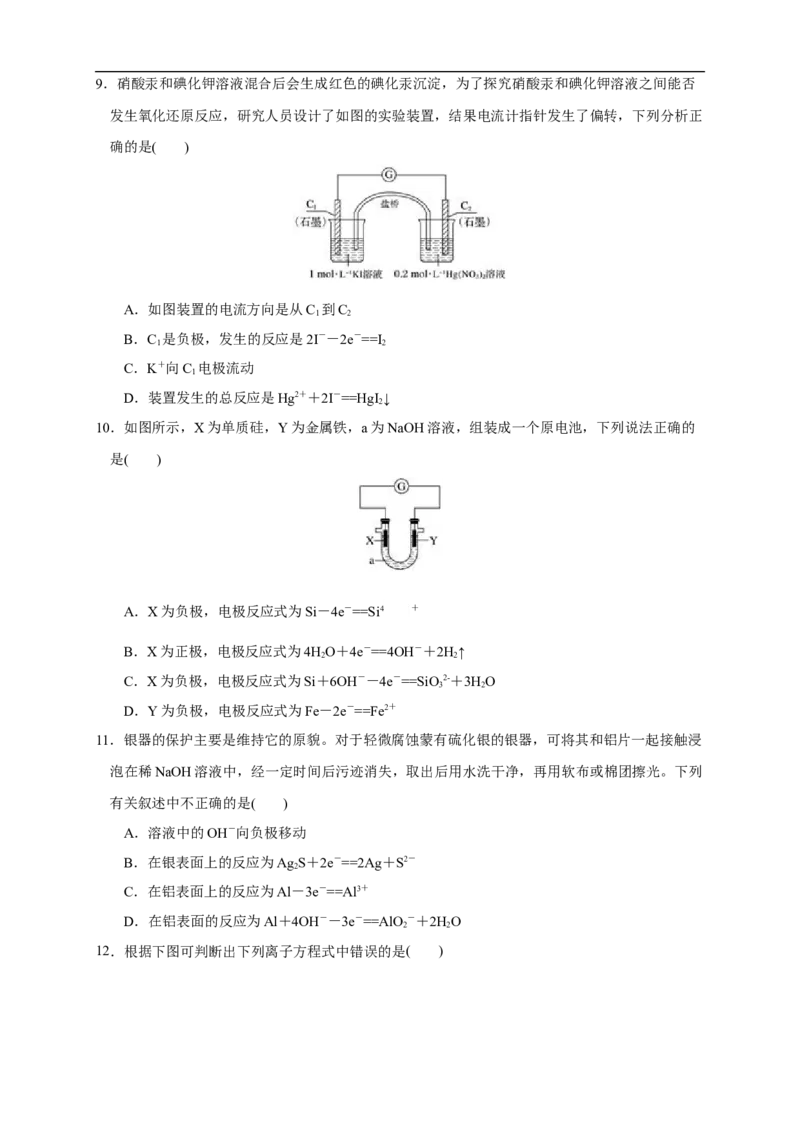
49.硝酸汞和碘化钾溶液混合后会生成红色的碘化汞沉淀,为了探究硝酸汞和碘化钾溶液之间能否
发生氧化还原反应,研究人员设计了如图的实验装置,结果电流计指针发生了偏转,下列分析正
确的是( )
A.如图装置的电流方向是从C 到C
1 2
B.C 是负极,发生的反应是2I--2e-==I
1 2
C.K+向C 电极流动
1
D.装置发生的总反应是Hg2++2I-==HgI ↓
2
10.如图所示,X为单质硅,Y为金属铁,a为NaOH溶液,组装成一个原电池,下列说法正确的
是( )
A.X为负极,电极反应式为Si-4e-==Si4 +
B.X为正极,电极反应式为4HO+4e-==4OH-+2H↑
2 2
C.X为负极,电极反应式为Si+6OH--4e-==SiO2-+3HO
3 2
D.Y为负极,电极反应式为Fe-2e-==Fe2+
11.银器的保护主要是维持它的原貌。对于轻微腐蚀蒙有硫化银的银器,可将其和铝片一起接触浸
泡在稀NaOH溶液中,经一定时间后污迹消失,取出后用水洗干净,再用软布或棉团擦光。下列
有关叙述中不正确的是( )
A.溶液中的OH-向负极移动
B.在银表面上的反应为Ag S+2e-==2Ag+S2-
2
C.在铝表面上的反应为Al-3e-==Al3+
D.在铝表面的反应为Al+4OH--3e-==AlO -+2HO
2 2
12.根据下图可判断出下列离子方程式中错误的是( )A.2Ag(s)+Cd2+(aq)==2Ag+(aq)+Cd(s)
B.Co2+(aq)+Cd(s)==Co(s)+Cd2+(aq)
C.2Ag+(aq)+Cd(s)==2Ag(s)+Cd2+(aq)
D.2Ag+(aq)+Co(s)==2Ag(s)+Co2+(aq)
13.①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流
向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。据
此判断这四种金属活动性由大到小的顺序是( )
A.①③②④ B.①③④② C.③④②① D.③①②④
14.下列四种金属制品的镀层损坏后,金属腐蚀速率最快的是( )
A.镀铝塑扣 B.食品罐头盒(镀锡)
C.白铁水桶(镀锌) D.镀银铜质奖章
15.根据原电池的有关知识,下列反应不能用于设计成原电池的是( )
A.2H+O==2H O
2 2 2
B.2CHOH+3O==2CO +4HO
3 2 2 2
C.Zn+2HCl==ZnCl +H↑
2 2
D.NaOH+HCl==NaCl+HO
2
16.(双选)某电池的总反应离子方程式为2Fe3++Fe==3Fe2+,不能实现该反应的原电池是( )
正极 负极 电解质溶液的溶质
A Cu Fe FeCl
3
B C Fe Fe(NO )
3 3
C Fe Zn Fe (SO )
2 4 3
D Ag Fe CuSO
4
17.如图是一个原电池装置,请按要求填空。
(1)正极材料是________,负极材料是________。(2)电子的流向是由________(填“Fe”或“Cu”,不同)极经外电路流向________极。
(3)写出电极反应式:负极___________________________________________,
正极______________________________________________________________。
(4)该原电池中发生的总反应离子方程式为______________________________。
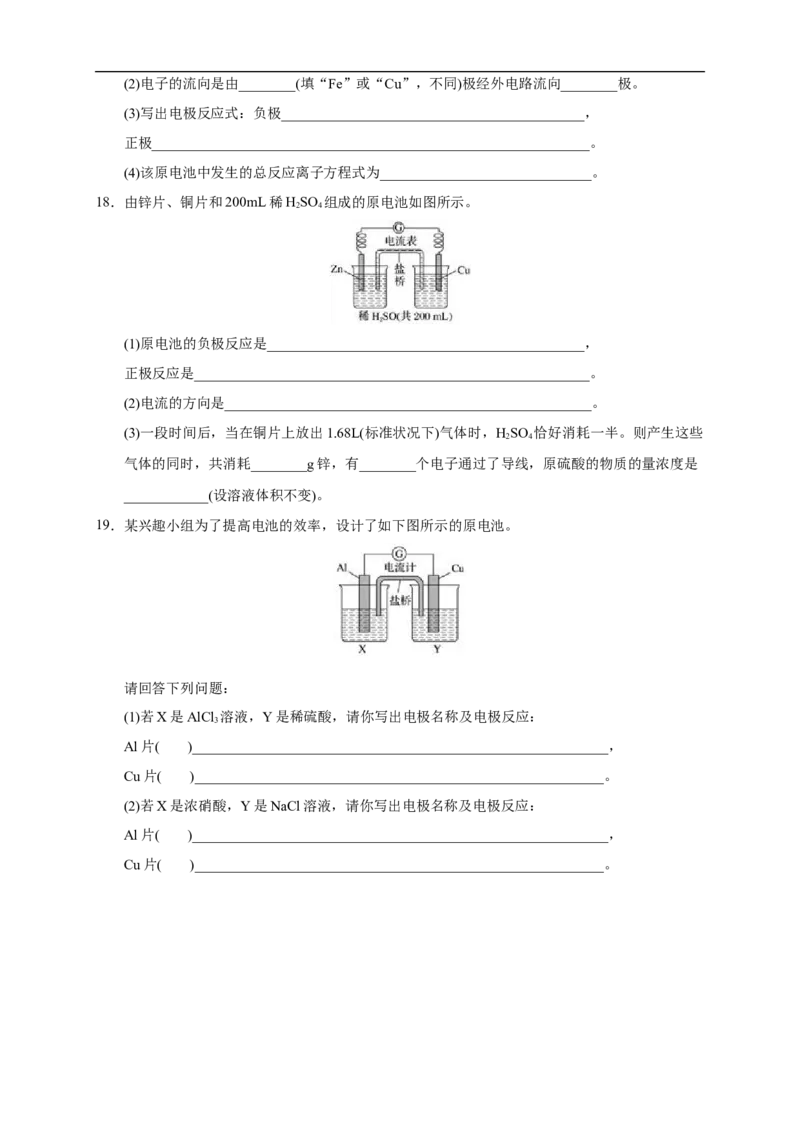
18.由锌片、铜片和200mL稀HSO 组成的原电池如图所示。
2 4
(1)原电池的负极反应是_____________________________________________,
正极反应是________________________________________________________。
(2)电流的方向是____________________________________________________。
(3)一段时间后,当在铜片上放出1.68L(标准状况下)气体时,HSO 恰好消耗一半。则产生这些
2 4
气体的同时,共消耗________g锌,有________个电子通过了导线,原硫酸的物质的量浓度是
____________(设溶液体积不变)。
19.某兴趣小组为了提高电池的效率,设计了如下图所示的原电池。
请回答下列问题:
(1)若X是AlCl 溶液,Y是稀硫酸,请你写出电极名称及电极反应:
3
Al片( )___________________________________________________________,
Cu片( )__________________________________________________________。
(2)若X是浓硝酸,Y是NaCl溶液,请你写出电极名称及电极反应:
Al片( )___________________________________________________________,
Cu片( )__________________________________________________________。