文档内容
姓 名 准考证号
岳阳市 2024 届高三教学质量监测(三)
化 学
注意事项:
1.本试卷共8页,18道题,满分100分,考试用时75分钟。
2.答卷前,考生务必将自己的学校、班级、考号和姓名填写在答题卡指定位置。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡对应的标号涂黑,如需改动,用
橡皮擦干净后,再选涂其它答案标号。
4.非选择题必须用黑色字迹的签字笔作答,答案必须写在答题卡各题目指定区域内;如需
改动,先划掉原来的答案,然后再写上新答案;不准使用铅笔和涂改液。不按以上要求作
答无效。
5.考生必须保证答题卡的整洁。考试结束后,只交答题卡。
可能用到的相对原子质量:H-1C-12N-14O-16Na-23Al-27P-31S-32Cl-35.5Fe-56
一、选择题:本题共14小题,每小题3分,共计42分。在每小题列出的四个选项中,只有一
项是符合题目要求的。
1.化学和生活、科技、社会发展息息相关,下列说法错误的是
A.神舟系列飞船返回舱使用氮化硅耐高温材料,Si N 属于共价晶体
3 4
B.三星堆黄金面具出土时光亮且薄如纸,说明金不活泼和有良好的延展性
C.利用CO 合成了高级脂肪酸,实现了无机小分子向有机高分子的转变
2
D.高铁酸钾(K FeO )对饮用水有杀菌消毒和净化的作用
2 4
2.NF 常用于微电子工业,可由反应4NH +3F Cu 3NH F+NF 制备。下列说法正确的是
3 3 2 4 3
A.NH 的VSEPR模型 B.中子数为2的H原子可表示为2H
3 1
C.F原子的结构示意图为 D.NH F的电子式为
4
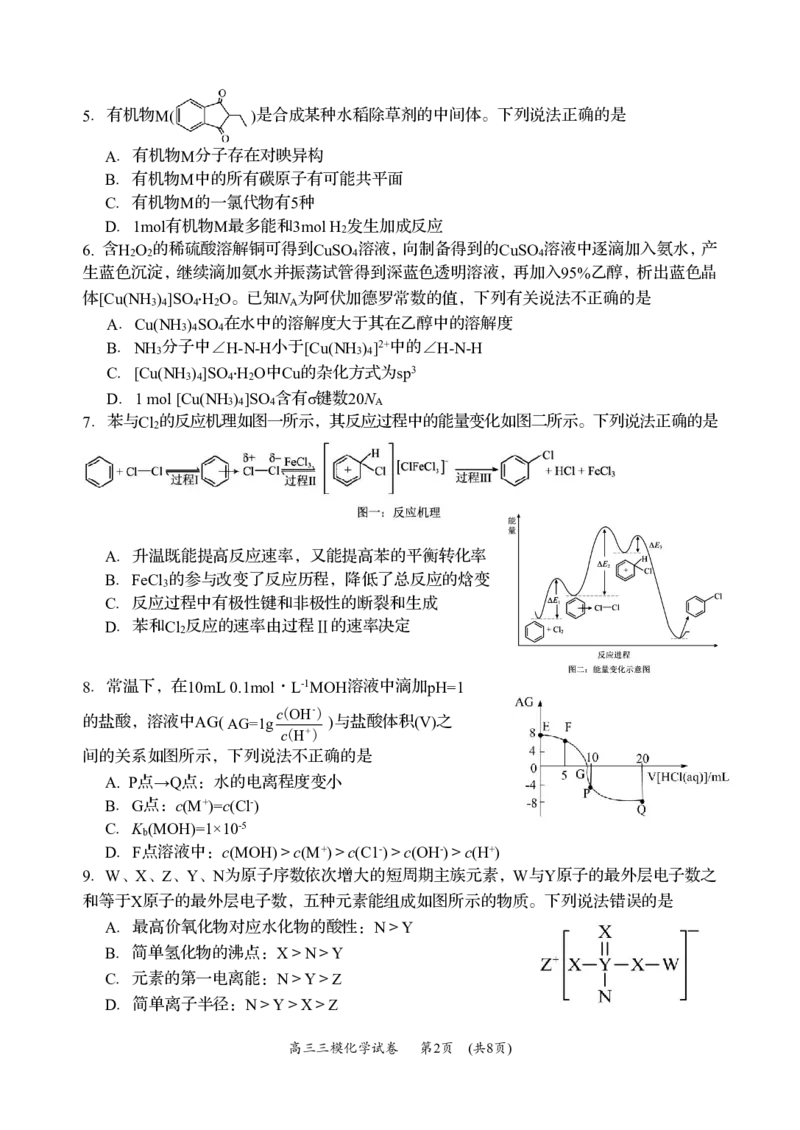
3.实验室由硫铁矿烧渣(含FeO、Fe
2
O
3
、SiO
2
等)制取无水氯化铁的实验原理和装置不.能.达
到实验目的的是
甲 乙 丙 丁
A.用装置甲溶解硫铁矿烧渣 B.用装置乙过滤得到含Fe2+、Fe3+混合溶液
C.用装置丙氧化得到FeC1 溶液 D.用装置丁蒸干溶液获得无水FeC1
3 3
4.下列离子方程式正确的是
A.将碘单质溶于碘化钾溶液中:I +I- I -
2 3
B.用浓氨水吸收烟气中的SO :SO +2OH-=SO 2-+H O
2 2 3 2
C.以铜为电极电解饱和氯化钠溶液阳极电极反应式:2Cl--2e-=Cl ↑
2
D.CH BrCOOH与足量氢氧化钠溶液共热:CH BrCOOH+OH- CH BrCOO-+H O
2 2 2 2
高三三模化学试卷 第1页 (共8页)
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}5.有机物M( )是合成某种水稻除草剂的中间体。下列说法正确的是
A.有机物M分子存在对映异构
B.有机物M中的所有碳原子有可能共平面
C.有机物M的一氯代物有5种
D.1mol有机物M最多能和3molH 发生加成反应
2
6. 含H O 的稀硫酸溶解铜可得到CuSO 溶液,向制备得到的CuSO 溶液中逐滴加入氨水,产
2 2 4 4
生蓝色沉淀,继续滴加氨水并振荡试管得到深蓝色透明溶液,再加入95%乙醇,析出蓝色晶
体[Cu(NH ) ]SO ·H O。已知N 为阿伏加德罗常数的值,下列有关说法不正确的是
3 4 4 2 A
A.Cu(NH ) SO 在水中的溶解度大于其在乙醇中的溶解度
3 4 4
B.NH 分子中∠H-N-H小于[Cu(NH ) ]2+中的∠H-N-H
3 3 4
C.[Cu(NH ) ]SO ·H O中Cu的杂化方式为sp3
3 4 4 2
D.1mol[Cu(NH ) ]SO 含有σ键数20N
3 4 4 A
7.苯与Cl 的反应机理如图一所示,其反应过程中的能量变化如图二所示。下列说法正确的是
2
A.升温既能提高反应速率,又能提高苯的平衡转化率
B.FeCl 的参与改变了反应历程,降低了总反应的焓变
3
C.反应过程中有极性键和非极性的断裂和生成
D.苯和Cl 反应的速率由过程Ⅱ的速率决定
2
8.常温下,在10mL0.1mol·L-1MOH溶液中滴加pH=1
c(OH-)
的盐酸,溶液中AG(AG=1g )与盐酸体积(V)之
c(H+)
间的关系如图所示,下列说法不正确的是
A. P点→Q点:水的电离程度变小
B.G点:c(M+)=c(Cl-)
C.K (MOH)=1×10-5
b
D.F点溶液中:c(MOH)>c(M+)>c(C1-)>c(OH-)>c(H+)
9.W、X、Z、Y、N为原子序数依次增大的短周期主族元素,W与Y原子的最外层电子数之
和等于X原子的最外层电子数,五种元素能组成如图所示的物质。下列说法错误的是
A.最高价氧化物对应水化物的酸性:N>Y
B.简单氢化物的沸点:X>N>Y
C.元素的第一电离能:N>Y>Z
D.简单离子半径:N>Y>X>Z
高三三模化学试卷 第2页 (共8页)
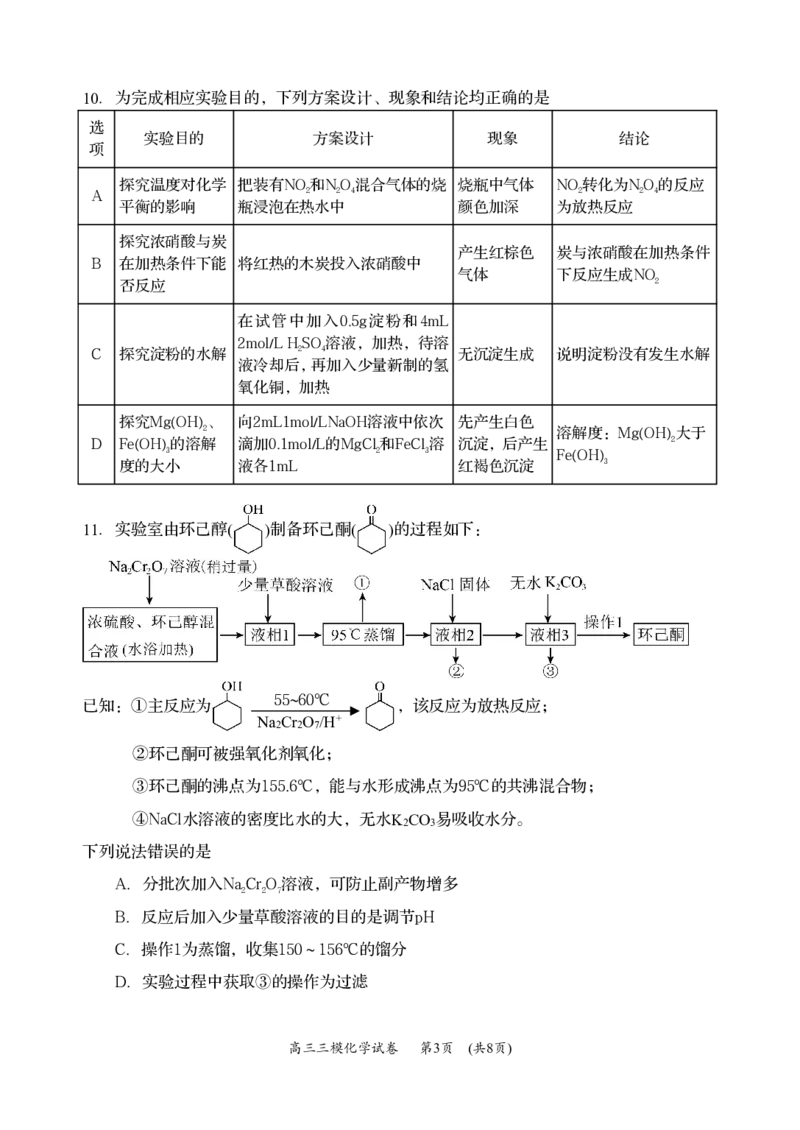
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}10.为完成相应实验目的,下列方案设计、现象和结论均正确的是
选
实验目的 方案设计 现象 结论
项
探究温度对化学 把装有NO和NO混合气体的烧 烧瓶中气体 NO转化为NO的反应
A 2 2 4 2 2 4
平衡的影响 瓶浸泡在热水中 颜色加深 为放热反应
探究浓硝酸与炭
产生红棕色 炭与浓硝酸在加热条件
B 在加热条件下能 将红热的木炭投入浓硝酸中
气体 下反应生成NO
否反应 2
在试管中加入0.5g淀粉和4mL
2mol/LHSO溶液,加热,待溶
C 探究淀粉的水解 2 4 无沉淀生成 说明淀粉没有发生水解
液冷却后,再加入少量新制的氢
氧化铜,加热
探究Mg(OH)、 向2mL1mol/LNaOH溶液中依次 先产生白色
2 溶解度:Mg(OH)大于
D Fe(OH)的溶解 滴加0.1mol/L的MgCl和FeCl溶 沉淀,后产生 2
3 2 3 Fe(OH)
度的大小 液各1mL 红褐色沉淀 3
11.实验室由环己醇( )制备环己酮( )的过程如下:
55~60℃
已知:①主反应为 ,该反应为放热反应;
Na Cr O /H+
2 2 7
②环己酮可被强氧化剂氧化;
③环己酮的沸点为155.6℃,能与水形成沸点为95℃的共沸混合物;
④NaCl水溶液的密度比水的大,无水K CO 易吸收水分。
2 3
下列说法错误的是
A.分批次加入NaCrO溶液,可防止副产物增多
2 2 7
B.反应后加入少量草酸溶液的目的是调节pH
C.操作1为蒸馏,收集150~156℃的馏分
D.实验过程中获取③的操作为过滤
高三三模化学试卷 第3页 (共8页)
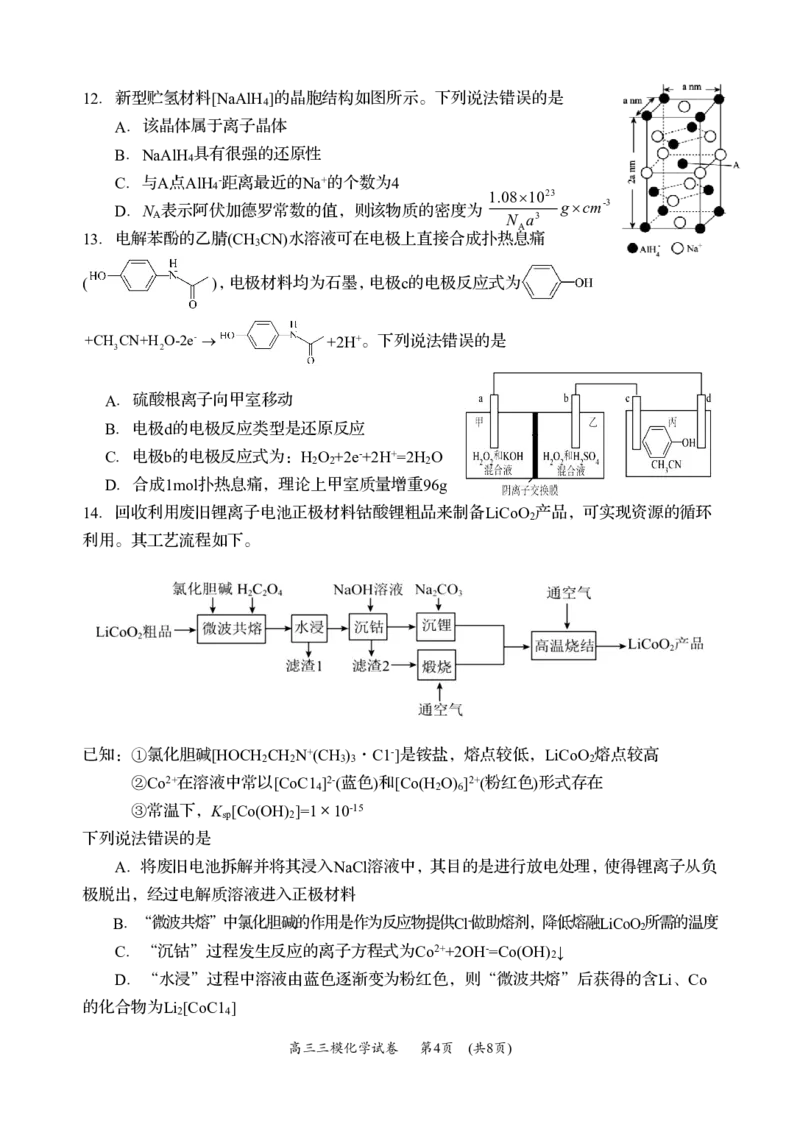
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}12.新型贮氢材料[NaAlH ]的晶胞结构如图所示。下列说法错误的是
4
A.该晶体属于离子晶体
B.NaAlH 具有很强的还原性
4
C.与A点AlH -距离最近的Na+的个数为4
4
1.081023
D.N 表示阿伏加德罗常数的值,则该物质的密度为 gcm-3
A N a3
A
13.电解苯酚的乙腈(CH CN)水溶液可在电极上直接合成扑热息痛
3
( ),电极材料均为石墨,电极c的电极反应式为
+CH CN+H O-2e- +2H+。下列说法错误的是
3 2
A.硫酸根离子向甲室移动
B.电极d的电极反应类型是还原反应
C.电极b的电极反应式为:H O +2e-+2H+=2H O
2 2 2
D.合成1mol扑热息痛,理论上甲室质量增重96g
14.回收利用废旧锂离子电池正极材料钴酸锂粗品来制备LiCoO 产品,可实现资源的循环
2
利用。其工艺流程如下。
已知:①氯化胆碱[HOCH CH N+(CH ) ·C1-]是铵盐,熔点较低,LiCoO 熔点较高
2 2 3 3 2
②Co2+在溶液中常以[CoC1 ]2-(蓝色)和[Co(H O) ]2+(粉红色)形式存在
4 2 6
③常温下,K [Co(OH) ]=1×10-15
sp 2
下列说法错误的是
A.将废旧电池拆解并将其浸入NaCl溶液中,其目的是进行放电处理,使得锂离子从负
极脱出,经过电解质溶液进入正极材料
B.“微波共熔”中氯化胆碱的作用是作为反应物提供Cl-做助熔剂,降低熔融LiCoO所需的温度
2
C.“沉钴”过程发生反应的离子方程式为Co2++2OH-=Co(OH) ↓
2
D.“水浸”过程中溶液由蓝色逐渐变为粉红色,则“微波共熔”后获得的含Li、Co
的化合物为Li [CoC1 ]
2 4
高三三模化学试卷 第4页 (共8页)
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}二、非选择题:(共4小题,共58分)
15.(14分)C1 是工业制备的一种重要原料,很多物质的制备都需要用到氯气,比如工业上
2
用C1 制备POC1 ,反应原理为:P (白磷)+6C1 =4PC1 ,2PC1 +O =2POC1 。已知:PC1 、POC1
2 3 4 2 3 3 2 3 3 3
的部分性质如下:
熔点/℃ 沸点/℃ 相对分子质量 其它
PCl 112 75.5 137.5 遇水生成H PO 和HCl
3 3 3
POCl 2 105.3 153.5 遇水生成H PO 和HCl
3 3 4
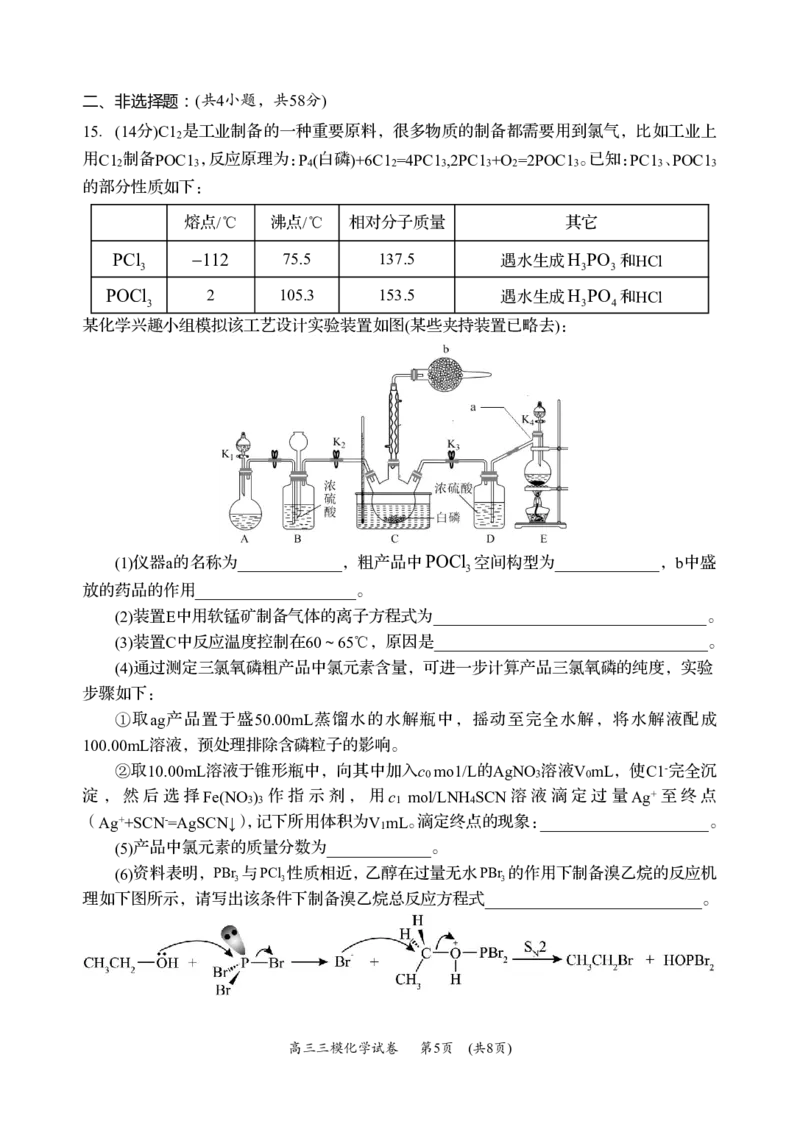
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置已略去):
(1)仪器a的名称为_____________,粗产品中POCl 空间构型为_____________,b中盛
3
放的药品的作用____________________。
(2)装置E中用软锰矿制备气体的离子方程式为__________________________________。
(3)装置C中反应温度控制在60~65℃,原因是__________________________________。
(4)通过测定三氯氧磷粗产品中氯元素含量,可进一步计算产品三氯氧磷的纯度,实验
步骤如下:
①取ag产品置于盛50.00mL蒸馏水的水解瓶中,摇动至完全水解,将水解液配成
100.00mL溶液,预处理排除含磷粒子的影响。
②取10.00mL溶液于锥形瓶中,向其中加入c mo1/L的AgNO 溶液V mL,使C1-完全沉
0 3 0
淀,然后选择Fe(NO ) 作指示剂,用c mol/LNH SCN溶液滴定过量Ag+至终点
3 3 1 4
(Ag++SCN-=AgSCN↓),记下所用体积为V mL。滴定终点的现象:_____________________。
1
(5)产品中氯元素的质量分数为_____________。
(6)资料表明,PBr 与PCl 性质相近,乙醇在过量无水PBr 的作用下制备溴乙烷的反应机
3 3 3
理如下图所示,请写出该条件下制备溴乙烷总反应方程式___________________________。
高三三模化学试卷 第5页 (共8页)
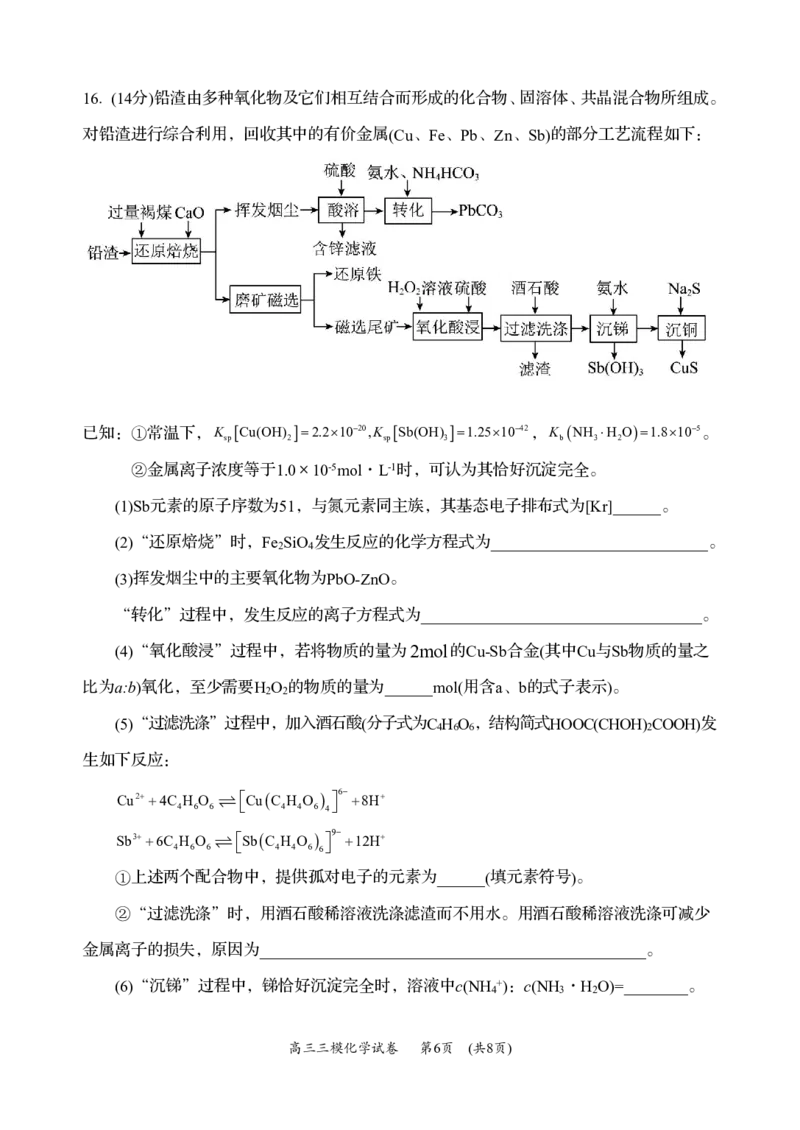
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}16.(14分)铅渣由多种氧化物及它们相互结合而形成的化合物、固溶体、共晶混合物所组成。
对铅渣进行综合利用,回收其中的有价金属(Cu、Fe、Pb、Zn、Sb)的部分工艺流程如下:
已知:①常温下,K Cu(OH) 2.21020,K Sb(OH) 1.251042,K NH H O1.8105。
sp 2 sp 3 b 3 2
②金属离子浓度等于1.0×10-5mol·L-1时,可认为其恰好沉淀完全。
(1)Sb元素的原子序数为51,与氮元素同主族,其基态电子排布式为[Kr]______。
(2)“还原焙烧”时,Fe SiO 发生反应的化学方程式为___________________________。
2 4
(3)挥发烟尘中的主要氧化物为PbO-ZnO。
“转化”过程中,发生反应的离子方程式为___________________________________。
(4)“氧化酸浸”过程中,若将物质的量为2mol的Cu-Sb合金(其中Cu与Sb物质的量之
比为a:b)氧化,至少需要H O 的物质的量为______mol(用含a、b的式子表示)。
2 2
(5)“过滤洗涤”过程中,加入酒石酸(分子式为CHO,结构简式HOOC(CHOH)COOH)发
4 6 6 2
生如下反应:
Cu24C
4
H
6
O
6
CuC
4
H
4
O
6
4
6 8H
Sb36C
4
H
6
O
6
SbC
4
H
4
O
6
6
9 12H
①上述两个配合物中,提供孤对电子的元素为______(填元素符号)。
②“过滤洗涤”时,用酒石酸稀溶液洗涤滤渣而不用水。用酒石酸稀溶液洗涤可减少
金属离子的损失,原因为________________________________________________。
(6)“沉锑”过程中,锑恰好沉淀完全时,溶液中c(NH +):c(NH ·H O)=________。
4 3 2
高三三模化学试卷 第6页 (共8页)
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}17.(15分)2024年上海国际碳中和技术博览会以“中和科技、碳索未来”为主题,重点聚焦
二氧化碳的捕捉、利用与封存(CCUS)等问题。回答下列问题:
I.CO 是典型的温室气体,Sabatier反应可实现CO 转化为甲烷,实现CO 的资源化利用。
2 2 2
合成CH 过程中涉及如下反应:
4
甲烷化反应(主反应):①CO (g)4H (g) CH (g)2H O(g) ΔH 164.7kJmol1
2 2 4 2 1
逆变换反应(副反应):②CO (g)+H (g)CO(g)+H O(g) ΔH =+41.1kJmol-1
2 2 2 2
(1)反应③2CO(g)2H (g)CO (g)CH (g) ΔH ___________,该反应在
2 2 4
___________(填“高温”“低温”或“任何温度”)下能自发进行。
(2)下列叙述中能说明反应①达到平衡状态的是________(填字母)。
A.断裂4molC-H的同时断裂1molC=O B.恒温恒容条件下,体系压强不再变化
C.恒温恒容条件下,气体的密度不再变化 D.v (CO )=v (H O)
正 2 逆 2
c(CH )·c2(H O)
E.绝热恒容条件下, 4 2 不再变化
c(CO )·c4(H )
2 2
nH
4
(3)科研小组按 2 = 进行投料,下面探究影响CH 选择性的一些因素。
nCO 1 4
2
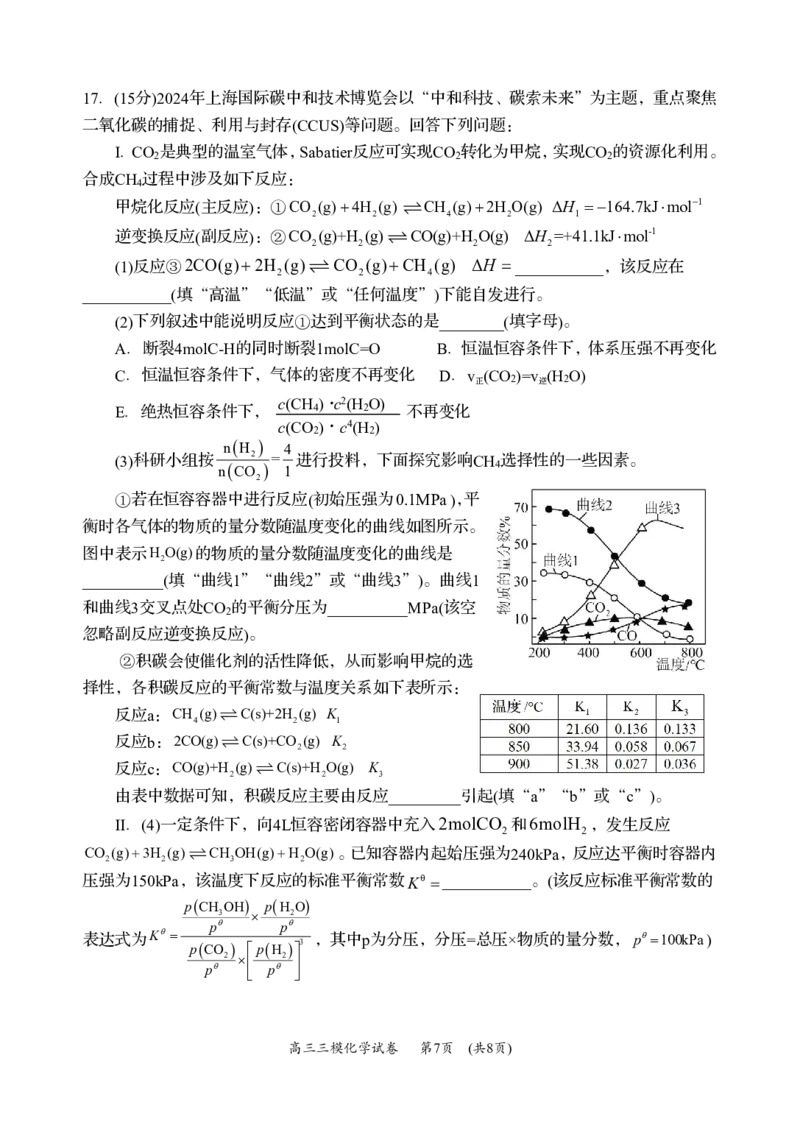
①若在恒容容器中进行反应(初始压强为0.1MPa),平
衡时各气体的物质的量分数随温度变化的曲线如图所示。
图中表示H O(g)的物质的量分数随温度变化的曲线是
2
__________(填“曲线1”“曲线2”或“曲线3”)。曲线1
和曲线3交叉点处CO 的平衡分压为__________MPa(该空
2
忽略副反应逆变换反应)。
②积碳会使催化剂的活性降低,从而影响甲烷的选
择性,各积碳反应的平衡常数与温度关系如下表所示:
反应a:CH (g)C(s)+2H (g) K
4 2 1
反应b:2CO(g)C(s)+CO (g) K
2 2
反应c:CO(g)+H (g)C(s)+H O(g) K
2 2 3
由表中数据可知,积碳反应主要由反应_________引起(填“a”“b”或“c”)。
II.(4)一定条件下,向4L恒容密闭容器中充入2molCO 和6molH ,发生反应
2 2
CO (g)3H (g)CH OH(g)H O(g)。已知容器内起始压强为240kPa,反应达平衡时容器内
2 2 3 2
压强为150kPa,该温度下反应的标准平衡常数K ___________。(该反应标准平衡常数的
pCH OH pH O
3 2
p p
表达式为K ,其中p为分压,分压=总压×物质的量分数,p100kPa)
pCO pH 3
2 2
p
p
高三三模化学试卷 第7页 (共8页)
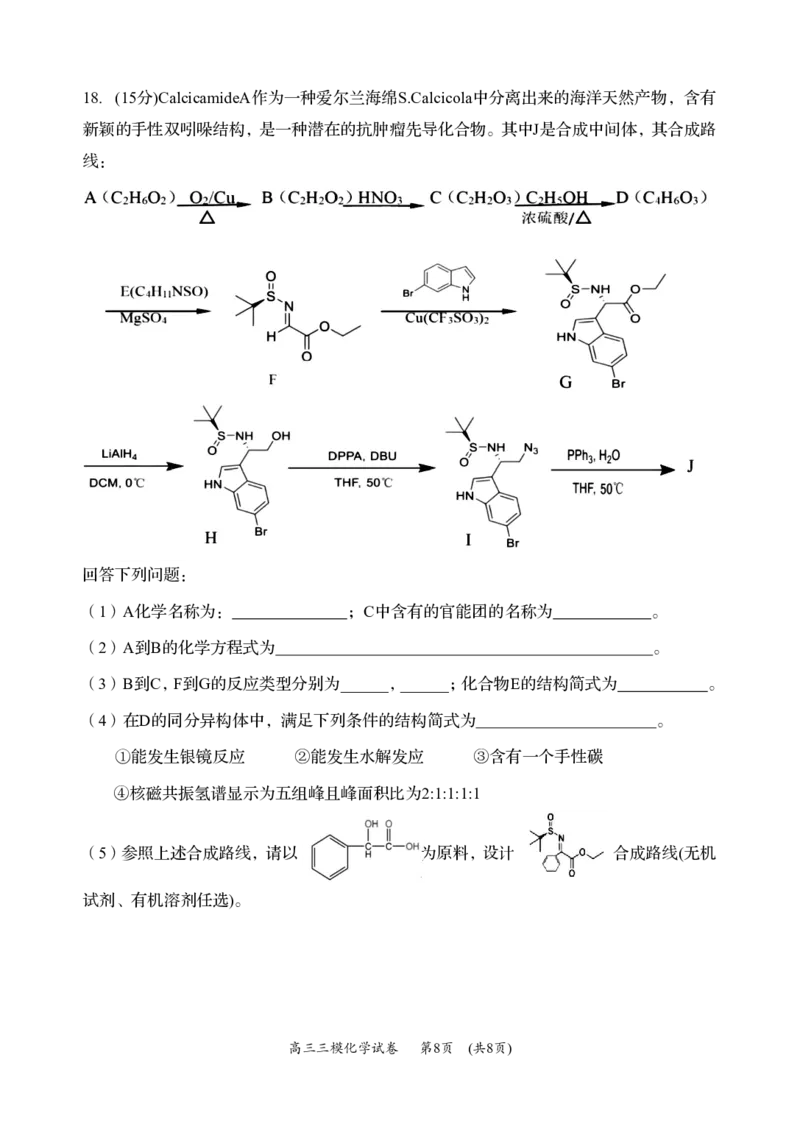
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}18.(15分)CalcicamideA作为一种爱尔兰海绵S.Calcicola中分离出来的海洋天然产物,含有
新颖的手性双吲哚结构,是一种潜在的抗肿瘤先导化合物。其中J是合成中间体,其合成路
线:
回答下列问题:
(1)A化学名称为: ;C中含有的官能团的名称为 。
(2)A到B的化学方程式为 。
(3)B到C,F到G的反应类型分别为______,______;化合物E的结构简式为 。
(4)在D的同分异构体中,满足下列条件的结构简式为 。
①能发生银镜反应 ②能发生水解发应 ③含有一个手性碳
④核磁共振氢谱显示为五组峰且峰面积比为2:1:1:1:1
(5)参照上述合成路线,请以 为原料,设计 合成路线(无机
试剂、有机溶剂任选)。
高三三模化学试卷 第8页 (共8页)
{#{QQABJYoEggCgApBAARgCEQXiCkIQkAEACIoGgBAMoAAAyRFABCA=}#}