文档内容
人教版(2019)必修第一册第一章第三节 氧化还原反应
课时训练三
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.古医典富载化学知识,下述之物见其氧化性者为
A.金(Au):“虽被火亦未熟"
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳( ):“色黄,以苦酒(醋)洗刷则白”
2.下列分类标准不正确的是
A.化学反应分为氧化还原反应、非氧化还原反应(标准:是否有电子的转移)
B.分散系分为溶液、胶体、浊液(标准:能否产生丁达尔效应)
C.纯净物分为单质、化合物(标准:组成纯净物的元素种类数)
D.化合物分为电解质、非电解质(标准:在水溶液中或熔融状态下能否导电)
3.下列反应中属于氧化还原反应的是
A.NH +HCl=NH Cl B.2Fe(OH) Fe O+3H O
3 4 3 2 3 2
C.3Fe+4H O(g) Fe O+4H ↑ D.CaCO +2HCl=CaCl +H O+CO↑
2 3 4 2 3 2 2 2
4.下列反应中,不属于氧化还原反应的是
A.3Cl+6KOH 5KCl+KClO +3H O
2 3 2
B.2NO +2NaOH=NaNO +NaNO +H O
2 3 2 2
C.Cu+2FeCl =CuCl +2FeCl
3 2 2
D.NaOH+HCl=H O+NaCl
2
5.下列关于氧化还原反应的叙述正确的是
A.H 还原CuO的反应只属于还原反应
2
B.置换反应都是氧化还原反应,所以,3CO+Fe O 2Fe+3CO 既是置换反应又是
2 3 2
氧化还原反应C.3O 2O 是氧化还原反应
2 3
D.复分解反应一定不是氧化还原反应
6.下列化学方程式中,表示电子转移的方向和数目都正确的是
A.
B. -
C.
D.
7.关于反应KHIO +9HI=2KI+4I +6H O,下列说法正确的是
2 3 6 2 2
A. KHIO 发生氧化反应 B.KI是还原产物
2 3 6
C.生成12.7g I 时,转移0.1mol电子 D.还原剂与氧化剂的物质的量之比为
2
7:1
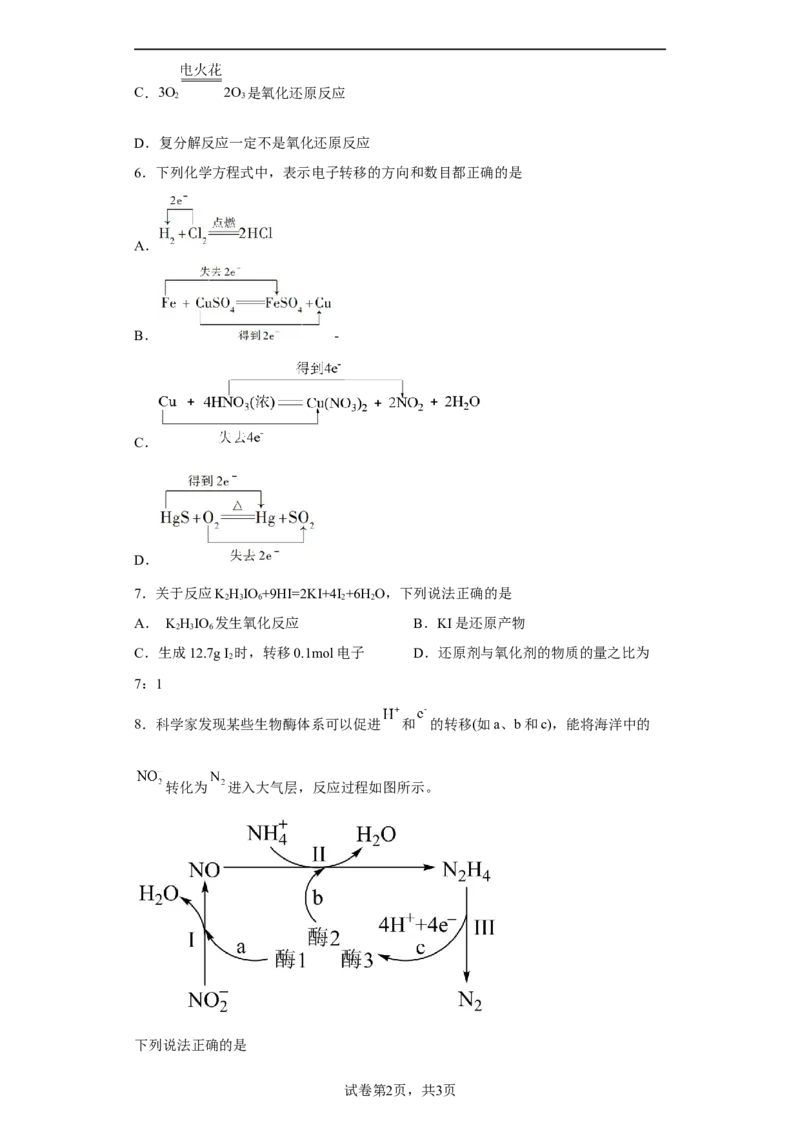
8.科学家发现某些生物酶体系可以促进 和 的转移(如a、b和c),能将海洋中的
转化为 进入大气层,反应过程如图所示。
下列说法正确的是
试卷第2页,共3页A.过程Ⅰ中 发生氧化反应
B.a和b中转移的 数目相等
C.过程Ⅱ中参与反应的
D.过程Ⅰ→Ⅲ的总反应为
9.下列有关说法正确的是
A.厨房可用食醋除水垢,食醋的作用是作氧化剂
B.某食品包装袋内装有一包铁粉,它的主要作用是作干燥剂
C.病人补铁( )的同时需补维生素C,维生素C的作用是作还原剂
D.洁厕灵和“84”消毒液混合使用可增强消毒杀菌效果,体现了两者的强氧化性
10.关于反应 ,下列说法正确的是
A. 发生还原反应
B. 既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2∶1
D. 发生反应,转移 电子
11.用电石(主要成分为CaC ,含CaS和Ca P 等)制取乙炔时,常用CuSO 溶液除
2 3 2 4
去乙炔中的杂质。反应为:
①CuSO+H S=CuS↓+H SO
4 2 2 4
②11PH +24CuSO+12H O=3HPO +24H SO +8Cu P↓
3 4 2 3 4 2 4 3
下列分析不正确的是
A.CaS、Ca P 发生水解反应的化学方程式:CaS+2H O=Ca(OH) +H S↑、
3 2 2 2 2
Ca P+6H O=3Ca(OH) +2PH↑
3 2 2 2 3
B.不能依据反应①比较硫酸与氢硫酸的酸性强弱
C.反应②中每24 mol CuSO 氧化11 mol PH
4 3
D.用酸性KMnO 溶液验证乙炔还原性时,HS、PH 有干扰
4 2 3
12.关于反应8NH +6NO=7N +12H O,下列说法正确的是
3 2 2 2
A.NH 中H元素被氧化
3
B.NO 在反应过程中失去电子
2
C.还原剂与氧化剂的物质的量之比为3:4D.氧化产物与还原产物的质量之比为4:3
13.实验室制备 过程为:①高温下在熔融强碱性介质中用 氧化 制
备 ;②水溶后冷却,调溶液 至弱碱性, 歧化生成 和
;③减压过滤,将滤液蒸发浓缩、冷却结晶,再减压过滤得 。下列说法
正确的是
A.①中用瓷坩埚作反应器
B.①中用 作强碱性介质
C.②中 只体现氧化性
D. 转化为 的理论转化率约为66.7%
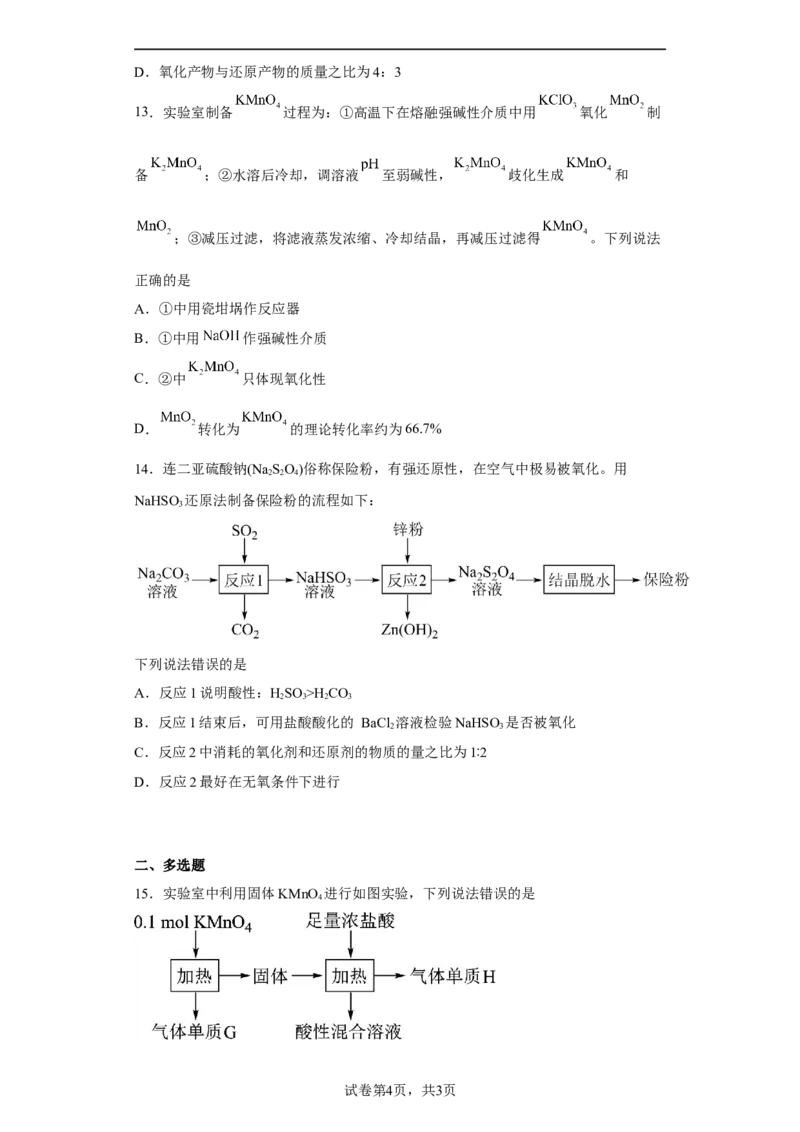
14.连二亚硫酸钠(Na SO)俗称保险粉,有强还原性,在空气中极易被氧化。用
2 2 4
NaHSO 还原法制备保险粉的流程如下:
3
下列说法错误的是
A.反应1说明酸性:HSO >H CO
2 3 2 3
B.反应1结束后,可用盐酸酸化的 BaCl 溶液检验NaHSO 是否被氧化
2 3
C.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2
D.反应2最好在无氧条件下进行
二、多选题
15.实验室中利用固体KMnO 进行如图实验,下列说法错误的是
4
试卷第4页,共3页A.G与H均为氧化产物 B.实验中KMnO 只作氧化剂
4
C.Mn元素至少参与了3个氧化还原反应 D.G与H的物质的量之和可能为
0.25mol
三、填空题
16.高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸
钾。
2Fe(OH) +3ClO-+4OH-=2FeO +3Cl-+5H O
3 2
(1)FeO 中铁元素化合价为____,在该反应中氧化剂是____,还原剂是____,氧化产
物是____。
(2)请用双线桥表示反应中电子转移情况:____。
(3)根据化合价,推测FeO 能和下列____反应(填序号)。
A.KMnO B.SO C.HS D.O
4 2 2 2
17.已知反应:
① ② ③
④ ⑤ ⑥
(1)上述反应不属于氧化还原反应的有____(填序号,下同)。 被氧化的是____,
被还原的是____,属于氧化还原反应,但其中的 既不被氧化又不被还原的是
_____。
(2)用双线桥法表示反应②的电子转移方向和数目:______。
(3)用单线桥法表示反应③的电子转移方向和数目:______。
(4)写出反应④的离子方程式:______。
18.回答下列问题:
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO
4KMnO +MnO+O ↑,其中被氧化的元素是___________(填元素符号),还原产物是
2 4 2 2
___________(填化学式)。
(2)反应方程式:KCr O+14HCl 2KCl+2CrCl +3Cl↑+7H O中还原剂是___________,
2 2 7 3 2 2
氧化产物是___________。
(3)下面三个方法都可以用来制氯气:
①4HCl(浓)+MnO MnCl +Cl↑+2H O
2 2 2 2
②KClO +6HCl(浓)=3Cl ↑+KCl+3H O
3 2 2
③KMnO +HCl(浓)→KCl+MnCl +Cl↑+H O(未配平)
4 2 2 2
根据以上三个反应,回答下列有关问题:
1、反应②的离子方程式为___________。
II、反应①中,氧化产物与还原产物的质量比为___________。
III、已知反应④:4HCl+O 2Cl+2H O(g),该反应也能制得氯气。提示:反应
2 2 2
条件越简单反应越容易发生,说明性质越强烈。则MnO 、O、KMnO 三种物质氧化
2 2 4
性由强到弱的顺序为___________。
IV、配平③______KMnO +_____HCl(浓)=_____KCl+____MnCl +_____Cl↑+____H O,
4 2 2 2
___________
19.亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
亚硝酸钠加热到320℃以上会分解产生 、 和 ,其水溶液呈碱性,能与
溶液反应生成难溶于水、易溶于酸的 。由于 有毒性,将含该物
质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方
法之一如下:
___________ ___________KI+___________=___________NO↑+___________
___________ ___________ ___________
(1)请完成该化学方程式并配平。___________
试卷第6页,共3页(2)从物质分类角度来看, 是___________(填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理 并不是最佳方法,其原因是___________。从环保角度来
讲,要将 转化为氮气,所用物质的___________(填“氧化性”或“还原性”)应
该比KI更___________(填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是___________(填序号)。
A.分别溶于水
B.分别溶于水并滴加 酸化的 溶液
C.分别加强热并收集气体检验
D.用筷子分别蘸取固体品尝味道
(5)误食 会导致人体血红蛋白中的 转化为 而中毒,该过程中 表
现出的性质与下列___________(填序号)反应中 表现出的性质相同。
A.
B.
C.
D.
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式,
并用单线桥表示其电子转移的方向和数目:___________。
20.有下列反应:
①2HO+Cl +SO=H SO +2HCl
2 2 2 2 4
②2KMnO+16HCl(浓)= 2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
根据上述两个反应回答:
(1)氧化性强弱顺序为_______,还原性强弱顺序为_______。
(2)反应①中氧化产物和还原产物的质量之比为_______。
(3)反应②中浓盐酸表现出的性质是_______。A.还原性 B.酸性 C.氧化性
四、实验题
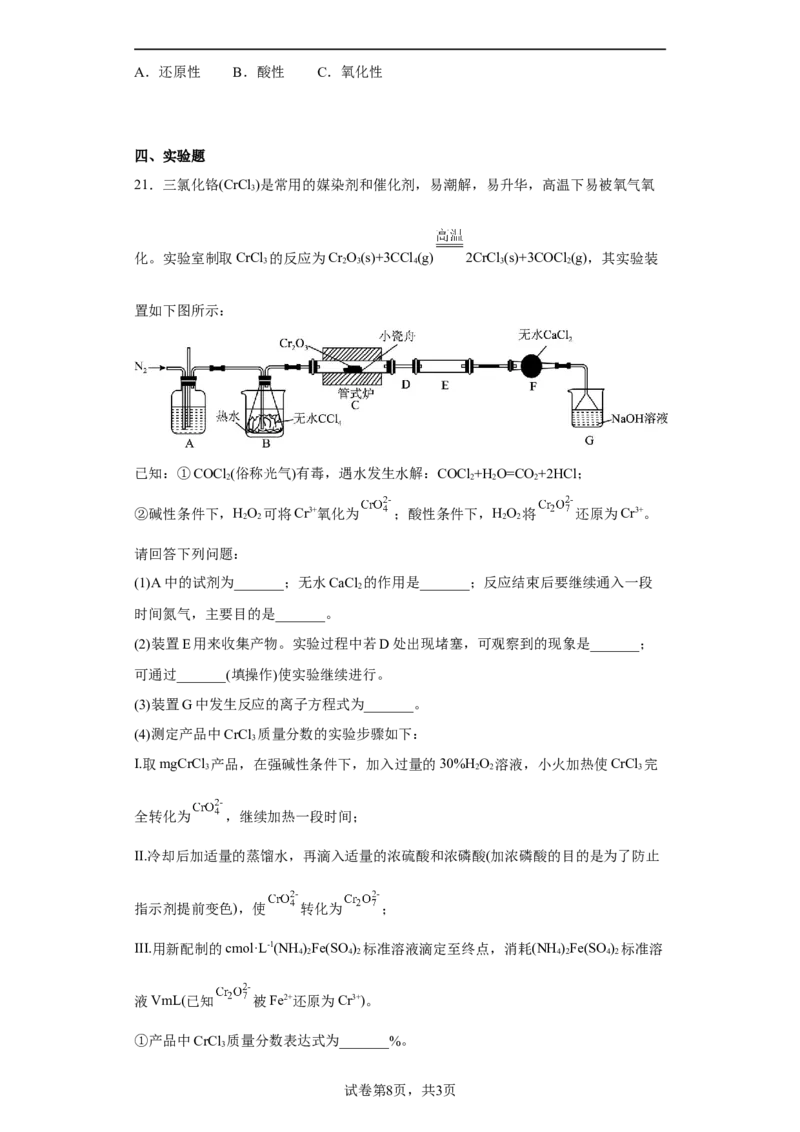
21.三氯化铬(CrCl )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧
3
化。实验室制取CrCl 的反应为Cr O(s)+3CCl (g) 2CrCl (s)+3COCl (g),其实验装
3 2 3 4 3 2
置如下图所示:
已知:①COCl (俗称光气)有毒,遇水发生水解:COCl +H O=CO+2HCl;
2 2 2 2
②碱性条件下,HO 可将Cr3+氧化为 ;酸性条件下,HO 将 还原为Cr3+。
2 2 2 2
请回答下列问题:
(1)A中的试剂为_______;无水CaCl 的作用是_______;反应结束后要继续通入一段
2
时间氮气,主要目的是_______。
(2)装置E用来收集产物。实验过程中若D处出现堵塞,可观察到的现象是_______;
可通过_______(填操作)使实验继续进行。
(3)装置G中发生反应的离子方程式为_______。
(4)测定产品中CrCl 质量分数的实验步骤如下:
3
I.取mgCrCl 产品,在强碱性条件下,加入过量的30%H O 溶液,小火加热使CrCl 完
3 2 2 3
全转化为 ,继续加热一段时间;
II.冷却后加适量的蒸馏水,再滴入适量的浓硫酸和浓磷酸(加浓磷酸的目的是为了防止
指示剂提前变色),使 转化为 ;
III.用新配制的cmol·L-1(NH )Fe(SO ) 标准溶液滴定至终点,消耗(NH )Fe(SO ) 标准溶
4 2 4 2 4 2 4 2
液VmL(已知 被Fe2+还原为Cr3+)。
①产品中CrCl 质量分数表达式为_______%。
3
试卷第8页,共3页②下列操作将导致产品中CrCl 质量分数测定值偏低的是_______(填字母标号)。
3
A.步骤I中未继续加热一段时间
B.步骤III中所用(NH )Fe(SO ) 溶液已变质
4 2 4 2
C.步骤II中未加浓磷酸
D.步骤III中读数时,滴定前俯视,滴定后平视
22.硫氰化钾(KSCN)是一种用途广泛的化学药品,常用于合成树脂、杀虫杀菌剂等。
某实验小组用下图所示的装置制备硫化钾。
已知 是一种难溶于水的无色液体,密度为1.26 难溶于 ,回答下列
问题:
(1)制备 溶液:三颈烧瓶内盛放有 、水和催化剂,实验开始时,打开 ,
( 处于关闭状态)加热装置A、D,使A中产生的氨气缓缓通入到三颈烧瓶中,反应
至 消失,反应的方程式为: 。
①装置A中______(填“能”或者“不能”)直接加热 固体制取氨气
②仪器B的名称是:______。
③装置C的作用是:_____。
④三颈烧瓶左侧导管口必须插入到下层的 液体中,主要原因是_____(写出一条原因
即可)。
(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭 ,移开水浴,将装置D继续加热至105℃, 完全分解后(反应方程式为 ),打开 ,继续保持溶液温度为
105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为____。
②装置E可用于处理尾气,已知酸性重铬酸钾溶液能将 氧化生成浅黄色沉淀。铬
元素被还原为 ,写出其氧化 的离子方程式_____。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、______、过
滤、洗涤、干燥,得到硫氰化钾晶体。
试卷第10页,共3页参考答案:
1.C
【详解】A.金“虽被火亦未熟”是指金单质在空气中被火灼烧也不反应,反应金的化学
性质很稳定,与其氧化性无关,A不合题意;
B.石灰(CaO):“以水沃之,即热蒸而解”是指CaO+H O=Ca(OH) ,反应放热,产生大量的
2 2
水汽,而CaO由块状变为粉末状,未发生氧化还原反应,与其氧化性无关,B不合题意;
C.石硫黄即S:“能化……银、铜、铁,奇物”是指2Ag+S Ag S、Fe+S FeS、2Cu+S
2
Cu S,反应中S作氧化剂,与其氧化性有关,C符合题意;
2
D.石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”是指
3
CaCO +2CH COOH=(CH COO) Ca+H O+CO↑,未发生氧化还原反应,与其氧化性无关,D
3 3 3 2 2 2
不合题意;
故答案为:C。
2.B
【详解】A.根据是否有电子转移(化合价升降),化学反应可分为氧化还原反应和非氧
化还原反应,A项正确;
B.分散系可分为溶液、胶体、浊液,分类标准是分散质微粒直径的大小,B项错误;
C.根据组成纯净物的元素种类数,纯净物可分为单质和化合物,C项正确;
D.根据在水溶液中或熔融状态下能否导电,化合物可分为电解质和非电解质,D项正确;
故选:B。
3.C
【详解】A.该反应中元素化合价不变,因此不属于氧化还原反应,A错误;
B.该反应中元素化合价不变,因此不属于氧化还原反应,B错误;
C.在该反应中,有Fe、H两种元素化合价发生变化,因此反应属于氧化还原反应,C正
确;
D.该反应中没有元素化合价发生变化,因此反应不属于氧化还原反应,D错误;
故选C。
4.D【详解】A.3Cl+6KOH 5KCl+KClO +3H O,反应过程中,氯元素化合价改变,属于
2 3 2
氧化还原反应,故不选A;
B.2NO +2NaOH=NaNO +NaNO +H O,反应过程中,氮元素化合价改变,属于氧化还原
2 3 2 2
反应,故不选B;
C.Cu+2FeCl =CuCl +2FeCl ,反应过程中,铜元素、铁元素化合价改变,属于氧化还原反
3 2 2
应,故不选C;
D.NaOH+HCl=H O+NaCl,反应过程中,元素化合价不变,不属于氧化还原反应,故选
2
D;
选D。
5.D
【详解】A.氧化还原反应是一个整体,氧化反应和还原反应同时在一个反应中,在
CuO+H Cu+H O反应过程中,对CuO而言是失去氧被还原,发生还原反应,对H 而
2 2 2
言,则是得到氧被氧化,发生氧化反应,A错误;
B.置换反应都是氧化还原反应,但CO与Fe O 的反应不是置换反应,B错误;
2 3
C.反应前后氧元素化合价都没有变化,属于非氧化还原反应,C错误;
D.复分解反应只是反应物相互交换成分重新组合成新物质,没有电子转移,所以复分解
反应一定不是氧化还原反应,D正确;
故选:D。
6.B
【详解】A.方程式中氢气失去电子,氯气得到电子,箭头由氢气指向氯气,箭头方向标
反,应为 ,A错误;
B.铁与硫酸铜溶液发生置换反应,铁失去2个电子,铜离子得到2个电子,双线桥表示为:
,B正确;
答案第2页,共2页C.Cu由0价升高到+2价,转移2e-,HNO 中部分N由+5价降低到+4价,转移2×e-,
3
正确的表示方法为 ,C错误;
D.HgS中汞元素由+2价降低到0价,得到2e-,O 中氧元素由0价降低到-2价,得到
2
2×2e-,故反应中共得到6e-,HgS中硫元素由-2价升高到+4价,失去6e-,正确的表示方法
为 ,D错误;
故选B。
7.D
【详解】A.反应中I元素的化合价降低,发生得电子的反应,发生还原反应,A错误;
B.KI中的I-由HI变化而来,化合价没有发生变化,KI既不是氧化产物也不是还原产物,
B错误;
C.12.7g I 的物质的量为0.05mol,根据反应方程式,每生成4mol I 转移7mol电子,则生
2 2
成0.05mol I 时转移电子的物质的量为0.0875mol,C错误;
2
D.反应中HI为还原剂,KHIO 为氧化剂,在反应中每消耗1mol KHIO 就有7mol HI失
2 3 6 2 3 6
电子,则还原剂与氧化剂的物质的量的比为7:1,D正确;
故答案选D。
8.D
【详解】A.由图示可知,过程I中NO 转化为NO,氮元素化合价由+3价降低到+2价,
NO 作氧化剂,被还原,发生还原反应,A错误;
B.由图示可知,过程I为NO 在酶1的作用下转化为NO和HO,依据得失电子守恒、电
2荷守恒和原子守恒可知,反应的离子方程式为:NO +2H++e- NO+H O,生成1molNO,a
2
过程转移1mole-,过程II为NO和NH 在酶2的作用下发生氧化还原反应生成HO和
2
NH,依据得失电子守恒、电荷守恒和原子守恒可知,反应的离子方程式为:NO+NH
2 4
+3e-+2H+ HO+NH,消耗1molNO,b过程转移4mol e-,转移电子数目不相等,B错误;
2 2 4
C.由图示可知,过程II发生反应的参与反应的离子方程式为:NO+NH +3e-+2H+
HO+NH,n(NO):n(NH )=1:1,C错误;
2 2 4
D.由图示可知,过程I的离子方程式为NO +2H++e- NO+H O,过程II的离子方程式为
2
NO+NH +3e-+2H+ HO+NH,过程III的离子方程式为NH N↑+4H++4e-,则过程
2 2 4 2 4 2
Ⅰ→Ⅲ的总反应为NO + NH = N↑+2H O,D正确;
2 2
答案选D。
9.C
【详解】A.厨房可食醋除水垢,没有元素化合价变化,属于非氧化还原反应,故A错误;
B.某食品包装袋内装有一包铁粉,它的主要作用是防止食品氧化变质,故B错误;
C.病人补铁( )的同时需补维生素C,维生素C能防止 被氧化为 ,作用是作还
原剂,故C正确;
D.洁厕灵和“84”消毒液混合使用会生成有毒的氯气,盐酸体现还原性,故D错误;
选C。
10.B
【分析】NaSO+H SO =Na SO +S ↓+SO ↑ +H O,该反应的本质是硫代硫酸根离子在酸性
2 2 3 2 4 2 4 2 2
条件下发生歧化反应生成硫和二氧化硫,化合价发生变化的只有S元素一种,硫酸的作用
是提供酸性环境。
答案第4页,共2页【详解】A.HSO 转化为硫酸钠和水,其中所含元素的化合价均未发生变化,故其没有发
2 4
生还原反应,A说法不正确;
B.NaSO 中的S的化合价为+2,其发生歧化反应生成S(0价)和SO (+4价),故其既是氧
2 2 3 2
化剂又是还原剂,B说法正确;
C.该反应的氧化产物是SO ,还原产物为S,氧化产物与还原产物的物质的量之比为
2
1:1,C说法不正确;
D.根据其中S元素的化合价变化情况可知,1mol Na SO 发生反应,要转移2 mol电子,
2 2 3
D说法不正确。
综上所述,本题选B。
11.C
【详解】A.水解过程中元素的化合价不变,根据水解原理结合乙炔中常混有HS、PH 可
2 3
知CaS的水解方程式为CaS+2H O=Ca(OH) +H S↑;Ca P 水解方程式为
2 2 2 3 2
Ca P+6H O=3Ca(OH) +2PH↑,A项正确;
3 2 2 2 3
B.该反应能发生是因为有不溶于水也不溶于酸的CuS生成,因此反应①不能说明HS的
2
酸性强于HSO ,事实上硫酸的酸性强于氢硫酸,B项正确;
2 4
C.反应②中Cu元素化合价从+2价降低到+1价,得到1个电子,P元素化合价从-3价升高
到+5价,失去8个电子,则24molCuSO 完全反应时,可氧化PH 的物质的量是24mol÷8=
4 3
3mol,C项错误;
D.HS、PH 均被KMnO 酸性溶液氧化,所以会干扰KMnO 酸性溶液对乙炔性质的检验,
2 3 4 4
D项正确;
答案选C。
12.D
【分析】由反应8NH +6NO==7N +12H O可知,其中NH 的N元素的化合价由-3升高到
3 2 2 2 3
0、NO 中的N元素的化合价由-+4降低到0,因此,NH 是还原剂, NO 是氧化剂。
2 3 2
【详解】A.NH 中H元素的化合价没有发生变化,故其未被氧化,被氧化的是N元素,A
3
不正确;
B.NO 在反应过程中得到电子,B不正确;
2
C.该反应中,NH 是还原剂,NO 是氧化剂。由化学方程式可知,还原剂与氧化剂的物质
3 2
的量之比为4:3,C说法不正确;
D.该反应中氧化产物和还原产物均为N。还原剂被氧化后得到氧化产物,氧化剂被还原
2后得到还原产物,还原剂与氧化剂的物质的量之比为4:3,因此,氧化产物与还原产物的
质量之比为4:3 ,D说法正确。
综上所述,本题选D。
13.D
【分析】由题中信息可知,高温下在熔融强碱性介质中用KClO 氧化 MnO 制备
3 2
KMnO ,然后水溶后冷却调溶液pH至弱碱性使KMnO 歧化生成KMnO 和MnO ,Mn元
2 4 2 4 4 2
素的化合价由+6变为+7和+4。
【详解】A.①中高温下在熔融强碱性介质中用KClO 氧化 MnO 制备KMnO ,由于瓷坩
3 2 2 4
埚易被强碱腐蚀,故不能用瓷坩埚作反应器,A说法不正确;
B.制备KMnO 时为为防止引入杂质离子,①中用KOH作强碱性介质,不能用 ,B
4
说法不正确;
C.②中KMnO 歧化生成KMnO 和MnO ,故其既体现氧化性又体现还原性,C说法不正
2 4 4 2
确;
D.根据化合价的变化分析,KMnO 歧化生成KMnO 和MnO 的物质的量之比为2:1,根
2 4 4 2
据Mn元素守恒可知,MnO 中的Mn元素只有 转化为KMnO ,因此,MnO 转化为
2 4 2
KMnO 的理论转化率约为66.7%,D说法正确;
4
综上所述,本题选D。
14.C
【详解】A.反应1为二氧化硫通入碳酸钠溶液生成亚硫酸氢钠和二氧化碳,则说明酸性:
HSO >H CO,A正确;
2 3 2 3
B. 反应1结束后,溶液中为亚硫酸氢钠溶液,不与氯化钡反应,若加入可用盐酸酸化的
BaCl 溶液,出现白色沉淀,则沉淀为硫酸钡,可证明NaHSO 被氧化,B正确;
2 3
C. 反应2为 ,亚硫酸氢钠中硫化合价从+4下降到
+3,还原剂是锌,化合价从0升高到+2价,消耗的氧化剂和还原剂的物质的量之比为
2:1,C错误;
D.连二亚硫酸钠(Na SO)俗称保险粉,有强还原性,在空气中极易被氧化,反应2最好在
2 2 4
无氧条件下进行,D正确;
答案选C。
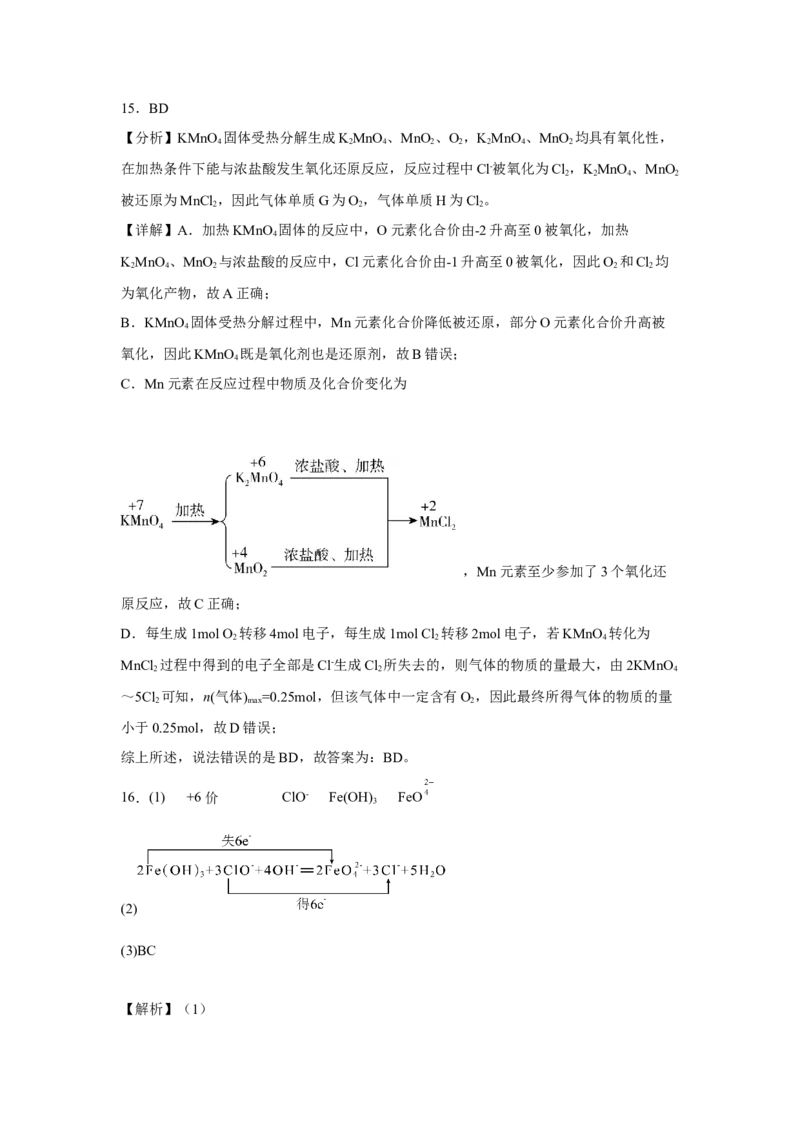
答案第6页,共2页15.BD
【分析】KMnO 固体受热分解生成KMnO 、MnO 、O,KMnO 、MnO 均具有氧化性,
4 2 4 2 2 2 4 2
在加热条件下能与浓盐酸发生氧化还原反应,反应过程中Cl-被氧化为Cl,KMnO 、MnO
2 2 4 2
被还原为MnCl ,因此气体单质G为O,气体单质H为Cl。
2 2 2
【详解】A.加热KMnO 固体的反应中,O元素化合价由-2升高至0被氧化,加热
4
KMnO 、MnO 与浓盐酸的反应中,Cl元素化合价由-1升高至0被氧化,因此O 和Cl 均
2 4 2 2 2
为氧化产物,故A正确;
B.KMnO 固体受热分解过程中,Mn元素化合价降低被还原,部分O元素化合价升高被
4
氧化,因此KMnO 既是氧化剂也是还原剂,故B错误;
4
C.Mn元素在反应过程中物质及化合价变化为
,Mn元素至少参加了3个氧化还
原反应,故C正确;
D.每生成1mol O 转移4mol电子,每生成1mol Cl 转移2mol电子,若KMnO 转化为
2 2 4
MnCl 过程中得到的电子全部是Cl-生成Cl 所失去的,则气体的物质的量最大,由2KMnO
2 2 4
~5Cl 可知,n(气体) =0.25mol,但该气体中一定含有O,因此最终所得气体的物质的量
2 max 2
小于0.25mol,故D错误;
综上所述,说法错误的是BD,故答案为:BD。
16.(1) +6价 ClO- Fe(OH) FeO
3
(2)
(3)BC
【解析】(1)FeO 中O元素为-2价,则铁元素化合价为+6价,Cl元素化合价降低,氧化剂是ClO-,Fe
元素化合价升高,还原剂是Fe(OH) ,氧化产物是FeO ;
3
(2)
Fe元素从+3升高到+6,有2个Fe原子变价,失去6个电子,Cl元素从+1降至-1,有3个
Cl原子变价,得到6个电子,用双线桥表示反应中电子转移情况:
(3)
FeO 中铁元素化合价为+6价,是高价态,具有氧化性,能与还原性物质反应,即能与
SO 、HS反应,故选BC。
2 2
17. ①⑤⑥ ③ ④ ②
【详解】(1)反应①⑤⑥中无元素化合价的改变,不属于氧化还原反应; 中O元素被氧
化为 时, 作还原剂,故 被氧化的是③; 中H元素被还原为 时,
作氧化剂, 被还原的是④;反应②中仅N元素的化合价发生改变,因此 既是氧化
剂又是还原剂, 既不是氧化剂又不是还原剂;
(2) 反应②中N元素的化合价既升高,又降低,用双线桥法表示为:
答案第8页,共2页;
(3)反应③中水中氧元素化合价升高,失去电子,氟单质化合价降低,得到电子,用单线桥
法表示为: ;
(4)反应④生成的氢氧化钠为强碱,故离子方程式为: 。
18.(1) O KMnO 、MnO
2 4 2
(2) HCl Cl
2
(3) ClO +6H++5Cl-=3Cl↑+3H O 71:126 KMnO >MnO >O
2 2 4 2 2
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
【解析】(1)反应2KMnO KMnO +MnO+O ↑,KMnO 中氧元素的化合价升高,生成
4 2 4 2 2 4
O,KMnO 中锰元素的化合价降低,生成KMnO 和MnO ,故被氧化的元素是O,还原产
2 4 2 4 2
物是KMnO 、MnO ,故答案为:O;KMnO 、MnO ;
2 4 2 2 4 2
(2)KCr O+14HCl 2KCl+2CrCl +3Cl↑+7H O,HCl中氯元素化合价从-1价升高到0价,
2 2 7 3 2 2
故还原剂是HCl,氧化产物是Cl,故答案为:HCl;Cl;
2 2
(3)I:KClO+6HCl(浓)=3Cl ↑+KCl+3H O反应中,KClO、HCl和KCl均是易溶性的强电
3 2 2 3
解质,拆分为离子,其它写成分子,改写为离子方程式为ClO +6H++5Cl-=3Cl↑+3H O,故
2 2
答案为:ClO +6H++5Cl-=3Cl↑+3H O;Ⅱ:4HCl(浓)+MnO MnCl +Cl↑+2H O反应中,
2 2 2 2 2 2
MnO 是氧化剂,HCl是还原剂,氧化产物与还原产物的物质的量比为1:1,所以氧化产物
2与还原产物的质量比为71:126,故答案为:71:126;Ⅲ:根据反应①4HCl(浓)+MnO
2
MnCl +Cl↑+2H O、③KMnO +HCl(浓)→KCl+MnCl +Cl↑+H O(未配平)、④4HCl+O
2 2 2 4 2 2 2 2
2Cl+2H O(g)可知,③不需要条件,①的反应条件是加热,④的反应条件是加热和
2 2
催化剂,反应条件越少的氧化还原反应越容易发生,越容易发生的氧化还原反应氧化剂的
氧化性越强,所以氧化性强弱为KMnO >MnO >O,故答案为:氧化剂;KMnO >MnO
4 2 2 4 2
>O。Ⅳ:反应中Mn元素化合价从+7价降低到+2价,得到5个电子,氯元素化合价从-
2
1价升高到0价,失去1个电子,依据电子得失守恒和原子守恒可知配平后的方程式为
2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O。
4 2 2 2
19.(1)2NaNO + 2KI + 2H SO = 2NO↑+I + K SO + Na SO + 2H O
2 2 4 2 2 4 2 4 2
(2)ef
(3) 反应生成了NO,该物质会造成大气污染 还原性 强
(4)D
(5)C
(6)
【解析】(1)根据方程式可知,碘化钾中碘元素的化合价从- 1价升高到0价,失去1个电
子,做还原剂。亚硝酸钠中氮元素的化合价从+ 3价降低到+ 2价,得到1个电子,做氧化剂。
则根据电子守恒可知氧化剂和还原剂的物质的量之比时1:1。根据原子守恒可知,反应物中
还有硫酸生成,生成物还有水生成,则反应的化学方程式是2NaNO + 2KI + 2H SO =
2 2 4
2NO↑+I + K SO + Na SO + 2H O;
2 2 4 2 4 2
(2)从物质分类角度来看, 是正盐、由钠离子和亚硝酸根离子构成的离子化合物、
是电解质;答案选ef;
(3)用上述反应来处理 并不是最佳方法,因为反应生成了NO,该物质会造成大气
污染;亚硝酸根有毒,从环保角度来讲,要处理NaNO ,所用的物质的还原性比KI更强,
2
答案第10页,共2页使其N元素化合价由+3价变为无污染的0价氮,如NaNO +NHCl=NaCl+N ↑+2H O,故答
2 4 2 2
案为:是反应生成了NO,该物质会造成大气污染;还原性;强;
(4)A .亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,
滴加酚酞试液,亚硝酸钠溶液出现红色,氯化钠溶液无现象,可以用酚酞试液区分NaNO
2
和NaCl,选项A不符合;B.加入AgNO 溶液,均生成白色沉淀,但亚硝酸银能溶于硝酸,
3
AgCl不溶,现象不同,可区别,选项B不符合;C.加强热亚硝酸钠分解生成氮气和氧气,
而氯化钠不分解,反应现象不同,可以用加强热收集气体检验来区分NaNO 和NaCl,选项
2
C不符合;D.化学药品不能用来品尝味道,所以不能鉴别,选项D符合;答案选D;
(5)误食NaNO 会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,则Fe2+失电子变为
2
Fe3+化合价升高,作还原剂,NaNO 作氧化剂,体现氧化性,与HO 表现出的性质相同,
2 2 2
即HO 也体现氧化性;A. ,HO 中氧原子既失电子,又得电
2 2 2 2
子,氧元素的化合价部分升高,部分降低,HO 体现氧化性和还原性,选项A不符合;
2 2
B. ,HO 中氧原子失电子,化合价升高,HO 体现还原性,选项
2 2 2 2
B不符合;C. ,HO 中氧原子得电子,化合价降
2 2
低,HO 体现氧化性,选项C符合;D.
2 2
,HO 中氧原子失电子,化合价升
2 2
高,HO 体现还原性,选项D不符合; 答案选C;
2 2
(6)亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,反应的化学方程式为
NaNO +NHCl=N ↑+NaCl+2HO,反应中N元素的化合价由+3价降低为0价,N元素也
2 4 2 2
从-3价升为0价,该反应转移3e-,用单线桥表示其电子转移的方向和数目为
。
20.(1) KMnO >Cl>H SO SO >Cl->Mn2+
4 2 2 4 2(2)98∶73
(3)AB
【详解】(1)氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物,由反应①知
氯气把二氧化硫氧化为硫酸,故氧化性Cl>H SO ,还原性SO >Cl-;由反应②知氧化性
2 2 4 2
KMnO >Cl,还原性Cl->Mn2+;则氧化性强弱顺序为KMnO >Cl>H SO ,还原性强弱顺序
4 2 4 2 2 4
为SO >Cl->Mn2+;
2
(2)在反应①中氧化产物为HSO ,还原产物为HCl,其质量之比为98∶73;
2 4
(3)在反应②中HCl被氧化为Cl,表现的是还原性,同时还生成了KCl和MnCl ,表现
2 2
的是酸性,所以浓盐酸表现出还原性和酸性,故答案为:AB。
21. 浓HSO 防止G中水蒸气进入E及C装置 将 COCl 排入装置
2 4 2
G 中并被充分吸收,回收尾气 C装置内压强增大,A中导管内液面上升
对D处稍加热
AC
【分析】实验室制取CrCl 的反应为Cr O(s)+3CCl (g) 2CrCl (s)+3COCl (g),CrCl 易潮
3 2 3 4 3 2 3
解高温下易被氧气氧化,所以要防止装置内在高温条件下不能存在空气,反应结束后继续
通入一段时间氮气,让CrCl 在氮气氛围中冷却,防止空气进入使CrCl 氧化;A中装浓
3 3
HSO ,干燥N 并防止空气中水蒸气进入C装置;无水CaCl 防止G中水蒸气进入E及C
2 4 2 2
装置;反应结束后继续通入一段时间氮气,将 COCl 排入装置 G 中并被充分吸收,回收
2
尾气;
【详解】(1)根据题目信息:CrCl 易潮解高温下易被氧气氧化,所以要防止装置内在高温条
3
件下不能存在空气,反应结束后继续通入一段时间氮气,主要目的是让CrCl 在氮气氛围中
3
冷却,防止空气进入使CrCl 氧化;A中装浓HSO ,作用是干燥N 并防止空气中水蒸气进
3 2 4 2
入C装置;无水CaCl 的作用是防止G中水蒸气进入E及C装置;反应结束后继续通入一
2
段时间氮气,主要目的是将 COCl 排入装置 G 中并被充分吸收,回收尾气;
2
(2)若D处出现堵塞,则C装置内压强增大,A中导管内液面上升;D处堵塞是因CrCl 升
3
华后在D处凝聚而产生的,故可对D处稍加热,使实验能继续进行;
(3)装置G中可以看做是COCl 先与水反应生成二氧化碳和氯化氢,二氧化碳和氯化氢再与
2
答案第12页,共2页氢氧化钠反应,故反应方程式为 ;
(4)①测定过程中的物质的量的关系为: ,得失
电子守恒,原子守恒,产品中CrCl 的物质的量为: ,产品中的CrCl 的质
3 3
量分数表达式为: ;
②A.步骤Ⅰ未继续加热一段时间,过量的HO 在步骤Ⅱ中会将 还原为Cr3+,则滴定
2 2
时消耗标准溶液(NH )Fe(SO ) 体积减小,测定的CrCl 质量分数偏低,A正确;
4 2 4 2 3
B. 步骤Ⅲ中所(NH )Fe(SO ) 已变质,则滴定用标准液体积偏大,测出的CrCl 质量分数偏
4 2 4 2 3
高,B错误;
C. 步骤Ⅱ中未加浓磷酸,指示剂会提前变色,读取标准液体积小于实际,测出的CrCl 质
3
量分数偏低,C正确;
D.步骤Ⅲ中读数时滴定前俯视(读数偏小),滴定后平视,读取标准液的体积偏大。测出的
CrCl 质量分数偏高,D错误。
3
故选AC。
22.(1) 不能 球形干燥管 通过观察C中的气泡流速,控制A中产生
氨气的速度 防倒吸
(2) NH SCN+KOH KSCN+NH ↑+H O 3 +Cr O +8H+=3S↓+2Cr3++7H O
4 3 2 2 2
(3)冷却结晶
【分析】加热氯化铵和氢氧化钙的混合物制取氨气,用碱石灰干燥后,在三颈烧瓶中氨气
与CS 反应生成NH SCN、NH HS,滴入KOH生成KSCN,滤去三颈烧瓶中的固体催化剂,
2 4 4
再减压蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体;
(1)
①装置A中直接加热 固体生成氨气和HCl,在试管口冷凝又形成 固体,不能
制取氨气;②仪器B的名称是:球形干燥管;
③通过观察C中的气泡流速,控制A中产生氨气的速度;
④插入下层液体是为了让氨气和二硫化碳充分接触,充分反应,还可以起到防倒吸的作用;
(2)
①由于二硫化碳不溶于水,故当液面不再分层的时候,说明二硫化碳反应完全;装置D中
NH SCN和KOH反应生成KSCN,化学方程式是NH SCN+KOH KSCN+NH ↑+H O;
4 4 3 2
②装置E中, 被酸性重铬酸钾氧化生成浅黄色沉淀S,铬元素被还原为 ,反应的
离子方程式3 +Cr O +8H+=3S↓+2Cr3++7H O;
2 2
(3)
先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到
硫氰化钾晶体。
答案第14页,共2页