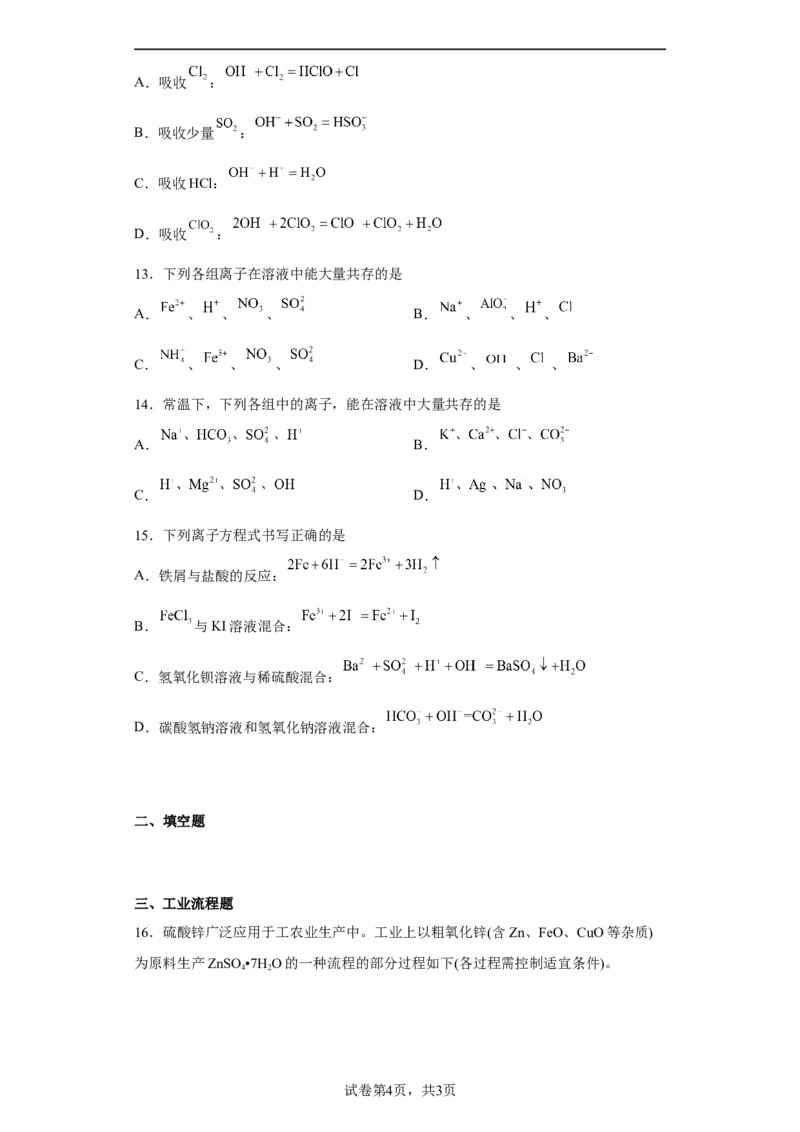文档内容
第一章第二节离子反应跟踪训练--人教版(2019)必修第一
册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.室温下,下列各组离子在指定溶液中能大量共存的是
A.能使石蕊变红的溶液: 、 、 、
B. 的 溶液: 、 、 、
C.无色透明的溶液: 、 、 、
D.能使酚酞变红的溶液: 、 、 、
2.下列溶液中,各组离子能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D.
3.某兴趣小组用如图装置研究溶液的导电性,把X溶液逐滴加入含少量酚酞的
溶液中。下列说法不正确的是
序
装置 X溶液 现象
号
I 盐酸 溶液红色褪去,无沉淀,灯泡亮度稍微变暗
溶 溶液红色不变,有白色沉淀生成,灯泡亮度稍
II
液 微变暗
溶 溶液红色褪去,有白色沉淀生成,灯泡亮度:
III
液 变暗→熄灭→变亮
A.实验I中溶液红色褪去,说明发生了反应
B.实验II中溶液红色不变,灯泡亮度稍微变暗,说明溶液中依然存在大量的 与C.实验III中溶液红色褪去,有白色沉淀生成,灯泡由暗→灭→亮,说明发生了反应
D.将实验II中 溶液换成 溶液,现象与原实验Ⅱ中的现象相同
4.在水溶液中一定能大量共存的一组离子是
A.Al3+、Ba2+、Br-、OH- B.K+、Na+、 、
C.Cl-、ClO-、Fe2+、H+ D.Na+、H+、 、
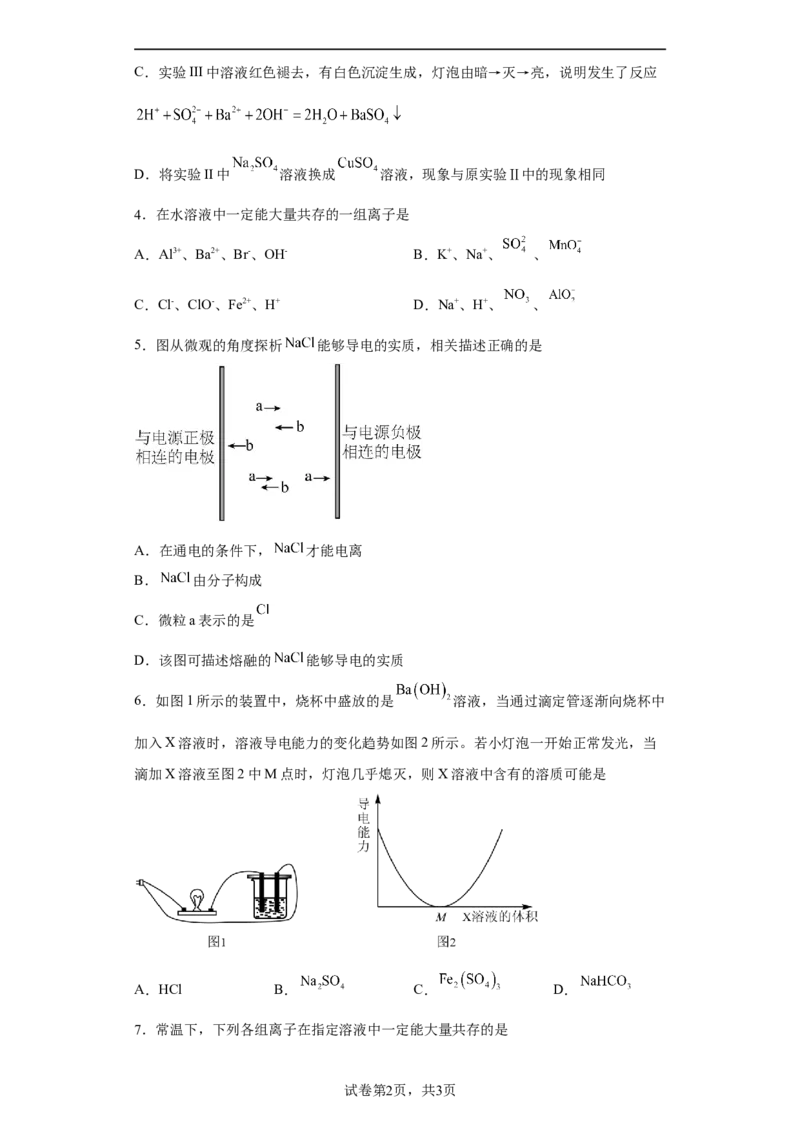
5.图从微观的角度探析 能够导电的实质,相关描述正确的是
A.在通电的条件下, 才能电离
B. 由分子构成
C.微粒a表示的是
D.该图可描述熔融的 能够导电的实质
6.如图1所示的装置中,烧杯中盛放的是 溶液,当通过滴定管逐渐向烧杯中
加入X溶液时,溶液导电能力的变化趋势如图2所示。若小灯泡一开始正常发光,当
滴加X溶液至图2中M点时,灯泡几乎熄灭,则X溶液中含有的溶质可能是
A.HCl B. C. D.
7.常温下,下列各组离子在指定溶液中一定能大量共存的是
试卷第2页,共3页A.澄清透明溶液中: 、 、 、
B.与 反应能放出 的溶液中: 、 、 、
C.无色透明溶液中: 、 、 、
D.含有大量 的溶液: 、 、 、
8.下列离子方程式中,正确的是
A.将稀硫酸滴到铜片上:
B.铜片插入硝酸银溶液中:
C.钠与水反应:
D.稀盐酸滴在石灰石上:
9.下列溶液中的离子因发生氧化还原反应而不能大量共存的是
A.Fe2+、H+、MnO 、SO B.Cu2+、Al3+、NO 、C1-
C.K+、Al3+ 、OH-、SO D.Ba2+ 、Na+、CO 、 ClO-
10.宏观辨识与微观探析是化学学科核心素养之一,下列对应离子方程式书写正确的
是
A.铝与氢氧化钠溶液反应:
B.用醋酸除去水垢:
C.向氢氧化钡溶液中加入稀硫酸:
D.用 制作印刷电路板:
11.下列各组离子在溶液中可大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
12.实验室常用NaOH溶液吸收处理尾气,下列相关反应的离子方程式正确的是A.吸收 :
B.吸收少量 :
C.吸收HCl:
D.吸收 :
13.下列各组离子在溶液中能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
14.常温下,下列各组中的离子,能在溶液中大量共存的是
A. B.
C. D.
15.下列离子方程式书写正确的是
A.铁屑与盐酸的反应:
B. 与KI溶液混合:
C.氢氧化钡溶液与稀硫酸混合:
D.碳酸氢钠溶液和氢氧化钠溶液混合:
二、填空题
三、工业流程题
16.硫酸锌广泛应用于工农业生产中。工业上以粗氧化锌(含Zn、FeO、CuO等杂质)
为原料生产ZnSO•7H O的一种流程的部分过程如下(各过程需控制适宜条件)。
4 2
试卷第4页,共3页(1)氧化锌与稀硫酸反应的离子方程式为_______。
(2)过程I需要持续强制通风,原因是该过程中生成的氢气具有_______性。
(3)过程II中,滤渣Y含有Fe(OH) ,其中铁元素的化合价是_______。
3
(4)过程III中,加入锌粉的主要目的是除去铜,该反应的离子方程式为_______。
17.“侯氏制碱法”是我国化工专家侯德榜为世界制破工业作出的突出贡献。实验中
需要使用纯净的氯化钠,某实验小组利用以下流程对粗盐进行提纯:
(1)工业上粗盐(含Ca2+、Mg2+、 等杂质)经除杂得到氯化钠,粗盐提纯的流程如下:
①粗盐溶液中加入足量BaCl 溶液,发生反应的离子方程式为_______。
2
②加入足量NaCO 溶液生成沉淀的化学式为_______。
2 3
③加入稀盐酸调节溶液pH约为7,即可得到NaCl溶液,其中生成气泡的离子方程式
为_______。
④由NaCl溶液得到NaCl晶体的实验操作名称为_______。
(2)取16g纯碱产品(含杂质),加入足量水溶解,再加入足量BaCl 溶液,过滤,干燥沉
2
淀,得到沉淀19.7g,则纯碱的纯度为_______%。参考答案:
1.B
【详解】A.能使石蕊变红的溶液显酸性,酸性条件下 会与 、 发生氧化还原反
应,不能大量共存,A错误;
B. 、 、 、 之间不反应,且都不与 溶液反应,在溶液中能够大量共存,
B正确;
C.含 的溶液呈蓝色,无色溶液中不能存在,C错误;
D.能使酚酞变红的溶液显碱性, 能与氢氧根离子生成 沉淀,不能大量存在,
D错误;
故选B。
2.A
【详解】A. 、 、 、 四种离子之间不发生反应,可以大量共存,A项正
确;
B. 能氧化 ,不能大量共存,B项错误;
C. 能与 反应,不能大量共存,C项错误;
D. 与 能形成 沉淀,与SO 生成微溶物,不能大量共存,D项错误;
故选A。
3.D
【详解】A.实验I中 溶液中加入 ,酚酞红色退去,发生反应 ,
A正确;
B.实验II中 与 反应,溶液红色不变,有白色沉淀生成,灯泡亮度稍微变
暗,说明溶液中依然存在大量的 与 ,B正确;
C.实验III中 加入 ,发生反应 ,溶液红色褪去,有白色沉淀生成,灯泡由暗→灭→亮,C正确;
D.实验II中 与 反应,生成 蓝色沉淀,D错误;
故选D。
4.B
【详解】A.Al3+与OH-反应生成氢氧化铝或偏铝酸根,不能大量共存,故A错误;
B.该组离子彼此不发生反应,可以大量共存,故B正确;
C.ClO-、Fe2+能发生氧化还原反应,不能大量共存,故C错误;
D. 与氢离子反应生成氢氧化铝或铝离子,不能大量共存,故D错误;
故选:B。
5.D
【详解】A. 在水分子作用下即可电离生成 、 ,A错误;
B. 由离子构成,B错误;
C.阳离子向与电源负极相连的阴极移动,微粒a表示的是 ,C错误;
D.由图可知可描述熔融的 能够导电的实质,D正确;
故选D。
6.C
【分析】从图中可以看出,当加入X溶液达到M点时,溶液的导电能力几乎为0,表明此
时溶液中离子的浓度接近0。
【详解】A.向 溶液中加入HCl溶液,生成 和 , 为可溶性强电解
质,溶液中离子的浓度不可能接近0,A项不符合题意;
B.向 溶液中加入 溶液,生成 沉淀和NaOH,NaOH为可溶性强碱,
溶液中离子浓度不可能接近0,B项不符合题意;
C.向 溶液中加入 溶液,生成 沉淀和 沉淀,当加入一定
量 后,溶液中离子浓度可能接近0,C项符合题意;
D.向 溶液中加入 溶液,生成 沉淀、NaOH或 等,溶液中
答案第2页,共2页离子的浓度不可能接近0,D项不符合题意;
故选C。
7.A
【详解】A.澄清透明溶液中: 、 、 、 能大量共存,A正确;
B.与 反应能放出 的溶液可能为酸可能为碱,若为碱溶液时不能与 大量共存,B
错误;
C.无色溶液中, 不能大量共存,C错误;
D.含有大量 的溶液中 不能大量共存,D错误;
故选A。
8.C
【详解】A.稀硫酸滴在铜片上,不发生反应,无法写出反应的离子方程式,故A错误;
B.二者发生置换反应生成铜离子和Ag,离子方程式为Cu+2Ag+=Cu2++2Ag,故B错误;
C.钠与水反应生成氢氧化钠和氢气: ,故C正确;
D.稀盐酸滴在石灰石上反应生成氯化钙和二氧化碳、水,反应的离子方程式为
CaCO +2H+=Ca2++H O+CO↑,故D错误;
3 2 2
故选C。
9.A
【详解】A.酸性条件下,高锰酸根会与亚铁离子发生氧化还原反应,A符合题意;
B.Cu2+、Al3+、NO 、Cl-几种离子可以大量共存,B不符合题意;
C.铝离子与氢氧根会生成沉淀而不共存,C不符合题意;
D.钡离子与碳酸根生成沉淀而不共存,D不符合题意;
故选A。
10.A
【详解】A.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气:
,A正确;B.醋酸为弱酸不能拆, ,B错误;
C.向氢氧化钡溶液中加入稀硫酸生成硫酸钡和水:
,C错误;
D.铁离子和铜反应生成亚铁离子、铜离子, ,D错误;
故选A。
11.B
【详解】A. 和 生成硫酸钡沉淀而不共存,A不符合题意;
B. 、 、 、 四种离子可以在溶液中大量共存,B符合题意;
C. 和 反应生成二氧化碳气体,C不符合题意;
D. 和 生成氢氧化铜沉淀而不共存,D不符合题意;
故选B。
12.C
【详解】A.氯气和氢氧化钠生成氯化钠、次氯酸钠、水, ,A
错误;
B.氢氧化钠和少量二氧化硫生成亚硫酸钠和水, ,B错误;
C.盐酸和氢氧化钠生成水,C正确;
D.二氧化氯和氢氧根离子反应生成氯离子和 ,反应为 ,
D错误;
故选C。
13.C
【详解】A.酸性条件下 、 发生氧化还原反应而不能大量共存,A错误;
B. 、 反应不能大量共存,B错误;
答案第4页,共2页C. 、 、 、 互不反应,可以大量共存,C正确;
D. 、 反应生成沉淀不能大量共存,D错误;
故选C。
14.D
【详解】A.H+与 反应生成二氧化碳和水,不能大量共存,A不符合题意;
B.Ca2+与 反应生成沉淀,不能大量共存,B不符合题意;
C.Mg2+与OH-反应生成沉淀,不能大量共存,C不符合题意;
D.各个离子间可以大量共存,D符合题意;
故答案为:D。
15.D
【详解】A.不符合客观事实,正确的为: ,故A错误;
B.不符合电荷守恒,正确的为: ,故B错误;
C.不符合化学式配比,正确的为: ,故C错
误;
D.碳酸氢钠溶液和氢氧化钠溶液混合反应生成碳酸钠: ,故D
正确;
故选:D。
16.(1)
(2)可燃
(3)+3价
(4)
【分析】粗氧化锌加入硫酸,Zn、FeO、CuO均可以溶解生成锌离子、二价铁离子、铜离
子,滤渣X为不溶物,滤液中加入高锰酸钾氧化二价铁离子转化为三价铁离子,使三价铁离子转化为沉淀,除去三价铁离子,在滤液中加入锌粉,单质锌可以置换铜离子生成单质
铜,除去铜离子,再经过一系列变化得到ZnSO•7H O,据此分析。
4 2
【详解】(1)氧化锌与稀硫酸反应生成可溶的硫酸锌和水: ;
(2)H 具有可燃性,易燃易爆,所以过程I需要强制通风;
2
(3)根据化合价代数和为零, 中铁元素化合价为+3;
(4)锌与硫酸铜溶液发生置换反应生成铜: 。
17.(1) Ba2++ = BaSO↓ BaCO 、CaCO +2H+=CO ↑+HO 蒸发结晶
4 3 3 2 2
或蒸发
(2)66.25
【分析】粗盐溶液加入足量氯化钡除去硫酸根离子、加入足量氢氧化钠除去镁离子、加入
足量碳酸钠除去过量钡离子、钙离子,过滤滤液加入稀盐酸除去过量氢氧根离子、碳酸根
离子,蒸发结晶得到氯化钠。
【详解】(1)①粗盐溶液中加入足量BaCl 溶液,钡离子和硫酸根离子生成硫酸钡沉淀,
2
发生反应的离子方程式为Ba2++ = BaSO↓。
4
②加入足量NaCO 溶液,碳酸钠和过量钡离子生成碳酸钡沉淀、和钙离子生成碳酸钙沉淀,
2 3
故生成沉淀的化学式为BaCO 、CaCO 。
3 3
③加入稀盐酸调节溶液pH约为7,即可得到NaCl溶液,其中生成气泡的反应为氢离子和
过量的碳酸根离子生成二氧化碳、水,离子方程式为 +2H+=CO ↑+HO。
2 2
④由NaCl溶液得到NaCl晶体的实验操作名称为蒸发结晶或蒸发;
(2)氯化钡和碳酸钠生成碳酸钡沉淀,根据碳酸根离子守恒可知,纯碱的纯度为
。
答案第6页,共2页