文档内容
必修第一册 第二章 第三节 物质的量 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1. 2022年6月5日10时44分,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭,在我国
酒泉卫星发射中心点火发射。偏二甲肼(C HN)是一种高能燃料,燃烧产生的巨大能量可作为
2 8 2
航天运载火箭的推动力。下列叙述正确的是( )
A.偏二甲肼的摩尔质量为60 g
B.6.02×1023个偏二甲肼分子的质量约为60 g
C.1 mol 偏二甲肼分子的质量为 60 g·mol-1
D.6 g 偏二甲肼含有 N 个偏二甲肼分子
A
2. 下列说法正确的是( )
A.摩尔既是物质的数量单位又是物质的质量单位
B.阿伏加德罗常数是12 kg 12C中含有的碳原子数
C.1 mol水分子中含有2 mol氢原子和1 mol氧原子
D.一个NO分子的质量是a g,一个NO 分子的质量是b g,则氧原子的摩尔质量是(b-a) g
2
3. N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.22.4 L(标准状况)氮气中含有7N 个中子
A
B.1 mol重水比1 mol水多N 个质子
A
C.12 g石墨烯和12 g金刚石均含有N 个碳原子
A
D.1 L 1 mol·L-1 NaCl溶液含有28N 个电子
A
4. 同温同压下,分别用等质量的H 、CO、CO 、NH 四种气体吹起四个气球,其中由H 吹起的
2 2 3 2
是( )
5.下列溶液中,跟100 mL 0.5 mol·L-1 NaCl溶液中所含的Cl-物质的量浓度相同的是( )
A.100 mL 0.5 mol·L-1 MgCl 溶液
2
B.200 mL 0.25 mol·L-1 AlCl 溶液
3
C.50 mL 1 mol·L-1 NaCl溶液
D.25 mL 0.5 mol·L-1 HCl溶液
6. 用NaCl固体配制0.1 mol·L-1的NaCl溶液,下列操作或说法正确的是( )
A.将5.85 g NaCl固体放入1 000 mL容量瓶中,加水溶解并准确定容
B.称量时,将固体NaCl直接放在天平左盘上
C.固体溶解、冷却后将溶液直接转移到容量瓶中,然后向容量瓶中加水至刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
7. 如果a g 某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(式中N 表示阿伏
A
1
学科网(北京)股份有限公司加德罗常数)( )
A.L B.L C.L D.L
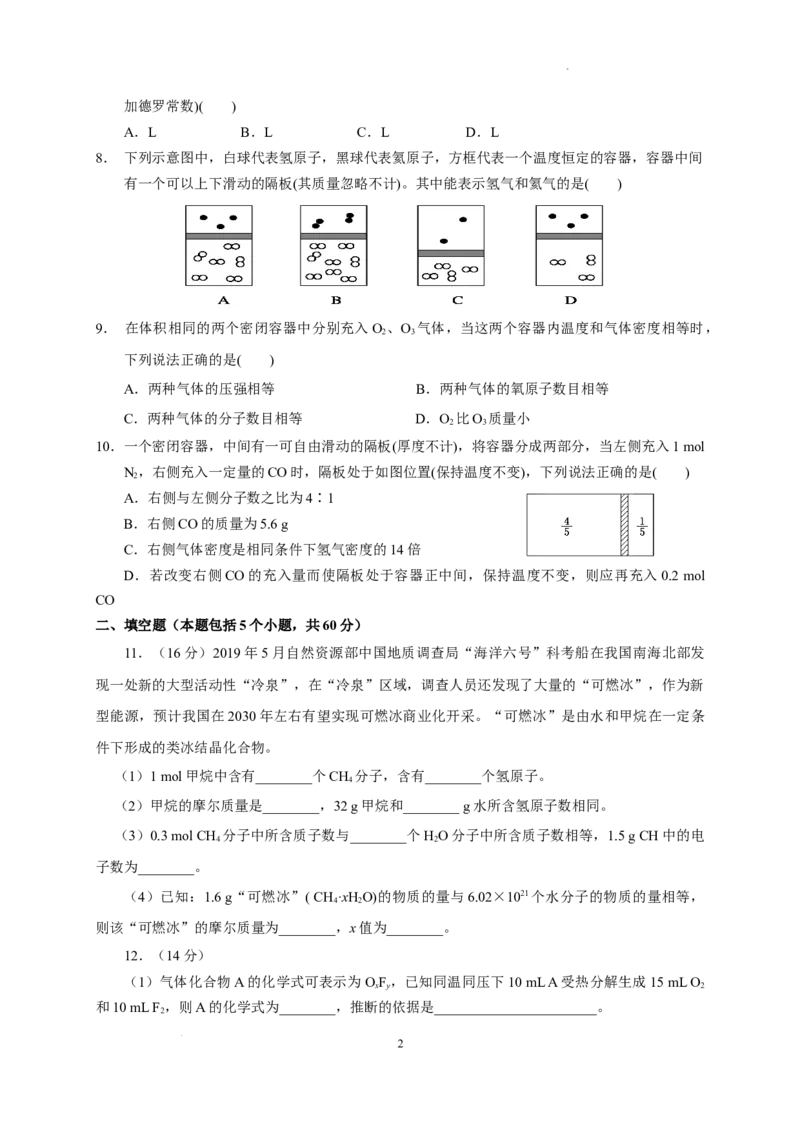
8. 下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表一个温度恒定的容器,容器中间
有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示氢气和氦气的是( )
9. 在体积相同的两个密闭容器中分别充入O 、O 气体,当这两个容器内温度和气体密度相等时,
2 3
下列说法正确的是( )
A.两种气体的压强相等 B.两种气体的氧原子数目相等
C.两种气体的分子数目相等 D.O 比O 质量小
2 3
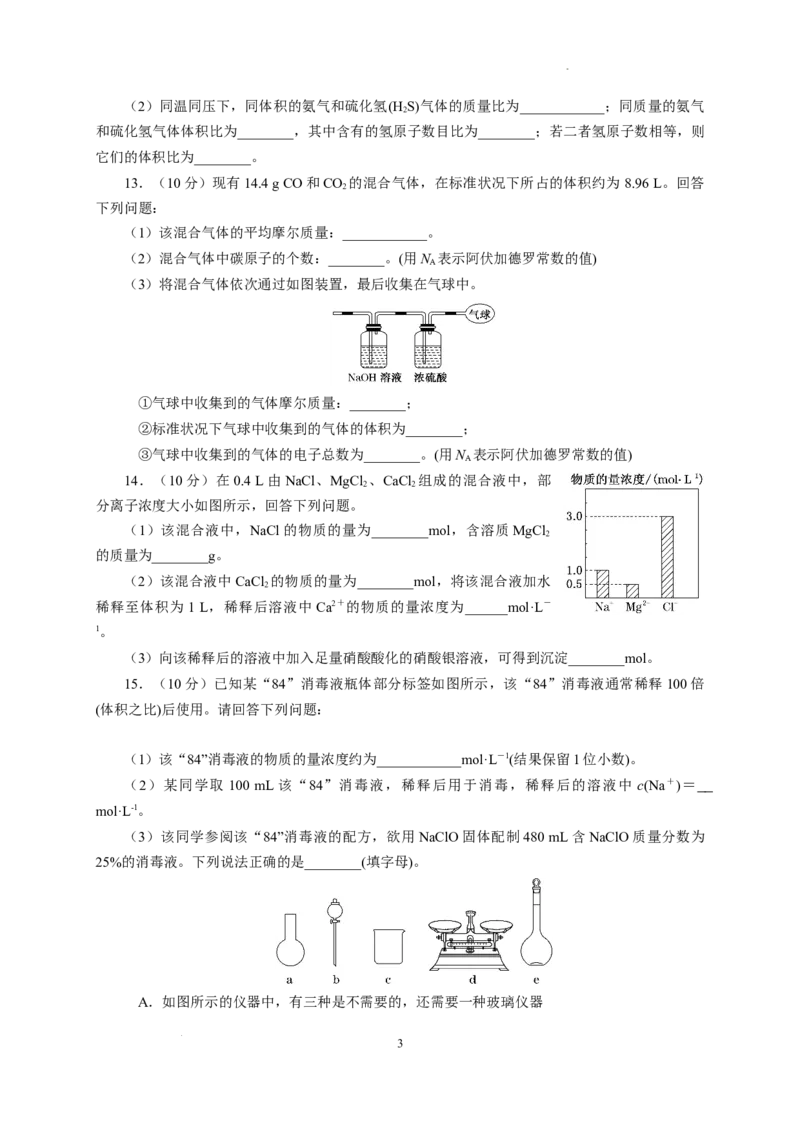
10.一个密闭容器,中间有一可自由滑动的隔板(厚度不计),将容器分成两部分,当左侧充入1 mol
N,右侧充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的是( )
2
A.右侧与左侧分子数之比为4∶1
B.右侧CO的质量为5.6 g
C.右侧气体密度是相同条件下氢气密度的14倍
D.若改变右侧CO的充入量而使隔板处于容器正中间,保持温度不变,则应再充入0.2 mol
CO
二、填空题(本题包括5个小题,共60分)
11.(16分)2019年5月自然资源部中国地质调查局“海洋六号”科考船在我国南海北部发
现一处新的大型活动性“冷泉”,在“冷泉”区域,调查人员还发现了大量的“可燃冰”,作为新
型能源,预计我国在2030年左右有望实现可燃冰商业化开采。“可燃冰”是由水和甲烷在一定条
件下形成的类冰结晶化合物。
(1)1 mol甲烷中含有________个CH 分子,含有________个氢原子。
4
(2)甲烷的摩尔质量是________,32 g甲烷和________ g水所含氢原子数相同。
(3)0.3 mol CH 分子中所含质子数与________个HO分子中所含质子数相等,1.5 g CH中的电
4 2
子数为________。
(4)已知:1.6 g“可燃冰”( CH ·xHO)的物质的量与6.02×1021个水分子的物质的量相等,
4 2
则该“可燃冰”的摩尔质量为________,x值为________。
12.(14分)
(1)气体化合物A的化学式可表示为OF,已知同温同压下10 mL A受热分解生成15 mL O
x y 2
和10 mL F ,则A的化学式为________,推断的依据是_______________________。
2
2
学科网(北京)股份有限公司(2)同温同压下,同体积的氨气和硫化氢(H S)气体的质量比为____________;同质量的氨气
2
和硫化氢气体体积比为________,其中含有的氢原子数目比为________;若二者氢原子数相等,则
它们的体积比为________。
13.(10分)现有14.4 g CO和CO 的混合气体,在标准状况下所占的体积约为 8.96 L。回答
2
下列问题:
(1)该混合气体的平均摩尔质量:____________。
(2)混合气体中碳原子的个数:________。(用N 表示阿伏加德罗常数的值)
A
(3)将混合气体依次通过如图装置,最后收集在气球中。
①气球中收集到的气体摩尔质量:________;
②标准状况下气球中收集到的气体的体积为________;
③气球中收集到的气体的电子总数为________。(用N 表示阿伏加德罗常数的值)
A
14.(10分)在0.4 L由NaCl、MgCl 、CaCl 组成的混合液中,部
2 2
分离子浓度大小如图所示,回答下列问题。
(1)该混合液中,NaCl的物质的量为________mol,含溶质MgCl
2
的质量为________g。
(2)该混合液中CaCl 的物质的量为________mol,将该混合液加水
2
稀释至体积为1 L,稀释后溶液中Ca2+的物质的量浓度为______mol·L-
1。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀________mol。
15.(10分)已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常稀释100倍
(体积之比)后使用。请回答下列问题:
(1)该“84”消毒液的物质的量浓度约为____________mol·L-1(结果保留1位小数)。
(2)某同学取 100 mL 该“84”消毒液,稀释后用于消毒,稀释后的溶液中 c(Na+)=
mol·L-1。
(3)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480 mL含NaClO质量分数为
25%的消毒液。下列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
3
学科网(北京)股份有限公司B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(4)“84”消毒液与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84
g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84”消毒液的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________mL。
【解析】
1.答案 B
解析: 偏二甲肼的摩尔质量应为 60 g·mol-1,A错误;6.02×1023个偏二甲肼分子约为1 mol,其
质量约为60 g,B正确;6 g偏二甲肼的物质的量为=0.1 mol,含有的分子数为0.1N ,D错误。
A
解析:
2.答案 C
解析:摩尔是物质的量的单位,A错误;N 是12 kg 12C中含有的碳原子数,B错误;(b-a) g是一
A
个O原子的质量, B错误。
3.答案 C
4.答案:C
解析: 4解析:气体的物质的量n=,在同温同压下,气体摩尔体积相同,气体的体积V=n·V ,
m
即V=V ,可知,摩尔质量越小,体积越大,四种气体中氢气的摩尔质量最小,故体积最大,故选
m
C。
5.答案 D
解析: 物质的量浓度与溶液的体积无关,100 mL 0.5 mol·L-1 NaCl溶液中c(Cl-)=0.5 mol·L-1,
而A、B、C、D项中,c(Cl-)分别为1 mol·L-1、0.75 mol·L-1、1 mol·L-1、0.5 mol·L-1,故D项正
确。
6.答案 D
解析: A项,固体应在烧杯中溶解,容量瓶不能用来稀释溶液或溶解固体;B项,称量固体NaCl
时不能直接放在天平左盘上,应放在称量纸上;C项,配制一定物质的量浓度的溶液时,转移溶液
后需用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转移至容量瓶中,然后再加蒸馏水,当加水
至距离刻度线1~2 cm处时,要改用胶头滴管定容,不能直接加水至刻度线。
7.答案 A
8.答案 A
9.答案 B
解析: 相同体积相同密度时,两容器气体的质量相等,且都由氧元素组成,则氧原子的质量、个
4
学科网(北京)股份有限公司数以及物质的量相等,B正确、D错误;氧原子个数相等时,气体的物质的量之比为 n(O )∶n(O )
2 3
=3∶2,两种气体的压强之比为3∶2,A错误;物质的量与分子数成正比,则两种气体的分子数目
之比是3∶2,C错误。
10.答案 C
解析:左右两侧气体温度、压强相同,相同条件下,体积之比等于物质的量之比,左右体积之比为
4∶1,则左右气体物质的量之比为4∶1,所以右侧气体物质的量=0.25 mol,质量=28 g·mol-
1×0.25 mol=7 g,A、B错误;相同条件下密度与摩尔质量成正比,则右侧气体密度是相同条件下
氢气密度的=14倍,C正确;隔板处于容器正中间时,左右两侧气体的物质的量相等,则需要再充
入CO的物质的量为1 mol-0.25 mol=0.75 mol,D错误。
11.答案:(1)N (或6.02×1023) 4N (或2.408×1024)
A A
(2)16 g·mol-1 72
(3)0.3N (或1.806×1023) 0.8N
A A
(4)160 g·mol-1 8
12.答案: (1) OF 阿伏加德罗定律
3 2
(2)1∶2 2∶1 3∶1 2∶3
解析: (1)根据阿伏加德罗定律可知10OF===15O +10F
x y 2 2
根据原子守恒得故x=3,y=2。
(2)同温同压下,同体积的氨气和硫化氢气体的物质的量相等,故质量比为 17∶34=1∶2;同
质量的氨气和硫化氢气体物质的量之比为∶=2∶1,即体积之比为2∶1;氢原子数目之比为
(2×3)∶(1×2)=3∶1,若二者氢原子数相等时,物质的量之比为∶=2∶3,即体积之比为2∶3。
13.答案: (1)3 6 g·mol-1 (2) 0.4N
A
(3) ①28 g·mol-1 ② 4.48 L ③ 2.8N
A
解析:(1)混合气体的体积为8.96 L,则其物质的量n===0.4 mol,混合气体的平均摩尔质量
为=36 g·mol-1。(2)设混合气体中 CO的物质的量为x mol,CO 的物质的量为y mol,则根据混合
2
物的质量为14.4 g可得28x+44y=14.4 ①;根据气体的物质的量为0.4 mol,可得x+y=0.4 ②;
解得x=0.2,y=0.2;由于CO和CO 中均含1个碳原子,故0.2 mol CO和0.2 mol CO 中共含0.4
2 2
mol C原子即0.4N 个。(3)将混合气体依次通过图中装置,则CO 会被NaOH溶液吸收,剩余CO,
A 2
被浓硫酸干燥后,则在气球中收集到的是干燥纯净的 CO气体,①摩尔质量为28 g·mol-1;②体积
V=nV =0.2 mol×22.4 L·mol-1=4.48 L;③电子的物质的量为0.2 mol×14=2.8 mol,电子总数为
m
2.8N 。
A
14.答案: (1)0.4 19 (2)0.2 0.2 (3)1.2
解析:由图可知c(Na+)=c(NaCl)=1.0 mol·L-1。c(Mg2+)=c(MgCl )=0.5 mol·L-1,则c(CaCl )
2 2
==0.5 mol·L-1。
5
学科网(北京)股份有限公司(1)n(NaCl)=1.0 mol·L-1×0.4 L=0.4 mol,m(MgCl )=0.5 mol·L-1×0.4 L×95 g·mol-1=19 g。
2
(2)n(CaCl )=0.5 mol·L-1×0.4 L=0.2 mol,c(Ca2+)==0.2 mol·L-1。
2
(3)原溶液中n(Cl-)=3 mol·L-1×0.4 L=1.2 mol,由反应Ag++Cl-===AgCl↓可知,生成AgCl
沉淀为1.2 mol。
15.答案:(1)4.0 (2)0.04 (3)C (4)①4.6 ②250.0
解析:(1)由c=得,c(NaClO)= mol·L-1≈4.0 mol·L-1。
(2)稀释前后溶液中NaClO的物质的量不变,则有100 mL×10-3 L·mL-1×4.0 mol·L-1=100
mL×10-3 L·mL-1×c(NaClO)×100,得稀释后 c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04
mol·L-1。
(3)选项A,需用托盘天平称取NaClO固体,需用烧杯溶解NaClO,需用玻璃棒进行搅拌和引
流,需用容量瓶和胶头滴管来定容,图示仪器中的a、b不需要,但还需要玻璃棒和胶头滴管;选
项B,配制过程中需要加水,所以洗涤干净后的容量瓶不必烘干;选项C,未洗涤烧杯和玻璃棒将
导致配制的溶液中溶质的物质的量减小,结果偏低;选项 D,应选取500 mL的容量瓶进行配制,
然后取出480 mL即可,所以需要NaClO的质量为0.5 L×4.0 mol·L-1×74.5 g· mol-1=149.0 g。
(4)①根据HSO 的组成可知,溶液中c(H+)=2c(H SO )=4.6 mol·L-1。②2 L 2.3 mol·L-1的稀
2 4 2 4
硫酸中溶质的物质的量为2 L×2.3 mol·L-1=4.6 mol,设需要98%(密度为1.84 g·cm-3)的浓硫酸的体
积为V mL,则有=4.6 mol,解得V=250.0。
6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司