文档内容
山西省榆次第一中学校 李金虎
选择性必修 1 化学反应原理 第二章第二节 化学平衡
专题 “等效思想”解答化学平衡应用题
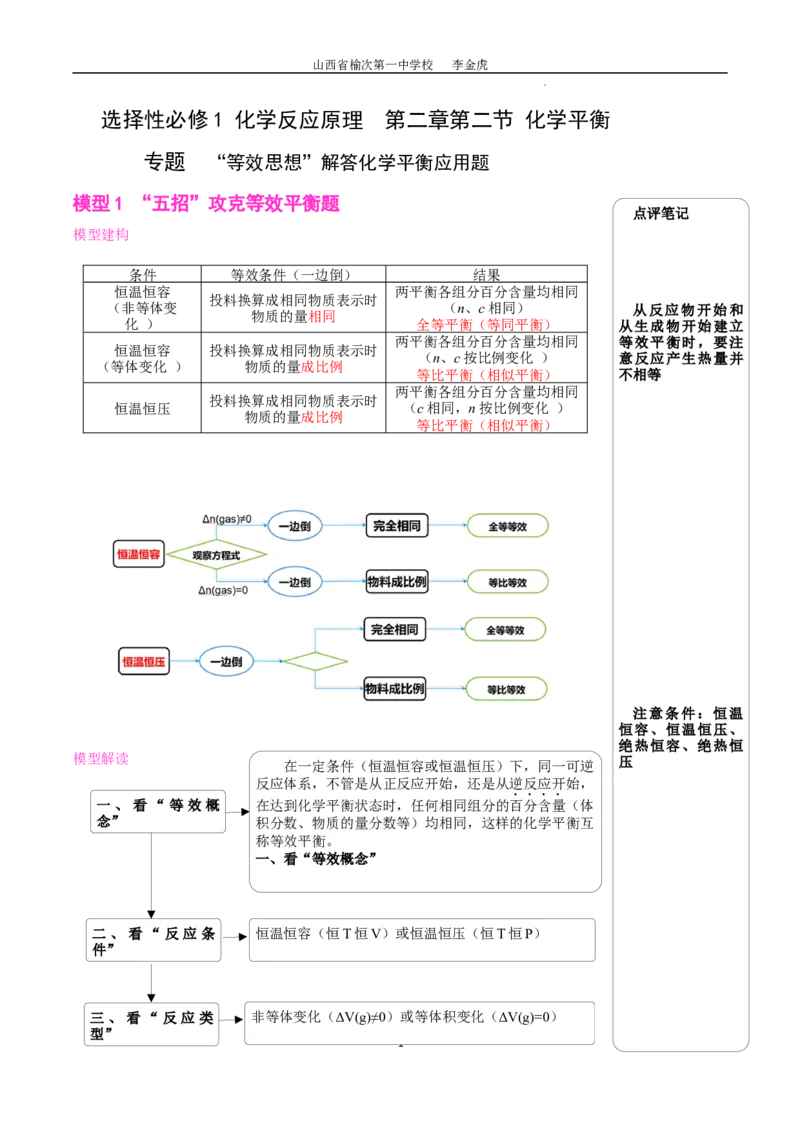
模型1 “五招”攻克等效平衡题
点评笔记
模型建构
条件 等效条件(一边倒) 结果
恒温恒容 两平衡各组分百分含量均相同
投料换算成相同物质表示时
(非等体变 (n、c相同) 从反应物开始和
物质的量相同
化 ) 全等平衡(等同平衡) 从生成物开始建立
两平衡各组分百分含量均相同 等效平衡时,要注
恒温恒容 投料换算成相同物质表示时
(n、c按比例变化 ) 意反应产生热量并
(等体变化 ) 物质的量成比例
等比平衡(相似平衡) 不相等
两平衡各组分百分含量均相同
投料换算成相同物质表示时
恒温恒压 (c相同,n按比例变化 )
物质的量成比例
等比平衡(相似平衡)
注意条件:恒温
恒容、恒温恒压、
绝热恒容、绝热恒
模型解读 压
在一定条件(恒温恒容或恒温恒压)下,同一可逆
反应体系,不管是从正反应开始,还是从逆反应开始,
一 、 看 “ 等 效 概 在达到化学平衡状态时,任何相同组分的百分含量(体
念” 积分数、物质的量分数等)均相同,这样的化学平衡互
称等效平衡。
一、看“等效概念”
二 、 看 “ 反 应 条 恒温恒容(恒T恒V)或恒温恒压(恒T恒P)
件”
三 、 看 “ 反 应 类 非等体变化(ΔV(g)≠0)或等体积变化(ΔV(g)=0)
型”
1
学科网(北京)股份有限公司山西省榆次第一中学校 李金虎
极值转化法(一边倒) 点评笔记
无论平衡从哪个方向建立,在判断时都可根据
题给条件和反应计量系数把生成物全部推算为反应
四 、 看 “ 极 值 转 物或把反应物全部推算成生成物,再与原平衡加入
化” 的物质的量相比较,若物质的量“相当”则为等效
平衡。
五 、 看 “ 等 效 判 全等等效(等同等效)或等比等效(相似等效)
断”
模型示例
【模型典例】
在一定温度下,把2 mol SO 和1 mol O 通入一固定容积的密闭容器中,发生如
2 2
下反应,2SO +O 2SO ,当此反应进行到一定程度时反应混合物就处于化学平
2 2 3
衡状态。现在该容器中维持温度不变,令a、b、c分别代表初始时加入的SO 、O、
2 2
SO 的物质的量,如果a、b、c取不同的数值,它们必须满足一定的相互关系,才能
3
保证达到平衡状态时,反应混合物中三种气体的百分含量仍跟上述平衡完全相同。请
填空:
(1)若a=0,b=0,则c=___________。
(2)若a=0.5,则b=___________,c=___________。
(3)a、b、c的取值必须满足的一般条件是___________,___________。(请
用两个方程式表示,其中一个只含a和c,另一个只含b和c)
【模型思路】第一招 看条件(恒温恒容)
第二招 看反应类型 [非等体积变化(△V(g)≠0)]
第三招 极值转化法(一边倒)
第四招 判断等效列等式
【模型快解】
(1)恒温恒容条件下反应前后体积改变的反应
判断方法:投料换算成相同物质表示时物质的量相同即等效。
例如:2SO (g)+O(g) 2SO (g)
2 2 3
① 2 mol 1 mol 0
② 0 0 2 mol
③ 0.5 mol 0.25 mol 1.5 mol
④ a mol b mol c mol
上述①②③三种配比,按化学方程式的化学计量关系均转化为反应物,则 SO 均
2
为2 mol,O 均为1 mol,三者建立的平衡状态完全相同。④中a、b、c三者的关系满
2
足:c+a=2,+b=1,即与上述平衡等效。
【答案】(1)c=2 (2)b=0.25,c=1.5 (3)c+a=2,+b=1(或
2b+c=2)。
2
学科网(北京)股份有限公司山西省榆次第一中学校 李金虎
模型训练
解题笔记
1.在t ℃时,向2 L恒容密闭容器中放入1 mol A和1 mol B,发生下列反应:
A(g)+B(g) C(g)+2D(g),平衡时C的含量为m %,保持其他条件不变,若按下列配
比将物质放入容器中达到平衡时,C的含量仍为m %的是 (
)
A.2 mol A和1 mol B B.2 mol D和A、B、C各1 mol
C.1 mol C和2 mol D D.1 mol C和1 mol D
2.某温度下,在一容积可变的容器中,反应 2A(g) + B(g) 2C(g)达到平衡时,
A、B和C的物质的量分别为 4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混
合物中三者的物质的量做如下调整,可使平衡右移的是 (
)
A.均减半 B.均加倍 C.均增加1 mol D.均减少1 mol
3.在一恒温恒容密闭容器中,A、B气体可建立如下平衡: 2A(g)+2B(g)
C(g)+3D(g)现分别从两条途径建立平衡:Ⅰ. A、B的起始量均为2mol;Ⅱ. C、D的起
始量分别为2mol和6mol。下列叙述不正确的是 (
)
A.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同
B.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同
C.达到平衡时,途径Ⅰ的和途径Ⅱ体系内混合气体平均相对分子质量相同
D.达到平衡时,途径Ⅰ的气体密度为途径Ⅱ密度的1/2
4.在一个容积固定的密闭容器中充入1 mol HI,建立如下平衡:H(g)+I (g)
2 2
2HI(g),测得HI的转化率为a%。其他条件不变,在上述平衡体系中再充入1 mol HI,
待平衡建立时HI的转化率为b%,则a、b的关系为 ( )
A.a>b B.a<b C.a=b D.无法确定
5.一个真空密闭恒容容器中盛有1 mol PCl ,加热到200 ℃发生如下反应:
5
PCl
5
(g) PCl
3
(g)+Cl
2
(g) ,反应达到平衡时,混合气体中PCl
5
所占体积分数为
M%,。若同一温度的同一容器中,最初投入2 mol PCl ,反应达平衡时,混合气体中
5
PCl 所占体积分数为N%。则M和N的关系是
5
( )
A.M>N B.M<N C.M=N D.无法确定
6.把晶体NO 放入一固定容积的密闭容器中气化并建立NO(g) 2NO (g)平衡,
2 4 2 4 2
然后保持温度不变,再通入与起始时等量的NO 气体,反应再次达平衡,则新平衡
2 4
NO 的转化率与原平衡比 (
2 4
)
A.变小 B.变大 C.不变 D.无法确定
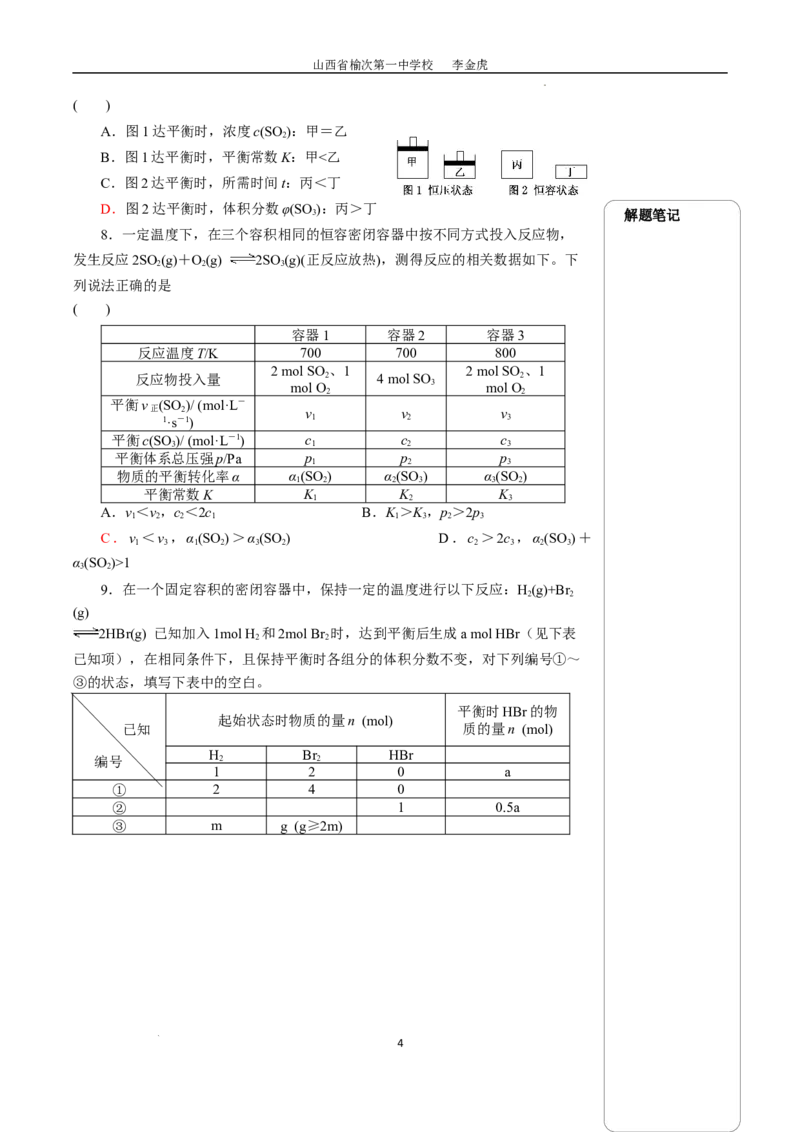
7.一定条件下存在反应:2SO (g)+O(g) 2SO (g),其正反应放热。图1、图2
2 2 3
表示起始时容器甲、丙体积都是V,容器乙、丁体积都是V/2;向甲、丙内都充入2a
mol SO 和a mol O 并保持恒温;向乙、丁内都充入a mol SO 和0.5a mol O 并保持绝
2 2 2 2
热(即与外界无热量交换),在一定温度时开始反应。下列说法正确的是
3
学科网(北京)股份有限公司山西省榆次第一中学校 李金虎
( )
A.图1达平衡时,浓度c(SO ):甲=乙
2
B.图1达平衡时,平衡常数K:甲<乙
C.图2达平衡时,所需时间t:丙<丁
D.图2达平衡时,体积分数φ(SO ):丙>丁
3 解题笔记
8.一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,
发生反应2SO (g)+O(g) 2SO (g)(正反应放热),测得反应的相关数据如下。下
2 2 3
列说法正确的是
( )
容器1 容器2 容器3
反应温度T/K 700 700 800
2 mol SO 、1 2 mol SO 、1
反应物投入量 2 4 mol SO 2
mol O 3 mol O
2 2
平衡v (SO )/ (mol·L-
正 2 v v v
1·s-1) 1 2 3
平衡c(SO )/ (mol·L-1) c c c
3 1 2 3
平衡体系总压强p/Pa p p p
1 2 3
物质的平衡转化率α α(SO ) α(SO ) α(SO )
1 2 2 3 3 2
平衡常数K K K K
1 2 3
A.v<v,c<2c B.K >K ,p>2p
1 2 2 1 1 3 2 3
C.v <v ,α(SO )>α(SO ) D.c >2c ,α(SO )+
1 3 1 2 3 2 2 3 2 3
α(SO )>1
3 2
9.在一个固定容积的密闭容器中,保持一定的温度进行以下反应:H(g)+Br
2 2
(g)
2HBr(g) 已知加入1mol H 和2mol Br 时,达到平衡后生成a mol HBr(见下表
2 2
已知项),在相同条件下,且保持平衡时各组分的体积分数不变,对下列编号①~
③的状态,填写下表中的空白。
平衡时HBr的物
起始状态时物质的量n (mol)
已知 质的量n (mol)
H Br HBr
编号 2 2
1 2 0 a
① 2 4 0
② 1 0.5a
③ m g (g≥2m)
4
学科网(北京)股份有限公司山西省榆次第一中学校 李金虎
答案:
1.解析:选C 利用极值转化法(一边倒)可进行判断。
2.解析:选C 在容积可变的情况下,从对平衡混合物中三者的物质的量对各物质的量的浓度影响角
度思考.在“均减半”或“均加倍”时,相当于A、B、C三种物质的浓度都没有改变,“均增加1mol”
时相当于A、C物质的浓度减小,B物质的浓度增大,平衡右移;“均减小1mol”时相当于A、C物质的
浓度增大,B物质的浓度减小,平衡左移。
3.解析:选B
2A(g)+2B(g) C(g)+3D(g)
Ⅰ 2mol 2mol
Ⅱ 2mol 6mol
Ⅱ所加物质完全转化为A、B时,可生成4 molA、4 molB,与Ⅰ 物质的量比值相等,由反应可知,
反应前后气体的化学计量数相等,压强对平衡移动没有影响,则Ⅰ、Ⅱ为等效平衡状态,体系内混合气体
的百分组成相同,混合气体平均相对分子质量相同,由于容器体积相等,Ⅱ气体质量是Ⅰ气体质量的2倍,
则达到平衡时,途径Ⅰ的气体密度为途径Ⅱ密度的12,则B、C、D正确,A错误。
4.解析:选C 在平衡体系中再充入1 mol HI,相当于加压,由反应可知,反应前后气体的化学计
量数相等,加压平衡不移动,HI的转化率不变。
5.解析:选B 最初投入2 mol PCl ,在恒温恒容条件下,相当于回加压,平衡左移,PCl 所占体积
5 5
分数增大。
6.解析:选A 过程假设:
思维程序:第①步两容器平衡后状态一模一样。
第②步撤去隔板没有任何变化。
第③步压缩时平衡逆向移动,故NO 的转化率变小。
2 4
7.解析:选C 容器Ⅰ中从正反应开始到达平衡,该反应为放热,容器Ⅱ中从逆反应开始到达平衡,
该反应为吸热,无法比较Q 与Q 的大小,故A错误;容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1
1 2
mol CO和1 mol H O,压强不影响该化学平衡,但容器Ⅲ中反应的物质量大,放热多,到达平衡时温度更
2
高,该反应正反应是放热反应,温度升高平衡逆向移动,则容器Ⅲ中CO的转化率低,CO的百分含量高,
故B错误;容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应方向移
动,则容器Ⅱ中反应的平衡常数大于容器Ⅰ,C正确,温度相同时,容器Ⅰ中CO的转化率与容器Ⅱ中
CO 的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡
2
向正反应移动,二氧化碳的转化率比两容器相同温度对容器Ⅱ中CO 的转化率低,故容器Ⅰ中CO的转化
2
5
学科网(北京)股份有限公司山西省榆次第一中学校 李金虎
率与容器Ⅱ中CO 的转化率之和小于1,故D错误。
2
8.解析:选C 比较容器1、2,容器2中投料相当于容器1中的2倍,相当于容器2中起始压强是1
中的2倍,所以平衡时用2中各物质表示的反应速率均大于1中;由于2中压强大,更有利于反应正向移
动,故平衡时c>2c,A错误。比较容器1、3,3中温度高,由正反应放热可知,升高温度平衡向逆反应方
2 1
向移动,平衡常数减小,所以K >K ;比较容器2、3中投料,2中投料相当于3中2倍,3中温度高,且
1 3
平衡逆向移动,所以一定有p <2p ,B错误。比较容器1、3,只有温度不同,3中温度高,反应速率快,
2 3
则有v <v ;3中更有利于反应逆向进行,SO 的转化率低,则有α(SO )>α(SO ),C正确。比较容器2、
1 3 2 1 2 3 2
3,2中投料相当于3中2倍,若建立相同平衡,则c =2c ,但2中压强大,温度低,有利于反应向生成SO
2 3 3
的方向进行,则c>2c;容器2、3分别从不同方向建立平衡,若建立相同平衡则有α(SO )+α(SO )=1,
2 3 2 3 3 2
但由于2中温度低、压强大,更利于反应向生成SO 的方向进行,α(SO )减小,故α(SO )+α(SO )<1,D
3 2 3 2 3 3 2
错误。
9.解析: ①2a ② 0 mol、0.5 mol ③x=2(g-2m)、y=a(g-m)
6
学科网(北京)股份有限公司山西省榆次第一中学校 李金虎
7
学科网(北京)股份有限公司