文档内容
高一化学上学期第一次月考-(基础 B 卷)
班级___________ 姓名___________ 学号____________ 分数____________
(考试时间:90分钟 试卷满分:100分)
考试范围:第一章 物质及其变化 难度:★★★☆☆
注意事项:
1.本试卷分第I卷(选择题)和第II卷(非选择题)两部分。答卷前,考生务必将自己的班级、姓名、
学号填写在试卷上。
2.回答第I卷时,选出每小题答案后,将答案填在选择题上方的答题表中。
3.回答第II卷时,将答案直接写在试卷上。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
答案
第Ⅰ卷(选择题 54 分)
一、选择题:本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.纪录片《我在故宫修文物》表现了文物修复者穿越古今与百年之前的人进行对话的职业体验,让我们
领略到历史与文化的传承。下列文物修复和保护的过程中涉及化学变化的是( )
A B C D
银器用除锈剂除锈 变形的金属香炉复原 古画水洗除尘 木器表面擦拭烫蜡
2.物质分类是化学研究的重要方法之一。化学工作者经常根据物质的组成对物质进行分类研究。近年来
发现,在金星大气层中存在三氧化二碳(C O)。下列物质与C O 属于同一类物质的是( )
2 3 2 3
A.KOH、Mg(OH) B.HSO 、HCO
2 2 4 2 3
C.SO 、NO D.NaSO 、KClO
2 2 3 3
3.血液属于胶体,透析是除去肾衰竭病人血液中的毒性物质、从而拯救病人生命的重要方法。透析的原
理是( )
A.蒸发 B.电泳 C.过滤 D.渗析4.下列有关FeCl 溶液和Fe(OH) 胶体的叙述正确的是( )
3 3
A.将饱和FeCl 溶液滴加到NaOH溶液中可制得Fe(OH) 胶体
3 3
B.Fe(OH) 胶体带正电,FeCl 溶液呈电中性
3 3
C.两种分散系的分散质具有相同的粒子直径
D.利用丁达尔效应可将两种液体区分开
5.雾霾、PM2.5已经成为公众耳熟能详的热词。“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒
物,也称为可入肺颗粒物。下列有关说法中,错误的是( )
A.雾霾有可能产生丁达尔效应
B.雾霾的形成与工业排放的烟气和汽车尾气有关系
C.“PM2.5”分散在大气中形成气溶胶,性质稳定,没有必要纳入空气质量评价指标
D.雾霾天气严重危害人体健康
5.铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。
图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是( )
A.复分解反应、复分解反应、化合反应、置换反应
B.中和反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
6.下列各选项中,不能满足如图一步关系选项是( )A.X为铜、Y为氧化铜、Z为硫酸铜 B.X为二氧化碳、Y氧气、Z为一氧化碳
C.X为碳酸钙、Y氧化钙、Z为氢氧化钙 D.X为氢氧化钠、Y氯化钠、Z为碳酸钠
7.下列说法正确的是( )
A.将 AgCl 放入水中不能导电,故 AgCl 不是电解质
B.CO 溶于水得到的溶液能导电,所以 CO 是电解质
2 2
C.固态的 NaCl 不导电,熔融态的 NaCl 能导电,NaCl 是电解质
D.金属能导电,所以金属是电解质
8.下列物质中存在自由移动的Cl-的是:
A.熔融的KClO B.NaCl固体 C.液态HCl D.MgCl 溶液
3 2
9.下列反应的离子方程式不正确的是( )
A.铁与稀盐酸反应:2Fe+6H+= 2Fe3++3H↑
2
B.氢氧化钠溶液与盐酸反应:OH-+H+= H O
2
C.锌与硫酸铜溶液反应:Zn+Cu2+ = Zn2++Cu
D.氯化钡溶液与稀硫酸反应:Ba2++SO 2-= BaSO↓
4 4
10.下列各组反应中,不能用同一个离子方程式表示的是( )
A.盐酸分别与NaOH溶液、Ca(OH) 溶液反应
2
B.硫酸分别与NaOH溶液、Ba(OH) 溶液反应
2
C.硝酸分别与NaCO 溶液、KCO 溶液反应
2 3 2 3
D.锌分别与稀盐酸、稀硫酸反应
11.水溶液中能大量共存的一组离子是
A.NH +、Ba2+、Br-、CO2- B.Cl-、SO 2-、Fe2+、H+
4 3 3
C.K+、Na+、SO 2-、MnO - D.Na+、H+、NO -、HCO -
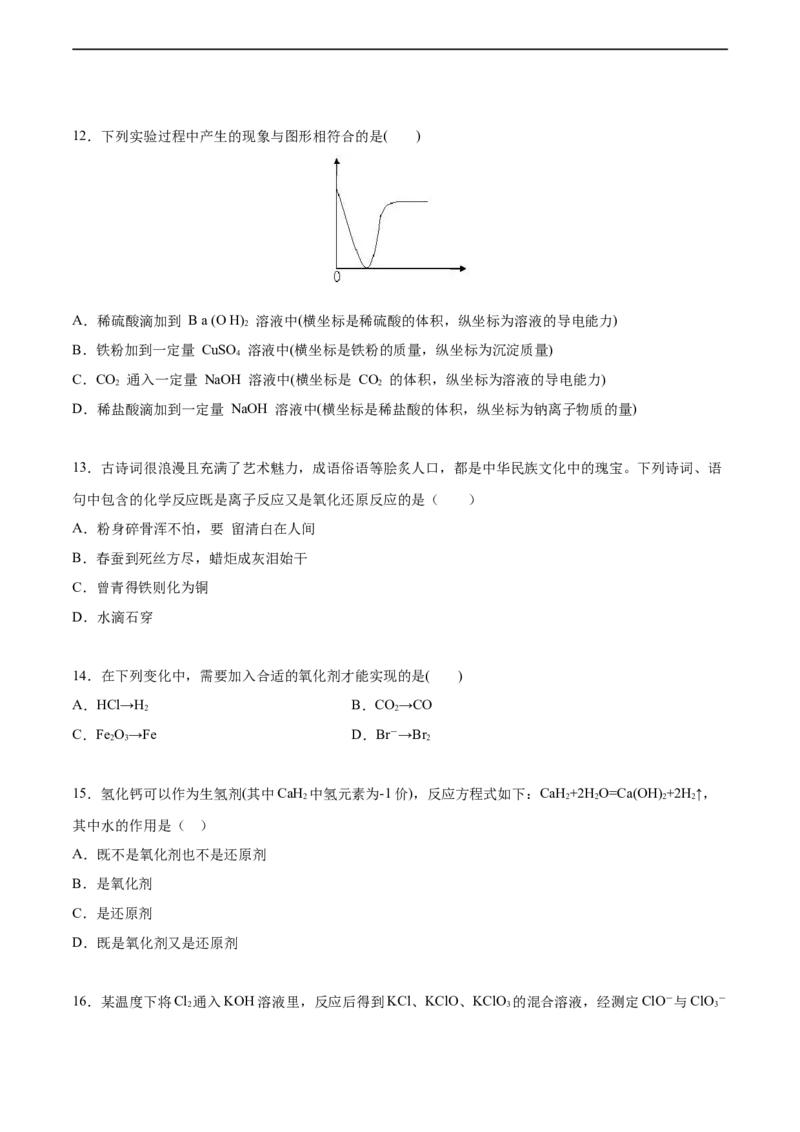
4 4 3 312.下列实验过程中产生的现象与图形相符合的是( )
A.稀硫酸滴加到 B a (O H) 溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
2
B.铁粉加到一定量 CuSO 溶液中(横坐标是铁粉的质量,纵坐标为沉淀质量)
4
C.CO 通入一定量 NaOH 溶液中(横坐标是 CO 的体积,纵坐标为溶液的导电能力)
2 2
D.稀盐酸滴加到一定量 NaOH 溶液中(横坐标是稀盐酸的体积,纵坐标为钠离子物质的量)
13.古诗词很浪漫且充满了艺术魅力,成语俗语等脍炙人口,都是中华民族文化中的瑰宝。下列诗词、语
句中包含的化学反应既是离子反应又是氧化还原反应的是( )
A.粉身碎骨浑不怕,要 留清白在人间
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.曾青得铁则化为铜
D.水滴石穿
14.在下列变化中,需要加入合适的氧化剂才能实现的是( )
A.HCl→H B.CO→CO
2 2
C.Fe O→Fe D.Br-→Br
2 3 2
15.氢化钙可以作为生氢剂(其中CaH 中氢元素为-1价),反应方程式如下:CaH+2H O=Ca(OH) +2H ↑,
2 2 2 2 2
其中水的作用是( )
A.既不是氧化剂也不是还原剂
B.是氧化剂
C.是还原剂
D.既是氧化剂又是还原剂
16.某温度下将Cl 通入KOH溶液里,反应后得到KCl、KClO、KClO 的混合溶液,经测定ClO-与ClO -
2 3 3的物质的量浓度之比为11∶1,则Cl 与KOH反应时,被还原的氯元素和被氧化的氯元素的物质的量之比
2
为( )
A.1∶3 B.4∶3 C.2∶1 D.3∶1
17.已知还原性:HSO (SO ) >I->Fe2+>NO,据此判断下列反应不能发生的是
2 3 2
A.HSO +I +H O=2HI+ H SO B.NO+SO =NO+SO
2 3 2 2 2 4 3 2 2
C.2FeCl +2HI= 2FeCl +2HCl+I D.3FeCl +4HNO =2FeCl +NO↑+2H O+Fe(NO )
3 2 2 2 3 3 2 3 3
18.已知Co O 在酸性溶液中易被还原成Co2+,Co O 、Cl 、FeCl 、I 的氧化性依次减弱,下列反应在水
2 3 2 3 2 3 2
溶液中不可能发生的是( )
A.3Cl+6FeI===2FeCl +4FeI
2 2 3 3
B.Cl+2KI===2KCl+I
2 2
C.Co O+6HCl===2CoCl +Cl↑+3HO
2 3 2 2 2
D.2FeCl +Cl===2FeCl
2 2 3
第 II 卷(非选择题 46 分)
二、(非选择题46分)
19.(6分)对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。
Ⅰ.现有以下物质:①HO ②Cu ③BaCO ④Fe(OH) 胶体 ⑤酒精 ⑥CO ⑦稀硫酸
2 3 3 2
(1)以上物质中属于混合物的是________(填序号,下同),属于电解质的是________。
(2)向④中逐滴滴加⑦,可观察到的现象是_____________________。
Ⅱ.虽然分类的方法不同,但四种基本反应类型和离子反应、氧化还原反应之间也存在着一定的关系。
(3)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示离子反应的是________(填字母)。
(4)有同学认为所有酸碱中和反应均可表示为H++OH-=H O。请举个例子反驳上述观点(用离子方程式表
2
示)_____________。
20.(10分)有A、B、C、D四种化合物,分别由K+、Ba2+、SO 2—、CO2−、OH—中的两种组成,它们
4 3
具有下列性质:
①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈
碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D的化学式。A、________,B、________,C、________,D、________。
(2)写出下列反应的离子方程式。
B与盐酸反应:_______________________________________________,
C与硫酸反应:_______________________________________________,
E(少量)与澄清石灰水反应:____________________________________。
21.(10分)现有甲、乙、丙三名同学分别进行Fe(OH) 胶体的制备实验。
3
I 甲同学向氯化铁溶液中加入少量的NaOH溶液;
II 乙同学直接加热饱和FeCl 溶液;
3
III 丙同学向25mL沸水中逐滴加入5~6滴FeCl 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
3
(1)其中操作正确的同学是______;他的操作中涉及到的化学反应方程式为 。
(2)证明有Fe(OH) 胶体生成的现象是 。
3
(3)丁同学将所制得的Fe(OH) 胶体分成两份,并进行下列实验:
3
①将其中一份装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,
这表明 。
②向另一份中不断滴加稀硫酸,观察到的现象是 。
22.(10分)按要求填空。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是________________,只有还原性的是
______________,既有氧化性又有还原性的是______________。
(2)某同学写出以下三个化学方程式:(未配平)
①NO+HNO→NO+HO
3 2 3 2
②NH +NO→HNO +HO
3 2 2
③NO+HO→HNO +HNO
2 4 2 3 2
其中你认为不可能实现的是__________________。
(3)下列三个氧化还原反应中,氧化性最强的物质的是______________。若溶质中Cl-与I-共存,为了氧化
I-而Cl-不被氧化,除单质外,还应用上述反应中的________________作氧化剂。
①2FeCl +2KI=2FeCl +2KCl+I
3 2 2
②2FeCl +Cl=2FeCl
2 2 3
③2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
23.(10分)根据反应8NH +3Cl=6NHCl+N ,回答下列问题。
3 2 4 2(1)氧化剂______,还原剂________。
(2)氧化产物______,还原产物_______。
(3)氧化剂与还原剂的物质的量之比:_________________________。
(4)用单线桥的方法表示该反应的电子转移情况。 。
(5)用双线桥的方法表示该反应的电子转移情况。 。