文档内容
{{##{{QQQQAABBLJYYigsE4googYAkIAITIAAACABB5hLCAAwwEUMoCCkkmKQQskIAIjLAQCgAMQwgVGCgJEOAAE4oDAgIBAQFAIBFIAAB=}A#A}=}#}{{##{{QQQQAABBLJYYigsE4googYAkIAITIAAACABB5hLCAAwwEUMoCCkkmKQQskIAIjLAQCgAMQwgVGCgJEOAAE4oDAgIBAQFAIBFIAAB=}A#A}=}#}{{##{{QQQQAABBLJYYigsE4googYAkIAITIAAACABB5hLCAAwwEUMoCCkkmKQQskIAIjLAQCgAMQwgVGCgJEOAAE4oDAgIBAQFAIBFIAAB=}A#A}=}#}{{##{{QQQQAABBLJYYigsE4googYAkIAITIAAACABB5hLCAAwwEUMoCCkkmKQQskIAIjLAQCgAMQwgVGCgJEOAAE4oDAgIBAQFAIBFIAAB=}A#A}=}#}{{##{{QQQQAABBLJYYigsE4googYAkIAITIAAACABB5hLCAAwwEUMoCCkkmKQQskIAIjLAQCgAMQwgVGCgJEOAAE4oDAgIBAQFAIBFIAAB=}A#A}=}#}{{##{{QQQQAABBLJYYigsE4googYAkIAITIAAACABB5hLCAAwwEUMoCCkkmKQQskIAIjLAQCgAMQwgVGCgJEOAAE4oDAgIBAQFAIBFIAAB=}A#A}=}#}镇江市 2024~2025 学年度第一学期高三期初质量监测
化学答案
2024.09
一、选择题(共13题,每题3分,共39分)
1 2 3 4 5 6 7 8 9 10
B A D B C B C C D D
11 12 13
A D C
二、非选择题
14 .本题共15分。
(1)3d9 2分
(2)增大氧气的溶解度,加快化学反应速率 2分
(3)适当增大溶液pH,促使萃取平衡正向移动,提高铜的萃取率 2分
(4)Na++3Fe3++2SO2-+3H O+3MgO=NaFe (SO ) (OH) ↓+3Mg2+ 2分
4 2 3 4 2 6
(5)1∶3 2分
(6)9.3 2分
(7)根据滴定方程式Ni2++ H Y2−=== NiY2−+2H+可知,恰好滴定到终点时,
2
n(Ni2+)=n(
1
H
2
Y 2 )=C•V=0.05000mol•L−1×0.05000L=2.500××10−3mol,
滴定取了25mL粗品溶液,则100mL该溶液中含Ni2+的物质的量为
4×2.500×10−3mol=1.000×10−2mol 1分
即NiSO •7H O的物质的量为1.000×10−2mol,则
4 2
m(NiSO •7H O)=n(NiSO •7H O)×M(NiSO •7H O)=1.000×10−2mol×281g•mol−1=2.81g
4 2 4 2 4 2
1分
则粗品中NiSO •7H O的纯度= 2 . 8 1 g ×100% =93.67% 1分
4 2
3.000g
15. 本题共15分。
(1)(酚)羟基 醛基 2分
OH
3分
N N
(2)
O
(3)7∶3 2分
COOH
O H C C H O 3分
(4)OH OH OOCCH 3
CH COOCH
(5) 3 2
O HCHO,(CH 3 ) 2 NH N O (CH 3 CO) 2 O O
CH 3 CN CH 3 COOK
OOCCH 3 OH
CH 3 COOCH 2 COOH _ HOCH COOH
2
O 2/催化剂 (1 )OH ,
(2 ) H+
(每步1分,全对得5分)
16. 本题共15分。
(1)①Na S 2分
2
②c(HS−) > c(H S) > c(S2−) 2分
2
③6.9×103 2分
(2)①FeS+3HCrO-+10H+=Fe(OH) ↓+SO2-+3Cr3++5H O 2分
4 3 4 2
②pH增大,溶液中OH−浓度增大,FeS胶粒吸附OH−增多,吸附六价铬离子减少;生
成的Fe(OH) 和Cr(OH) 覆盖在硫化亚铁表面,阻止硫化亚铁进一步还原六价铬离子。
3 3
3分
(3)滴入适量的柠檬酸钠溶液;(1分)水浴加热至70℃,加入硫代乙酰胺溶液,(1分)
充分反应后,静置过滤,用蒸馏水洗涤,(1分)直至向最后一次洗涤后的滤液加BaCl
2
溶液无沉淀 (1分) 4分
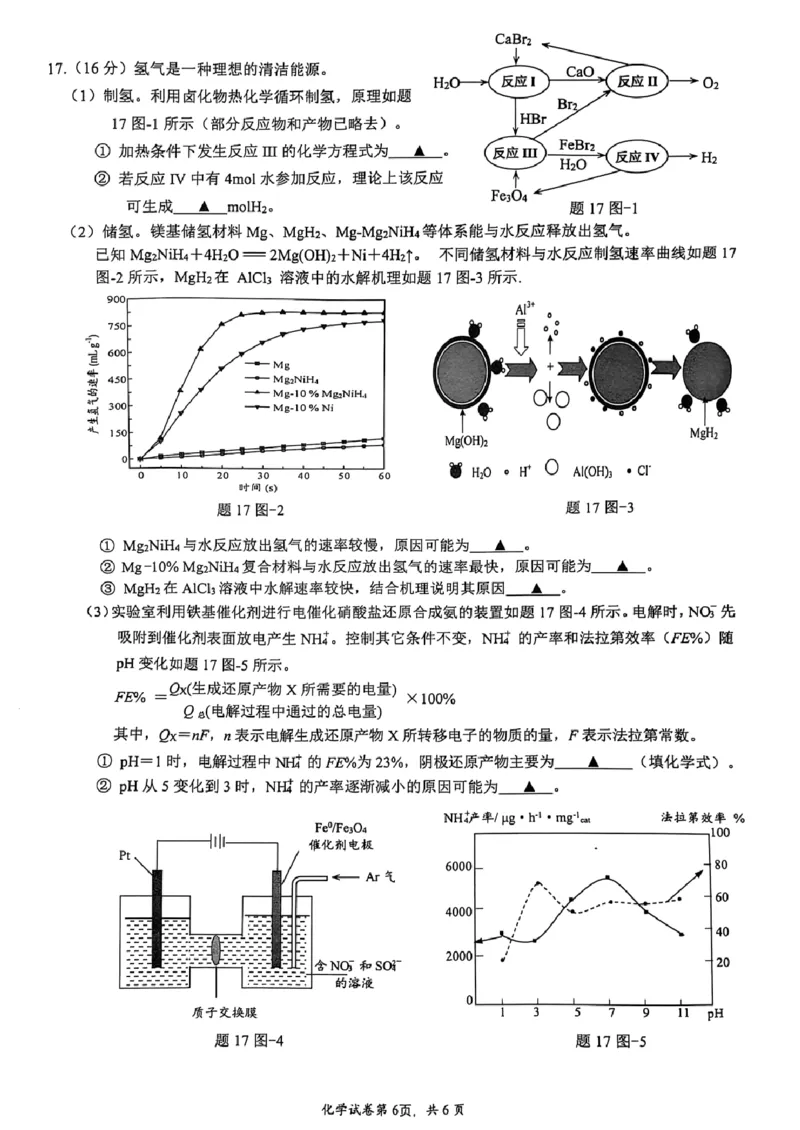
17. 本题共16分。
△
(1) ①Fe O +8HBr =====3FeBr +Br +4H O 2分
3 4 2 2 2
②1mol 2分
(2)①Mg NiH 与水反应,产生的Mg(OH) 沉淀覆盖在反应物表面,阻止反应的进一步进
2 4 2
行,放出氢气的速率较慢。 2分
②Mg NiH 水解产生超细 Ni 颗粒,形成许多Mg-Ni原电池,加快化学反应;同时反
2 4
应放热,溶液温度上升,镁和Mg NiH 水解反应速率更快。 2分
2 4
③ AlCl 溶液水解:Al3++3H O=Al(OH) +6H+,Al3+水解产生的大量H+和Cl−
3 2 3
会腐蚀破坏MgH 表面生成的Mg(OH) 保护膜,加快MgH 水解速率。 3分
2 2 2
(3)①H 和NH+(或H ) 2分
2 4 2
②pH从5变化到3时,溶液中H+浓度逐渐增大,析氢反应速率增大,且氢气阻碍NO-
3
吸附到催化剂表面,使NO- 还原的速率下降,NH+ 产率降低。 3分
3 4
2