文档内容
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}}#}=AABANRiBAAoIAFwGgSACChkQKACg2wQCgRAAAAAoiggACQDBAQQ{#{{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}}#}=AABANRiBAAoIAFwGgSACChkQKACg2wQCgRAAAAAoiggACQDBAQQ{#{{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}2025 届贵州省六校联盟高考实用性联考卷(三)
化学参考答案
一、选择题:本题共14小题,每小题3分。
题号 1 2 3 4 5 6 7
答案 B D C A C A A
题号 8 9 10 11 12 13 14
答案 C C D B D D B
【解析】
1.“丹砂烧之成水银,积变又还成丹砂”,是指丹砂(HgS)在空气中灼烧变成Hg和S,积变
又还成丹砂指Hg和S又化合成HgS,这里描述的化学反应是不可逆的,B错误。
2.第一能层只有s能级,没有p能级,A错误。中子数为1的氦核素质量数应为3,B错误。
图中表示的是 反−2−丁烯的球棍模型,C错误。
3.维生素C作抗氧化剂,是由于其结构能被氧化为脱氢抗坏血酸而发挥抗氧化作用。
4.酚羟基不能与NaHCO 反应。
3
5.A项,1mol SiO 中含有4mol的Si—O键;B项,标准状况下戊烷不是气体;D项,一般
2
情况下,由于 I-还原性强于Fe2+,故氯气先氧化I-,当有2mol Fe2+被氧化时,表明I-已
反应完,该过程中转移电子总数大于2N 。
A
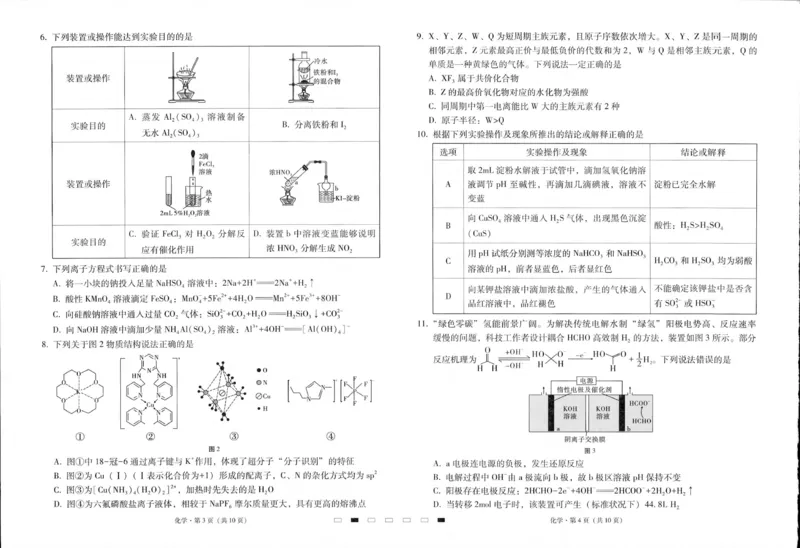
6.B项,铁粉与I 加热可发生反应;C项,用该装置验证FeCl 对H O 分解反应有催化作用,
2 3 2 2
应确保两支试管反应温度一致;D项,硝酸易挥发,挥发出来的硝酸将碘离子氧化成碘单
质也可以导致b中溶液变蓝。
7.将一小块的钠投入足量NaHSO 溶液中:2Na + 2H⁺= 2Na⁺ + H ↑,A正确。酸性条件
4 2
下不能生成OH-,B错误。CO 过量应生成HCO,C错误。漏写了离子反应,因为NaOH
2 3
溶液过量,铵根离子也参与离子反应,D错误。
8.图①中18−冠−6通过配位键与钾离子作用,A错误。图②C、N杂化方式为sp2、sp3,B错
误。图③由于氧的电负性较大,N电负性比O小,更容易提供孤电子对,氨气与铜离子形
成配位键比水与铜离子形成配位键稳定,因此加热时该离子先失去的配位体是H O, C正
2
确。图④物质中阳离子的空间位阻较大,与六氟合磷离子形成的离子键弱于钠离子,虽然
摩尔质量更大,但离子键较弱,熔沸点低于六氟合磷酸钠,D错误。
化学参考答案·第1页(共6页)
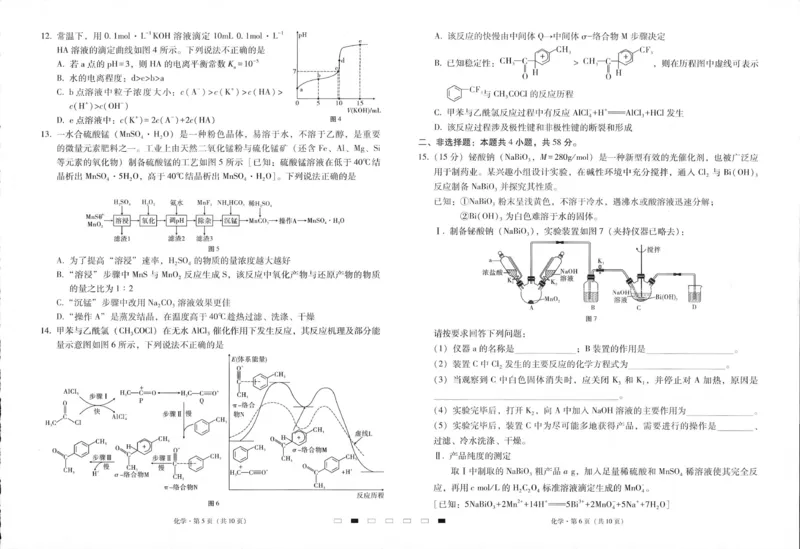
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}9.由题意可知Z是N或者P元素,X、Y、Z同周期且相邻,故X、Y、Z可能为第二周期的
B、C、N或者第三周期的Al、Si、P,Q是Cl,W与Q相邻主族,故W可能为O或S。
XF 可能是 BF 或者 AlF ,后者是离子化合物,A 错误。Z 的最高价氧化物对应的水化物
3 3 3
为HNO 或者H PO ,H PO 不是强酸,B错误。不管W是O(N、F)或者S(P、Cl),
3 3 4 3 4
同周期中比它第一电离能大的主族元素都有两种,C正确。若W是O,则原子半径W<Q,
若W是S,则原子半径W>Q,D错误。
10.淀粉水解液加氢氧化钠,再加碘液,氢氧化钠会与碘单质反应,A错误。硫酸铜(CuSO )
4
与硫化氢(H S)反应的原理基于复分解反应,生成极难溶的硫化铜(CuS),H S为二元
2 2
弱酸,H SO 为二元强酸,B错误。要证明是否为弱酸,可以通过测定相同浓度的弱酸盐
2 4
溶液的碱性的强弱,故NaHSO 显红色是HSO电离导致的结果,不是水解,故不能说亚
3 3
硫酸为弱酸,C错误。满足条件的还有可能是高锰酸钾,D正确。
1
11.由分析可知,a 为阴极,b 为阳极,阳极反应:①HCHO+OH-−e-HCOOH+ H ,
2
2
②HCOOH+OH-=HCOO-+H O,阴极反应 2H O+2e-=H ↑+2OH-,故 b 极溶
2 2 2
液pH降低,转移2mol电子时,阴、阳两极各生成1mol H ,共2mol H ,故B错误。
2 2
12.0.1mol·L−1HA溶液的pH3,则c(H+)=c(A-)=10−3,代入平衡常数的表达式即可算出,
A正确。酸的电离、碱的电离对水的电离起抑制作用,d点溶质为强碱弱酸盐KA,对水
的电离起促进作用,c点溶质为KA和HA,且由图像可知c点呈中性,不影响水的电离,
所以水的电离程度:d >c >b >a,B正确。b点溶液中溶质为等物质的量浓度的HA和KA,
溶液pH7,溶液呈酸性,说明HA电离程度大于A-水解程度,所以c(A)c(HA),钾离子
不水解,且HA电离程度和A-水解程度都较小,所以c(A)c(K)c(HA)c(H)c(OH),
C正确。e点溶液是物质的量之比为2∶3的HA和KOH反应后的溶液,溶液中存在物料
守恒,2c(K)3c(A),即2c(K)3c(A)3c(HA),D错误。
13.“溶浸”过程中硫酸发挥其酸性作用,要提高溶浸速率,需要适当增大c(H+),若硫酸浓度
过大,由于溶剂水的百分含量过小,只有部分硫酸可以电离,c(H+)比较小,A 错误。氧
化产物与还原产物的物质的量之比为 1∶1,B 错误。“沉锰”过程中,Na CO 溶液碱性
2 3
更强,会导致生成氢氧化锰 ,C错误。
14.根据反应历程可知,中间体Q→中间体σ−络合物M该步骤活化能最大,反应速率慢,故
该步骤为决速步骤,A正确。组成结构相似的物质,能量越低越稳定,由两种物质的稳定
性可知,后者能量较高,因此,参与反应的物质能量较高,其能量轮廓图曲线(虚线L)
化学参考答案·第2页(共6页)
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}应在甲苯的实线图之上,B错误。甲苯与乙酰氯反应过程中AlCl 作催化剂,参与反应后
3
又重新生成,Ⅰ中生成四氯合铝离子后,又会发生反应AlCl H=AlCl HCl,C
4 3
正确。该过程涉及极性键和非极性键的断裂和形成,D正确。
二、非选择题:本题共4小题,共58分。
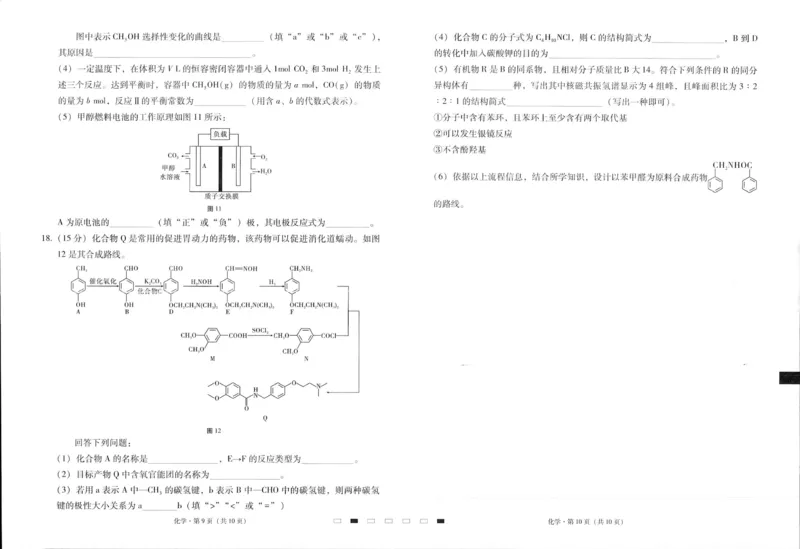
15.(除特殊标注外,每空2分,共15分)
(1)恒压滴液漏斗(或恒压分液漏斗)(1分) 除去Cl 中混有的HCl(1分)
2
(2)3NaOH+Cl +Bi(OH) =NaBiO +3H O+2NaCl(反应物和生成物化学式均正确给1
2 3 3 2
分,方程式配平,即化学计量系数均正确给1分)
(3)防止Cl 过量使C中溶液呈酸性,导致NaBiO 分解( 答到:Cl 过量使C中溶液呈
2 3 2
酸性给1分,答到:导致NaBiO 分解给1分)
3
(4)除去A中残留的Cl (或将A中剩余的Cl 反应掉)
2 2
(5)在冷水浴中结晶或在冰水浴中结晶(答到:冷却(降温)结晶只给 1 分,有套用模
板的嫌疑,没有进行具体情境下的问题分析)
28cV
(6) %
a
(7)不能(1分) 酸性条件下,ClO-也能将Cl-氧化生成Cl(或在酸性条件下,NaClO
2
也可与NaCl反应得到Cl 。只提到NaClO或ClO-与NaCl或Cl-反应,给1分,要同时
2
答到酸性条件才给2分)
【解析】(1)盛放浓盐酸的仪器的名称为恒压滴液漏斗(或恒压分液漏斗);B装置用于除
去氯气中混有的氯化氢,盛放的试剂是饱和食盐水。
( 2 ) C 装 置 中 Bi(OH) 被 氯 气 氧 化 为 NaBiO , 化 学 方 程 式 为
3 3
Bi(OH) +3NaOH+Cl =NaBiO +2NaCl+3H O。
3 2 3 2
(3)防止Cl 过量使溶液呈酸性,导致NaBiO 分解,当观察到C中白色固体消失时,应
2 3
关闭K 和K ,并停止对A装置加热。
3 1
(4)氯气有毒,实验完毕后,打开K ,向甲中加入NaOH溶液的主要作用是除去甲装置
2
中残留Cl 。
2
(5)NaBiO 不溶于冷水,遇沸水或酸溶液迅速分解,故因将C反应得到的悬浊液用冷水
3
或者冰水降温结晶获得产品。
(6)根据得失电子守恒建立关系式:5 NaBiO ~2MnO~5H C O ,当达到滴定终点时,消
3 4 2 2 4
耗 c mol/L 的草酸标准溶液 VmL,则 n(NaBiO )=n(H C O )=c mol/L×V×10−3L=cV×
3 2 2 4
cV103280 280cV
10−3mol,该产品的纯度为 100% %。
a a
(7)不能;C中含有NaBiO 和NaClO,酸性条件下,ClO-也能将Cl-氧化生成Cl 。
3 2
化学参考答案·第3页(共6页)
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}16.(除特殊标注外,每空2分,共14分)
(1)CaSO 、BaSO (写对1个给1分,见之有分,只要看到其中的正确答案就按1个给
4 4
1分)
(2)2Fe3++H S=2Fe2++S↓+2H+ (反应物和生成物化学式均正确给 1 分,方程式配
2
平,即化学计量系数均正确给1分)
(3)将 Fe2+氧化为 Fe3+,使 Fe 元素以 Fe(OH) 分离出来(只答到将亚铁离子氧化为三价
3
铁给1分,答到使Fe元素以Fe(OH) 分离出来给1分)
3
(4)2.7×10−7(1分)
(5)9.78%
(6)2Ni2 ClO 4OH=2NiOOHCl H O(反应物和生成物化学式均正确给
2
1分,方程式配平,即化学计量系数均正确给1分)
(7)①5 ②18(1分)
【解析】(1)硫酸与氧化镍、氧化铁、氧化钙、氧化铜、氧化钡分别生成硫酸盐产物,其
中硫酸钡难溶,硫酸钙微溶,因此浸出渣的主要成分为CaSO 和BaSO 。
4 4
(2)“酸浸”过后溶液中含有Fe3+具有氧化性,可与H S反应,2Fe3++H S=2Fe2++S↓
2 2
+2H+ 。
(3)操作B的目的是除铁,但是Fe2+沉淀所需pH更大,很难分离,故将其氧化为Fe3+,
使Fe元素以Fe(OH) 分离出来。
3
(4)由CaF的K =c(Ca2+)×c2 (F-)可知,所需的c(Ca2+)为2.7×10−7。
sp
(5)根据分解反应方程式可算失重率为9.78% 。
(6)2Ni2 ClO 4OH=2NiOOHCl H O。
2
17.(除特殊标注外,每空2分,共14分)
(1)−49.4kJ/mol(不写单位扣一分,不写“−”不得分) K ×K (1分)
2 3
(2)a、b(少选1个或多选1个扣1分,如abc得1分,acd得0分)
(3)a 反应Ⅰ为放热反应,升高温度,平衡逆向移动,导致CH OH的选择性降低(答
3
到:反应Ⅰ为放热反应,升高温度,平衡逆向移动给1分,答到:导致CH OH的选择性
3
降低给1分)
b(ab)
(4)
(1ab)(33ab)
(5)负(1分) CH OH – 6e- + H O=CO ↑+6H+(反应物和生成物化学式均正确,
3 2 2
且表示的是失电子给1分,电极反应配平,即化学计量系数均正确给1分)
化学参考答案·第4页(共6页)
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}【 解 析 】( 1 ) 由 盖 斯 定 律 可 知 , 反 应 Ⅱ + 反 应 Ⅲ 可 得 反 应 Ⅰ , 则
H H H 49.4kJmol1,则K K K 。
1 2 3 1 2 3
(2)反应Ⅰ是反应前后气体分子数之和不相等的反应,所以恒温、恒容条件下压强在改
总质量
变,a正确。混合气体的平均摩尔质量= ,反应前后,气体总质量不变,但是
总物质的量
总物质的量在变,故平均摩尔质量在改变,b 正确。甲醇和水 1∶1 生成,物质的量一直
不变,c错误。焓变是常数,一直不变,d错误。答案选ab。
(3)反应Ⅰ为放热反应,温度升高,平衡逆向移动,甲醇选择性下降,故图中表示CH OH
3
选择性变化的曲线是a;Ⅱ为吸热反应,温度升高,平衡正向移动,一氧化碳选择性升高,
故图中表示CO选择性变化的曲线是b;则图中曲线c表示CO 平衡转化率。
2
(4)设达到平衡时 H 为 x mol,H O 为 y mol,根据碳原子守恒可得:
2 2
n(CO)n(CO )n(CH OH)1mol,故n(CO )(1ab)mol,根据氢原子守恒可得:
2 3 2
2n(H )4n(CH OH)2n(H O)6mol ,即 2x4a2y6 ,根据氧原子守恒可得:
2 3 2
n(CO)2n(CO )n(CH OH)n(H O)2mol,即b2(1ab)a y2,联立方程
2 3 2
解 得 : x33ab , yab , 故 反 应 Ⅱ 的 平 衡 常 数 为
c(CO)cH O b(ab)
2 。
cCO cH (1ab)(33ab)
2 2
(5)由题可知,A为负极,电极反应式为CH OH – 6e- + H O=CO ↑+6H+
3 2 2
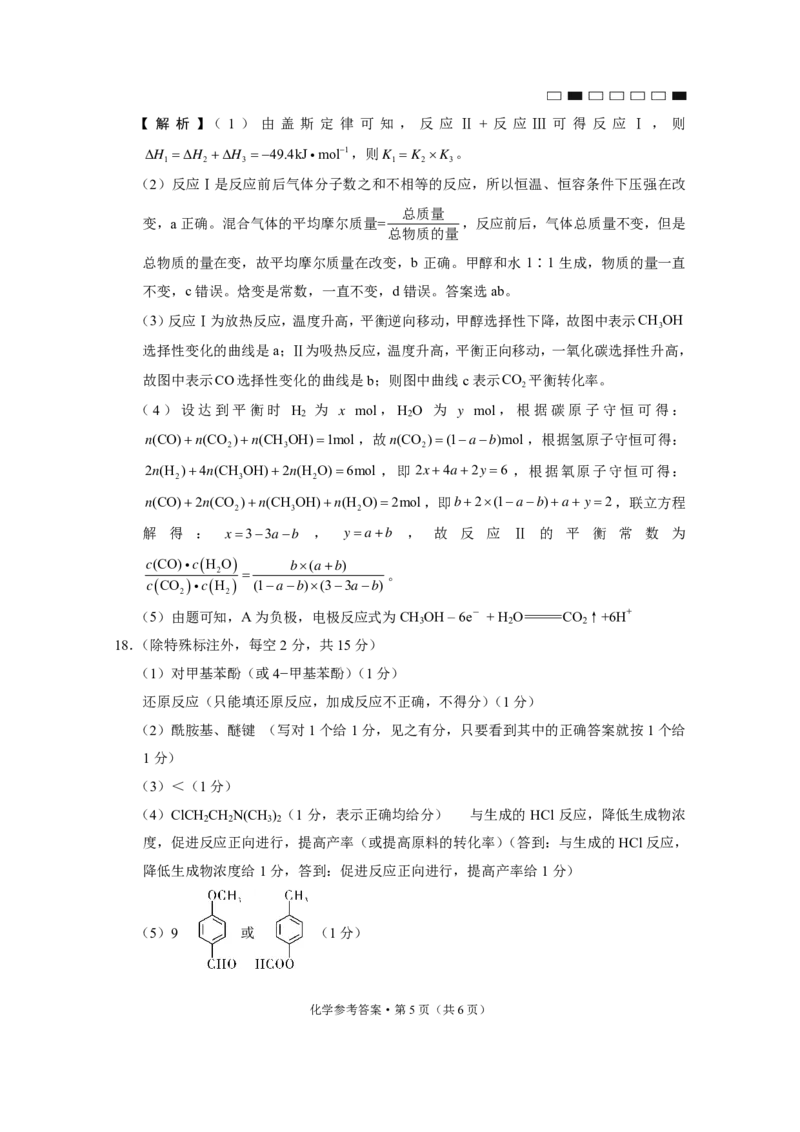
18.(除特殊标注外,每空2分,共15分)
(1)对甲基苯酚(或4−甲基苯酚)(1分)
还原反应(只能填还原反应,加成反应不正确,不得分)(1分)
(2)酰胺基、醚键 (写对1个给1分,见之有分,只要看到其中的正确答案就按1个给
1分)
(3)<(1分)
(4)ClCH CH N(CH ) (1 分,表示正确均给分) 与生成的 HCl 反应,降低生成物浓
2 2 3 2
度,促进反应正向进行,提高产率(或提高原料的转化率)(答到:与生成的HCl反应,
降低生成物浓度给1分,答到:促进反应正向进行,提高产率给1分)
(5)9 或 (1分)
化学参考答案·第5页(共6页)
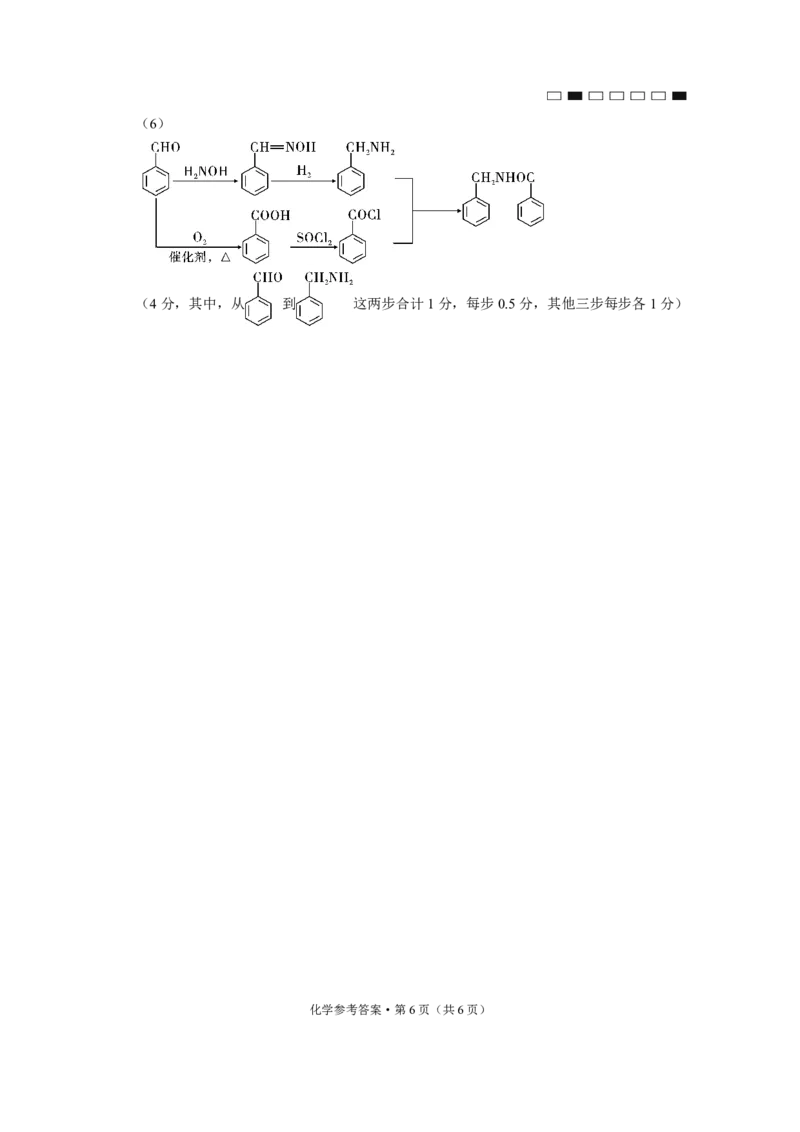
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}(6)
(4分,其中,从 到 这两步合计1分,每步0.5分,其他三步每步各1分)
化学参考答案·第6页(共6页)
{#{QQABDQCAggioAAAAARgCQw2gCAKQkhCCASgGwFAIoAABiRNABAA=}#}