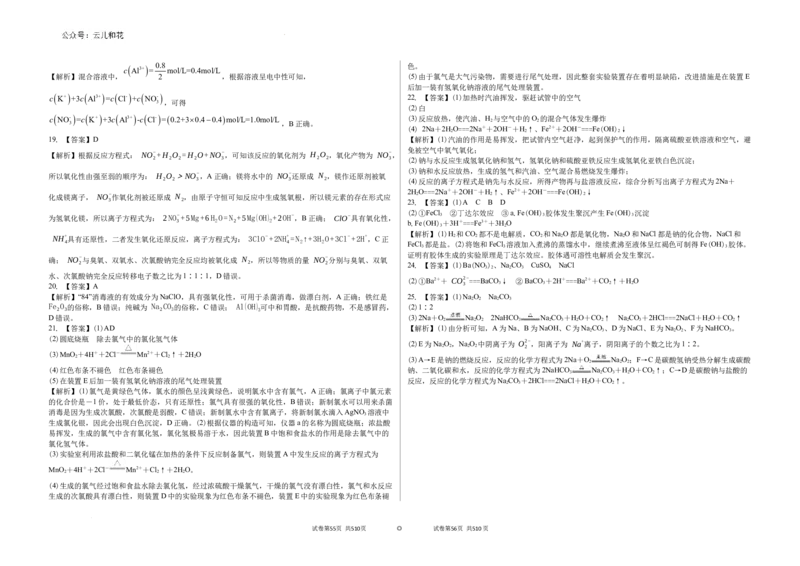文档内容
A. 18 g水中含有的氢原子数目为N
白城市第一中学 2024-2025 学年度高一上学期期中考试 A
B. 1 mol氩气分子所含的原子数目为2N
A
C. 标准状况下,以任意比混合的氢气和一氧化碳气体共8.96 L,在足量氧气中充分燃烧时消耗氧气的分
化学试卷
子数为0.4N
A
本试题卷分选择题和非选择题两部分,共6页,满分100分,考试时间75分钟。 D. 0.5 mol硝酸中含有的氧原子数目为1.5N
A
9. 在水溶液中能够大量共存的一组离子是( )
考生注意:
A. K+、Fe3+、SO B. Mg2+、Al3+、OH-
1.答题前,请务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔分别填写在试题卷和答题纸规定的位置 C. Ag+、Ba2+、Cl- D. Ca2+、NH 、CO
10. 下列关于铁及其化合物的说法正确的是( )
上。
A. 红热的铁能与水蒸气反应,生成Fe O 和H
3 4 2
2.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上的作答一律
B. Fe(OH) 在空气中充分灼烧得到FeO
2
C. FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
无效。
D. 过量铁与氯气或者稀盐酸反应均可制得FeCl
2
3.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可先使用2B铅笔,确
11. 类推是化学学习和研究常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确与否。根
定后必须使用黑色字迹的签字笔或钢笔描黑。 据你所掌握的知识,判断下列类推结论中正确的是( )
A. 燃烧不能用CO 灭火,故Na燃烧也不能用CO 灭火 B. Al在O 中燃烧生成 ,故Fe在O 中燃
一、单选题(本大题共20小题,每小题1.5分,共30分。) 2 2 2 2
烧生成
1. 现有以下物质:①NaCl溶液、②CH COOH、③NH 、④BaSO 、⑤蔗糖、⑥H O,其中属于电解质的
3 3 4 2
C. CO 与 反应生成 和O ,故SO 与Na O 反应生成 和O D. Al与NaOH溶液反应生成
是( ) 2 2 2 2 2 2
H ,故 与NaOH溶液反应也生成
A. ②③④ B. ②④⑥ C. ③④⑤ D. ①②④ 2
12. 实验中要用的盐酸可由密度为1.2 g⋅cm−3 、质量分数为36.5%的浓盐酸稀释得到,20 mL该浓盐酸可
2. 下列物质能导电且属于电解质的是( )
以稀释得到6.0 mol⋅L−1 盐酸的体积为( )
A. 铜 B. 稀硫酸 C. NaCl固体 D. 熔融KCl
A. 25 mL B. 30 mL C. 35 mL D. 40 mL
3. 在溶液中,能大量共存的离子组是( )
13. 在溶液的配制过程中会引起浓度偏高的是( )
A. Na+、H+、 CO2−、 NO− B. Mg2+、OH-、 SO2−、 NO− A. 配制500 mL 0.1 mol/L 的硫酸铜溶液,用托盘天平称取胆矾8.0 g
3 3 4 3
B. 配制NaOH溶液时,NaOH固体放在烧杯中称量时间过长
C. K+、Fe3+、 SO2−、 NO− D. Na+、H+、Cl-、OH- C. 定容时,仰视刻度线
4 3
D. 配制NaOH溶液时,将称量好的NaOH固体放入小烧杯中溶解,未经冷却立即转移到容量瓶中并定容
4. 已知在酸性溶液中,2RO +10I-+xH+===5I +2R2++yH O,则RO 中R的化合价是( )
2 2
14. 有Na O、Na O 、Na CO 、NaHCO 、NaCl中的某几种组成的混合物,向混合物中加入足量的盐酸有
A. +4 B. +5 C. +6 D. +7 2 2 2 2 3 3
气体放出,将放出的气体通过过量的NaOH溶液后,气体体积有所减少,若将上述混合物在空气中充分加
5. 在Cl +H O===HCl+HClO中,氯气是( )
2 2
热,也有气体放出,且加热后残留固体物质的质量比加热前有所增加,下列推断正确的是( )
A. 只做氧化剂 B. 只做还原剂
A. 混合物中一定不含有Na O B. 混合物中一定不含有Na CO 和NaCl
C. 既做氧化剂又做还原剂 D. 既不做氧化剂又不做还原剂 2 2 3
C. 混合物中是否含有Na CO 和NaCl无法确定 D. 混合物中一定不含有Na O 和NaCl
6. 向紫色石蕊溶液中分别加入(或通入)足量的下列物质,最后不能使溶液变成无色的是( ) 2 3 2 2
15. 疫情防控期间,家庭和各种公共场所需要大量使用“84清毒液”,某兴趣小组利用NaClO固体配制一
A. Cl B. 新制氯水 C. Na O D. NaOH
2 2 2
定浓度的“84消毒液”,下列有关说法正确的是( )
7. 下列对常见离子的检验方法及结论一定正确的是( )
A. 加入稀盐酸,产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有 CO2−
3
B. 加入氯化钡溶液,有白色沉淀产生,再加盐酸,沉淀不消失,一定有Ag+
C. 加入盐酸,无现象,再加氯化钡溶液,产生白色沉淀,一定有 SO2−
4
A. 上述仪器在配制过程中一定不需要的有两种 B. 仪器①使用前必须检查是否漏液并保持干燥
D. 加入碳酸钠溶液,产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+
C. 仪器④中测量的实际质量为31.6 g D. 定容时,如果不慎加多了液体,只能重新配制
8. 用N 代表阿伏加德罗常数的值,下列说法中正确的是( )
A
16. 下列反应的离子方程式书写错误的是( )
试卷第15页 共510页 ◎ 试卷第16页 共510页
学科网(北京)股份有限公司A. 氨水与稀硫酸反应:OH-+H+===H O B. Na CO 溶液与足量稀硝酸反应:CO +2H+===CO ↑+H O
2 2 3 2 2
C. NaCl溶液与AgNO 溶液反应:Cl-+Ag+===AgCl↓ D. 铝片与稀盐酸反应:2Al+6H+===2Al3++
3
3H ↑
2
17. 下列实验过程不能达到实验目的的是( )
A. 答案A B. 答案B C. 答案C D. 答案D
二、非选择題(本大題共5小题,共40分)
21. 氯气是一种重要的化工原料,在工农业生产生活中有着重要的应用。某化学兴趣小组同学利用以下装
置制备氯气并对氯气的性质进行探究。
A. 答案A B. 答案B C. 答案C D. 答案D
18. 在 2L KCl、AlCl 、Al(NO ) 的混合溶液中,
3 3 3
c K+ =0.2molL-1,c Cl- =0.4molL-1,n Al3+ =0.8mol NO
,计算分析判断,则 c( 3)为( )
A. 0.6 mol·L-1 B. 1.0 mol·L-1 C. 1.2 mol·L-1 D. 2.2 mol·L-1
19. 去除废水中含氮离子是目前水质改善的热点研究课题,常见的化学方法是用
NH+
将含氮离子还原为氮
4
(1)有关氯气、氯水和氯离子的性质,下列说法正确的是________(填字母)。
气或先用臭氧、双氧水、次氯酸钠等氧化 NO−,再用还原剂除去。去除废水中含有的 NO−、 NO−的一种原 A.氯水的颜色呈浅黄绿色,说明氯水中含有氯气
2 2 3
B.氯离子和氯气都具有很强的氧化性
理如下: NO−+H O =H O+NO−(Ⅰ), 6NO−+6H++5CH OH=3N ↑+5CO ↑+13H O(Ⅱ)。下列说法不正 C.新制氯水可以用来杀菌消毒,是因为生成强酸次氯酸
2 2 2 2 3 3 3 2 2 2
D.将新制氯水滴入硝酸银溶液,会出现白色沉淀
确的是( )
(2)仪器a的名称为________,装置B中饱和食盐水的作用是____________________________。
A. 氧化性由强至弱的顺序为 H O >NO− (3)装置A中发生反应的离子方程式为______________________________________。
2 2 3
(4)装置D中的实验现象为_____________________________________________________,
B. 用镁将水中的 NO−还原成 N 的离子方程式为 2NO−+5Mg+6H O=N +5Mg(OH) +2OH− 装置E中的实验现象为_________________________________________________。
3 2 3 2 2 2
(5)整套实验装置存在着明显缺陷,你的改进措施是________________________________。
C. 根据上述资料可知 ClO−与 NH+ 不共存,反应为 3ClO−+2NH+=N ↑+3H O+3Cl−+2H+ 22. 钠与硫酸亚铁溶液反应,很难完整地观察到反应全过程的有关现象。有人用如图装置进行实验改进:
4 4 2 2
先在试管内新制备的硫酸亚铁溶液上面覆盖一薄层汽油,然后将试管放入烧杯中,待试管内汽油层消失后,
D. 等物质的量 NO−分别与臭氧、双氧水、次氯酸钠完全反应转移电子数之比为3∶1∶1 往试管内投入一小粒钠并迅速塞上带导管的单孔塞。
2
20. 下列生活中的物质其有效成分与用途的对应关系正确的是( )
(1)实验中汽油的作用是______________________________________________________。
(2)加入钠后观察到液面上有大量气泡逸出,溶液中有________色沉淀生成。
(3)如果往试管中加入汽油后立即投入钠粒,可能发生爆炸,其原因是
试卷第25页 共510页 ◎ 试卷第26页 共510页
学科网(北京)股份有限公司________________________________________________________________________。 C→D:______________________________________________
(4)写出钠与FeSO 溶液反应的离子方程式:_______________________________________。
4
23. 如图所示为一“铁链”图案,某化学兴趣小组的同学在图案上分别写了H 、CO 、Na O、NaCl、FeCl
2 2 2 3
五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。
(1)将分类依据代号填入相应的括号内:
( )两种物质都不是电解质
( )两种物质都是钠的化合物
( )两种物质都是氧化物
( )两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,加热至沸腾,向烧杯中逐滴加入图中某物质的饱和溶液,继续煮沸可制得
一种红褐色胶体。
①该物质的化学式为________。
②证明有胶体生成的实验原理是_______________________________________。
③向该胶体中逐滴加入稀盐酸,会发生一系列变化:
a.先产生红褐色沉淀,原因是___________________________________________。
b.随后红褐色沉淀溶解,此时发生反应的离子方程式是______________________
___________________________________________________________。
24. 有一包白色固体粉末,其中可能含有NaCl、Ba(NO ) 、CuSO 、Na CO 中的一种或几种,现做以下实
3 2 4 2 3
验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,溶液呈无色;
②向①的沉淀中加入足量稀硝酸,固体完全溶解,并有气泡产生;
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生;
④另取①中过滤后的溶液加入足量AgNO 溶液,产生白色沉淀。
3
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是________________,一定不含有的物质是__________,可能含有的物质
是__________(均填化学式)。
(2)写出①、②中变化的离子方程式:
①________________________________________________________________________;
②________________________________________________________________________。
25. A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色固体,判断:
(1)写出化学式:E__________________、C__________________。
(2)E中阴、阳离子个数比为_____________________________;
(3)写出有关反应的化学方程式:
A→E:______________________________________________;
F→C:_______________________________________________;
试卷第35页 共510页 ◎ 试卷第36页 共510页
学科网(北京)股份有限公司【解析】A.铁与水蒸气在高温下生成Fe O 和H ,故A正确;
参考答案 3 4 2
B.氢氧化亚铁具有还原性,在空气中灼烧氧气将+2价Fe氧化+3价Fe,最终不能得到FeO,故B错误;
1. 【答案】B C.FeO是一种黑色粉末,不稳定,在空气里加热,最终被氧化成黑色的Fe O ,故C错误;
3 4
【解析】在水溶液里或熔融状态下自身能导电的化合物叫做电解质。①NaCl溶液是混合物,不是电解质; D.铁无论过量还是不足,与氯气在加热条件下反应,均生成FeCl ,故D错误。
3
②CH COOH溶于水可导电,是电解质;③NH 溶于水生成NH ·H O,生成的溶液可导电,但不是自身导 11. 【答案】A
3 3 3 2
电,是非电解质;④BaSO 在熔融状态下可电离出离子,可以导电,是电解质;⑤蔗糖溶于水不能电离出 【解析】A.由于钠比镁活泼,镁能与CO 反应,则钠也能与CO 反应,故 燃烧不能用CO 灭火,故Na
4 2 2 2
离子,溶液不导电,是非电解质;⑥H O可微弱地电离出H+和OH-,可导电,是电解质。 燃烧也不能用CO 灭火,A项正确;
2 2
2. 【答案】D B.Fe在O 中燃烧生成Fe O ,B项错误;
2 3 4
【解析】电解质是指在水溶液里或熔融状态下能够导电的化合物,且必须是自身发生电离产生能够自由移 C. 与 反应生成Na SO ,C项错误;
2 4
动的离子;能够导电的物质必须有能够自由移动的电子或者离子,如金属单质或少数非金属单质、溶于水 D.Al具有两性,能和NaOH溶液反应生成NaAlO 和H ,而Mg不具有两性,不能和NaOH溶液反应,D
2 2
或某些熔融状态下的电解质,据此分析解题。铜虽然能导电,但它是单质不是化合物,故既不是电解质也 项错误;
不是非电解质,A错误;稀硫酸能够导电,但其是混合物,故既不是电解质也不是非电解质,B错误; 12. 【答案】D
NaCl固体中没有能够自由移动的离子,故不能导电,C错误;熔融KCl中有自由移动的K+和Cl-,能导电,
【解析】密度为 1.2 g⋅cm−3 、质量分数为36.5%的浓盐酸的物质的量浓度为c=
且是化合物,属于电解质,D正确;故答案为D。
3. 【答案】C =12.0 mol/L,稀释前后溶质的物质的量不变,20 mL该浓盐酸可以稀释得到 6.0 mol⋅L−1 盐酸的体积为
【解析】H+和 CO2−反应放出CO 气体,不能大量共存,A错误;Mg2+和OH-反应生成Mg(OH) 沉淀, =40mL,故选D。
3 2 2
13. 【答案】D
不能大量共存,B错误;K+、Fe3+、 SO2−、 NO−间不会发生反应,可以大量共存,C正确;H+和OH-
4 3 【解析】配制500 mL 0.1 mol/L 的硫酸铜溶液,需要称取胆矾的质量为0.5 L×0.1 mol/L×250 g/mol=
反应生成H O,不能大量共存,D错误。 12.5 g,称取的质量偏少,浓度偏低,故A错误;配制NaOH溶液时,NaOH固体放在烧杯中称量时间过
2
4. 【答案】D 长,会吸收空气中的水蒸气和二氧化碳,导致氢氧化钠的质量偏少,浓度偏低,故B错误;定容时,仰视
【解析】据得失电子守恒可知,10I-~5I ,失10e-,2RO ~2R2+,得10e-,即R的化合价为+7价。 刻度线,导致溶液的体积偏大,浓度偏低,故C错误;配制NaOH溶液时,将称量好的NaOH固体放入小
2
5. 【答案】C 烧杯中溶解,未经冷却立即转移到容量瓶中并定容,导致溶液的正常温度下体积偏小,浓度偏高,故D正
【解析】 Cl 中氯元素的化合价既降低又升高,因此氯气既做氧化剂又做还原剂。 确。
2
6. 【答案】D 14. 【答案】C
【解析】Cl 溶于水生成HClO,HClO具有漂白性,能使紫色石蕊溶液变成无色,A不符合题意;新制氯水 【解析】向混合物中加入足量的盐酸,有气体放出。将气体通过足量的NaOH溶液,气体体积减少,说明
2
中含有HClO,HClO具有漂白性,能使紫色石蕊溶液变成无色,B不符合题意;Na O 具有漂白性,能使 生成的气体中有与氢氧化钠溶液不反应的气体,则原固体中一定含有过氧化钠,至少含有碳酸钠和碳酸氢
2 2
紫色石蕊溶液变成无色,C不符合题意;NaOH具有碱性,没有漂白性,能使紫色石蕊溶液变成蓝色,不 钠中的一种;氧化钠可与二氧化碳、水等反应,因此又将上述混合物在空气中加热,有气体放出且固体质
能使紫色石蕊溶液变成无色,D符合题意。 量增加,所以原固体中一定含有碳酸氢钠和氧化钠,因此原固体中一定含有过氧化钠、碳酸氢钠和氧化钠,
7. 【答案】C 碳酸钠和氯化钠是否存在不能确定。
8. 【答案】D 15. 【答案】D
18g 【解析】利用次氯酸钠固体配制一定浓度的84消毒液时需要用到带砝码的托盘天平、烧杯、玻璃棒、胶头
【解析】计算确定相关粒子的物质的量:水分子中所含氢原子的物质的量为 ×2=2 mol,氩
18g∙mol−1 滴管、容量瓶,不需要用到分液漏斗,故A错误;仪器①容量瓶使用前必须检查是否漏液,因定容时需要
加入蒸馏水,所以不需要保持干燥,故B错误;烧杯与砝码放反,测量的实际质量为28.4 g,故C错误;
气所含原子的物质的量为1 mol×1=1 mol,2H +O 2H O、2CO+O 2CO ,H 、CO不 定容时,如果不慎加多了液体说明配制实验失败,只能重新配制,故D正确。
2 2 2 2 2 2
16. 【答案】A
管怎样混合,参加反应的O 体积是混合气体体积的一半,为4.48 L,则O 物质的量是0.2 mol,分子 【解析】一水合氨是弱碱不能拆写,氨水与稀硫酸反应:NH ·H O+H+===H O+NH ,A错误。
2 2 3 2 2
数为0.2N ,硝酸所含氧原子的物质的量为0.5 mol×3=1.5 mol。 17. 【答案】D
A
9. 【答案】A 【解析】NaHCO 与Na CO 溶液均能与澄清石灰水反应生成白色碳酸钙沉淀,D错误。
3 2 3
【解析】Mg2+和Al3+均与OH-反应不共存,B错误;Ag+和Cl-生成沉淀不共存,C错误;Ca2+和CO 生 18. 【答案】B
成沉淀不共存,D错误。
10. 【答案】A
试卷第45页 共510页 ◎ 试卷第46页 共510页
学科网(北京)股份有限公司c
Al3+
=
0.8
mol/L=0.4mol/L
色。
【解析】混合溶液中, 2 ,根据溶液呈电中性可知, (5)由于氯气是大气污染物,需要进行尾气处理,因此整套实验装置存在着明显缺陷,改进措施是在装置E
后加一装有氢氧化钠溶液的尾气处理装置。
c K+ +3c Al3+ =c Cl- +c NO- 22. 【答案】(1)加热时汽油挥发,驱赶试管中的空气
3 ,可得
(2)白
c NO- =c K+ +3c Al3+ -c Cl- =0.2+30.40.4mol/L=1.0mol/L (3)反应放热,使汽油、H 与空气中的O 的混合气体发生爆炸
2 2
3 ,B正确。
(4) 2Na+2H O===2Na++2OH-+H ↑、Fe2++2OH-===Fe(OH) ↓
2 2 2
19. 【答案】D 【解析】(1)汽油的作用是易挥发,把试管内空气赶净,起到保护气的作用,隔离硫酸亚铁溶液和空气,避
免被空气中氧气氧化;
【解析】根据反应方程式: NO−+H O =H O+NO−,可知该反应的氧化剂为 H O ,氧化产物为 NO−,
2 2 2 2 3 2 2 3 (2)钠与水反应生成氢氧化钠和氢气,氢氧化钠和硫酸亚铁反应生成氢氧化亚铁白色沉淀;
(3)钠和水反应放热,生成的氢气和汽油、空气混合易燃烧发生爆炸;
所以氧化性由强至弱的顺序为: H O >NO−,A正确;镁将水中的 NO−还原成 N ,镁作还原剂被氧
2 2 3 3 2 (4)反应的离子方程式是钠先与水反应,所得产物再与盐溶液反应,综合分析写出离子方程式为2Na+
2H O===2Na++2OH-+H ↑、Fe2++2OH-===Fe(OH) ↓
化成镁离子, NO−作氧化剂被还原成 N ,由原子守恒可知反应中生成氢氧根,所以镁元素的存在形式应 2 2 2
3 2 23. 【答案】(1)A C B D
(2)①FeCl ②丁达尔效应 ③a.Fe(OH) 胶体发生聚沉产生Fe(OH) 沉淀
为氢氧化镁,所以离子方程式为: 2NO−+5Mg+6H O=N +5Mg(OH) +2OH−,B正确; ClO−具有氧化性, 3 3 3
3 2 2 2 b.Fe(OH) +3H+===Fe3++3H O
3 2
【解析】(1)H 和CO 都不是电解质,CO 和Na O都是氧化物,Na O和NaCl都是钠的化合物,NaCl和
NH+ 具有还原性,二者发生氧化还原反应,离子方程式为: 3ClO−+2NH+=N ↑+3H O+3Cl−+2H+ ,C正 2 2 2 2 2
4 4 2 2 FeCl 都是盐。(2)将饱和FeCl 溶液加入煮沸的蒸馏水中,继续煮沸至液体呈红褐色可制得Fe(OH) 胶体。
3 3 3
证明有胶体生成的实验原理是丁达尔效应。胶体遇可溶性电解质会发生聚沉。
确; NO−与臭氧、双氧水、次氯酸钠完全反应均被氧化成 N ,所以等物质的量 NO−分别与臭氧、双氧
2 2 2 24. 【答案】(1)Ba(NO ) 、Na CO CuSO NaCl
3 2 2 3 4
水、次氯酸钠完全反应转移电子数之比为1∶1∶1,D错误。
(2)①Ba2++ CO2−===BaCO ↓ ②BaCO +2H+===Ba2++CO ↑+H O
20. 【答案】A 3 3 3 2 2
【解析】“84”消毒液的有效成分为NaClO,具有强氧化性,可用于杀菌消毒,做漂白剂,A正确;铁红是 25. 【答案】(1)Na O Na CO
2 2 2 3
Fe O 的俗称,B错误;纯碱为 Na CO 的俗称,C错误; Al(OH) 可中和胃酸,是抗酸药物,不是感冒药, (2)1∶2
2 3 2 3 3
D错误。 (3)2Na+O Na O 2NaHCO Na CO +H O+CO ↑ Na CO +2HCl===2NaCl+H O+CO ↑
2 2 2 3 2 3 2 2 2 3 2 2
21. 【答案】(1)AD 【解析】(1)由分析可知,A为Na、B为NaOH、C为Na CO 、D为NaCl、E为Na O 、F为NaHCO 。
2 3 2 2 3
(2)圆底烧瓶 除去氯气中的氯化氢气体
(2)E为Na O ,Na O 中阴离子为 O2−,阳离子为 Na+离子,阴阳离子的个数之比为1∶2。
2 2 2 2 2
(3)MnO +4H++2Cl- Mn2++Cl ↑+2H O
2 2 2
(3)A→E是钠的燃烧反应,反应的化学方程式为2Na+O Na O ;F→C是碳酸氢钠受热分解生成碳酸
2 2 2
(4)红色布条不褪色 红色布条褪色 钠、二氧化碳和水,反应的化学方程式为2NaHCO Na CO +H O+CO ↑;C→D是碳酸钠与盐酸的
3 2 3 2 2
(5)在装置E后加一装有氢氧化钠溶液的尾气处理装置 反应,反应的化学方程式为Na CO +2HCl===2NaCl+H O+CO ↑。
2 3 2 2
【解析】(1)氯气是黄绿色气体,氯水的颜色呈浅黄绿色,说明氯水中含有氯气,A正确;氯离子中氯元素
的化合价是-1价,处于最低价态,只有还原性;氯气具有很强的氧化性,B错误;新制氯水可以用来杀菌
消毒是因为生成次氯酸,次氯酸是弱酸,C错误;新制氯水中含有氯离子,将新制氯水滴入AgNO 溶液中
3
生成氯化银,因此会出现白色沉淀,D正确。(2)根据仪器的构造可知,仪器a的名称为圆底烧瓶;浓盐酸
易挥发,生成的氯气中含有氯化氢,氯化氢极易溶于水,因此装置B中饱和食盐水的作用是除去氯气中的
氯化氢气体。
(3)实验室利用浓盐酸和二氧化锰在加热的条件下反应制备氯气,则装置A中发生反应的离子方程式为
MnO +4H++2Cl- Mn2++Cl ↑+2H O。
2 2 2
(4)生成的氯气经过饱和食盐水除去氯化氢,经过浓硫酸干燥氯气,干燥的氯气没有漂白性,氯气和水反应
生成的次氯酸具有漂白性,则装置D中的实验现象为红色布条不褪色,装置E中的实验现象为红色布条褪
试卷第55页 共510页 ◎ 试卷第56页 共510页
学科网(北京)股份有限公司