文档内容
高一化学下学期期中专项复习
综合检测卷 03
一.选择题(每小题3分,共48分,每题只有一个正确选项)
1.下列关于无机非金属材料的说法中,不正确的是
A.高纯硅可用于制造半导体材料
B.氧化铝陶瓷属于新型无机非金属材料,它是生物陶瓷
C.氮化硅陶瓷属于新型无机非金属材料,可用于制造陶瓷发动机的受热面
D.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
2.化学在生产和日常生活中有着重要的应用。下列说法正确是
A.普通玻璃的主要成分是二氧化硅
B.向煤中加入适量石灰石,使煤燃烧产生的SO 最终生成CaSO,可减少对大气的污染
2 3
C.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N 和CO
2 2
D.大量燃烧化石燃料排放的废气中含CO、SO , 从而使雨水的pH=5.6形成酸雨
2 2
3.下列对浓硫酸的叙述正确的是
A.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
B.浓硫酸具有强氧化性,SO 、H、具有还原性,故浓硫酸不能干燥SO 、H
2 2 2 2
C.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
D.浓硫酸与亚硫酸钠反应制取SO 时,浓硫酸表现出强氧化性
2
4.下列叙述不正确的是
A.NH 易液化,液氨常用作制冷剂
3
B.稀 HNO 和活泼金属反应时主要得到氢气
3
C.铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处
D.利用氨气极易溶于水,氨气可以做喷泉实验
5.对溶液中的离子进行鉴定,下列实验所得结论不合理的是
A.向溶液中加入盐酸,产生使澄清石灰水变浑浊的无色气体,则溶液中可能含有
B.向溶液中加入稀硝酸后,再加入 溶液有白色沉淀生成,则溶液中一定含有
C.加入 溶液有白色沉淀产生,再加盐酸,沉淀不溶解,原溶液中一定含有
D.向溶液中加入 溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推该溶液中一定含有
6.下列离子方程式正确的是
A.实验室用氯化铵和熟石灰制氨: +OH- NH ↑+HO
3 2B.向氨水中加盐酸:NH ·H O+H+= +HO
3 2 2
C.铜与稀硝酸反应:3Cu+8H++2 =3Cu2++2NO↑+4H O
2 2
D.将SO 通入到BaCl 溶液中:SO +HO+Ba2+=BaSO ↓+2H+
2 2 2 2 3
7.反应3A(g)+B(g)═2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质
表示为:①v ═1mol/(L•min) ,②v ═0.5 mol/(L•min), ③v ═0.5 mol/(L•min),三种情况下该反应速率大
A C B
小的关系正确的是( )
A.②>③>① B.①>②>③ C.③>①>② D.②>①>③
8.有M、N、P、E四种金属,已知:①M+N2+=N+M2+;②M、P用导线连接后放入硫酸氢钠溶液中,M
表面有大量气泡产生;③N、E用导线连接后放入E的硫酸盐溶液中,电极反应为E2++2e-=E、N-2e-=N2+。
则四种金属的还原性由强到弱的顺序是
A.P、M、N、E B.E、N、M、P C.P、N、M、E D.E、P、M、N
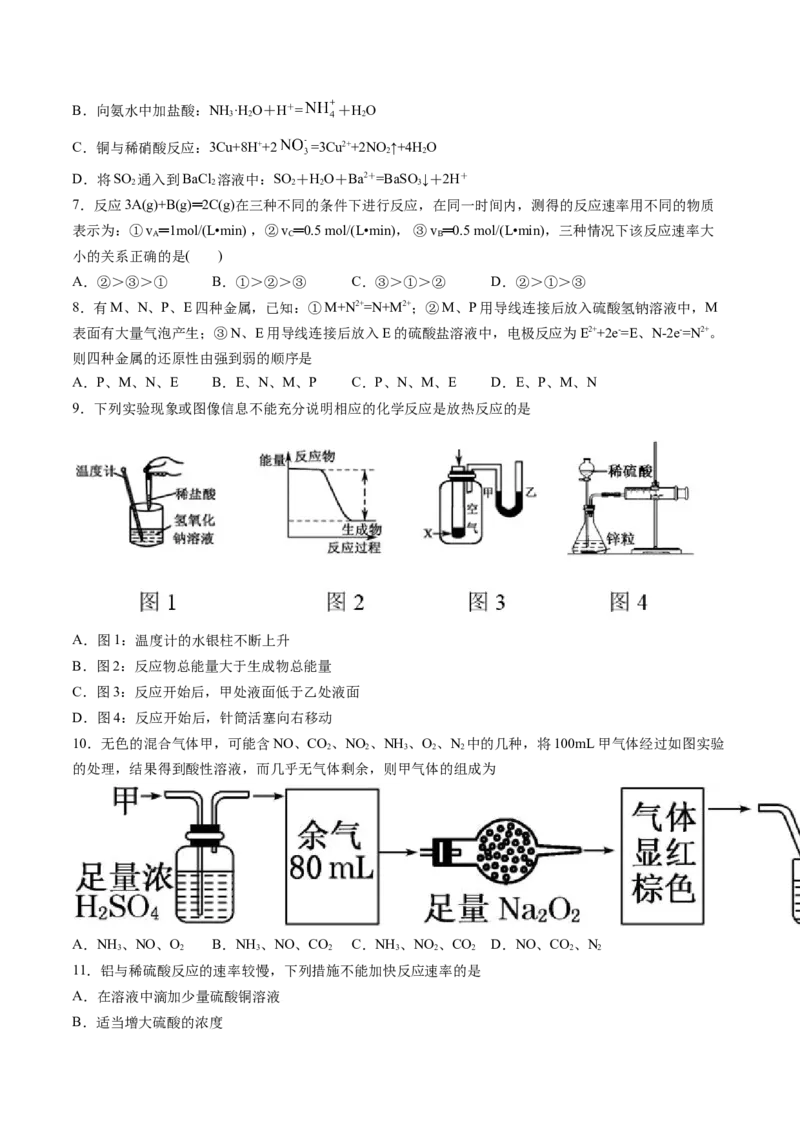
9.下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是
A.图1:温度计的水银柱不断上升
B.图2:反应物总能量大于生成物总能量
C.图3:反应开始后,甲处液面低于乙处液面
D.图4:反应开始后,针筒活塞向右移动
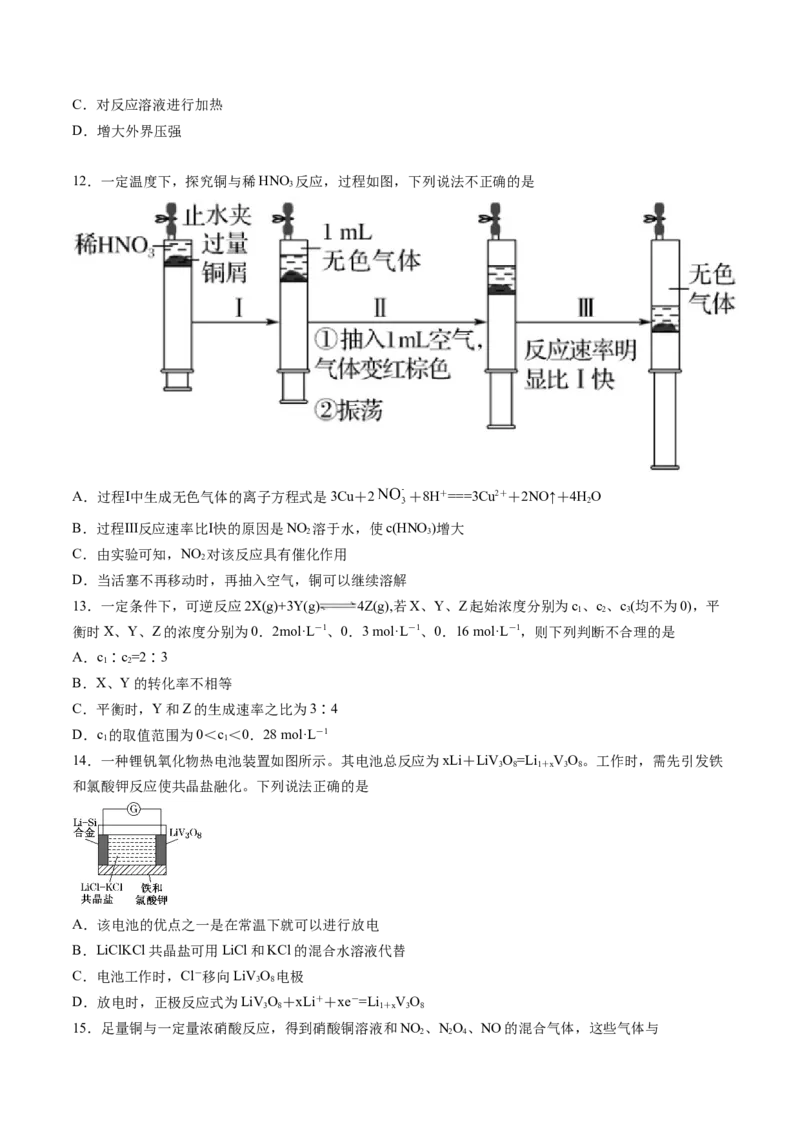
10.无色的混合气体甲,可能含NO、CO、NO 、NH 、O、N 中的几种,将100mL甲气体经过如图实验
2 2 3 2 2
的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为
A.NH 、NO、O B.NH 、NO、CO C.NH 、NO 、CO D.NO、CO、N
3 2 3 2 3 2 2 2 2
11.铝与稀硫酸反应的速率较慢,下列措施不能加快反应速率的是
A.在溶液中滴加少量硫酸铜溶液
B.适当增大硫酸的浓度C.对反应溶液进行加热
D.增大外界压强
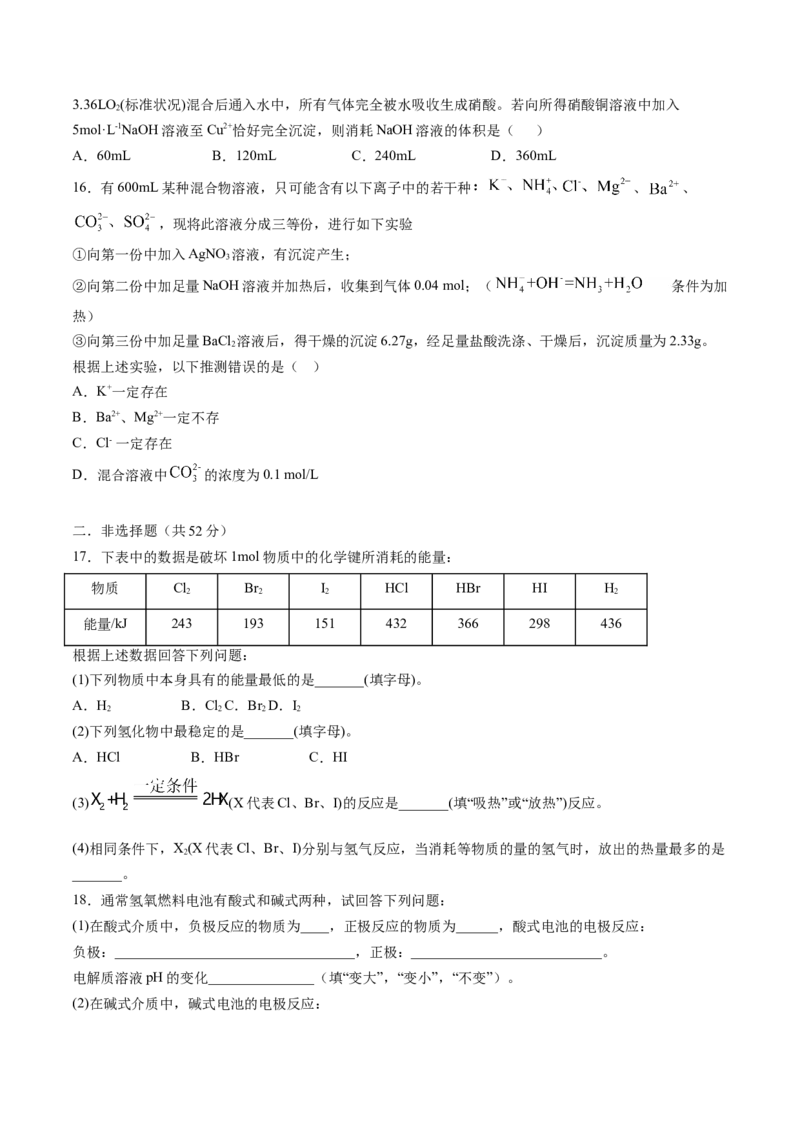
12.一定温度下,探究铜与稀HNO 反应,过程如图,下列说法不正确的是
3
A.过程Ⅰ中生成无色气体的离子方程式是3Cu+2 +8H+===3Cu2++2NO↑+4HO
2
B.过程Ⅲ反应速率比Ⅰ快的原因是NO 溶于水,使c(HNO )增大
2 3
C.由实验可知,NO 对该反应具有催化作用
2
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
13.一定条件下,可逆反应2X(g)+3Y(g) 4Z(g),若X、Y、Z起始浓度分别为c、c、c(均不为0),平
1 2 3
衡时X、Y、Z的浓度分别为0.2mol·L-1、0.3 mol·L-1、0.16 mol·L-1,则下列判断不合理的是
A.c∶c=2∶3
1 2
B.X、Y的转化率不相等
C.平衡时,Y和Z的生成速率之比为3∶4
D.c 的取值范围为0<c<0.28 mol·L-1
1 1
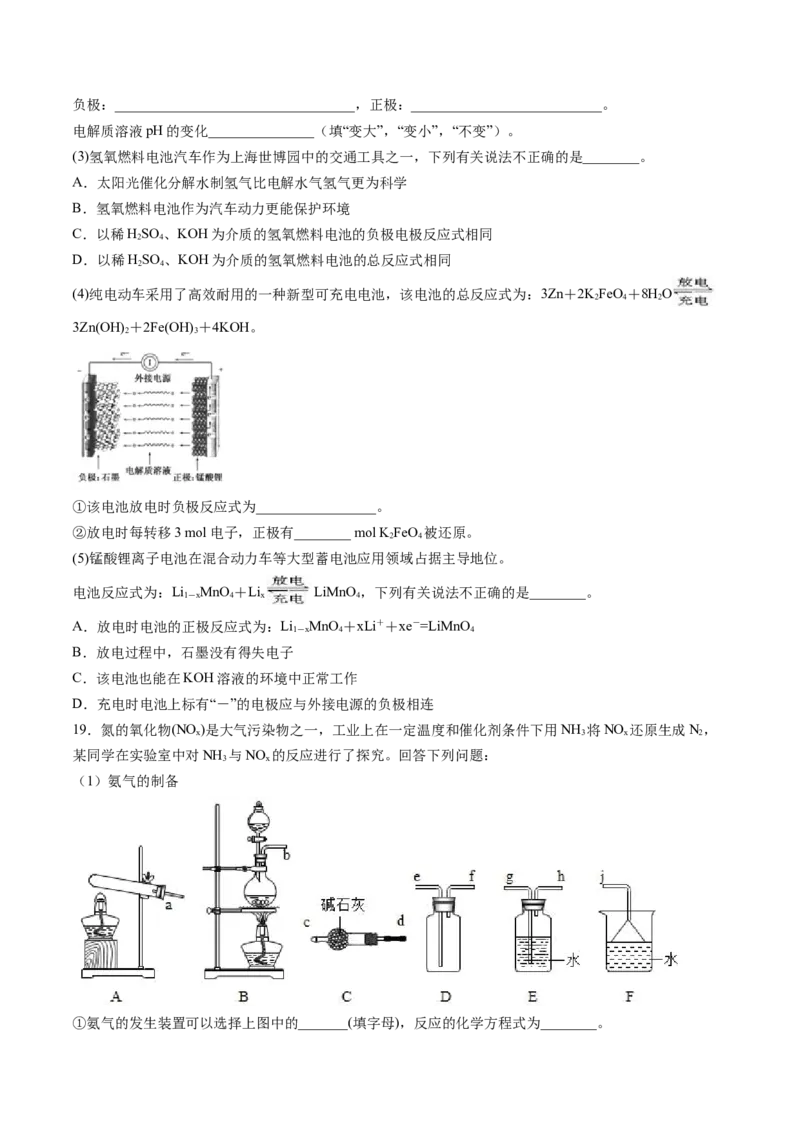
14.一种锂钒氧化物热电池装置如图所示。其电池总反应为xLi+LiV O=Li VO。工作时,需先引发铁
3 8 1+x 3 8
和氯酸钾反应使共晶盐融化。下列说法正确的是
A.该电池的优点之一是在常温下就可以进行放电
B.LiClKCl共晶盐可用LiCl和KCl的混合水溶液代替
C.电池工作时,Cl-移向LiV O 电极
3 8
D.放电时,正极反应式为LiV O+xLi++xe-=Li VO
3 8 1+x 3 8
15.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO 、NO、NO的混合气体,这些气体与
2 2 43.36LO (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入
2
5mol·L-1NaOH溶液至 Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60mL B.120mL C.240mL D.360mL
16.有600mL某种混合物溶液,只可能含有以下离子中的若干种 、 、
,现将此溶液分成三等份,进行如下实验
①向第一份中加入AgNO 溶液,有沉淀产生;
3
②向第二份中加足量NaOH溶液并加热后,收集到气体0.04 mol;( 条件为加
热)
③向第三份中加足量BaCl 溶液后,得干燥的沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
2
根据上述实验,以下推测错误的是( )
A.K+一定存在
B.Ba2+、Mg2+一定不存
C.Cl- 一定存在
D.混合溶液中 的浓度为0.1 mol/L
二.非选择题(共52分)
17.下表中的数据是破坏1mol物质中的化学键所消耗的能量:
物质 Cl Br I HCl HBr HI H
2 2 2 2
能量/kJ 243 193 151 432 366 298 436
根据上述数据回答下列问题:
(1)下列物质中本身具有的能量最低的是_______(填字母)。
A.H B.Cl C.Br D.I
2 2 2 2
(2)下列氢化物中最稳定的是_______(填字母)。
A.HCl B.HBr C.HI
(3) (X代表Cl、Br、I)的反应是_______(填“吸热”或“放热”)反应。
(4)相同条件下,X(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出的热量最多的是
2
_______。
18.通常氢氧燃料电池有酸式和碱式两种,试回答下列问题:
(1)在酸式介质中,负极反应的物质为____,正极反应的物质为______,酸式电池的电极反应:
负极:__________________________________,正极:___________________________。
电解质溶液pH的变化_______________(填“变大”,“变小”,“不变”)。
(2)在碱式介质中,碱式电池的电极反应:负极:__________________________________,正极:___________________________。
电解质溶液pH的变化_______________(填“变大”,“变小”,“不变”)。
(3)氢氧燃料电池汽车作为上海世博园中的交通工具之一,下列有关说法不正确的是________。
A.太阳光催化分解水制氢气比电解水气氢气更为科学
B.氢氧燃料电池作为汽车动力更能保护环境
C.以稀HSO 、KOH为介质的氢氧燃料电池的负极电极反应式相同
2 4
D.以稀HSO 、KOH为介质的氢氧燃料电池的总反应式相同
2 4
(4)纯电动车采用了高效耐用的一种新型可充电电池,该电池的总反应式为:3Zn+2KFeO+8HO
2 4 2
3Zn(OH) +2Fe(OH) +4KOH。
2 3
①该电池放电时负极反应式为_________________。
②放电时每转移3 mol电子,正极有________ mol K FeO 被还原。
2 4
(5)锰酸锂离子电池在混合动力车等大型蓄电池应用领域占据主导地位。
电池反应式为:Li MnO +Li LiMnO ,下列有关说法不正确的是________。
1-x 4 x 4
A.放电时电池的正极反应式为:Li MnO +xLi++xe-=LiMnO
1-x 4 4
B.放电过程中,石墨没有得失电子
C.该电池也能在KOH溶液的环境中正常工作
D.充电时电池上标有“-”的电极应与外接电源的负极相连
19.氮的氧化物(NO )是大气污染物之一,工业上在一定温度和催化剂条件下用NH 将NO 还原生成N,
x 3 x 2
某同学在实验室中对NH 与NO 的反应进行了探究。回答下列问题:
3 x
(1)氨气的制备
①氨气的发生装置可以选择上图中的_______(填字母),反应的化学方程式为________。②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序:发生装置→_________(按气流方向,用小写
字母表示)。
(2)二氧化氮的制备
二氧化氮可以用铜和浓硝酸制备,反应的化学方程式为_________。
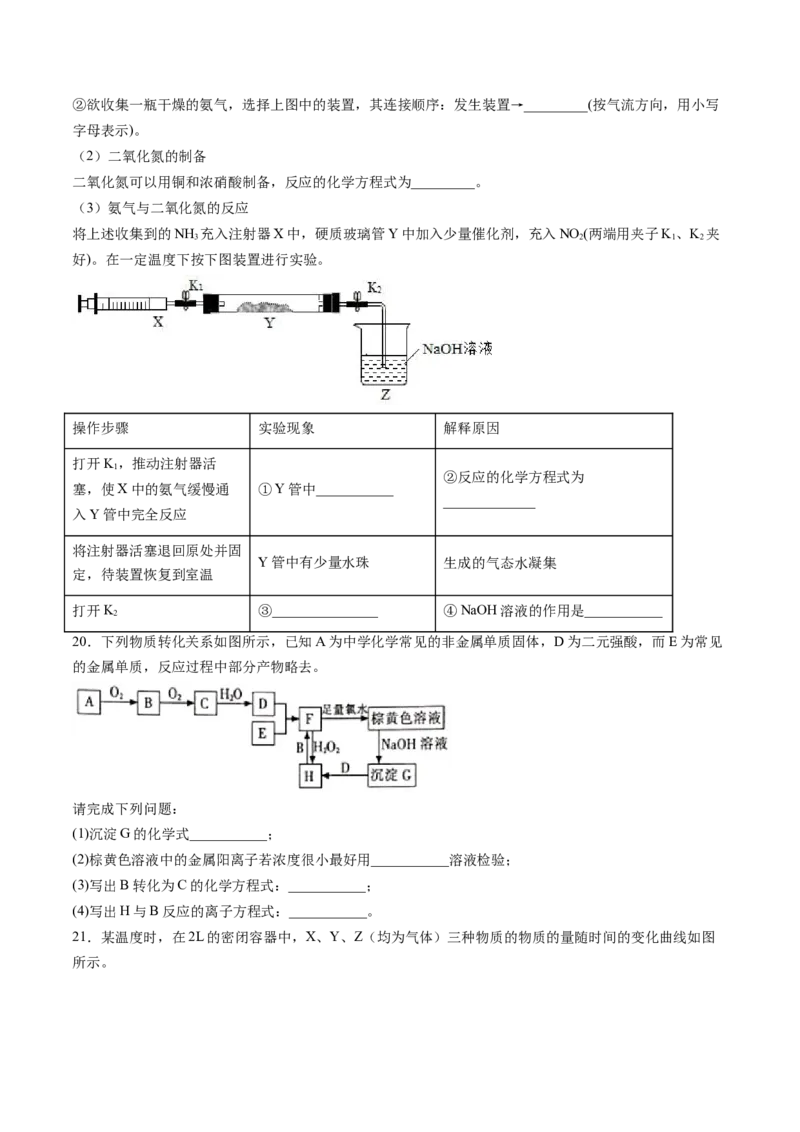
(3)氨气与二氧化氮的反应
将上述收集到的NH 充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO (两端用夹子K、K 夹
3 2 1 2
好)。在一定温度下按下图装置进行实验。
操作步骤 实验现象 解释原因
打开K,推动注射器活
1
②反应的化学方程式为
塞,使X中的氨气缓慢通 ①Y管中___________
_____________
入Y管中完全反应
将注射器活塞退回原处并固
Y管中有少量水珠 生成的气态水凝集
定,待装置恢复到室温
打开K ③_______________ ④NaOH溶液的作用是___________
2
20.下列物质转化关系如图所示,已知A为中学化学常见的非金属单质固体,D为二元强酸,而E为常见
的金属单质,反应过程中部分产物略去。
请完成下列问题:
(1)沉淀G的化学式___________;
(2)棕黄色溶液中的金属阳离子若浓度很小最好用___________溶液检验;
(3)写出B转化为C的化学方程式:___________;
(4)写出H与B反应的离子方程式:___________。
21.某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的物质的量随时间的变化曲线如图
所示。(1)由图中所给数据进行分析,该反应的化学方程式为___。
(2)反应从开始至2分钟,用X的浓度变化表示的平均反应速率为v(X)=___。
(3)2min反应达到平衡,容器内混合气体的平均相对分子质量比起始时___(填“增大”、“减小”或“无变
化”,下同);混合气体的密度比起始时___
(4)下列措施能加快反应速率的是___。
A.升高温度
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.选择高效的催化剂
(5)下列说法正确的是___。
A.化学反应的限度是不可能改变的
B.化学反应的限度与时间长短无关
C.升高温度改变化学反应的限度
D.增大Y的浓度,正反应速率加快,逆反应速率减慢
E.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢