文档内容
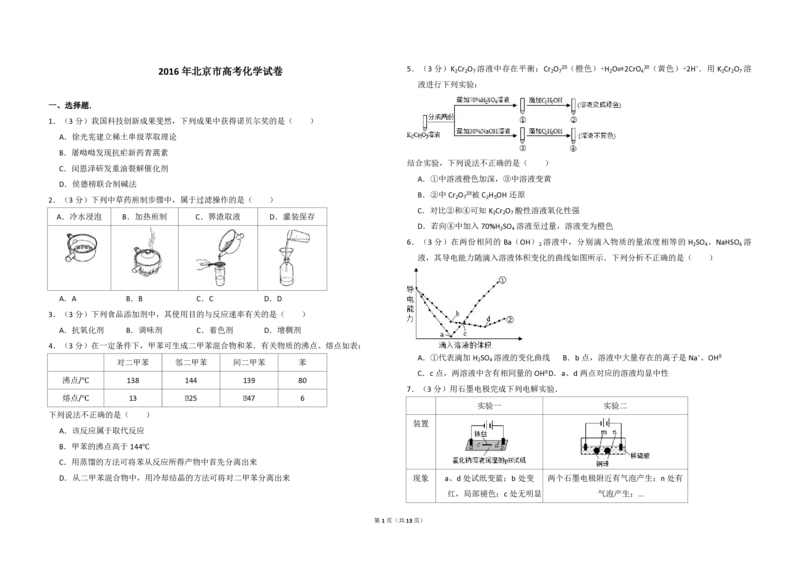
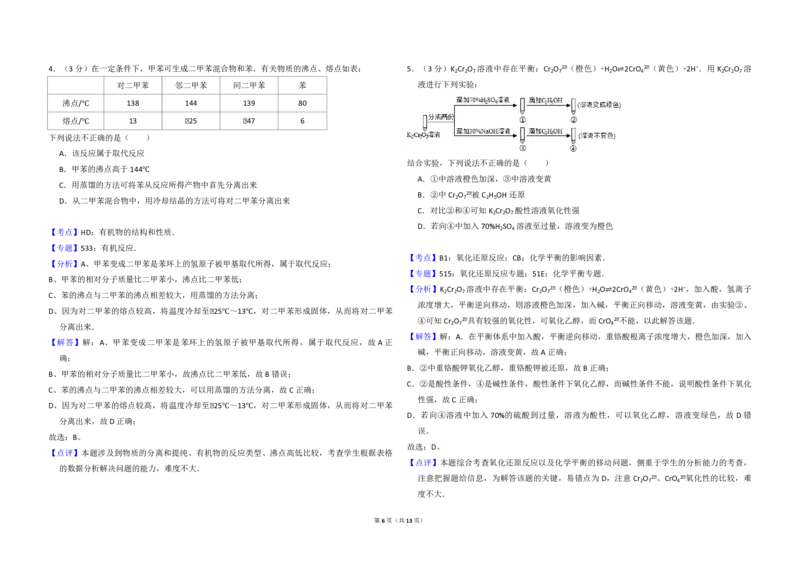
2016 年北京市高考化学试卷 5.(3分)K 2 Cr 2 O 7 溶液中存在平衡:Cr 2 O 7 2﹣(橙色)+H 2 O⇌2CrO 4 2﹣(黄色)+2H+.用 K 2 Cr 2 O 7 溶
液进行下列实验:
一、选择题.
1.(3分)我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
结合实验,下列说法不正确的是( )
C.闵恩泽研发重油裂解催化剂
A.①中溶液橙色加深,③中溶液变黄
D.侯德榜联合制碱法
B.②中 Cr O 2﹣被C H OH 还原
2.(3分)下列中草药煎制步骤中,属于过滤操作的是( ) 2 7 2 5
C.对比②和④可知 K Cr O 酸性溶液氧化性强
2 2 7
A.冷水浸泡 B.加热煎制 C.箅渣取液 D.灌装保存
D.若向④中加入 70%H SO 溶液至过量,溶液变为橙色
2 4
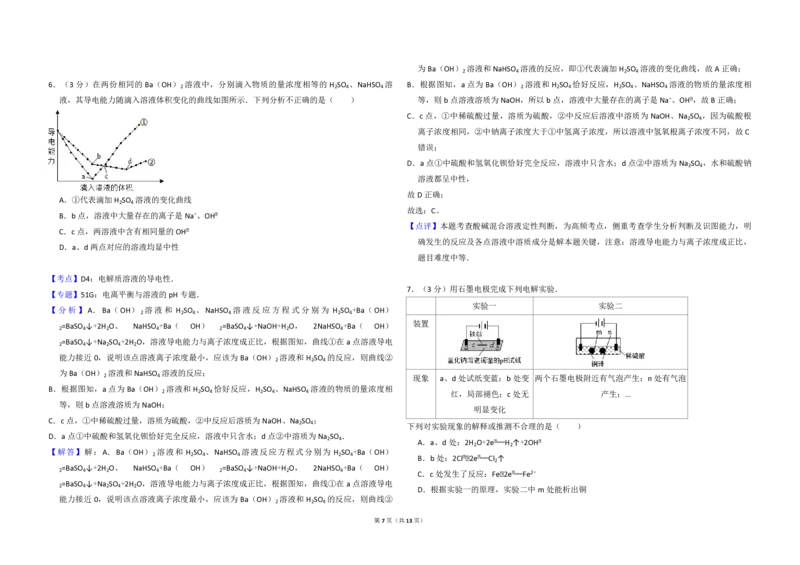
6.(3分)在两份相同的 Ba(OH) 溶液中,分别滴入物质的量浓度相等的 H SO 、NaHSO 溶
2 2 4 4
液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )
A.A B.B C.C D.D
3.(3分)下列食品添加剂中,其使用目的与反应速率有关的是( )
A.抗氧化剂 B.调味剂 C.着色剂 D.增稠剂
4.(3分)在一定条件下,甲苯可生成二甲苯混合物和苯.有关物质的沸点、熔点如表:
A.①代表滴加 H SO 溶液的变化曲线 B.b 点,溶液中大量存在的离子是Na+、OH﹣
对二甲苯 邻二甲苯 间二甲苯 苯 2 4
C.c点,两溶液中含有相同量的OH﹣ D.a、d 两点对应的溶液均显中性
沸点/℃ 138 144 139 80
7.(3分)用石墨电极完成下列电解实验.
熔点/℃ 13 ﹣25 ﹣47 6
实验一 实验二
下列说法不正确的是( )
装置
A.该反应属于取代反应
B.甲苯的沸点高于 144℃
C.用蒸馏的方法可将苯从反应所得产物中首先分离出来
D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来 现象 a、d 处试纸变蓝;b 处变 两个石墨电极附近有气泡产生;n 处有
红,局部褪色;c处无明显 气泡产生;…
第1页(共13页)变化
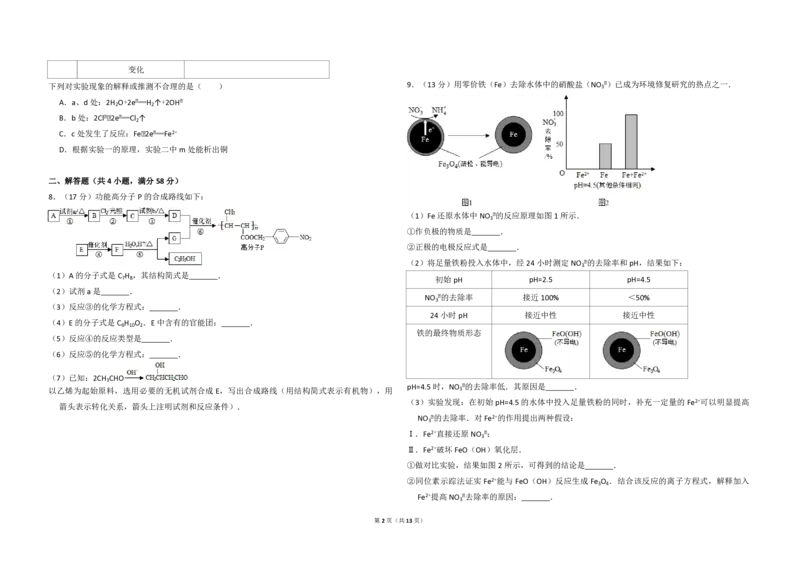
下列对实验现象的解释或推测不合理的是( ) 9.(13分)用零价铁(Fe)去除水体中的硝酸盐(NO
3
﹣)已成为环境修复研究的热点之一.
A.a、d 处:2H O+2e﹣═H ↑+2OH﹣
2 2
B.b 处:2Cl﹣﹣2e﹣═Cl ↑
2
C.c处发生了反应:Fe﹣2e﹣═Fe2+
D.根据实验一的原理,实验二中m处能析出铜
二、解答题(共 4小题,满分 58分)
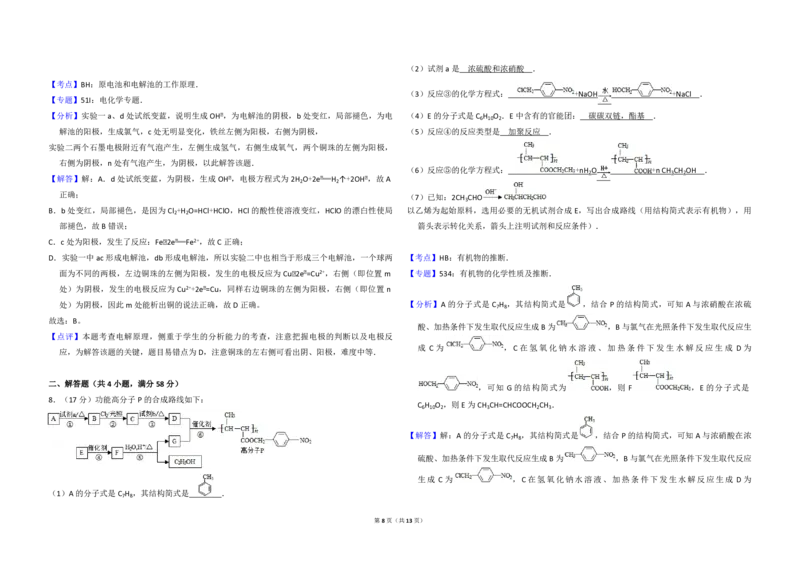
8.(17分)功能高分子 P的合成路线如下:
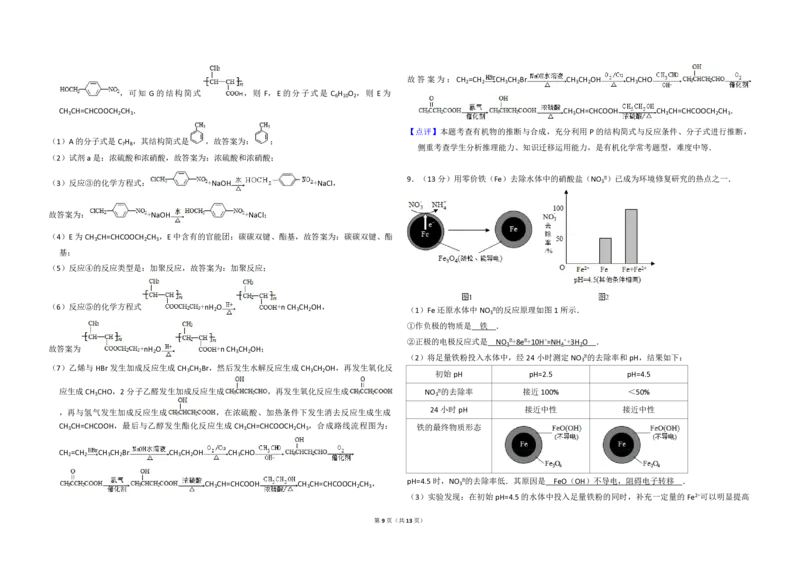
(1)Fe 还原水体中NO ﹣的反应原理如图1所示.
3
①作负极的物质是 .
②正极的电极反应式是 .
(2)将足量铁粉投入水体中,经24小时测定NO ﹣的去除率和pH,结果如下:
3
(1)A的分子式是C H ,其结构简式是 .
7 8 初始pH pH=2.5 pH=4.5
(2)试剂a 是 .
NO ﹣的去除率 接近100% <50%
3
(3)反应③的化学方程式: .
24小时pH 接近中性 接近中性
(4)E 的分子式是C H O .E 中含有的官能团: .
6 10 2
铁的最终物质形态
(5)反应④的反应类型是 .
(6)反应⑤的化学方程式: .
(7)已知:2CH CHO
3
pH=4.5时,NO ﹣的去除率低.其原因是 .
以乙烯为起始原料,选用必要的无机试剂合成 E,写出合成路线(用结构简式表示有机物),用 3
(3)实验发现:在初始 pH=4.5的水体中投入足量铁粉的同时,补充一定量的 Fe2+可以明显提高
箭头表示转化关系,箭头上注明试剂和反应条件).
NO ﹣的去除率.对Fe2+的作用提出两种假设:
3
Ⅰ.Fe2+直接还原NO ﹣;
3
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是 .
②同位素示踪法证实 Fe2+能与 FeO(OH)反应生成 Fe O .结合该反应的离子方程式,解释加入
3 4
Fe2+提高NO ﹣去除率的原因: .
3
第2页(共13页)(4)其他条件与(2)相同,经1小时测定NO ﹣的去除率和pH,结果如表: ②过程Ⅲ的目的是提纯,结合上述溶解度曲线,简述过程Ⅲ的操作:
3
初始pH pH=2.5 pH=4.5
NO ﹣的去除率 约10% 约3%
3
1小时pH 接近中性 接近中性
与(2)中数据对比,解释(2)中初始 pH 不同时,NO ﹣去除率和铁的最终物质形态不同的原
3
因: .
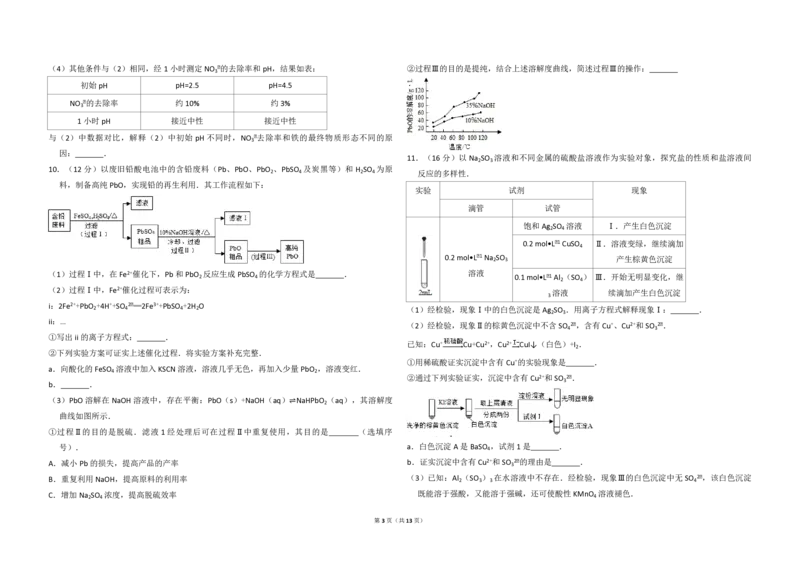
11.(16分)以 Na SO 溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间
2 3
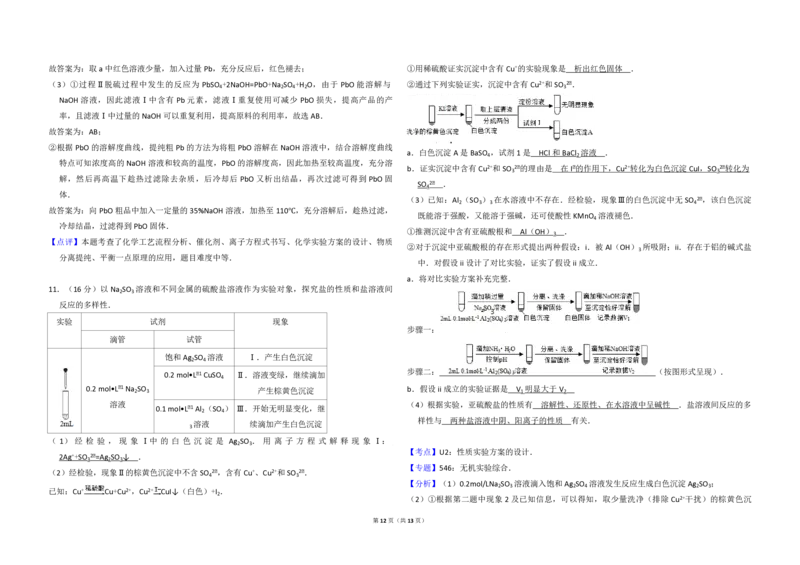
10.(12分)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO 、PbSO 及炭黑等)和 H SO 为原
2 4 2 4 反应的多样性.
料,制备高纯PbO,实现铅的再生利用.其工作流程如下:
实验 试剂 现象
滴管 试管
饱和Ag SO 溶液 Ⅰ.产生白色沉淀
2 4
0.2 mol•L﹣1 CuSO Ⅱ.溶液变绿,继续滴加
4
0.2 mol•L﹣1 Na 2 SO 3 产生棕黄色沉淀
(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO
2
反应生成PbSO
4
的化学方程式是 . 溶液
0.1 mol•L﹣1 Al (SO ) Ⅲ.开始无明显变化,继
2 4
(2)过程Ⅰ中,Fe2+催化过程可表示为:
溶液 续滴加产生白色沉淀
3
i:2Fe2++PbO +4H++SO 2﹣═2Fe3++PbSO +2H O
2 4 4 2 (1)经检验,现象Ⅰ中的白色沉淀是Ag SO .用离子方程式解释现象Ⅰ: .
2 3
ii:…
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO 2﹣,含有Cu+、Cu2+和SO 2﹣.
4 3
①写出ii 的离子方程式: .
已知:Cu+ Cu+Cu2+,Cu2+ CuI↓(白色)+I .
2
②下列实验方案可证实上述催化过程.将实验方案补充完整.
①用稀硫酸证实沉淀中含有Cu+的实验现象是 .
a.向酸化的 FeSO 溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO ,溶液变红.
4 2
②通过下列实验证实,沉淀中含有Cu2+和SO 2﹣.
3
b. .
(3)PbO 溶解在 NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)⇌NaHPbO (aq),其溶解度
2
曲线如图所示.
①过程Ⅱ的目的是脱硫.滤液 1经处理后可在过程Ⅱ中重复使用,其目的是 (选填序
号). a.白色沉淀 A是BaSO
4
,试剂1是 .
A.减小 Pb的损失,提高产品的产率 b.证实沉淀中含有 Cu2+和 SO
3
2﹣的理由是 .
B.重复利用 NaOH,提高原料的利用率 (3)已知:Al
2
(SO
3
)
3
在水溶液中不存在.经检验,现象Ⅲ的白色沉淀中无 SO
4
2﹣,该白色沉淀
C.增加Na 2 SO 4 浓度,提高脱硫效率 既能溶于强酸,又能溶于强碱,还可使酸性 KMnO 4 溶液褪色.
第3页(共13页)①推测沉淀中含有亚硫酸根和 .
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.被 Al(OH) 所吸附;ii.存在于铝的碱式盐
3
中.对假设ii 设计了对比实验,证实了假设ii 成立.
a.将对比实验方案补充完整.
步骤一:
步骤二: (按图形式呈现).
b.假设 ii 成立的实验证据是
(4)根据实验,亚硫酸盐的性质有 .盐溶液间反应的多样性与 有关.
第4页(共13页)【专题】545:物质的分离提纯和鉴别.
2016 年北京市高考化学试卷 【分析】过滤用于分离不溶性物质和液体的分离,一般利用固体的颗粒大小将固体和液体分离,
以此解答该题.
参考答案与试题解析
【解答】解:A.冷水浸泡属于物质的溶解,故A错误;
B.加热煎制属于加热,故B错误;
一、选择题.
C.箅渣取液将固体和液体分离,属于过滤操作,故 C 正确;
1.(3分)我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
D.灌装是液体转移,故D 错误。
A.徐光宪建立稀土串级萃取理论
故选:C。
B.屠呦呦发现抗疟新药青蒿素
【点评】本题考查物质的分离,侧重于学生的分析、实验能力的考查,题目密切联系生活,有利
C.闵恩泽研发重油裂解催化剂
于培养学生良好的科学素养,提高学生学习的积极性,难度不大.
D.侯德榜联合制碱法
3.(3分)下列食品添加剂中,其使用目的与反应速率有关的是( )
【考点】1A:化学史.
菁优网版权所有
A.抗氧化剂 B.调味剂 C.着色剂 D.增稠剂
【专题】56:化学应用.
【分析】2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖.
【考点】CA:化学反应速率的影响因素.
【解答】解:2015年10月,屠呦呦因发现青蒿素治疗疟疾的新疗法获诺贝尔生理学或医学奖。 菁优网版权所有
【专题】51F:化学反应速率专题.
故选:B。
【分析】一般来说,食品中常加入抗氧剂、调味剂、着色剂以及增稠剂等,其中加入抗氧化剂可
【点评】本题考查化学史,只要关注时事,平时注意积累,能轻松简答.
减缓食品的腐蚀,延长保质期,而调味剂、着色剂以及增稠剂与食品的色、态、味有关,以此
解答该题.
2.(3分)下列中草药煎制步骤中,属于过滤操作的是( )
【解答】解:A.抗氧化剂减少食品与氧气的接触,延缓氧化的反应速率,故A正确;
A.冷水浸泡 B.加热煎制 C.箅渣取液 D.灌装保存
B.调味剂是为了增加食品的味道,与速率无关,故 B错误;
C.着色剂是为了给食品添加某种颜色,与速率无关,故 C 错误;
D.增稠剂是改变物质的浓度,与速率无关,故D 错误。
故选:A。
【点评】本题考查常见食品的添加剂,与化学反应速率相结合综合考查学生的双基以及分析能
A.A B.B C.C D.D
力,侧重于化学与生活的考查,有利于培养学生良好的科学素养,难度不大,注意相关基础知
识的积累.
【考点】P9:物质的分离、提纯的基本方法选择与应用.
菁优网版权所有
第5页(共13页)4.(3分)在一定条件下,甲苯可生成二甲苯混合物和苯.有关物质的沸点、熔点如表: 5.(3分)K Cr O 溶液中存在平衡:Cr O 2﹣(橙色)+H O⇌2CrO 2﹣(黄色)+2H+.用 K Cr O 溶
2 2 7 2 7 2 4 2 2 7
对二甲苯 邻二甲苯 间二甲苯 苯 液进行下列实验:
沸点/℃ 138 144 139 80
熔点/℃ 13 ﹣25 ﹣47 6
下列说法不正确的是( )
A.该反应属于取代反应
结合实验,下列说法不正确的是( )
B.甲苯的沸点高于 144℃
A.①中溶液橙色加深,③中溶液变黄
C.用蒸馏的方法可将苯从反应所得产物中首先分离出来
B.②中 Cr O 2﹣被C H OH 还原
D.从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来 2 7 2 5
C.对比②和④可知 K Cr O 酸性溶液氧化性强
2 2 7
D.若向④中加入 70%H SO 溶液至过量,溶液变为橙色
【考点】HD:有机物的结构和性质. 2 4
菁优网版权所有
【专题】533:有机反应.
【考点】B1:氧化还原反应;CB:化学平衡的影响因素.
【分析】A、甲苯变成二甲苯是苯环上的氢原子被甲基取代所得,属于取代反应; 菁优网版权所有
【专题】515:氧化还原反应专题;51E:化学平衡专题.
B、甲苯的相对分子质量比二甲苯小,沸点比二甲苯低;
【分析】K Cr O 溶液中存在平衡:Cr O 2﹣(橙色)+H O⇌2CrO 2﹣(黄色)+2H+,加入酸,氢离子
C、苯的沸点与二甲苯的沸点相差较大,用蒸馏的方法分离; 2 2 7 2 7 2 4
浓度增大,平衡逆向移动,则溶液橙色加深,加入碱,平衡正向移动,溶液变黄,由实验②、
D、因为对二甲苯的熔点较高,将温度冷却至﹣25℃~13℃,对二甲苯形成固体,从而将对二甲苯
④可知Cr O 2﹣具有较强的氧化性,可氧化乙醇,而 CrO 2﹣不能,以此解答该题.
分离出来. 2 7 4
【解答】解:A.在平衡体系中加入酸,平衡逆向移动,重铬酸根离子浓度增大,橙色加深,加入
【解答】解:A、甲苯变成二甲苯是苯环上的氢原子被甲基取代所得,属于取代反应,故 A正
碱,平衡正向移动,溶液变黄,故 A正确;
确;
B.②中重铬酸钾氧化乙醇,重铬酸钾被还原,故 B正确;
B、甲苯的相对分子质量比二甲苯小,故沸点比二甲苯低,故 B错误;
C.②是酸性条件,④是碱性条件,酸性条件下氧化乙醇,而碱性条件不能,说明酸性条件下氧化
C、苯的沸点与二甲苯的沸点相差较大,可以用蒸馏的方法分离,故 C 正确;
性强,故C 正确;
D、因为对二甲苯的熔点较高,将温度冷却至﹣25℃~13℃,对二甲苯形成固体,从而将对二甲苯
D.若向④溶液中加入 70%的硫酸到过量,溶液为酸性,可以氧化乙醇,溶液变绿色,故 D 错
分离出来,故D 正确;
误。
故选:B。
故选:D。
【点评】本题涉及到物质的分离和提纯、有机物的反应类型、沸点高低比较,考查学生根据表格
【点评】本题综合考查氧化还原反应以及化学平衡的移动问题,侧重于学生的分析能力的考查,
的数据分析解决问题的能力,难度不大.
注意把握题给信息,为解答该题的关键,易错点为 D,注意 Cr O 2﹣、CrO 2﹣氧化性的比较,难
2 7 4
度不大.
第6页(共13页)为Ba(OH) 溶液和NaHSO 溶液的反应,即①代表滴加H SO 溶液的变化曲线,故A正确;
2 4 2 4
6.(3分)在两份相同的 Ba(OH) 溶液中,分别滴入物质的量浓度相等的 H SO 、NaHSO 溶 B.根据图知,a 点为 Ba(OH) 溶液和 H SO 恰好反应,H SO 、NaHSO 溶液的物质的量浓度相
2 2 4 4 2 2 4 2 4 4
液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( ) 等,则b 点溶液溶质为NaOH,所以b 点,溶液中大量存在的离子是Na+、OH﹣,故B正确;
C.c点,①中稀硫酸过量,溶质为硫酸,②中反应后溶液中溶质为 NaOH、Na SO ,因为硫酸根
2 4
离子浓度相同,②中钠离子浓度大于①中氢离子浓度,所以溶液中氢氧根离子浓度不同,故 C
错误;
D.a点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d 点②中溶质为 Na SO ,水和硫酸钠
2 4
溶液都呈中性,
故D 正确;
A.①代表滴加 H SO 溶液的变化曲线
2 4
故选:C。
B.b 点,溶液中大量存在的离子是Na+、OH﹣
【点评】本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析判断及识图能力,明
C.c点,两溶液中含有相同量的OH﹣
确发生的反应及各点溶液中溶质成分是解本题关键,注意:溶液导电能力与离子浓度成正比,
D.a、d 两点对应的溶液均显中性
题目难度中等.
【考点】D4:电解质溶液的导电性.
菁优网版权所有
7.(3分)用石墨电极完成下列电解实验.
【专题】51G:电离平衡与溶液的pH 专题.
实验一 实验二
【分析】A.Ba(OH) 溶液和 H SO 、NaHSO 溶液反应方程式分别为 H SO +Ba(OH)
2 2 4 4 2 4
=BaSO ↓+2H O、 NaHSO +Ba( OH) =BaSO ↓+NaOH+H O, 2NaHSO +Ba( OH)
装置
2 4 2 4 2 4 2 4
=BaSO ↓+Na SO +2H O,溶液导电能力与离子浓度成正比,根据图知,曲线①在 a 点溶液导电
2 4 2 4 2
能力接近 0,说明该点溶液离子浓度最小,应该为 Ba(OH) 溶液和 H SO 的反应,则曲线②
2 2 4
为Ba(OH) 溶液和NaHSO 溶液的反应;
2 4 现象 a、d 处试纸变蓝;b 处变 两个石墨电极附近有气泡产生;n 处有气泡
B.根据图知,a 点为 Ba(OH) 溶液和 H SO 恰好反应,H SO 、NaHSO 溶液的物质的量浓度相
2 2 4 2 4 4 红,局部褪色;c处无 产生;…
等,则b 点溶液溶质为NaOH;
明显变化
C.c点,①中稀硫酸过量,溶质为硫酸,②中反应后溶质为NaOH、Na SO ;
2 4 下列对实验现象的解释或推测不合理的是( )
D.a 点①中硫酸和氢氧化钡恰好完全反应,溶液中只含水;d 点②中溶质为Na SO .
2 4 A.a、d 处:2H O+2e﹣═H ↑+2OH﹣
2 2
【解答】解:A.Ba(OH) 溶液和 H SO 、NaHSO 溶液反应方程式分别为 H SO +Ba(OH)
2 2 4 4 2 4 B.b 处:2Cl﹣﹣2e﹣═Cl ↑
2
=BaSO ↓+2H O、 NaHSO +Ba( OH) =BaSO ↓+NaOH+H O, 2NaHSO +Ba( OH)
2 4 2 4 2 4 2 4 C.c处发生了反应:Fe﹣2e﹣═Fe2+
=BaSO ↓+Na SO +2H O,溶液导电能力与离子浓度成正比,根据图知,曲线①在 a 点溶液导电
2 4 2 4 2 D.根据实验一的原理,实验二中m处能析出铜
能力接近 0,说明该点溶液离子浓度最小,应该为 Ba(OH) 溶液和 H SO 的反应,则曲线②
2 2 4
第7页(共13页)(2)试剂a 是 浓硫酸和浓硝酸 .
【考点】BH:原电池和电解池的工作原理.
菁优网版权所有
(3)反应③的化学方程式: +NaOH +NaCl .
【专题】51I:电化学专题.
【分析】实验一 a、d 处试纸变蓝,说明生成 OH﹣,为电解池的阴极,b 处变红,局部褪色,为电 (4)E 的分子式是C H O .E 中含有的官能团: 碳碳双链,酯基 .
6 10 2
解池的阳极,生成氯气,c处无明显变化,铁丝左侧为阳极,右侧为阴极, (5)反应④的反应类型是 加聚反应 .
实验二两个石墨电极附近有气泡产生,左侧生成氢气,右侧生成氧气,两个铜珠的左侧为阳极,
右侧为阴极,n 处有气泡产生,为阴极,以此解答该题.
(6)反应⑤的化学方程式: +nH O +n CH CH OH .
2 3 2
【解答】解:A.d 处试纸变蓝,为阴极,生成 OH﹣,电极方程式为 2H O+2e﹣═H ↑+2OH﹣,故 A
2 2
正确;
(7)已知:2CH CHO
3
B.b 处变红,局部褪色,是因为 Cl +H O=HCl+HClO,HCl 的酸性使溶液变红,HClO的漂白性使局 以乙烯为起始原料,选用必要的无机试剂合成 E,写出合成路线(用结构简式表示有机物),用
2 2
部褪色,故B错误; 箭头表示转化关系,箭头上注明试剂和反应条件).
C.c处为阳极,发生了反应:Fe﹣2e﹣═Fe2+,故C 正确;
D.实验一中 ac形成电解池,db 形成电解池,所以实验二中也相当于形成三个电解池,一个球两 【考点】HB:有机物的推断.
菁优网版权所有
面为不同的两极,左边铜珠的左侧为阳极,发生的电极反应为 Cu﹣2e﹣=Cu2+,右侧(即位置 m 【专题】534:有机物的化学性质及推断.
处)为阴极,发生的电极反应为 Cu2++2e﹣=Cu,同样右边铜珠的左侧为阳极,右侧(即位置 n
处)为阴极,因此m处能析出铜的说法正确,故 D 正确。 【分析】A的分子式是 C
7
H
8
,其结构简式是 ,结合 P的结构简式,可知 A与浓硝酸在浓硫
故选:B。
酸、加热条件下发生取代反应生成 B为 ,B与氯气在光照条件下发生取代反应生
【点评】本题考查电解原理,侧重于学生的分析能力的考查,注意把握电极的判断以及电极反
成 C 为 ,C 在氢氧化钠水溶液、加热条件下发生水解反应生成 D 为
应,为解答该题的关键,题目易错点为 D,注意铜珠的左右侧可看出阴、阳极,难度中等.
二、解答题(共 4小题,满分 58分)
,可知 G的结构简式为 ,则 F ,E 的分子式是
8.(17分)功能高分子 P的合成路线如下:
C H O ,则E 为CH CH=CHCOOCH CH .
6 10 2 3 2 3
【解答】解:A的分子式是 C H ,其结构简式是 ,结合 P的结构简式,可知 A与浓硝酸在浓
7 8
硫酸、加热条件下发生取代反应生成 B为 ,B与氯气在光照条件下发生取代反应
生成 C 为 ,C 在氢氧化钠水溶液、加热条件下发生水解反应生成 D 为
(1)A的分子式是C H ,其结构简式是 .
7 8
第8页(共13页)故答案为:CH =CH CH CH Br CH CH OH CH CHO
2 2 3 2 3 2 3
,可知 G的结构简式 ,则 F,E 的分子式是 C H O ,则 E 为
6 10 2
CH CH=CHCOOCH CH . CH CH=CHCOOH CH CH=CHCOOCH CH .
3 2 3 3 3 2 3
【点评】本题考查有机物的推断与合成,充分利用 P的结构简式与反应条件、分子式进行推断,
(1)A的分子式是C H ,其结构简式是 ,故答案为: ;
7 8 侧重考查学生分析推理能力、知识迁移运用能力,是有机化学常考题型,难度中等.
(2)试剂a 是:浓硫酸和浓硝酸,故答案为:浓硫酸和浓硝酸;
9.(13分)用零价铁(Fe)去除水体中的硝酸盐(NO ﹣)已成为环境修复研究的热点之一.
(3)反应③的化学方程式: +NaOH +NaCl, 3
故答案为: +NaOH +NaCl;
(4)E 为 CH CH=CHCOOCH CH ,E 中含有的官能团:碳碳双键、酯基,故答案为:碳碳双键、酯
3 2 3
基;
(5)反应④的反应类型是:加聚反应,故答案为:加聚反应;
(6)反应⑤的化学方程式 +nH
2
O +n CH
3
CH
2
OH,
(1)Fe 还原水体中NO ﹣的反应原理如图1所示.
3
①作负极的物质是 铁 .
②正极的电极反应式是 NO ﹣+8e﹣+10H+=NH ++3H O .
3 4 2
故答案为 +nH O +n CH CH OH;
2 3 2
(2)将足量铁粉投入水体中,经24小时测定NO ﹣的去除率和pH,结果如下:
3
(7)乙烯与 HBr发生加成反应生成 CH CH Br,然后发生水解反应生成 CH CH OH,再发生氧化反
3 2 3 2
初始pH pH=2.5 pH=4.5
应生成 CH
3
CHO,2分子乙醛发生加成反应生成 ,再发生氧化反应生成 NO
3
﹣的去除率 接近100% <50%
,再与氢气发生加成反应生成 ,在浓硫酸、加热条件下发生消去反应生成生成
24小时pH 接近中性 接近中性
CH
3
CH=CHCOOH,最后与乙醇发生酯化反应生成 CH
3
CH=CHCOOCH
2
CH
3
,合成路线流程图为: 铁的最终物质形态
CH =CH CH CH Br CH CH OH CH CHO
2 2 3 2 3 2 3
CH CH=CHCOOH CH CH=CHCOOCH CH ,
pH=4.5时,NO
3
﹣的去除率低.其原因是 FeO(OH)不导电,阻碍电子转移 .
3 3 2 3
(3)实验发现:在初始 pH=4.5的水体中投入足量铁粉的同时,补充一定量的 Fe2+可以明显提高
第9页(共13页)NO ﹣的去除率.对 Fe2+的作用提出两种假设: 故答案为:铁;
3
Ⅰ.Fe2+直接还原NO ﹣; ②NO ﹣在正极得电子发生还原反应产生 NH +,根据图 2信息可知为酸性环境,则正极的电极反应
3 3 4
Ⅱ.Fe2+破坏FeO(OH)氧化层. 式为:NO ﹣+8e﹣+10H+=NH ++3H O,
3 4 2
①做对比实验,结果如图 2所示,可得到的结论是 本实验条件下,Fe2+不能直接还原 NO ﹣;在 故答案为:NO ﹣+8e﹣+10H+=NH ++3H O;
3 3 4 2
Fe和Fe2+共同作用下能提高NO ﹣的去除率 . (2)pH 越高,Fe3+越易水解生成 FeO(OH),而 FeO(OH)不导电,阻碍电子转移,所以 NO ﹣
3 3
②同位素示踪法证实 Fe2+能与 FeO(OH)反应生成 Fe O .结合该反应的离子方程式,解释加入 的去除率低.
3 4
Fe2+提高 NO ﹣去除率的原因: Fe2++2FeO(OH)=Fe O +2H+,Fe2+将不导电的 FeO(OH)转化 故答案为:FeO(OH)不导电,阻碍电子转移;
3 3 4
为可导电的Fe O ,利于电子转移 . (3)①从图 2的实验结果可以看出,单独加入 Fe2+时,NO ﹣的去除率为 0,因此得出 Fe2+不能直
3 4 3
(4)其他条件与(2)相同,经1小时测定NO ﹣的去除率和pH,结果如表: 接还原 NO ﹣;而 Fe和 Fe2+共同加入时 NO ﹣的去除率比单独 Fe高,因此可以得出结论:本实验
3 3 3
初始pH pH=2.5 pH=4.5 条件下,Fe2+不能直接还原 NO
3
﹣;在Fe 和Fe2+共同作用下能提高NO
3
﹣的去除率.
NO ﹣的去除率 约10% 约3% 故答案为:本实验条件下,Fe2+不能直接还原 NO 3 ﹣;在 Fe 和 Fe2+共同作用下能提高 NO 3 ﹣的去除
3
率;
1小时pH 接近中性 接近中性
②同位素示踪法证实了 Fe2+能与 FeO(OH)反应生成 Fe O ,离子方程式为:Fe2++2FeO(OH)
与(2)中数据对比,解释(2)中初始 pH 不同时,NO ﹣去除率和铁的最终物质形态不同的原 3 4
3
=Fe O +2H+,Fe2+将不导电的 FeO(OH)转化为可导电的Fe O ,利于电子转移.
因: 初始pH 低时,产生的 Fe2+充足;初始pH 高时,产生的 Fe2+不足 . 3 4 3 4
故答案为:Fe2++2FeO(OH)=Fe O +2H+,Fe2+将不导电的 FeO(OH)转化为可导电的 Fe O ,利
3 4 3 4
于电子转移;
【考点】BH:原电池和电解池的工作原理;FE:"三废"处理与环境保护;S4:铁及其化合物的性
(4)根据实验结果可知 Fe2+的作用是将不导电的 FeO(OH)转化为可导电的 Fe O ,而 NO ﹣的去
质实验. 3 4 3
菁优网版权所有
除率由铁的最终物质形态确定,因此可知实验初始 pH 会影响Fe2+的含量.
【专题】51I:电化学专题;52:元素及其化合物.
故答案为:初始pH 低时,产生的 Fe2+充足;初始pH 高时,产生的Fe2+不足.
【分析】(1)①Fe 还原水体中 NO ﹣,根据题意 Fe O 为电解质,则 Fe作还原剂,失去电子,作
3 3 4
【点评】考查化学反应原理,涉及电化学、氧化还原反应等相关知识,题中的 Fe 与 NO ﹣的反应
负极; 3
跟溶液酸碱性有关,抓住这一点是解题的关键,第Ⅱ问的解答有一定的难度,特别是阐述上的
②NO ﹣在正极得电子发生还原反应产生NH +,根据图 2信息可知为酸性环境;
3 4
准确性.
(2)由于 Fe O 为电解质,而电解质主要作用是为电子转移提供媒介,然后根据 FeO(OH)不导
3 4
电进行分析;
10.(12分)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO 、PbSO 及炭黑等)和 H SO 为原
(3)①根据图2中的三个实验结果进行分析; 2 4 2 4
料,制备高纯PbO,实现铅的再生利用.其工作流程如下:
②结合(2)题中的铁的最终物质形态结果差异进行分析;
(4)根据Fe2+的作用进行分析.
【解答】解:(1)①Fe还原水体中NO ﹣,则Fe 作还原剂,失去电子,作负极,
3
第10页(共13页)【考点】P8:物质分离和提纯的方法和基本操作综合应用;U3:制备实验方案的设计.
菁优网版权所有
【专题】546:无机实验综合.
【分析】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO 、PbSO 及炭黑等)和 H SO 为原料,制
2 4 2 4
备高纯 PbO,含铅废料加入硫酸亚铁、稀硫酸加热反应过滤得到 PbSO 粗品,加入 10%的氢氧
4
化钠溶液加热反应,冷却过滤得到 PbO 粗品,粗 PbO 溶解在 35%NaOH 溶液中配成高温下的饱
(1)过程Ⅰ中,在 Fe2+催化下,Pb和 PbO 反应生成 PbSO 的化学方程式是 Pb+PbO +2H SO ═
2 4 2 2 4 和溶液,冷却结晶、过滤得 PbO,
2PbSO +2H O .
4 2 (1)根据题给化学工艺流程知,过程Ⅰ中,在 Fe2+催化下,Pb、PbO 和 H SO 反应生成 PbSO 和
2 2 4 4
(2)过程Ⅰ中,Fe2+催化过程可表示为:
水;
i:2Fe2++PbO +4H++SO 2﹣═2Fe3++PbSO +2H O
2 4 4 2 (2)①催化剂通过参加反应,改变反应历程,降低反应的活化能,加快化学反应速率,而本身的
ii:…
质量和化学性质反应前后保持不变.根据题给信息知反应 i 中 Fe2+被 PbO 氧化为 Fe3+,则反应
2
①写出ii 的离子方程式: 2Fe3++Pb+SO 2﹣═PbSO +2Fe2+ .
4 4 ii 中Fe3+被Pb还原为Fe2+,据此书写离子方程式;
②下列实验方案可证实上述催化过程.将实验方案补充完整.
②a实验证明发生反应 i,则 b 实验需证明发生反应 ii,实验方案为取 a 中红色溶液少量,加入过
a.向酸化的 FeSO 溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO ,溶液变红.
4 2 量Pb,充分反应后,红色褪去;
b. 取a 中红色溶液少量,加入过量Pb,充分反应后,红色褪去 .
(3)①过程Ⅱ脱硫过程中发生的反应为 PbSO +2NaOH=PbO+Na SO +H O,而滤液Ⅰ中含有硫酸,
4 2 4 2
(3)PbO 溶解在 NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)⇌NaHPbO (aq),其溶解度
2 可降低溶液的pH,使平衡 PbO(s)+NaOH(aq)⇌NaHPbO (aq)逆向移动;
2
曲线如图所示.
②根据PbO 的溶解度曲线进行解答;
①过程Ⅱ的目的是脱硫.滤液 1经处理后可在过程Ⅱ中重复使用,其目的是 AB (选填序
【解答】解:(1)根据题给化学工艺流程知,过程Ⅰ中,在 Fe2+催化下,Pb、PbO 和 H SO 反应
2 2 4
号).
生成PbSO 和水,化学方程式为:Pb+PbO +2H SO ═2PbSO +2H O,
4 2 2 4 4 2
A.减小 Pb的损失,提高产品的产率
故答案为:Pb+PbO +2H SO ═2PbSO +2H O;
2 2 4 4 2
B.重复利用 NaOH,提高原料的利用率
(2)①催化剂通过参加反应,改变反应历程,降低反应的活化能,加快化学反应速率,而本身的
C.增加Na SO 浓度,提高脱硫效率
2 4 质量和化学性质反应前后保持不变.根据题给信息知反应 i 中 Fe2+被 PbO 氧化为 Fe3+,则反应
2
②过程Ⅲ的目的是提纯,结合上述溶解度曲线,简述过程Ⅲ的操作: 向 PbO 粗品中加入一定量
ii 中Fe3+被Pb还原为Fe2+,离子方程式为:2Fe3++Pb+SO 2﹣═PbSO +2Fe2+,
4 4
的35%NaOH 溶液,加热至 110℃,充分溶解后,趁热过滤,冷却结晶,过滤得到 PbO 固体
故答案为:2Fe3++Pb+SO 2﹣═PbSO +2Fe2+;
4 4
②a实验证明发生反应 i,则b 实验需证明发生反应ii,实验方案为:
a.向酸化的 FeSO 溶液中加入 KSCN溶液,溶液几乎无色,再加入少量 PbO ,溶液变红,亚铁离
4 2
子被氧化为铁离子,
b.取 a 中红色溶液少量,溶液中存在平衡,Fe3++3SCN﹣=Fe(SCN) ,加入过量 Pb,和平衡状态
3
下铁离子反应生成亚铁离子,平衡逆向进行充分反应后,红色褪去,
第11页(共13页)故答案为:取a 中红色溶液少量,加入过量Pb,充分反应后,红色褪去; ①用稀硫酸证实沉淀中含有Cu+的实验现象是 析出红色固体 .
(3)①过程Ⅱ脱硫过程中发生的反应为 PbSO +2NaOH=PbO+Na SO +H O,由于 PbO 能溶解与 ②通过下列实验证实,沉淀中含有Cu2+和SO 2﹣.
4 2 4 2 3
NaOH溶液,因此滤液Ⅰ中含有 Pb元素,滤液Ⅰ重复使用可减少 PbO 损失,提高产品的产
率,且滤液Ⅰ中过量的 NaOH可以重复利用,提高原料的利用率,故选AB.
故答案为:AB;
②根据 PbO 的溶解度曲线,提纯粗 Pb的方法为将粗 PbO 溶解在 NaOH溶液中,结合溶解度曲线
a.白色沉淀 A是BaSO ,试剂1是 HCl 和BaCl 溶液 .
4 2
特点可知浓度高的 NaOH溶液和较高的温度,PbO 的溶解度高,因此加热至较高温度,充分溶
b.证实沉淀中含有 Cu2+和 SO 2﹣的理由是 在 I﹣的作用下,Cu2+转化为白色沉淀 CuI,SO 2﹣转化为
3 3
解,然后再高温下趁热过滤除去杂质,后冷却后 PbO 又析出结晶,再次过滤可得到 PbO 固
SO 2﹣ .
4
体.
(3)已知:Al (SO ) 在水溶液中不存在.经检验,现象Ⅲ的白色沉淀中无 SO 2﹣,该白色沉淀
2 3 3 4
故答案为:向 PbO 粗品中加入一定量的 35%NaOH 溶液,加热至 110℃,充分溶解后,趁热过滤,
既能溶于强酸,又能溶于强碱,还可使酸性 KMnO 溶液褪色.
4
冷却结晶,过滤得到PbO 固体.
①推测沉淀中含有亚硫酸根和 Al(OH) .
3
【点评】本题考查了化学工艺流程分析、催化剂、离子方程式书写、化学实验方案的设计、物质
②对于沉淀中亚硫酸根的存在形式提出两种假设:i.被 Al(OH) 所吸附;ii.存在于铝的碱式盐
3
分离提纯、平衡一点原理的应用,题目难度中等.
中.对假设ii 设计了对比实验,证实了假设ii 成立.
a.将对比实验方案补充完整.
11.(16分)以 Na SO 溶液和不同金属的硫酸盐溶液作为实验对象,探究盐的性质和盐溶液间
2 3
反应的多样性.
实验 试剂 现象
步骤一:
滴管 试管
饱和Ag SO 溶液 Ⅰ.产生白色沉淀
2 4
0.2 mol•L﹣1 CuSO Ⅱ.溶液变绿,继续滴加
步骤二: (按图形式呈现).
4
0.2 mol•L﹣1 Na 2 SO 3 产生棕黄色沉淀 b.假设 ii 成立的实验证据是 V 1 明显大于V 2
溶液 (4)根据实验,亚硫酸盐的性质有 溶解性、还原性、在水溶液中呈碱性 .盐溶液间反应的多
0.1 mol•L﹣1 Al (SO ) Ⅲ.开始无明显变化,继
2 4
样性与 两种盐溶液中阴、阳离子的性质 有关.
溶液 续滴加产生白色沉淀
3
( 1) 经 检 验 , 现 象 Ⅰ中 的 白 色 沉 淀 是 Ag SO . 用 离 子 方 程 式 解 释 现 象 Ⅰ:
2 3
【考点】U2:性质实验方案的设计.
2Ag++SO 2﹣=Ag SO ↓ . 菁优网版权所有
3 2 3
【专题】546:无机实验综合.
(2)经检验,现象Ⅱ的棕黄色沉淀中不含SO 2﹣,含有Cu+、Cu2+和SO 2﹣.
4 3
【分析】(1)0.2mol/LNa SO 溶液滴入饱和Ag SO 溶液发生反应生成白色沉淀Ag SO ;
2 3 2 4 2 3
已知:Cu+ Cu+Cu2+,Cu2+ CuI↓(白色)+I .
2
(2)①根据第二题中现象 2及已知信息,可以得知,取少量洗净(排除 Cu2+干扰)的棕黄色沉
第12页(共13页)淀,滴加稀硫酸,沉淀变红(铜单质),则证明有 Cu+; 故答案为:Al3+、OH﹣;
②a.根据 BaSO 沉淀可知,加入的试剂为含Ba2+的化合物,可以选用BaCl ; ②根据假设可知实验的目的是证明产生的沉淀是 Al(OH) 还是铝的碱式盐,给定实验首先制备
4 2 3
b.由白色沉淀 A可知之前所取上层清液中有 SO 2﹣,由加入 KI生成白色沉淀可知棕黄色沉淀中含 出现象Ⅲ中的沉淀,然后采用滴加 NaOH溶液,因此对比实验首先要制备出 Al(OH) 沉淀,
4 3
有 Cu2+,Cu2+和 I﹣作用生成 CuI白色沉淀,由加淀粉无现象说明上层清液中无 I ,而 Cu2+和 I﹣反 然后滴加 NaOH溶液,若两者消耗的 NaOH体积相同,则现象Ⅲ中的沉淀就是 Al(OH) 沉
2 3
应生成I ,因而推断生成的 I 参与了其他反应,因而有还原剂SO 2﹣; 淀,若两者消耗的NaOH体积不同,则现象Ⅲ中的沉淀考虑是铝的碱式盐.
2 2 3
(3)①由题意,白色沉淀既能溶于强酸,又能溶于强碱,可以得到沉淀中含有 Al3+和 OH﹣,可使 铝的碱式盐和 NaOH溶液反应相当于铝离子和 NaOH反应,反应比例为 1:4,而 Al(OH) 和
3
酸性KMnO 溶液褪色是因为存在有还原性的亚硫酸根离子; NaOH反应比例为1:1,因此若V 明显大于V ,则假设 ii 成立;若V =V ,则假设i 成立.
4 1 2 1 2
②根据实验目的和对比实验设计原理进行解答;
(4)根据实验,亚硫酸盐具有溶解性、还原性、水解呈碱性,盐溶液间反应的多样性与两种盐溶
故答案为:a. ;
液中阴、阳离子的性质和反应条件有关.
b.假设 ii 成立的实验证据是 V 明显大于V ,
【解答】解:(1)实验Ⅰ中 0.2mol/LNa SO 溶液滴入饱和 Ag SO 溶液,由于 Ag SO 饱和溶液且 1 2
2 3 2 4 2 4
故答案为:V 明显大于V ;
溶液混合后稀释,因此不可能是 Ag SO 沉淀,考虑 SO 2﹣浓度较大,因此推断白色沉淀为 1 2
2 4 3
(4)题目中有多处暗示我们还原性,比如(3)中的沉淀可以使酸性高锰酸钾褪色,第二空,实
Ag SO ,反应的离子方程式为:2Ag++SO 2﹣=Ag SO ↓,故答案为:2Ag++SO 2﹣=Ag SO ↓;
2 3 3 2 3 3 2 3
验结论要紧扣实验目的,根据题目,我们探究的是 Na SO 溶液和不同金属的硫酸盐溶液反
(2)①依据反应 Cu+和稀硫酸反应铜和铜离子,若沉淀中含有 Cu+,加入稀硫酸会发生歧化反应 2 3
应,所以得到结论:盐溶液间反应的多样性与两种盐溶液中阴、阳离子的性质和反应条件有
生成铜单质,实验现象是有红色固体生成,
关.
故答案为:析出红色固体;
故答案为:还原性、水解呈碱性;两种盐溶液中阴、阳离子的性质有关.
② a. 分 析 实 验 流 程 可 知 实 验 原 理 为 2Cu2++4I﹣=2CuI+I 、 I +SO 2﹣+H O=SO 2﹣+2I﹣+2H+、
2 2 3 2 4
【点评】本题考查化学实验方案的分析、评价和设计.主要是离子检验和实验过程的理解应用,
SO 2﹣+Ba2+=BaSO ↓,根据 BaSO 沉淀可知,加入的试剂为含 Ba2+的化合物,可以选用 BaCl 溶
4 4 4 2
题目难度较大.
液,考虑沉淀A没有BaSO ,因此应在酸性环境中.
3
故答案为:HCl 和BaCl 溶液;
2
b.由白色沉淀 A可知之前所取上层清液中有 SO 2﹣,由加入 KI生成白色沉淀可知棕黄色沉淀中含
4
有 Cu2+,Cu2+和 I﹣作用生成 CuI白色沉淀,由加淀粉无现象说明上层清液中无 I ,而 Cu2+和 I﹣反
2
应生成I ,因而推断生成的 I 参与了其他反应,因而有还原剂SO 2﹣;
2 2 3
故答案为:棕黄色沉淀与 KI溶液反应生成白色沉淀(CuI),证明含有 Cu2+,白色沉淀 A为硫酸
钡,证明含有SO 2﹣;
3
(3)①根据题意知实验Ⅲ的白色沉淀中无 SO 2﹣,该白色沉淀既能溶于强酸,又能溶于强碱,还
4
可使酸性 KMnO 溶液褪色,可以推测沉淀中含有 Al3+和 OH﹣,可使酸性 KMnO 溶液褪色是因为
4 4
存在有还原性的亚硫酸根离子;
第13页(共13页)