文档内容
2017年全国高考新课标3卷理综(化学)(含答案)
可能用到的相对原子质量:H1 Li7 C12 N14 O16 S32 K39 Cr52 Mn55 Fe56
一、选择题:在每小题给出的四个选项中,只有一项是符合题目要求的。
7.化学与生活密切相关。下列说法错误的是
A.PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B.绿色化学要求从源头上消除或减少生产活动对环境的污染
C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
8.下列说法正确的是
A.植物油氢化过程中发生了加成反应
B.淀粉和纤维素互为同分异构体
C.环己烷与苯可用酸性KMnO 溶液鉴别
4
D.水可以用来分离溴苯和苯的混合物
9.下列实验操作规范且能达到目的的是
目的 操作
在50 mL酸式滴定管中装入盐酸,调整初始读
A. 取20.00 mL盐酸
数为30.00mL后,将剩余盐酸放入锥形瓶
B. 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C. 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上
配制浓度为0.010 mol·L-1的KMnO 称取KMnO 固体0.158 g,放入100 mL容量
D. 4 4
溶液 瓶中,加水溶解并稀释至刻度
10.N 为阿伏加德罗常数的值。下列说法正确的是
A
A.0.1 mol 的11B中,含有0.6N 个中子
A
B.pH=1的HPO 溶液中,含有0.1N 个H+
3 4 A
C.2.24L(标准状况)苯在O 中完全燃烧,得到0.6N 个CO 分子
2 A 2
D.密闭容器中1 mol PCl 与1 mol Cl 反应制备 PCl (g),增加2N 个P-Cl键
3 2 5 A
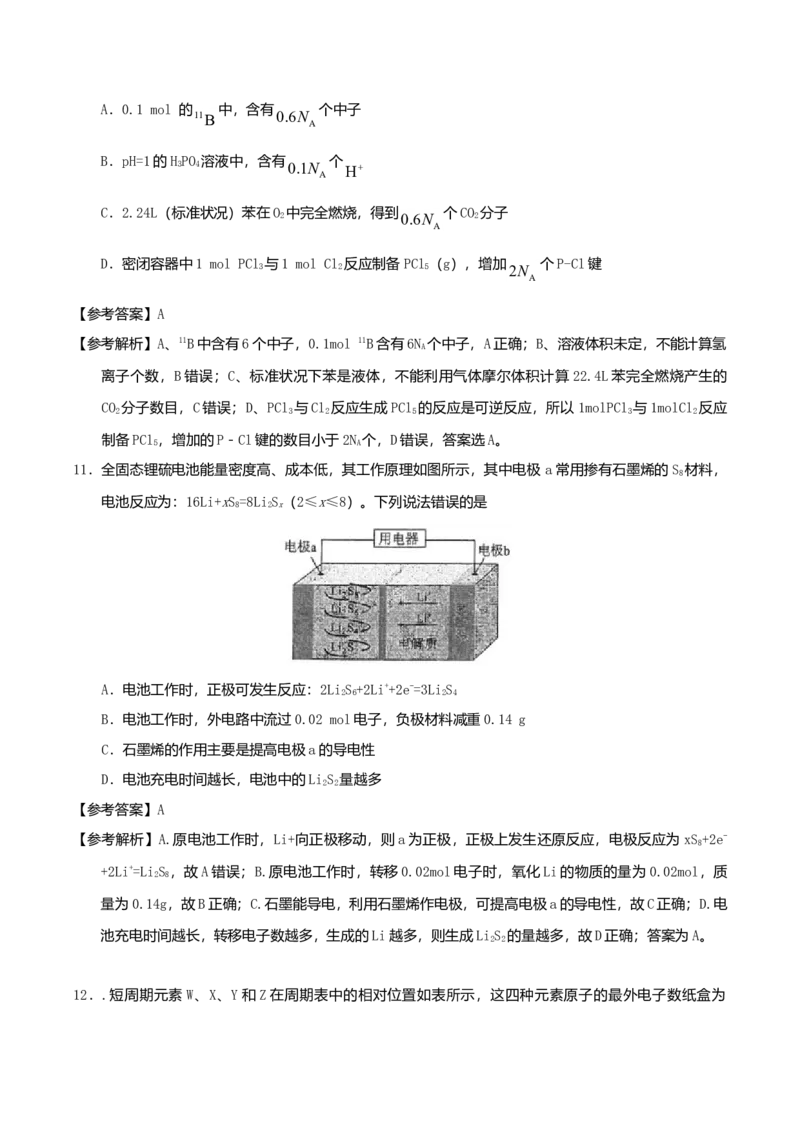
11.全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S 材料,
8
电池反应为:16Li+xS=8Li S(2≤x≤8)。下列说法错误的是
8 2 x
A.电池工作时,正极可发生反应:2LiS+2Li++2e-=3LiS
2 6 2 4B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中的LiS 量越多
2 2
12.短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数纸盒为
21。下列关系正确的是
W X
Y Z
A.氢化物沸点:WW
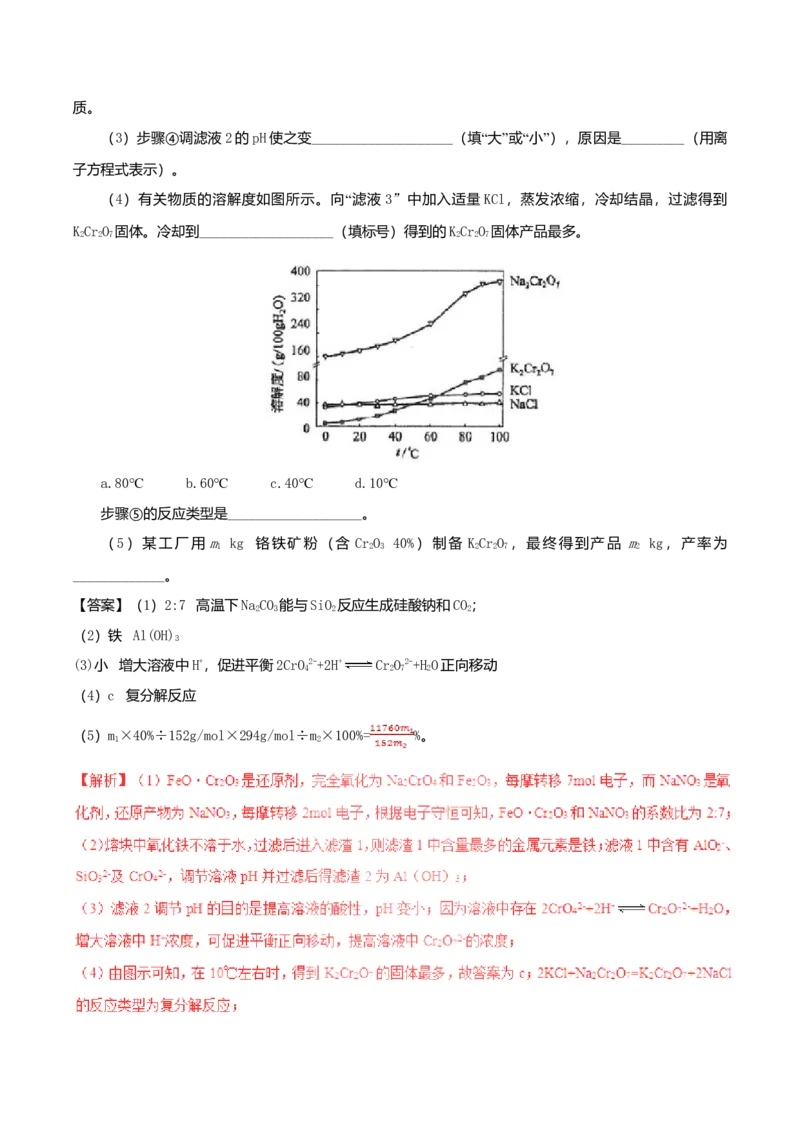
C.化合物熔点:YXCHOH>CO >H H O和CHOH均为极性分子,HO中氢键比甲醇多;CO 与H 均为非极
2 3 2 2 2 3 2 2 2
性分子,CO 相对分子质量较大、范德华力较大
2
(4)离子键和π键(Π6键) (5)0.148 0.076
36.(1) ,三氟甲苯;(2)浓HNO/浓HSO 、加热 取代反应
3 2 4
(3) +HCl 吸收反应生成的HCl
(4)C H FNO (5)9种
11 11 3 2 3
(6)
2017年高考新课标3卷理综化学7.化学与生活密切相关。下列说法错误的是
A.PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物
B.绿色化学要求从源头上消除或减少生产活动对环境的污染
C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
【参考答案】C
【参考解析】CaCO 受热分解,燃煤中加入CaO不能减小温室气体CO 的排放,故选C。
3 2
8.下列说法正确的是
A.植物油氢化过程中发生了加成反应
B.淀粉和纤维素互为同分异构体
C.环己烷与苯可用酸性KMnO 溶液鉴别
4
D.水可以用来分离溴苯和苯的混合物
【参考答案】A
【参考解析】A.植物没氢化过程发生油脂与氢气的加成反应,故A正确;B.淀粉和纤维素的聚合度不同,
造成它们的分子式不同,所以不是同分异构体,故B错误;C.环己烷与苯都不与酸性KMnO 溶液反应,
4
所以不能用该方法鉴别环己烷与苯,故C错误;D.溴苯与苯互溶,不能用水分离溴苯和苯的混合物,
故D错误;答案为A。
9.下列实验操作规范且能达到目的的是
目的 操作
在50 mL酸式滴定管中装入盐酸,调整初始读
A. 取20.00 mL盐酸
数为30.00mL后,将剩余盐酸放入锥形瓶
B. 清洗碘升华实验所用试管 先用酒精清洗,再用水清洗
C. 测定醋酸钠溶液pH 用玻璃棒蘸取溶液,点在湿润的pH试纸上
配制浓度为0.010molL1的KMnO 称取KMnO 固体0.158 g,放入100 mL容量瓶
D. 4 4
溶液 中,加水溶解并稀释至刻度
【参考答案】B
10. 为阿伏加德罗常数的值。下列说法正确的是
N
AA.0.1 mol 的 中,含有 个中子
11B 0.6N
A
B.pH=1的HPO 溶液中,含有 个
3 4 0.1N H
A
C.2.24L(标准状况)苯在O 中完全燃烧,得到 个CO 分子
2 0.6N 2
A
D.密闭容器中1 mol PCl 与1 mol Cl 反应制备 PCl(g),增加 个P-Cl键
3 2 5 2N
A
【参考答案】A
【参考解析】A、11B中含有6个中子,0.1mol 11B含有6N 个中子,A正确;B、溶液体积未定,不能计算氢
A
离子个数,B错误;C、标准状况下苯是液体,不能利用气体摩尔体积计算 22.4L苯完全燃烧产生的
CO 分子数目,C错误;D、PCl 与Cl 反应生成PCl 的反应是可逆反应,所以1molPCl 与1molCl 反应
2 3 2 5 3 2
制备PCl,增加的P-Cl键的数目小于2N 个,D错误,答案选A。
5 A
11.全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨烯的S 材料,
8
电池反应为:16Li+xS=8LiS(2≤x≤8)。下列说法错误的是
8 2 x
A.电池工作时,正极可发生反应:2LiS+2Li++2e-=3LiS
2 6 2 4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中的LiS 量越多
2 2
【参考答案】A
【参考解析】A.原电池工作时,Li+向正极移动,则a为正极,正极上发生还原反应,电极反应为 xS+2e-
8
+2Li+=LiS ,故A错误;B.原电池工作时,转移0.02mol电子时,氧化Li的物质的量为0.02mol,质
2 8
量为0.14g,故B正确;C.石墨能导电,利用石墨烯作电极,可提高电极a的导电性,故C正确;D.电
池充电时间越长,转移电子数越多,生成的Li越多,则生成LiS 的量越多,故D正确;答案为A。
2 2
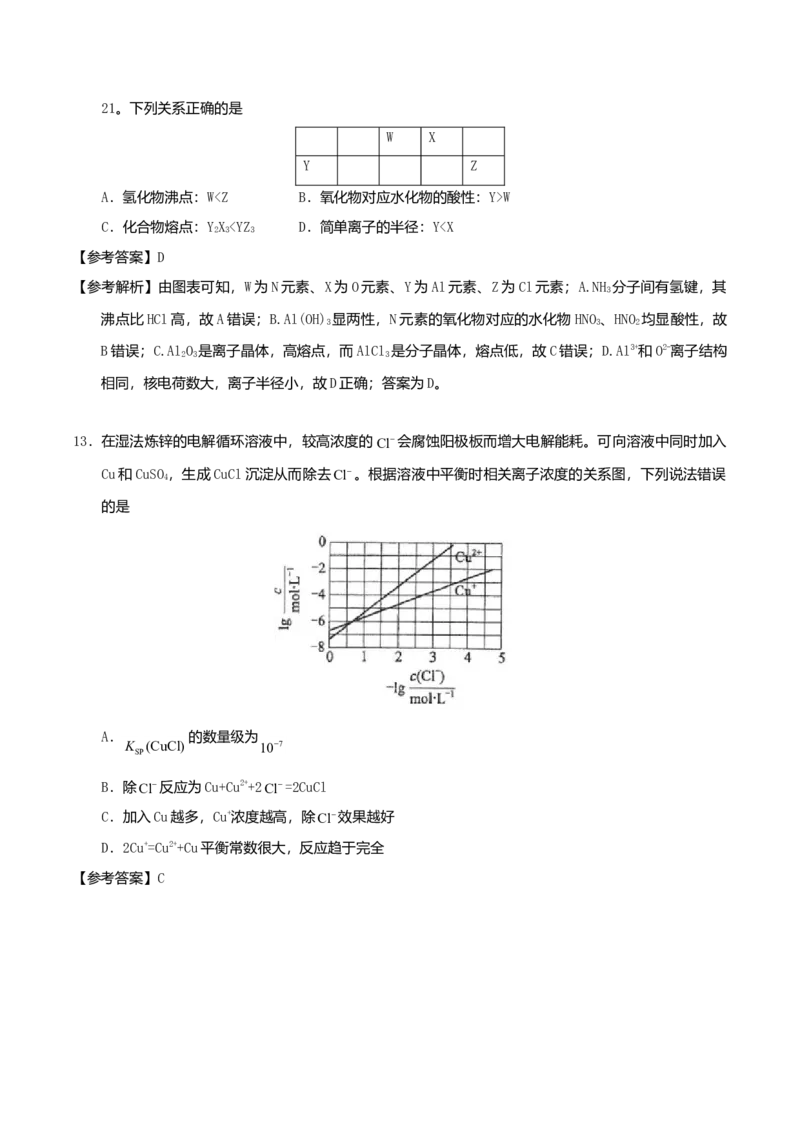
12..短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外电子数纸盒为21。下列关系正确的是
W X
Y Z
A.氢化物沸点:WW
C.化合物熔点:YXCHOH>CO>H ,常温下水和甲醇是液体而二氧化碳和氢气是气体,液体的沸点高于气体;水分子
2 3 2 2
中有两个氢原子都可以参与形成分子间氢键,而甲醇分子中只有一个羟基上的氢原子可用于形成分子间氢
键,所以水的沸点高于甲醇;二氧化碳的相对分子质量比氢气大,所以二氧化碳分子间作用力较大、沸点
较高。
(4)π键、离子键
(5) 3 2
0.448nm
4 2
【参考解析】
(1)Co 是 27 号元素,位于元素周期表第 4 周期第 VIII 族,其基态原子核外电子排布式为
1s22s22p63s23p63d74s2或[Ar]3d74s2。元素Mn与O中,由于O元素是非金属性而Mn是过渡元素,所以第一电离能较大的是O。O基态原子价电子为2s22p4,所以其核外未成对电子数是2,而Mn基态原子价电子排布为
3d54s2,所以其核外未成对电子数是5,因此核外未成对电子数较多的是Mn。
(2)CO 和CHOH的中心原子C原子的价层电子对数分别为2和4,所以CO 和CHOH分子中C原子的杂
2 3 2 3
化形式分别为sp和sp3。
(3)在CO 低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为HO>CHOH>CO>H,原因是
2 2 3 2 2
常温下水和甲醇是液体而二氧化碳和氢气是气体,液体的沸点高于气体;水分子中有两个氢原子都可以参
与形成分子间氢键,而甲醇分子中只有一个羟基上的氢原子可用于形成分子间氢键,所以水的沸点高于甲
醇;二氧化碳的相对分子质量比氢气大,所以二氧化碳分子间作用力较大、沸点较高。
(4)硝酸锰是离子化合物,硝酸根和锰离子之间形成离子键,硝酸根中N原子与3个氧原子形成 3个
σ键,硝酸根中有一个氮氧双键,所以还存在π键。
(5)
因为O2-是面心立方最密堆积方式,面对角线是O2-半径的4倍,即4r= a,解得r= 2 nm;MnO
2 0.420
4
也属于NaCl型结构,根据晶胞的结构,Mn2+构成的是体心立方堆积,体对角线是Mn2+半径的4倍,面上相
邻的两个Mn2+距离是此晶胞的一半,因此有 3 2 。
0.448nm
4 2
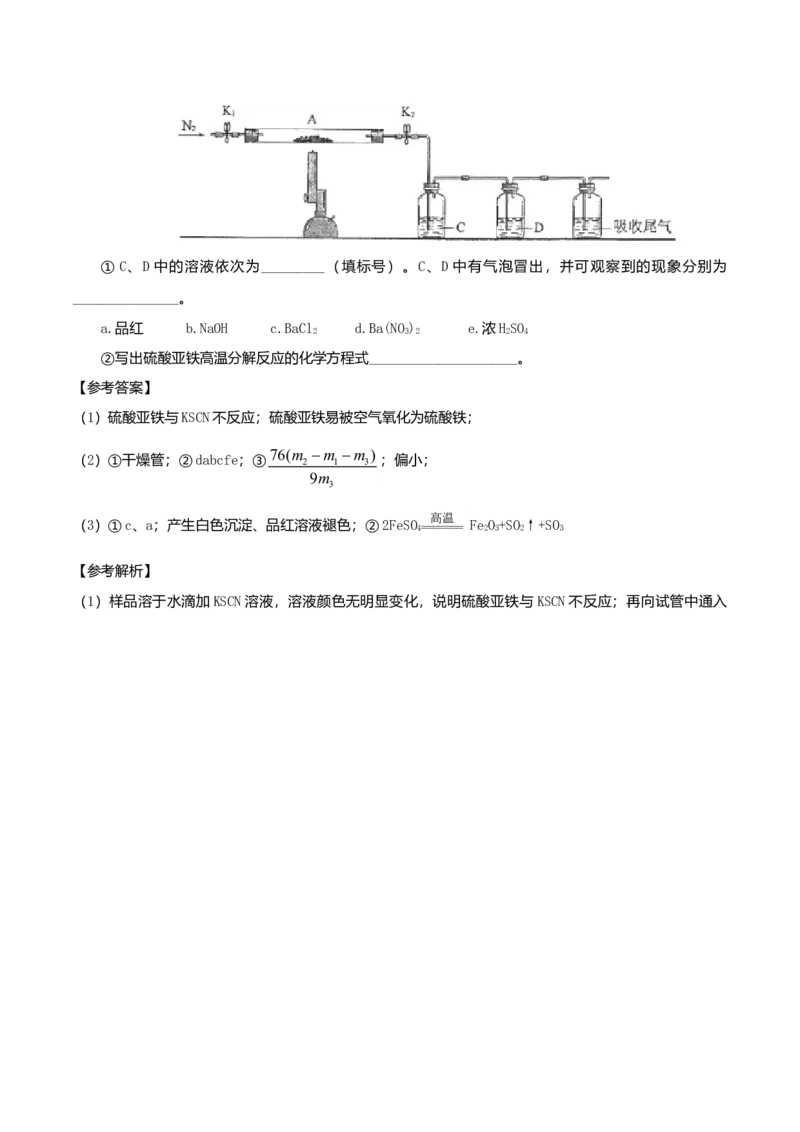
36.[化学——选修5:有机化学基础](15分)
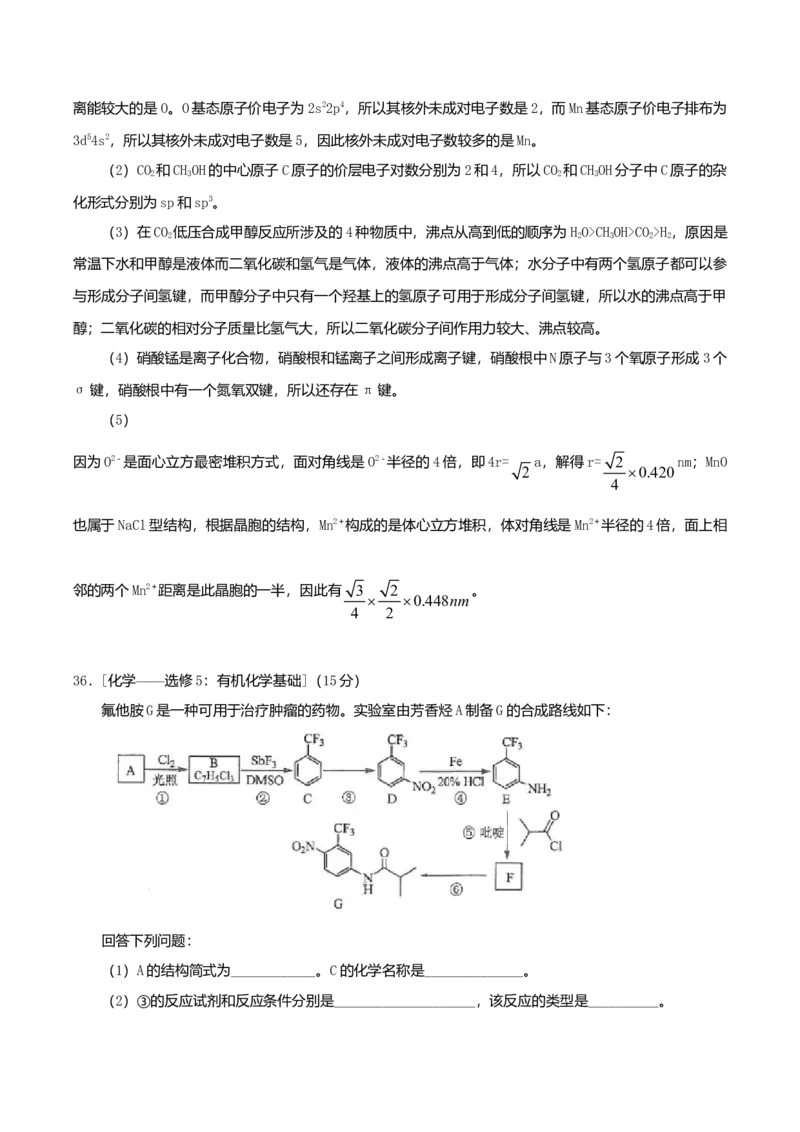
氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺( )是重要的精细化工中间体,写出由苯甲醚(
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
【参考答案】
(1) ,三氟甲苯;(2)浓硝酸、浓硫酸,并加热,反应类型是取代反应;(3)反应⑤的
—CH
3
化学方程式为:
,吡啶的作用是防止氨基被氧化;(4)C H ONF;(5)9种;(6)
11 11 3 3作用下-NO 转化成-NH,最后在吡啶作用下与CHCOCl反应生成目标产物,合成路线是:
2 2 3