文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题二 物质的性质与应用
专题 10 常见的盐
01考情透视·目标导航
02知识导图·思维引航
03考点突破·考法探究
考点一 常见的盐
考点二 复分解反应
考点三 化肥
04题型精研·考向洞悉
题型一 常见的盐
►考向01 常见的盐
►考向02 盐溶液的酸碱性
►考向03 常见盐的用途
►考向04 性质与用途的对应关系
►考向05 碳酸根离子的检验
►考向06 发酵粉中NaHCO 含量的测定
3
题型二 复分解反应
►考向01 复分解反应的判断
►考向02 复分解反应的应用——离子或物质的共存
►考向03 复分解反应的应用——物质的检验、鉴别和除杂
►考向04 复分解反应的应用——物质的推断
►考向05 复分解反应发生条件的探究
题型三 化肥
►考向01 常见化肥的种类
►考向02 化肥的作用
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
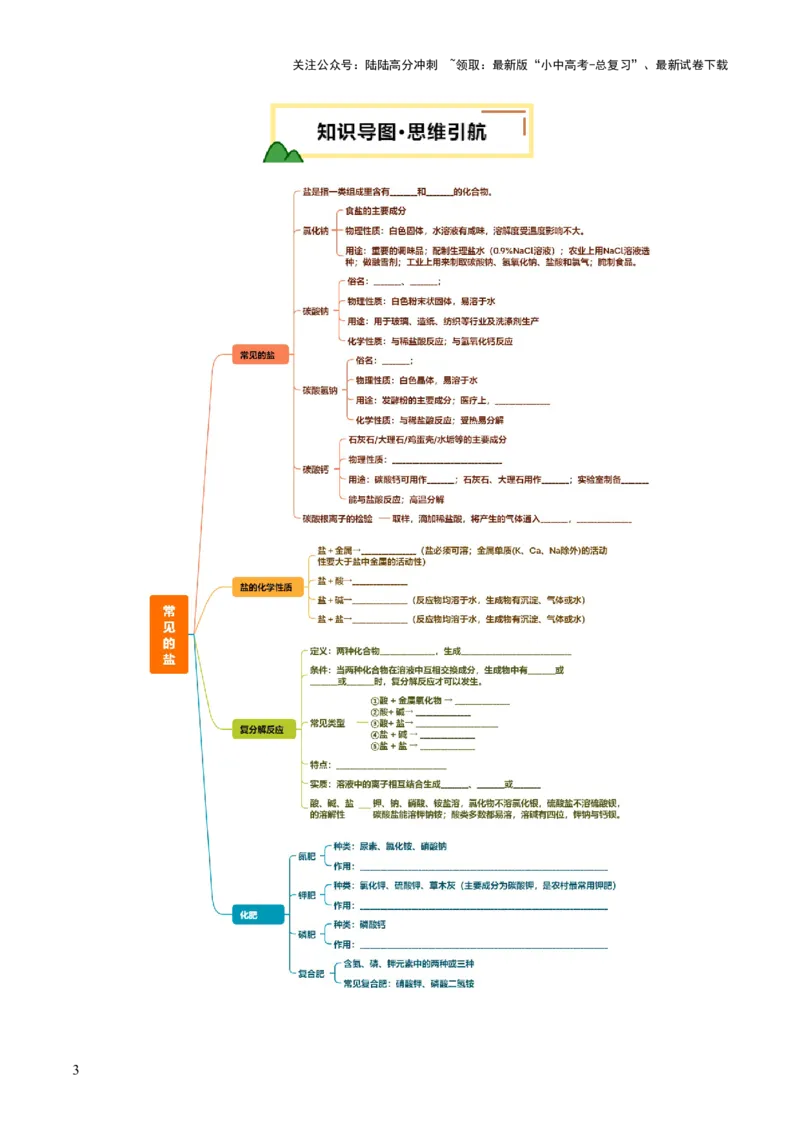
考点要求 课标要求 命题预测
常见的盐考查常结合 生产 生活 情境或
直接考查,题型多样化,可以是选择题、
了解食盐、纯碱、小苏打
填空题、流程题、实验题、科学探究题;
常见的盐 和碳酸钙等盐在日常生活中的应
复分解反应一般是直接考查,有时也结合
用。
生产生活情境。考查题型一般以选择题、
实验题、科学探究题等为主,少数穿插于
填空题、流程题等题型中。化肥的考查可
认识常见的复分解反应及 单独考查,也可与其他知识点相结合考
复分解反应
简单应用。 查,单独考查在选择题中出现,与其他知
识结合考查一般在填空题、流程题、综合
应用题中呈现。常见的考点有:食盐、纯
碱、小苏打和碳酸钙的物理性质和用途、
知道一些常用化肥及其在
化肥 复分解反应发生的条件及其探究、复分解
农业生产中的作用。
反应的应用、常用化肥的种类及用途。
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
考点一 常见的盐
1.盐的概念
盐是指一类组成里含有 (或 )和 的化合物。
2.常见的盐
名称 氯化钠 碳酸钠 碳酸氢钠 碳酸钙 高锰酸钾 硫酸铜 硝酸钠
化学式
3. 氯化钠、碳酸钠、碳酸氢钠和碳酸钙
(1)俗名、物理性质和用途
物质 俗称 物理性质 用途
重要的 ;配制 (
NaCl溶液);农业上用NaCl溶液
氯化钠 白色固体,水溶液有
的主要成分 ;做
NaCl 味,溶解度受温度影响
剂;工业上用来制取碳酸钠、
、 和氯气;腌制食品。
碳酸钠 (因水溶液呈碱 白色粉末状固体, 溶 用于玻璃、造纸、 等行业及
NaCO 性)、 于水 生产
2 3
碳酸氢钠 白色晶体, 的主要成分;
NaHCO 易溶于水 医疗上,治疗
3
碳酸钙 /大理石/鸡蛋 碳酸钙可用作 ;石灰石、大理
白色固体, 溶于水
CaCO 壳/水垢等的主要成分 石用作建筑材料;实验室制备
3
备注 氯化钠在自然界的分布很广, 、盐湖、盐井、盐矿都是氯化钠的来源。
(2)碳酸钠、碳酸氢钠和碳酸钙与盐酸反应
药品 实验现象 化学方程式 反应微观实质
反应快,产生大量气 与 结合生成HO
2
碳酸钠+稀盐酸
泡 和CO
2
碳酸氢钠+稀盐酸 反应快,产生大量气 与 结合生成HO
2
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
泡 和CO
2
产生气泡,反应速度
石灰石(或大理石 CO2-与 H+结合生成 HO
3 2
适中,适用于实验室 CaCO+2HCl =CaCl+HO+CO↑
3 2 2 2
+稀盐酸 和CO
2
制取二氧化碳
(3)碳酸氢钠受热易分解:
(4)碳酸钠与氢氧化钙(或氢氧化钡)反应
主要现象:有 生成
化学方程式: ;
(5)碳酸根离子的检验(CO2-)
3
检验方法:
【特别提醒】
1 .等质量的碳酸钠和碳酸氢钠分别与等质量等浓度的稀盐酸同时反应,反应更快的是碳酸氢钠。
2 .碳酸氢钠受热易分解、碳酸钠受热不易分解。
(6)碳酸钠和碳酸氢钠的鉴别:
①分别加热,分解产生CO 的是碳酸氢钠,不反应的是碳酸钠。
2
②分别滴加少量BaCl 或CaCl 溶液,有白色沉淀产生的是碳酸钠,无沉淀产生的是碳酸氢钠。
2 2
4.盐的化学性质
盐的化学性质 举例
①与某些金属反应 CuSO +Fe = FeSO +Cu
4 4
盐+金属→ ( 反应) 有 色固体析出,溶液由 色变为 色;
条件:盐必须 ;金属单质(K、Ca、Na除 2AgNO+Cu = Cu(NO)+2Ag
3 3 2
外)的活动性要 盐中金属的活动性 有银白色物体析出,溶液由无色变为 色
HCl+AgNO = AgCl↓+2HNO 有白色沉淀生成
3 3
②与酸反应
HSO +BaCl = BaSO↓+2HCl有白色沉淀生成
2 4 2 4
盐+酸→ (复分解反应)
NaCO+2HCl = 2NaCl+HO+CO↑有气泡产生
2 3 2 2
③与碱反应 NaCO+Ca(OH) = CaCO↓+2NaOH生成白色沉淀
2 3 2 3
盐+碱→ (复分解反应) 2NaOH+CuSO = Cu(OH) ↓+NaSO
4 2 2 4
反应物 ,生成物 生成蓝色沉淀,溶液由蓝色变为无色
④与某些盐反应 NaSO +BaCl = BaSO↓+2NaCl有白色沉淀生成
2 4 2 4
盐+盐→ (复分解反应) NaCl+AgNO = AgCl↓+NaNO 有白色沉淀生成
3 3
反应物 ,生成物
判断对错
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
1.盐中一定含有金属离子。( )
1.(2024·四川南充·中考真题)下列物质的俗名、化学式、分类完全正确的是
A.水银、Hg、单质 B.熟石灰、CaO、氧化物
C.苛性钠、NaOH、盐 D.纯碱、NaCO、碱
2 3
考点二 复分解反应
1.复分解反应
定义 两种化合物 ,生成另外 的反应
当两种化合物在溶液中互相交换成分,生成物中 或 或 生成
复分解反应发生的条件
时,复分解反应才可以发生。
① 酸 + 金属氧化物 →
②酸+ 碱→ 盐 + 水(也是中和反应)
** 错误的表达式 **酸+ 盐→ 另一种酸+ 另一种盐
复分解反应常见类型
** 错误的表达式 **盐 + 碱 → (条件:反应物需都可溶,且满足
复分解反应的条件)
** 错误的表达式 **盐 + 盐 → 两种新盐(条件:反应物需都可溶,且满足复
分解反应的条件)
复分解反应特点 反应前后元素的 不变。
溶液中的离子相互结合生成气体、沉淀或水,从而使溶液中的离子数量大幅减
复分解反应的实质
少。
【特别提醒】
非金属氧化物与碱的反应不是复分解反应。
2.酸、碱、盐的溶解性
物质类别 溶解性
酸 盐酸、硫酸、硝酸、碳酸都可溶
碱 氨水、 、氢氧化钾、氢氧化钡可溶于水, 微溶于水,其余均难溶(沉淀)
钾盐、钠盐、铵盐、硝酸盐都可溶;
氯化物除 难溶外,其余均可溶;
盐
硫酸盐除 难溶,Ag SO 、CaSO 微溶外,其余多数可溶;
2 4 4
碳酸盐除碳酸钾、碳酸钠、碳酸铵可溶,其余都难溶。
溶解性口诀 钾、钠、硝酸、铵盐溶,氯化物不溶氯化银,硫酸盐不溶硫酸钡,碳酸盐能溶钾钠铵;
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
酸类多数都易溶,溶碱有四位,钾钠与钙钡。
3.常见沉淀:
白色沉淀 ;
有色沉淀 蓝色沉淀、 红褐色沉淀
【特别提醒】
不溶性碱都能都能溶于酸(与酸反应)。不溶性盐除 AgCl 、 BaS O 既不溶于水也不溶于酸外,其余的不能
4
溶于水,但能溶于酸(与酸反应)。
4.不能大量共存的离子
(1)与H+不能共存的离子有: ;
(2)与OH-不能共存的离子有: 、 Zn2+等;
(3)与CO2-不能共存的离子有: ;
3
(4)与Ba2+不能共存的离子有: ;
(5)与Cl-不能共存的离子有: ;
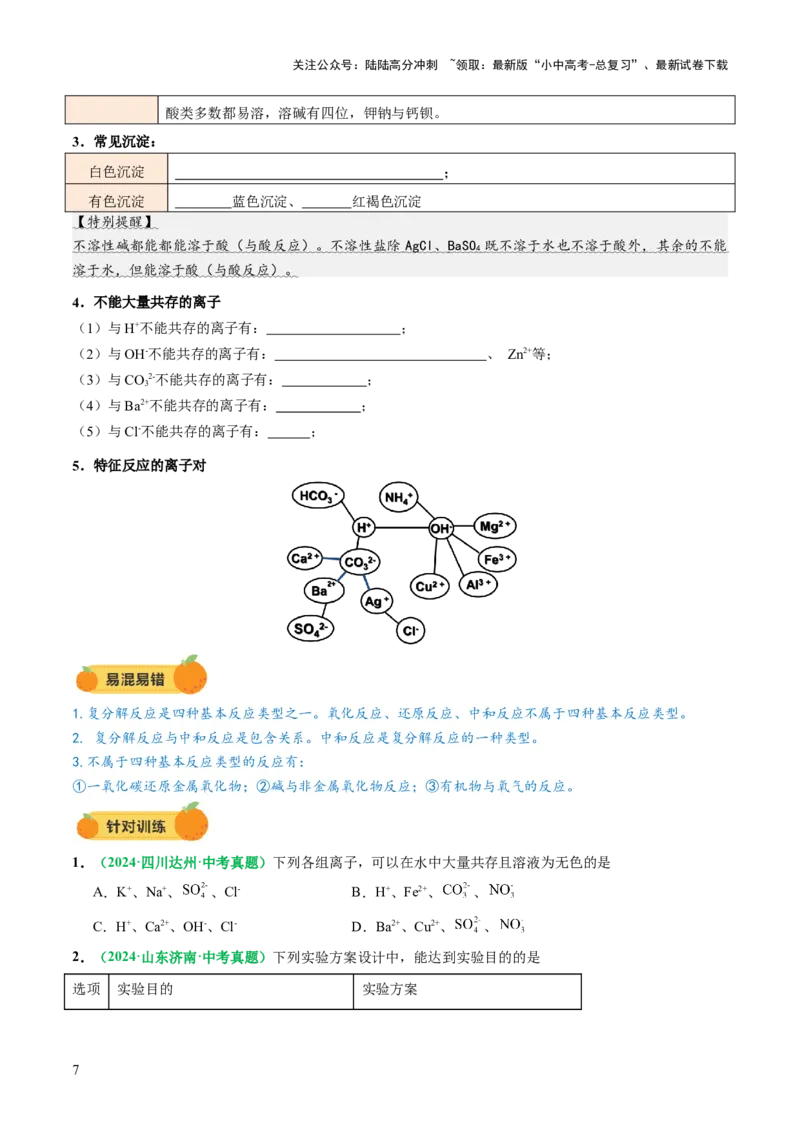
5.特征反应的离子对
1.复分解反应是四种基本反应类型之一。氧化反应、还原反应、中和反应不属于四种基本反应类型。
2. 复分解反应与中和反应是包含关系。中和反应是复分解反应的一种类型。
3.不属于四种基本反应类型的反应有:
①一氧化碳还原金属氧化物;②碱与非金属氧化物反应;③有机物与氧气的反应。
1.(2024·四川达州·中考真题)下列各组离子,可以在水中大量共存且溶液为无色的是
A.K+、Na+、 、Cl- B.H+、Fe2+、 、
C.H+、Ca2+、OH-、Cl- D.Ba2+、Cu2+、 、
2.(2024·山东济南·中考真题)下列实验方案设计中,能达到实验目的的是
选项 实验目的 实验方案
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A 除去 气体中混有的少量 通过足量 溶液,干燥
除去 溶液中混有的少量
B 加入过量稀硫酸
C 除去 溶液中混有的少量 加入适量 溶液,过滤
D 除去NaCl固体中混有的少量泥沙 加入足量水溶解,过滤,蒸发结晶
A.A B.B C.C D.D
考点三 化肥
1.常见化肥
种类 所含元素种类 常见化肥 作用 缺乏时症状
尿素CO(NH) :含氮量最高 促进植物茎、叶生长
2 2
氮肥 含氮元素 的 氮 肥 46.7% 、 氯 化 铵 茂盛、 (促
NH Cl、硝酸钠NaNO 苗)
4 3
氯化钾KCl、硫酸钾K 2 SO 4 促进作物生长,增强
钾肥 含钾元素 抗病虫害和 能
草 木 灰 : 主 要 成 分 为
力(壮秆)
,是农村最常用钾肥。
促进植物生长,增强 ,产
磷肥 含磷元素 磷酸钙[Ca 3 (PO 3 ) 2 ] 能力。(强 量降低,根系不
根) 发达
硝酸钾KNO
含氮、磷、钾元素 3
复合肥
中的两种或三种
磷酸二氢铵NH HPO
4 2 4
1.铵态氮肥防晒防潮,且均不能与碱性物质(如草木灰、熟石灰等)混合施用。
2.草木灰主要成分为KCO,是农村最常用钾肥, 其水溶液呈碱性。
2 3
1.(2024·贵州·中考真题)合理使用化学肥料,可提高农作物产量。下列物质属于磷肥的是
A. B. C. D.
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
题型一 常见的盐
►考向01 盐的俗名
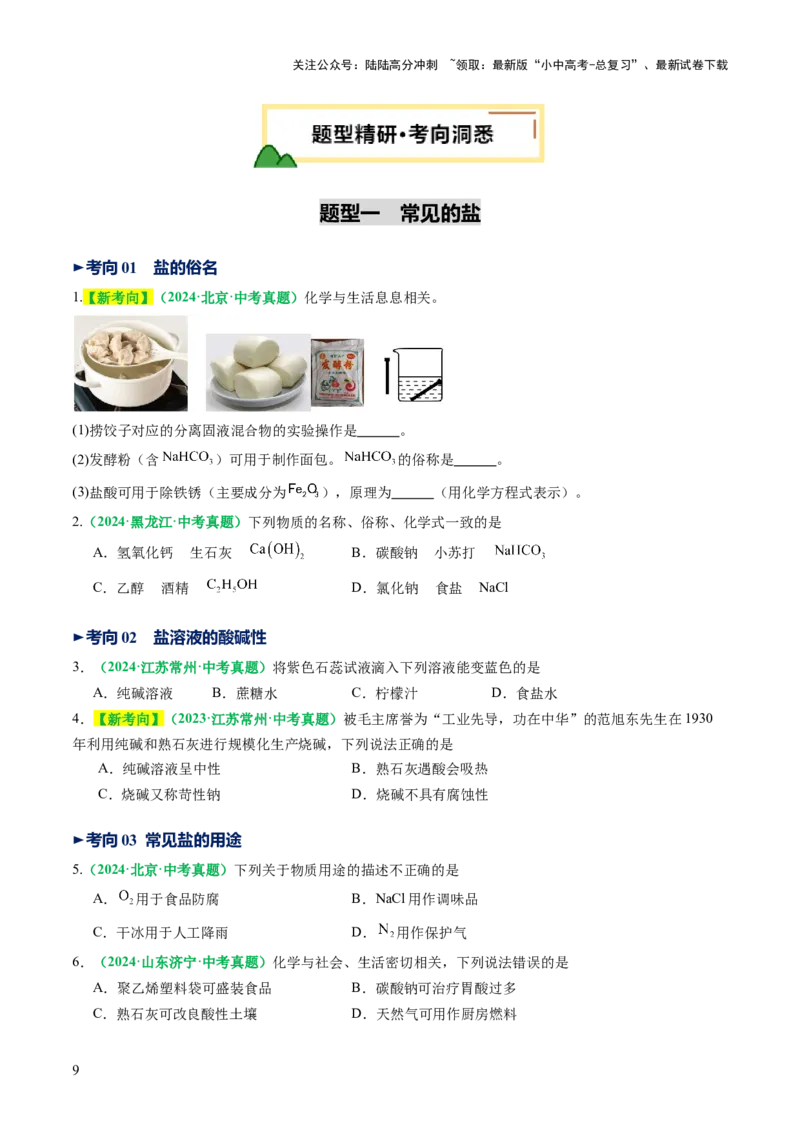
1.【新考向】(2024·北京·中考真题)化学与生活息息相关。
(1)捞饺子对应的分离固液混合物的实验操作是 。
(2)发酵粉(含 )可用于制作面包。 的俗称是 。
(3)盐酸可用于除铁锈(主要成分为 ),原理为 (用化学方程式表示)。
2.(2024·黑龙江·中考真题)下列物质的名称、俗称、化学式一致的是
A.氢氧化钙 生石灰 B.碳酸钠 小苏打
C.乙醇 酒精 D.氯化钠 食盐 NaCl
►考向02 盐溶液的酸碱性
3.(2024·江苏常州·中考真题)将紫色石蕊试液滴入下列溶液能变蓝色的是
A.纯碱溶液 B.蔗糖水 C.柠檬汁 D.食盐水
4.【新考向】(2023·江苏常州·中考真题)被毛主席誉为“工业先导,功在中华”的范旭东先生在1930
年利用纯碱和熟石灰进行规模化生产烧碱,下列说法正确的是
A.纯碱溶液呈中性 B.熟石灰遇酸会吸热
C.烧碱又称苛性钠 D.烧碱不具有腐蚀性
►考向03 常见盐的用途
5.(2024·北京·中考真题)下列关于物质用途的描述不正确的是
A. 用于食品防腐 B.NaCl用作调味品
C.干冰用于人工降雨 D. 用作保护气
6.(2024·山东济宁·中考真题)化学与社会、生活密切相关,下列说法错误的是
A.聚乙烯塑料袋可盛装食品 B.碳酸钠可治疗胃酸过多
C.熟石灰可改良酸性土壤 D.天然气可用作厨房燃料
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
►考向04 性质与用途的对应关系
7.【新考向】(2024·江苏宿迁·中考真题)下列物质的性质和用途对应关系正确的是
A.盐酸具有挥发性,常用作除铁锈
B.碳酸氢钠受热易分解,常用作治疗胃酸过多
C.浓硫酸具有强腐蚀性,常用作干燥剂
D.活性炭具有吸附性,常用作冰箱除味剂
8.(2024·山东威海·中考真题)化学服务于生活。下列做法中涉及的化学原理错误的是
选
做法 化学原理
项
A 用碳酸镁治疗胃酸过多 碳酸镁能与胃酸发生中和反应
B 用汽油去除衣服上的油渍 汽油能溶解油渍
C 洗净后的铁锅及时擦干水分 破坏铁生锈的条件能达到防锈目的
D 用小苏打烘焙糕点 NaHCO 受热易分解产生气体
3
A.A B.B C.C D.D
►考向05 碳酸根离子的检验
9.(2024·山东潍坊·中考真题)逻辑推理是一种重要的思维方法。下列推理正确的是
A.金刚石和石墨的组成元素相同,则二者的性质完全相同
B.某物质在氧气中完全燃烧生成 和 ,则该物质一定含有C、H元素
C.溶液是均一、稳定的混合物,则均一、稳定的物质一定是溶液
D.碳酸盐能和酸反应产生气体,则能和酸反应产生气体的物质一定是碳酸盐
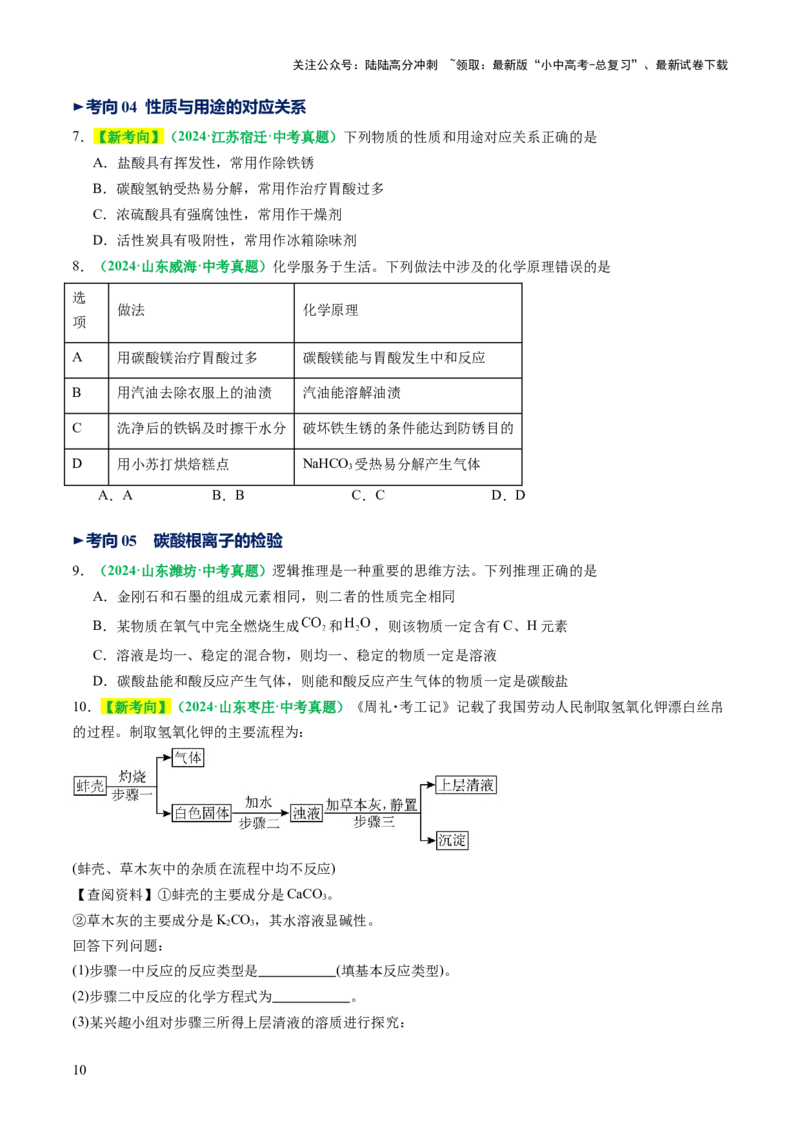
10.【新考向】(2024·山东枣庄·中考真题)《周礼・考工记》记载了我国劳动人民制取氢氧化钾漂白丝帛
的过程。制取氢氧化钾的主要流程为:
(蚌壳、草木灰中的杂质在流程中均不反应)
【查阅资料】①蚌壳的主要成分是CaCO 。
3
②草木灰的主要成分是KCO,其水溶液显碱性。
2 3
回答下列问题:
(1)步骤一中反应的反应类型是 (填基本反应类型)。
(2)步骤二中反应的化学方程式为 。
(3)某兴趣小组对步骤三所得上层清液的溶质进行探究:
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【提出问题】上层清液中的溶质是什么?
【作出猜想】猜想Ⅰ:KOH 猜想Ⅱ:KOH和
猜想Ⅲ:KOH和KCO 猜想Ⅳ:KOH、Ca(OH) 和KCO
2 3 2 2 3
有同学认为猜想Ⅳ不合理,理由是 。
【实验验证】
方案 实验 现象 结论
猜想Ⅱ不正
一 取少量上层清液于试管中,加入NaCO 溶液
2 3
确
二 取少量上层清液于试管中,加入 产生气泡 猜想Ⅲ正确
【反思评价】制取氢氧化钾的主要流程中能够循环利用的物质是 (填化学式)。
【拓展应用】为保证氢氧化钾较好的漂白丝帛的效果,对氢氧化钾的保存提一条合理化建议: 。
►考向06 发酵粉中NaHCO 含量的测定
3
11.【新考向】(2024·四川乐山·中考真题)发酵粉常用于制作馒头、糕点等,其主要成分为 .
某同学为测定某发酵粉样品中 的质量分数进行如下实验:取一个 空烧杯,向其中加入
发酵粉后缓慢加入 质量分数为20%的稀硫酸,待发酵粉中 完全反应后,测得烧杯及烧杯中
物质的总质量为 .
已知:① ;
②样品中其它成分不与硫酸反应.
回答下列问题:
(1) 中碳元素的化合价为 价.
(2) 中碳元素和氧元素的质量比为 .
(3)计算发酵粉样品中 的质量分数.(写出计算过程)
12.【新考向】(2024·四川南充·中考真题)为测定某食用小苏打(标签如图)中NaHCO 的质量分数,
3
取16.9g样品于烧杯中,分两次加入稀硫酸(该条件下杂质不参与反应),充分反应。测得实验数据如表
所示。
食用小苏打
主要成分:NaHCO
3
NaHCO 含量:
3
≥99%
加入稀硫酸的次数 第一次 第二次
加入稀硫酸的质量/g 50.0 50.0
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
生成气体的质量/g 5.0 3.8
(1)两次加稀硫酸后,生成二氧化碳的总质量是 g。
(2)通过计算说明样品中NaHCO 含量与标签是否相符(写出计算过程)。(反应的化学方程式为:
3
)
题型二 复分解反应
►考向01 复分解反应的判断
13.【新素材】(2024·河南·中考真题)《周礼·考工记》中记载,古人将含碳酸钙的贝壳制成石灰乳,在
草木灰(含KCO)的水溶液中加石灰乳,生成物能除去丝帛污渍。以上反应中不涉及的基本反应类型是
2 3
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
14.(2024·宁夏·中考真题)下列推理不正确的是
A.点燃一氧化碳前需要检验纯度,所以点燃可燃性气体前都要检验纯度
B.化合物是由不同种元素组成的,所以由不同种元素组成的纯净物一定是化合物
C.复分解反应有水或气体或沉淀生成,所以有水或气体或沉淀生成的反应一定是复分解反应
D.实验室制取氧气时要检查装置的气密性,所以制取所有气体时都要检查装置的气密性
►考向02 复分解反应的应用——离子或物质的共存
15.(2024·黑龙江·中考真题)下列各组离子在pH=10的溶液中能大量共存,且形成无色溶液的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
16.(2023·湖南常德·中考真题)下列各组物质在溶液中能够大量共存的是
A.BaCl 、NaNO 、CuCl B.NaCO、NaCl、HCl
2 3 2 2 3
C.HSO 、NaOH、KNO D.KCO、Ba(OH) 、KCl
2 4 3 2 3 2
►考向03 复分解反应的应用——物质的检验、鉴别和除杂
17.(2024·江苏宿迁·中考真题)物质的鉴别、检验、除杂和分离是重要的实验技能。下列实验方案设计
正确的是
选
实验目的 实验方案
项
A 鉴别氯化铵和硫酸铵 加入熟石灰粉末研磨,闻气味
B 检验蒸馏法淡化海水是否成功 取样,滴加几滴硝酸银溶液,观察现象
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C 除去硝酸钾溶液中的硝酸镁 滴加过量的氢氧化钾溶液,过滤
D 分离氯化钙和碳酸钙粉末 滴加足量的稀盐酸,蒸发结晶
A.A B.B C.C D.D
18.(2024·山东淄博·中考真题)下列有关物质检验、鉴别和除杂的实验设计,错误的是
选项 实验目的 实验设计
检验二氧化碳气体中混有氯化
A 将气体通入硝酸银溶液
氢
B 鉴别碳酸钠与碳酸氢钠固体 取样,分别加热,生成的气体通入澄清石灰水
除去氯化钠溶液中的少量氯化
C 加入适量碳酸钾溶液,过滤
钙
D 除去粗盐中的少量泥沙 加水溶解,过滤,蒸发结晶
A.A B.B C.C D.D
►考向04 复分解反应的应用——物质的推断
19.【新考向】(2024·江苏无锡·中考真题)取少量久置于空气中的碱石灰(NaOH和CaO的混合物)样
品M,加足量水溶解,出现白色沉淀。取上层清液 ,加足量稀盐酸,出现气泡。由实验得出的结论正确
的是
A.M中一定有NaCO B.N中一定有Ca(OH)
2 3 2
C.M中一定有CaCO D.N中一定有NaOH
3
20.(2024·江苏镇江·中考真题)以海水为原料生产的NaOH固体,可能含有NaCl、NaCO、NaSO ,
2 3 2 4
CaCl 、MgSO 中的一种或几种。进行如下实验。
2 4
(1)取适量固体加水溶解,得无色澄清溶液A,则原固体中一定不含 。
(2)取适量A溶液,加入过量BaCl 溶液,过滤得白色固体B。取固体B,加入过量稀盐酸,固体全部溶解,
2
产生气泡,则原固体中一定不含 。生成固体B反应的化学方程式为 。
(3)另取适量A溶液,先加入过量的稀 酸化,再滴加AgNO 溶液,产生白色沉淀,则原固体中一定含
3
。
►考向05 复分解反应发生条件的探究
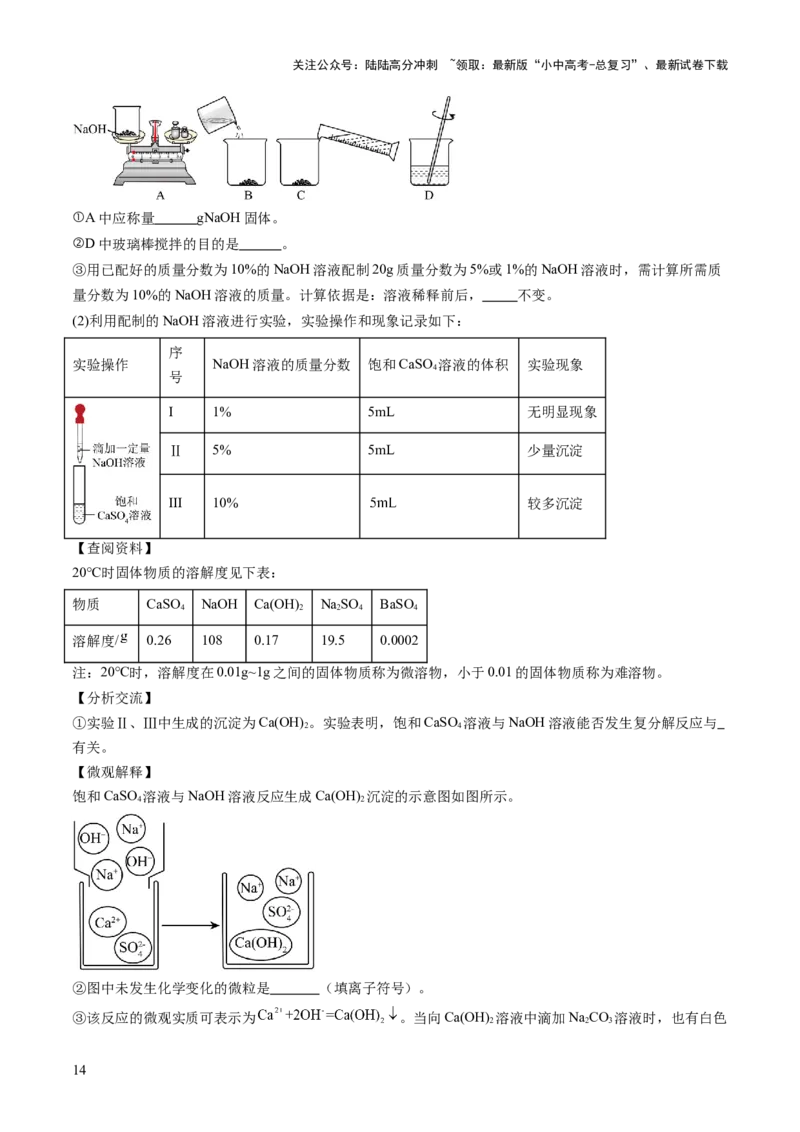
21.(2024·江苏连云港·中考真题)物质的溶解性与化学变化密切相关。兴趣小组对“CaSO 与NaOH能
4
否发生复分解反应”进行探究。
(1)配制100g质量分数为10%的NaOH溶液。主要操作流程如下:
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
①A中应称量 gNaOH固体。
②D中玻璃棒搅拌的目的是 。
③用已配好的质量分数为10%的NaOH溶液配制20g质量分数为5%或1%的NaOH溶液时,需计算所需质
量分数为10%的NaOH溶液的质量。计算依据是:溶液稀释前后, 不变。
(2)利用配制的NaOH溶液进行实验,实验操作和现象记录如下:
序
实验操作 NaOH溶液的质量分数 饱和CaSO 溶液的体积 实验现象
4
号
I 1% 5mL 无明显现象
Ⅱ 5% 5mL 少量沉淀
III 10% 较多沉淀
【查阅资料】
20℃时固体物质的溶解度见下表:
物质 CaSO NaOH Ca(OH) NaSO BaSO
4 2 2 4 4
溶解度/ 0.26 108 0.17 19.5 0.0002
注:20℃时,溶解度在0.01g~1g之间的固体物质称为微溶物,小于0.01的固体物质称为难溶物。
【分析交流】
①实验Ⅱ、Ⅲ中生成的沉淀为Ca(OH) 。实验表明,饱和CaSO 溶液与NaOH溶液能否发生复分解反应与
2 4
有关。
【微观解释】
饱和CaSO 溶液与NaOH溶液反应生成Ca(OH) 沉淀的示意图如图所示。
4 2
②图中未发生化学变化的微粒是 (填离子符号)。
③该反应的微观实质可表示为 。当向Ca(OH) 溶液中滴加NaCO 溶液时,也有白色
2 2 3
14关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
沉淀产生,反应的微观实质用同样的方法可表示为 。
【反思拓展】
④结合以上探究活动,下列说法正确的是 (填字母)。
a.其他条件不变,将实验Ⅲ中的NaOH溶液换成KOH溶液,也有沉淀产生
b.复分解反应中,溶解度较大的微溶物可向溶解度更小的微溶物或难溶物转化
c.向CaSO 溶液中滴加Ba(OH) 溶液,生成的沉淀为Ca(OH)
4 2 2
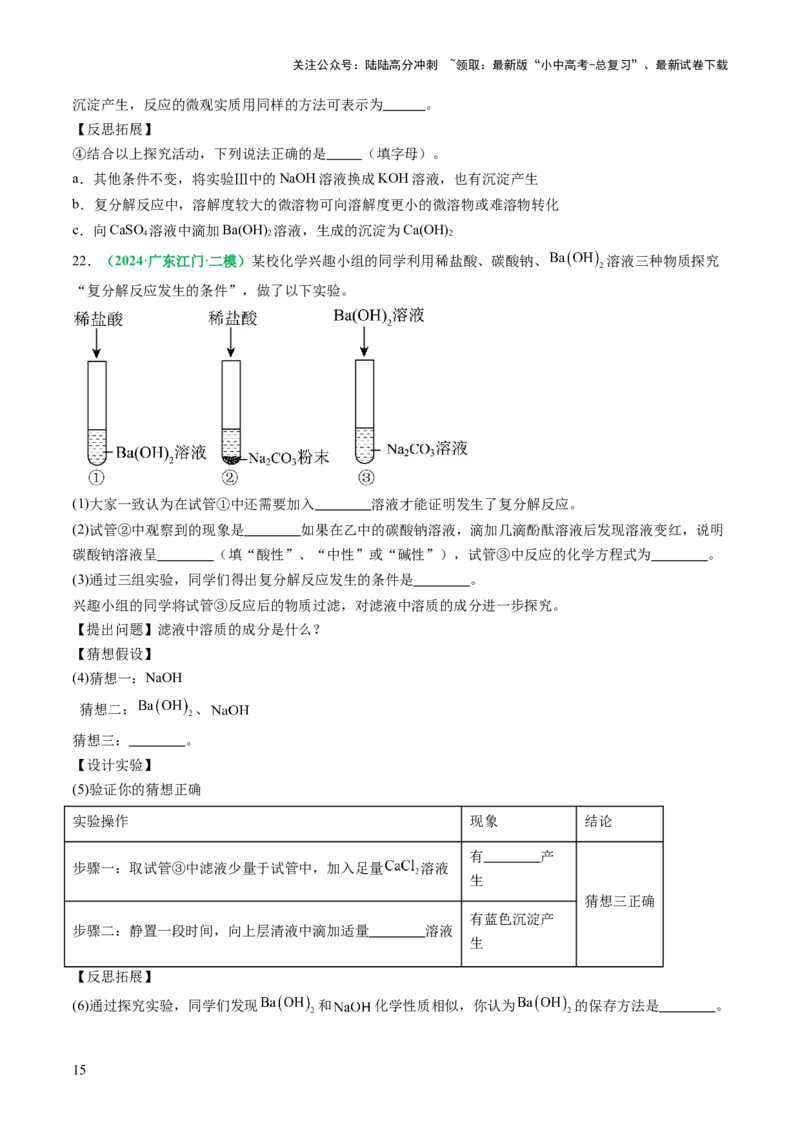
22.(2024·广东江门·二模)某校化学兴趣小组的同学利用稀盐酸、碳酸钠、 溶液三种物质探究
“复分解反应发生的条件”,做了以下实验。
(1)大家一致认为在试管①中还需要加入 溶液才能证明发生了复分解反应。
(2)试管②中观察到的现象是 如果在乙中的碳酸钠溶液,滴加几滴酚酞溶液后发现溶液变红,说明
碳酸钠溶液呈 (填“酸性”、“中性”或“碱性”),试管③中反应的化学方程式为 。
(3)通过三组实验,同学们得出复分解反应发生的条件是 。
兴趣小组的同学将试管③反应后的物质过滤,对滤液中溶质的成分进一步探究。
【提出问题】滤液中溶质的成分是什么?
【猜想假设】
(4)猜想一:NaOH
猜想二: 、
猜想三: 。
【设计实验】
(5)验证你的猜想正确
实验操作 现象 结论
有 产
步骤一:取试管③中滤液少量于试管中,加入足量 溶液
生
猜想三正确
有蓝色沉淀产
步骤二:静置一段时间,向上层清液中滴加适量 溶液
生
【反思拓展】
(6)通过探究实验,同学们发现 和 化学性质相似,你认为 的保存方法是 。
15关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
题型三 化肥
►考向01 常见化肥的种类
23.【新考向】(2024·山东潍坊·中考真题)某无土栽培营养液中含有 、 、 、
等,其中属于复合肥料的是
A. B. C. D.
24.(2024·江苏镇江·中考真题)下列归类正确的是
选
归类 内容
项
A 常见合金 青铜、硬铝、玻璃钢
B 营养物质 糖类、油脂、蛋白质
C 常见氮肥 碳铵、尿素、氯化钾
D 清洁能源 石油、风能、太阳能
A.A B.B C.C D.D
►考向02 化肥的作用
25.(2024·上海·中考真题)玉米叶发黄说明植物缺乏氮元素,应立即施用的化肥是
A. B. C. D.
26.(2024·四川德阳·中考真题)尿素是一种优良的氮肥,其化学式为 CO (NH )。下列说法错误的是
2 2
A.尿素的相对分子质量是60
B.尿素中碳元素与氢元素的质量之比是6:1
C.尿素中氮元素的质量分数约为46.7%
D.尿素能使植物枝繁叶茂、叶色浓绿
16