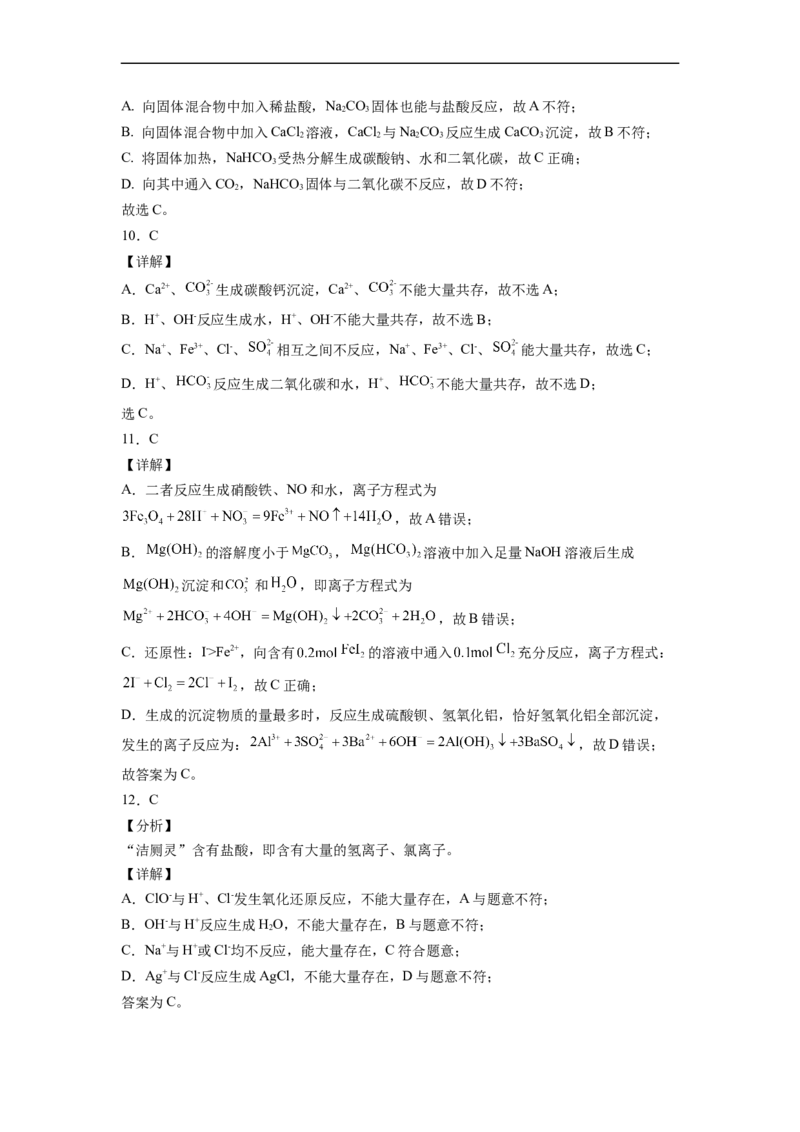文档内容
2022 届高三化学二轮复习金属钠及钠的化合物必刷卷
一、选择题(共17题)
1.下列有关说法错误的是
A.金属钠一般保存在煤油或石蜡中,剩余的钠应放回原瓶
B.将 NaO 加入酚酞溶液后,溶液先变红后褪色,并有大量的气泡产生
2 2
C.根据焰色为黄色,可以推知物质中一定含有钠元素
D.苏打是 NaHCO ,可用于中和过多胃酸、烘焙糕点
3
2.下列离子方程式书写正确的是 ( )
A.铝片加入氯化铜溶液中:Al+Cu2+=Al3++Cu
B.氢氧化钾溶液加入氯化铁溶液中:3OH-+FeCl = Fe(OH) ↓+3Cl-
3 3
C.石灰石加入稀盐酸中:CaCO +2H+= Ca2++CO↑+HO
3 2 2
D.氢氧化钡溶液加入稀硫酸中:Ba2++OH-+H++SO 2-=BaSO ↓+HO
4 4 2
3.下列说法中正确的是
A.Na在空气中缓慢氧化生成白色的NaO
2 2
B.Na在空气中燃烧生成NaO
2 2
C.Na在空气中燃烧生成淡黄色的NaO
2
D.Na在空气中燃烧生成白色的NaO
2 2
4.化学与生活生产密切相关。下列说法正确的是( )
A.“84”消毒液与洁厕灵(主要成分HCl)混合增强消毒效果
B.汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏土
C.泡沫灭火器可用于一般的起火,也适用于电器起火
D.盐碱地(含较多NaCO)不利于作物生长,可施加生石灰进行改良
2 3
5.下列实验现象所对应的离子方程式不正确的是
A.向淀粉KI溶液中滴加适量稀硫酸,在空气中放置一段时间后,溶液呈蓝色:
B.向 固体中滴加蒸馏水,产生无色气体:
C.向饱和 溶液中通入过量 气体,溶液中析出晶体:D.向滴有酚酞的 溶液中滴加 溶液,有白色沉淀生成,溶液褪色:
6.下列说法正确的是
A.用碳酸钠等物质可处理废水中的酸
B.含有碳酸氢钠的药片是抗酸药,服用时喝些醋能提高药效
C.灼烧某白色粉末,火焰成黄色,证明原粉末中有Na+,无K+
D.在酒精灯加热条件下,NaCO、NaHCO 固体都能发生分解
2 3 3
7.要从含Al3+、Fe3+、Ba2+、Ag+的溶液中分别沉淀出Fe3+、Ba2+、Ag+,加入试剂的顺序正确的是
A.HCl、HSO 、NaOH B.NaOH、HCl、HSO
2 4 2 4
C.HCl、HSO 、NH ·H O D.HCl、NaOH、HSO
2 4 3 2 2 4
8.现有3.60gNaCl、 和 的混合固体,加热足够长时间后,固体剩余3.29g;将剩余固体溶
于一定体积的盐酸中,产生0.448L气体(标准状况下),并将所得溶液稀释至100mL,测得所得溶液中
。下列说法正确的是
A.混合固体中 的质量为0.84g
B.混合固体中 的质量为2.12g
C.所加盐酸中,HCl的物质的量为0.04mol
D.最终所得溶液中
9.除去NaCO 固体中混有的少量NaHCO ,可采用的方法是( )
2 3 3
A.向固体混合物中加入稀盐酸 B.向固体混合物中加入CaCl 溶液
2
C.将固体加热 D.向其中通入CO
2
10.下列各组离子在溶液中能大量共存的是
A.Ca2+、Na+、 、 B.H+、 、OH-、Na+
C.Na+、Fe3+、Cl-、 D.H+、K+、 、11.下列离子方程式与所述事实相符且正确的是
A.磁性氧化铁溶于稀硝酸:
B. 溶液中加入足量NaOH溶液:
C.向含有 的溶液中通入 充分反应:
D.明矾溶液中加入 溶液至生成沉淀的物质的量最多:
12.以电解饱和食盐水为基础制取氯气、氢气、烧碱等产品的工业称为氯碱工业。氯及其化合物广泛应用
于日常生活中,例如常用的含氯消毒剂“84”消毒液(含有NaClO)、清洁剂“洁厕灵”(含有盐酸)等。“84”
消毒液与“洁厕灵”不能混合使用。在“洁厕灵”中,能大量存在的离子是
A.ClO- B.OH- C.Na+ D.Ag+
13.能用离子方程式“Ba2++SO 2-=BaSO ↓”表示的化学反应是
4 4
A.Ba(OH) +HSO =BaSO ↓+2HO
2 2 4 4 2
B.BaCO +HSO =BaSO +HO+CO↑
3 2 4 4 2 2
C.BaCl +HSO =BaSO ↓+2HCl
2 2 4 4
D.Zn+HSO =ZnSO +H↑
2 4 4 2
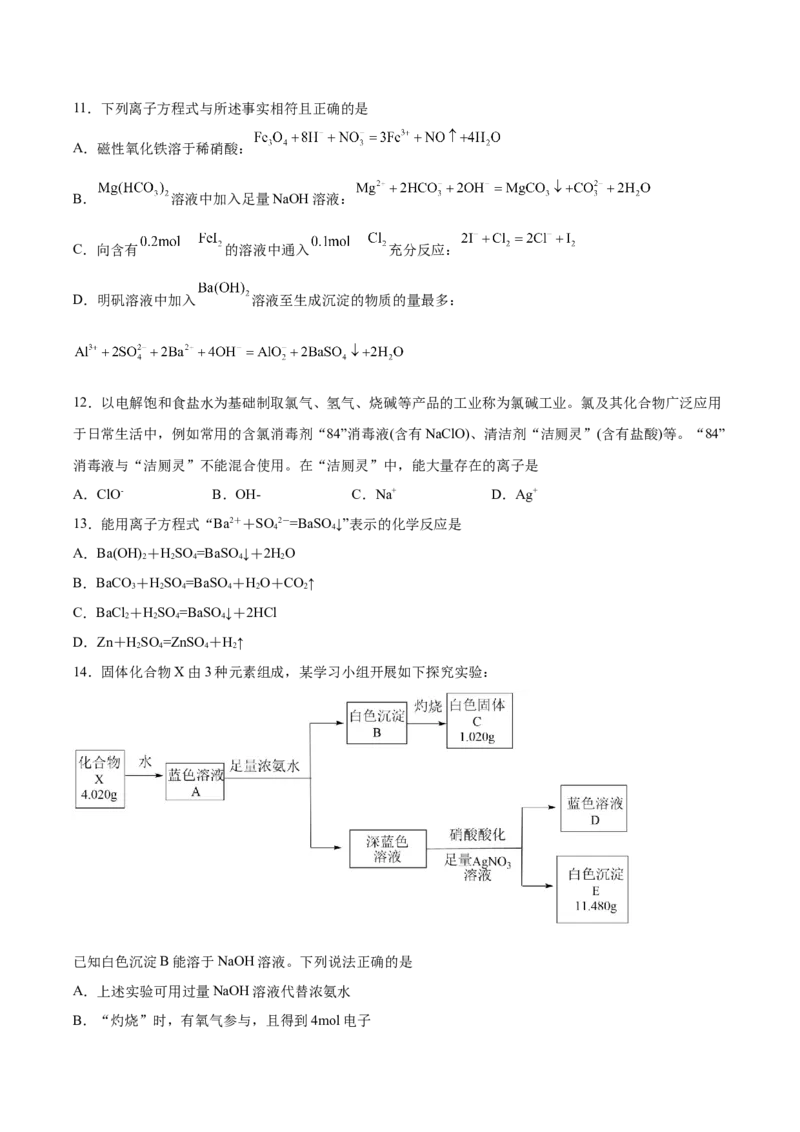
14.固体化合物X由3种元素组成,某学习小组开展如下探究实验:
已知白色沉淀B能溶于NaOH溶液。下列说法正确的是
A.上述实验可用过量NaOH溶液代替浓氨水
B.“灼烧”时,有氧气参与,且得到4mol电子C.蓝色溶液D中,溶质不止一种
D.通过上述流程,无法确定X的组成
15.某溶液中可能含有 H+、NH +、Fe2+、SO 2﹣、CO2﹣、Br﹣,且物质的量浓度相同;取样进行实验,结
4 4 3
果是:①测得溶液 pH=2;②加入氯水,溶液颜色变深。对原溶液描述错误的是( )
A.一定含有 Fe2+ B.一定含有 Br﹣
C.可能同时含 Fe2+、Br﹣ D.一定不含NH +
4
16.下列反应的离子方程式正确的是
A.盐酸与铁屑反应:2Fe+6H+=2Fe3++3H ↑
2
B.碳酸钙和稀盐酸反应:CaCO +2H+===Ca2++CO ↑+H O
3 2 2
C.醋酸与氢氧化钠溶液反应:H++OH-=H O
2
D.硫酸镁溶液与氢氧化钡溶液反应:Mg2++2OH-===Mg(OH) ↓
2
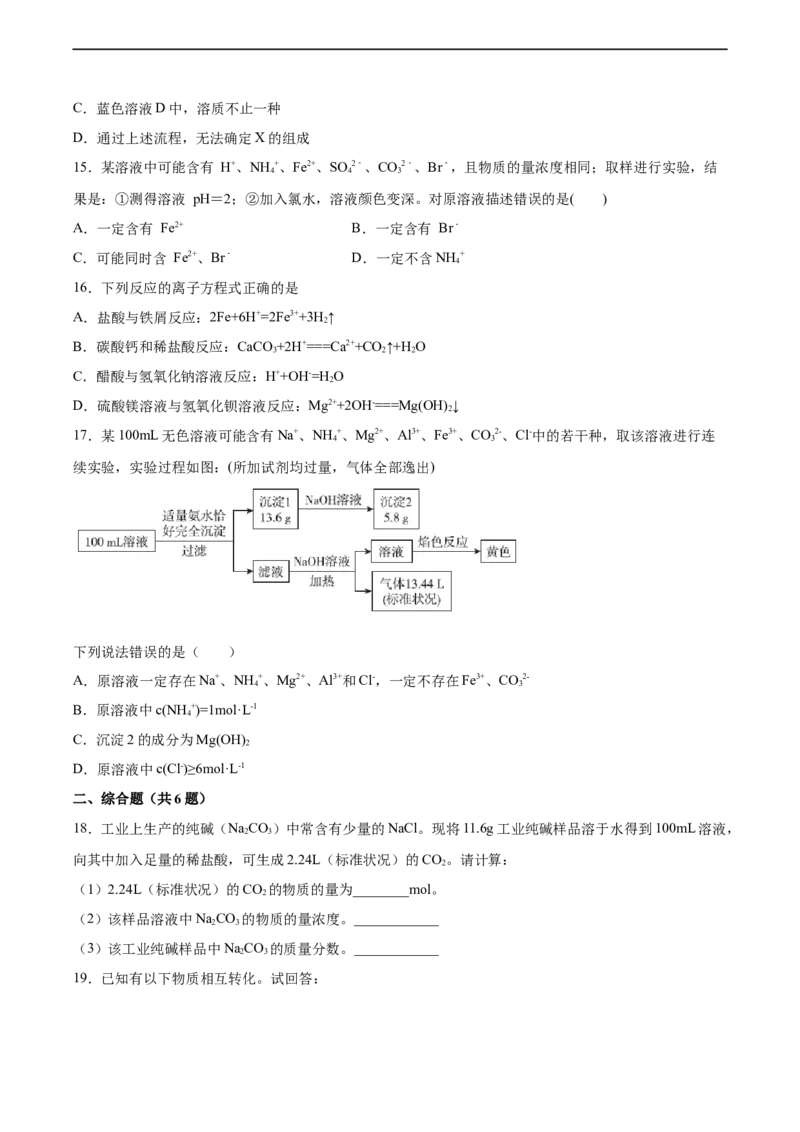
17.某100mL无色溶液可能含有Na+、NH +、Mg2+、Al3+、Fe3+、CO2-、Cl-中的若干种,取该溶液进行连
4 3
续实验,实验过程如图:(所加试剂均过量,气体全部逸出)
下列说法错误的是( )
A.原溶液一定存在Na+、NH +、Mg2+、Al3+和Cl-,一定不存在Fe3+、CO2-
4 3
B.原溶液中c(NH +)=1mol·L-1
4
C.沉淀2的成分为Mg(OH)
2
D.原溶液中c(Cl-)≥6mol·L-1
二、综合题(共6题)
18.工业上生产的纯碱(NaCO)中常含有少量的NaCl。现将11.6g工业纯碱样品溶于水得到100mL溶液,
2 3
向其中加入足量的稀盐酸,可生成2.24L(标准状况)的CO。请计算:
2
(1)2.24L(标准状况)的CO 的物质的量为________mol。
2
(2)该样品溶液中NaCO 的物质的量浓度。____________
2 3
(3)该工业纯碱样品中NaCO 的质量分数。____________
2 3
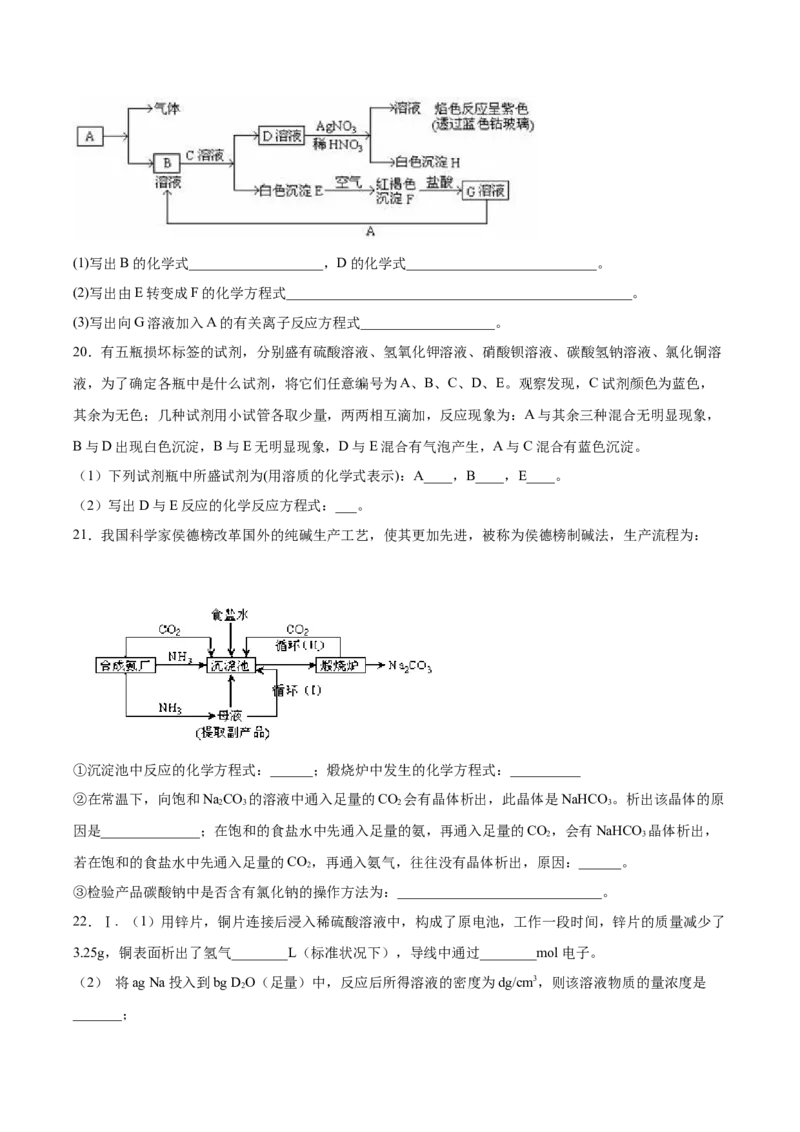
19.已知有以下物质相互转化。试回答:(1)写出B的化学式___________________,D的化学式___________________________。
(2)写出由E转变成F的化学方程式_________________________________________________。
(3)写出向G溶液加入A的有关离子反应方程式___________________。
20.有五瓶损坏标签的试剂,分别盛有硫酸溶液、氢氧化钾溶液、硝酸钡溶液、碳酸氢钠溶液、氯化铜溶
液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E。观察发现,C试剂颜色为蓝色,
其余为无色;几种试剂用小试管各取少量,两两相互滴加,反应现象为:A与其余三种混合无明显现象,
B与D出现白色沉淀,B与E无明显现象,D与E混合有气泡产生,A与C混合有蓝色沉淀。
(1)下列试剂瓶中所盛试剂为(用溶质的化学式表示):A____,B____,E____。
(2)写出D与E反应的化学反应方程式:___。
21.我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:
①沉淀池中反应的化学方程式:______;煅烧炉中发生的化学方程式:__________
②在常温下,向饱和NaCO 的溶液中通入足量的CO 会有晶体析出,此晶体是NaHCO 。析出该晶体的原
2 3 2 3
因是______________;在饱和的食盐水中先通入足量的氨,再通入足量的CO,会有NaHCO 晶体析出,
2 3
若在饱和的食盐水中先通入足量的CO,再通入氨气,往往没有晶体析出,原因:______。
2
③检验产品碳酸钠中是否含有氯化钠的操作方法为:_____________________________。
22.Ⅰ. (1)用锌片,铜片连接后浸入稀硫酸溶液中,构成了原电池,工作一段时间,锌片的质量减少了
3.25g,铜表面析出了氢气________L(标准状况下),导线中通过________mol电子。
(2) 将ag Na投入到bg D O(足量)中,反应后所得溶液的密度为dg/cm3,则该溶液物质的量浓度是
2
_______;Ⅱ. 将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)
⇌
2C(g)+2D
(g)。反应进行到10 s末时,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8
mol,则:
(1)用C表示10 s内正反应的平均反应速率为____________。
(2)反应前A的物质的量浓度是________。
(3)10 s末,生成物D的浓度为________。
23.有A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl 、NaHSO、NaCO 和AgNO 中的一种。已知:
2 4 2 3 3
①A与过量B反应有气体生成;②B与C反应有沉淀生成;③C与D反应有沉淀生成;④D与E反应有
沉淀生成;⑤A与过量E反应有气体生成;⑥在②和③的反应中生成的沉淀是同一种物质。请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是________。
(2)A是________,B是________,C是________,D是________,E是________。
(3)A与过量E反应的离子方程式是________________________________。
(4)A与少量E反应无气体产生,离子反应方程式为_________________________。参考答案
1.D
【详解】
A.钠密度比煤油大不与煤油反应、钠能与氧气反应、与水剧烈反应放出氢气。氢气、易
燃易爆,因此金属钠一般保存在煤油或石蜡中,剩余的钠应放回原瓶,A正确;
B. 将 NaO 加入酚酞溶液后,与水发生反应2NaO + 2H O=4NaOH+ O 、则有大量的气
2 2 2 2 2 2
泡产生、氢氧化钠使溶液变红、过氧化钠具有强氧化性、有漂白性,而导致褪色, B正确;
C.钠元素的焰色反应是黄色,根据焰色为黄色,可以推知物质中一定含有钠元素,C正确;
D. 小苏打是NaHCO 的俗称,具有弱碱性可用于中和过多胃酸、热不稳定性、受热分解
3
产生碳酸钠、水和二氧化碳,可用于烘焙糕点,D错误;
答案选D。
2.C
【详解】
A项,电荷不守恒,铝与氯化铜溶液反应的离子反应为2Al+3Cu2+=2Al3++3Cu,故A错误;
B项,氯化铁是可溶性的强电解质,应写成离子形式,氢氧化钾溶液加入氯化铁溶液中反
应的离子方程式为:3OH-+Fe3+=Fe(OH) ↓,故B错误;
3
C项,石灰石的主要成分CaCO 难溶于水,与稀盐酸反应的离子方程式为:CaCO +2H+=
3 3
Ca2++CO ↑+H O,故C正确;
2 2
D项,离子配比不对,氢氧化钡溶液加入稀硫酸中反应的离子方程式为:Ba2++2OH-+2H+
+SO2-=BaSO ↓+2H O,故D错误;
4 4 2
故答案选C。
3.B
【详解】
A.Na在空气中缓慢氧化生成白色的NaO,故A错误;
2
B.Na在空气中燃烧生成淡黄色固体NaO,故B正确;
2 2
C.Na在空气中燃烧生成淡黄色的NaO,故C错误;
2 2
D.Na在空气中燃烧生成淡黄色的NaO,故D错误;
2 2
故选B。
4.B
【详解】
A.盐酸与次氯酸根离子反应生成氯气,将“84”消毒液(主要成分为次氯酸钠)与洁厕灵
(含有盐酸)合用能够产生氯气,氯气有毒会污染环境,A错误;
B.不管是陶器还是瓷器,其主要原料都是黏士,B正确;
C.泡沫灭火器中加入的主要是碳酸氢钠和硫酸铝溶液,两者混合时发生双水解反应,生
成大量的二氧化碳泡沫,该泡沫能进行灭火,但是,喷出的二氧化碳气体泡沫中一定含有
水,形成电解质溶液,具有一定的导电能力,可能导致触电或电器短路,C错误;
D.生石灰遇水生成氢氧化钙,与碳酸钠反应生成CaCO 和NaOH,其水溶液呈碱性,不
3能改良土壤,D错误;
故选B。
5.C
【详解】
A.向淀粉KI溶液中滴加适量稀硫酸,在空气中放置一段时间后,KI被氧化得到I,溶液
2
呈蓝色: ,A正确;
B.向 固体中滴加蒸馏水,产生无色气体: ,B
正确;
C.向饱和 溶液中通入过量 气体,生成NaHCO ,其溶解度小于 ,在
3
溶液中析出: ,C错误;
D.向滴有酚酞的 溶液中滴加 溶液,有白色沉淀生成,溶液褪色:
,D正确;
故选C。
6.A
【详解】
A.碳酸钠能与酸发生反应生成钠盐、无毒,用碳酸钠等物质可处理废水中的酸,A正确;
B.碳酸氢钠能与醋酸发生反应生成醋酸钠、含有碳酸氢钠的药片是抗酸药,服用时喝些
醋则降低了药效,B错误;
C. 灼烧某白色粉末,火焰成黄色,证明原粉末中有Na+,但没有透过蓝色的钴玻璃观察
火焰,因此不能判断是否存在K+,C错误;
D. 在酒精灯加热条件下, NaHCO 固体能发生分解,NaCO 不分解、D错误;
3 2 3
答案选A。
7.A
【分析】
Ag+与HCl反应生成沉淀,Ba2+与硫酸反应生成沉淀,过滤后Fe3+与NaOH反应生成沉淀,
以此来解答。
【详解】
要从含Al3+、Fe3+、Ba2+、Ag+的溶液中分别沉淀出Fe3+、Ba2+、Ag+,首先加入过量的
HCl,形成AgCl沉淀,过滤后,向滤液中加入过量的HSO ,使Ba2+形成BaSO 沉淀,再
2 4 4
过滤,最后向滤液中加入过量的NaOH溶液,使Fe3+形成Fe(OH) 沉淀,过滤出来,而
3
Al3+与过量NaOH反应生成可溶性的NaAlO 留在溶液中,故试剂的顺序正确的是HCl、
2
HSO 、NaOH,合理选项是A。
2 4
8.A
【分析】
NaCl、 和 的混合固体,加热足够长时间后, 加热分解,得到的是NaCl和 ,质量减少的是二氧化碳和水的质量,利用差量法可以计算出碳酸氢钠
的质量,将剩余固体溶于一定体积的盐酸中,利用产生二氧化碳气体的物质的量计算出总
的碳酸钠的质量,利用碳元素守恒可以计算出原混合物中的碳酸钠的质量,从而得到原混
合物中氯化钠的质量,由此分析。
【详解】
A.3.60gNaCl、 和 的混合固体,加热足够长时间后,固体剩余3.29g,减
少了 ,减少的0.31g为碳酸氢钠分解产生的 与 的质量,设碳
酸氢钠的质量为m,
则 的质量m ,故A正确;
B.标准状况下0.448L二氧化碳的物质的量为 =0.02mol,根据C原子守恒可知,
剩余固体中含有 为0.02mol,根据A项可知,0.84g 的物质的量
=0.01mol,分解后生成0.005mol ,结合C原子守恒可知,原混合物中 的物
质的量为0.015mol,质量为 ,故B错误;
C.根据关系式 可知,生成0.02mol二氧化碳消耗HCl的物质的量为
,所得溶液稀释至100mL,测得所得溶液中 ,即所
得溶液中盐酸的物质的量为 ,则所加盐酸中HCl的物质
的量为0.04mol+0.01mol=0.05mol,故C错误;
D.最终所得溶液中 ,盐酸的物质的量为
,由于溶液中还存在NaCl,即碳酸钠与盐酸反应产生的
氯化钠和原固体混合物中含有的氯化钠,原固体混合物中含有的氯化钠的质量为
3.60g-0.84g-1.59g=1.17g,固体混合物中含有氯化钠的物质的量为 ,根
据 ,碳酸钠与盐酸反应产生的氯化钠的物质的量为0.04mol,最终
所得溶液中等于0.02mol+0.04mol+0.01mol=0.07mol, = =0.7mol/L,故D错误;
答案选A。
9.C
【详解】A. 向固体混合物中加入稀盐酸,NaCO 固体也能与盐酸反应,故A不符;
2 3
B. 向固体混合物中加入CaCl 溶液,CaCl 与NaCO 反应生成CaCO 沉淀,故B不符;
2 2 2 3 3
C. 将固体加热,NaHCO 受热分解生成碳酸钠、水和二氧化碳,故C正确;
3
D. 向其中通入CO,NaHCO 固体与二氧化碳不反应,故D不符;
2 3
故选C。
10.C
【详解】
A.Ca2+、 生成碳酸钙沉淀,Ca2+、 不能大量共存,故不选A;
B.H+、OH-反应生成水,H+、OH-不能大量共存,故不选B;
C.Na+、Fe3+、Cl-、 相互之间不反应,Na+、Fe3+、Cl-、 能大量共存,故选C;
D.H+、 反应生成二氧化碳和水,H+、 不能大量共存,故不选D;
选C。
11.C
【详解】
A.二者反应生成硝酸铁、NO和水,离子方程式为
,故A错误;
B. 的溶解度小于 , 溶液中加入足量NaOH溶液后生成
沉淀和 和 ,即离子方程式为
,故B错误;
C.还原性:I->Fe2+,向含有 的溶液中通入 充分反应,离子方程式:
,故C正确;
D.生成的沉淀物质的量最多时,反应生成硫酸钡、氢氧化铝,恰好氢氧化铝全部沉淀,
发生的离子反应为: ,故D错误;
故答案为C。
12.C
【分析】
“洁厕灵”含有盐酸,即含有大量的氢离子、氯离子。
【详解】
A.ClO-与H+、Cl-发生氧化还原反应,不能大量存在,A与题意不符;
B.OH-与H+反应生成HO,不能大量存在,B与题意不符;
2
C.Na+与H+或Cl-均不反应,能大量存在,C符合题意;
D.Ag+与Cl-反应生成AgCl,不能大量存在,D与题意不符;
答案为C。13.C
【详解】
A.Ba(OH) +HSO =BaSO ↓+2HO的离子方程式为Ba2++SO2-+2OH-
2 2 4 4 2 4
+2H+=BaSO ↓+2H O,故A错误;
4 2
B.BaCO +HSO =BaSO +HO+CO↑的离子方程式为:BaCO +SO2-
3 2 4 4 2 2 3 4
+2H+═BaSO ↓+2H O+CO↑,故B错误;
4 2 2
C.BaCl +HSO =BaSO ↓+2HCl的离子方程式为Ba2++SO2-=BaSO ↓,故C正确;
2 2 4 4 4 4
D.Zn+HSO =ZnSO +H↑的离子方程式为Zn+2H+=Zn2++H ↑,故D错误;
2 4 4 2 2
故答案为C。
14.C
【分析】
由白色沉淀B是由A和氨水生成的但是能溶于NaOH溶液,可知A为氢氧化铝沉淀,则C
为氧化铝1.020g;由蓝色溶液中加入硝酸酸化的硝酸银产生白色沉淀氯化银为11.480g,则
原溶液中含有铜离子的质量=总质量-铝离子的质量-氯离子的质量,可确定X的组成。
【详解】
A.因为白色沉淀B能溶于NaOH溶液,故不能用过量NaOH溶液代替浓氨水,A项错误;
B.“灼烧”时,是氢氧化铝的分解,没有氧气参与,B项错误;
C.蓝色溶液D中含有的溶质有多种, 、 、 、 等,C项正
确;
D.由图示数据并根据原子守恒可知,4.020gX中含有铝离子物质的量为
,含有氯离子物质的量为 ,由化合物应显电
中性可得三种离子物质的量比值为 ,则可得X的化学式为
,D项错误。
故选C。
15.A
【详解】
溶液 pH=2,呈酸性,H+一定有,CO2﹣不能存在,加入氯水,溶液颜色变深,溶液中可
3
能含有Fe2+ 和Br﹣之一或者两者都有,被氯气氧化成Fe3+和Br ,由于溶液中各离子的物质
2
的量浓度相同,符合电荷守恒,如设各离子的浓度是1mol/L,则有可能存在c(H+)
+2c(Fe2+)=2c(SO2﹣)+c(Br﹣),还有可能溶液中只含氢离子和溴离子,但NH +不能存在,故
4 4
答案选A,Fe2+可能存在,符合题意。
16.B
【详解】
A. 铁跟盐酸反应生成亚铁离子,反应的离子方程式 ,故A错误;B. 碳酸钙溶液跟盐酸反应氯化钙、二氧化碳和水,反应的离子方程式为
↑,故B正确;
C. 醋酸是弱酸不能拆成离子,醋酸跟氢氧化钠溶液反应的离子方程式为:
,故C错误;
D. 氢氧化钡跟硫酸镁溶液反应生成硫酸钡和氢氧化镁沉淀,反应的离子方程式为:
↓,故D错误;
故选:B。
17.A
【分析】
无色溶液,不可能有Fe3+,加入氨水,生成沉淀,且沉淀部分溶解于NaOH,则所得沉淀1
一定是Mg(OH) 、Al(OH) 的混合物,一定存在Mg2+、Al3+,Al(OH) 是7.8g,物质的量为
2 3 3
,沉淀2一定是Mg(OH) ,质量为5.8g,物质的量为 ;
2
碳酸根和Mg2+、Al3+不共存,一定不存在CO2-,所得到的滤液中加入氢氧化钠,出现气体,
3
为氨气,NH +的物质的量为 ,开始加入适量氨水沉淀Mg2+、Al3+,加入
4
氨水的物质的量为 ,则一定存在NH +,物质的量为0.1mol;
4
加入了NaOH再进行焰色反应,所以钠离子不能确定。
【详解】
A. 根据原溶液一定存在NH +、Mg2+、Al3+和Cl-,一定不存在Fe3+、CO2-,Na+不能判断,
4 3
A项错误;
B. 100mL溶液存在NH +的物质的量为0.1mol,则c(NH +)=1mol·L-1,B项正确;
4 4
C. 由分析可知沉淀2是Mg(OH) ,C项正确;
2
D. 根据电荷守恒,氯离子的物质的量≥ ,则原溶液
中c(Cl-)≥6mol·L-1,D项正确;
答案选A。
18.0.1 1 mol∙L-1 91.4%
【详解】
⑴2.24L(标准状况)的CO 的物质的量为 ,
2
故答案为:0.1;
⑵根据碳元素守恒,二氧化碳气体物质的量等于碳酸钠物质的量即0.1 mol,该样品溶液中
NaCO 的物质的量浓度
2 3
故答案为:1 mol∙L-1;⑶工业纯碱样品中NaCO 的质量分数 ,
2 3
故答案为:91.4%。
19.FeC1 KC1 4Fe(OH) + O + 2H O = 4Fe(OH) 2Fe3++ Fe = 3Fe2+
2 2 2 2 3
【分析】
D和硝酸酸化的硝酸银溶液产生白色沉淀H,银离子和氯离子反应生成H白色沉淀,则H
是AgCl,D中含有氯离子,混合溶液焰色反应呈紫色,则溶液中含有钾离子,根据元素守
恒知,D为KCl,红褐色沉淀是Fe(OH) ,氢氧化亚铁被氧气氧化生成,则E是Fe(OH) ,
3 2
氢氧化铁和盐酸反应生成氯化铁和水,则G是FeCl ;B和C发生复分解反应生成KCl和
3
Fe(OH) ,氯化铁和A反应生成B,二者发生化合反应,则B为FeCl ,A是Fe,C为
2 2
KOH,结合物质的性质分析解答。
【详解】
(1)通过以上分析知,B的化学式为FeCl ,D的化学式KCl;
2
(2)Fe(OH) 被氧气氧化生成氢氧化铁,反应方程式为4Fe(OH) +O +2H O=4Fe(OH) 。
2 2 2 2 3
(3)G是FeCl 溶液,A是铁,氯化铁和铁反应生成氯化亚铁,离子反应方程式为2Fe3+
3
+Fe=3Fe2+。
20.KOH Ba(NO ) NaHCO 2NaHCO +H SO =Na SO +2H O+2CO↑
3 2 3 3 2 4 2 4 2 2
【分析】
根据题干信息可知,C试剂颜色为蓝色判断C为CuCl 溶液。两两反应,D与B有白色沉
2
淀生成、D与E有气泡产生,则D为HSO 溶液、B为Ba(NO ) 溶液、E为NaHCO 溶液。
2 4 3 2 3
A与C产生蓝色沉淀,则A为KOH溶液。E与B无明显现象,符合实验现象。
【详解】
(1)由上述分析可知,A为KOH溶液、B为Ba(NO ) 溶液、E为NaHCO 溶液,
3 2 3
故答案为KOH;Ba(NO );NaHCO ;
3 2 3
(2)D为HSO 溶液,E为NaHCO 溶液,硫酸与碳酸氢钠反应生成硫酸钠、二氧化碳和
2 4 3
水,D与E反应化学反应方程式:2NaHCO +H SO =Na SO +2H O+2CO↑,
3 2 4 2 4 2 2
答案为:2NaHCO +H SO =Na SO +2H O+2CO↑。
3 2 4 2 4 2 2
21.
,碳酸氢钠的溶解度小于碳酸钠,故会有碳酸氢钠晶体析出
在水中的溶解度很小,产生 的量太少,不会析出晶体 取少量产品于试管
中,加水溶解,先加足量硝酸酸化,再加入硝酸银溶液,若有白色沉淀生成,则产品中含
有氯化钠
【分析】
向食盐水中先通氨气,再通二氧化碳,会析出碳酸氢钠晶体:
,碳酸氢钠受热分解得到碳酸钠。
【详解】① 在沉淀池中,氨气、二氧化碳、氯化钠、和水发生反应生成碳酸氢钠和氯化铵,方程
式: ,碳酸氢钠进入煅烧炉分解,方程式:
,
故答案为: ;
;
② 向饱和 溶液中通入 ,发生反应: ,
由于碳酸氢钠的溶解度小于碳酸钠,故会有碳酸氢钠晶体析出; 在水中的溶解度
很小,先通 得到的溶液中 含量很少,所以产生 的量很少,不会析出
晶体;
故答案为: ,碳酸氢钠的溶解度小于碳酸钠,故会有碳
酸氢钠晶体析出; 在水中的溶解度很小,产生 的量太少,不会析出晶体;
③ 检验碳酸钠中的氯化钠,首先要将固体溶于水,然后用硝酸酸化除掉碳酸根,
然后加硝酸银检验氯离子;
故答案为:取少量产品于试管中,加水溶解,先加足量硝酸酸化,再加入硝酸银溶液,
若有白色沉淀生成,则产品中含有氯化钠。
22.1.12 0.1 mol/L 0.04mol•L-1•s-1 1.5mol•L-1 0.4mol•L-1
【详解】
Ⅰ.(1)用锌片、铜片连接后浸入稀硫酸溶液中,构成了原电池,锌为负极,电极反应为:
Zn-2e-=Zn2+,铜为正极,电极反应为2H++2e-=H ↑,锌片的质量减少了3.25克,则物质的量
2
为 =0.05mol,转移的电子的物质的量为n(e-)=2n(Zn)=2n(H )=2×0.05mol=0.1mol,
2
则V(H )=0.05mol×22.4L/mol=1.12L,故答案为:1.12;0.1;
2
(2)将ag Na投入到bg D O(足量)中,发生2Na+2DO=2NaOD+D ↑,ag Na的物质的量为
2 2 2
= mol,生成的氢氧化钠为 mol,D 的物质的量为 mol,质量为
2
mol×4g/mol= g,反应后溶液的质量为ag+bg- g=(a+b- )g,溶液的体积为
= cm3,则该溶液物质的量浓度c= = =
mol/L,故答案为: mol/L;Ⅱ.(1)v(C)= =0.04mol•L-1•s-1,故答案为:0.04mol•L-1•s-1;
(2)3A(g)+B(g)⇌2C(g)+2D(g)。反应进行到10 s末时,测得A的物质的量为1.8 mol,C的
物质的量为0.8 mol,则反应的A为1.2mol,反应前A的物质的量浓度是
=1.5mol•L-1,故答案为:1.5mol•L-1;
(3)3A(g)+B(g)⇌2C(g)+2D(g)。反应进行到10 s末时,测得C的物质的量为0.8 mol,则生
成的D为0.8 mol ,10 s末,生成物D的浓度为 =0.4mol•L-1,故答案为:
0.4mol•L-1 。
23.AgCl Na CO HCl AgNO BaCl NaHSO +2H+=H O+
2 3 3 2 4 2
CO↑ +H+=
2
【分析】
①⑤反应中有气体,气体只能为 ,则A为NaCO,B、E分别为HCl、NaHSO 中的
2 3 4
一种,那么C、D分别为AgNO、BaCl 中的一种,在②和③的反应中生成的沉淀是同一种
3 2
物质,沉淀应为AgCl,则C为AgNO,B为HCl,D为BaCl ,故E为NaHSO,以此解答
3 2 4
该题。
【详解】
(1)在②和③的反应中生成的沉淀的化学式为AgCl;
(2)由上述分析可知,A为NaCO,B为HCl,C为AgNO,D为BaCl ,E为NaHSO;
2 3 3 2 4
(3)A与过量E反应的离子方程式为: +2H+=H O+CO↑;
2 2
(4) A与少量E反应无气体产生,离子反应方程式为: +H+= 。