文档内容
1.书写方法
2.书写关键——识记常见氧化剂、还原剂及产物预测
(1)常见的氧化剂及还原产物预测
氧化剂 还原产物预测
Mn2+(酸性);MnO (中性);
2
KMnO
4
MnO(碱性)
KCr O(酸性) Cr3+
2 2 7
浓硝酸 NO
2
稀硝酸 NO
X(卤素单质) X-
2
HO OH-(碱性);HO(酸性)
2 2 2
NaO NaOH(或NaCO)
2 2 2 3
NaClO(或ClO-) Cl-、Cl
2
NaClO Cl、ClO
3 2 2
PbO Pb2+
2
(2)常见的还原剂及氧化产物预测
还原剂 氧化产物预测
Fe2+ Fe3+(酸性);Fe(OH) (碱性)
3
SO (或HSO 、SO) SO
2 2 3S2-(或HS) S、SO (或SO)、SO
2 2
HC O CO
2 2 4 2
HO O
2 2 2
I-(或HI) I、IO
2
CO CO
2
金属单质(Zn、
Zn2+、Fe2+(与强氧化剂反应生成Fe3+)、Cu2+
Fe、Cu等)
1.[2021·全国甲卷,26(2)]碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方
面。回答下列问题:
以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成碘化物;再
3 2 3 3
向混合溶液中加入 NaIO 溶液,反应得到 I 。上述制备 I 的总反应的离子方程式为
3 2 2
________________________________________________________________________。
答案 2IO+5HSO===I+5SO+3H++HO
2 2
解析 先向NaIO 溶液中加入计量的NaHSO,生成碘化物即含I-的物质;再向混合溶液(含
3 3
I-)中加入NaIO 溶液,反应得到I ,上述制备I 的两个反应中I-为中间产物,总反应为IO
3 2 2
与HSO发生氧化还原反应,生成SO和I,根据得失电子守恒、电荷守恒及原子守恒配平离
2
子方程式即可得:2IO+5HSO===I+5SO+3H++HO。
2 2
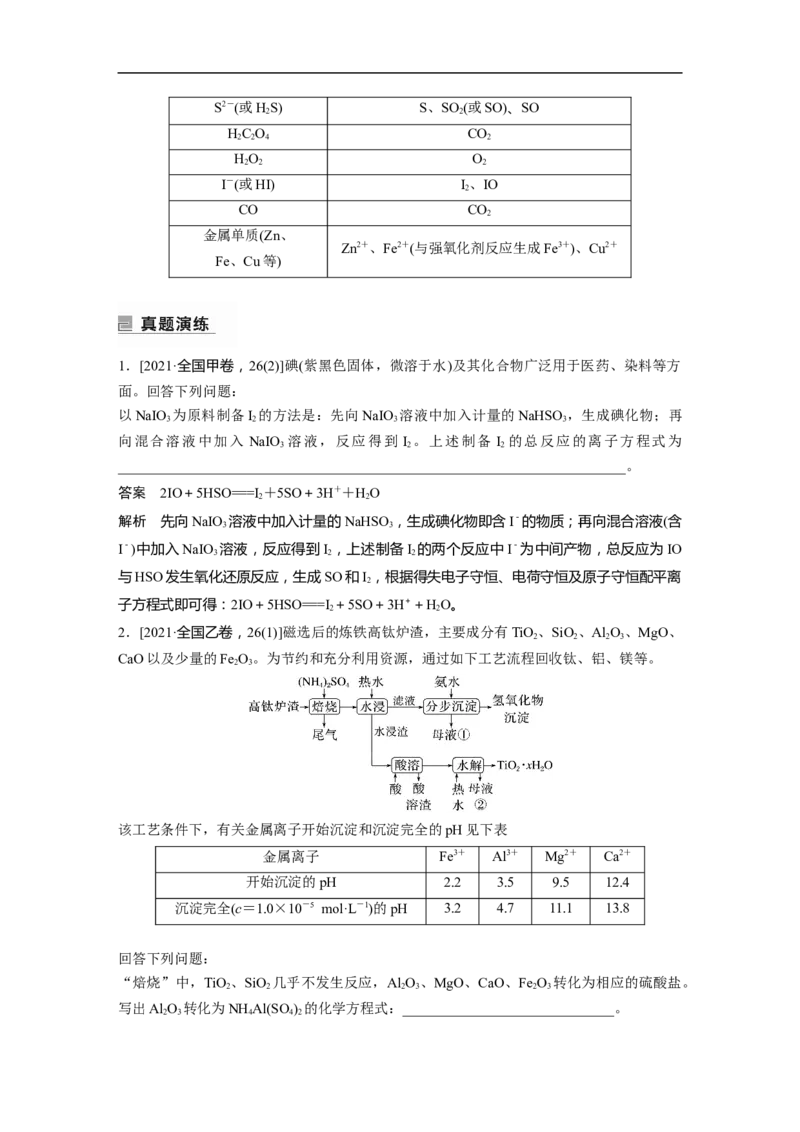
2.[2021·全国乙卷,26(1)]磁选后的炼铁高钛炉渣,主要成分有TiO、SiO、Al O、MgO、
2 2 2 3
CaO以及少量的Fe O。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×10-5 mol·L-1)的pH 3.2 4.7 11.1 13.8
回答下列问题:
“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相应的硫酸盐。
2 2 2 3 2 3
写出Al O 转化为NH Al(SO ) 的化学方程式:______________________________。
2 3 4 4 2答案 Al O+4(NH )SO =====2NH Al(SO )+6NH ↑+3HO↑
2 3 4 2 4 4 4 2 3 2
解析 氧化铝转化为硫酸铝铵发生的反应为氧化铝、硫酸铵在高温条件下反应生成硫酸铝铵、
氨气和水,反应的化学方程式为Al O+4(NH )SO =====2NH Al(SO )+6NH ↑+3HO↑。
2 3 4 2 4 4 4 2 3 2
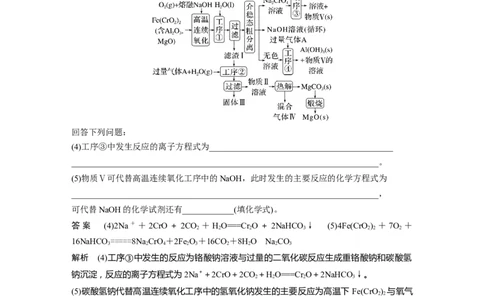
3.[2021·河北,15(4)(5)]绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设
计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气
以外的其他原料,不产生废弃物,实现了 Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺
流程如图:
回答下列问题:
(4)工序③中发生反应的离子方程式为___________________________________________
________________________________________________________________________。
(5)物质Ⅴ可代替高温连续氧化工序中的NaOH,此时发生的主要反应的化学方程式为
________________________________________________________________________,
可代替NaOH的化学试剂还有____________(填化学式)。
答案 (4)2Na++2CrO+2CO +HO===Cr O+2NaHCO ↓ (5)4Fe(CrO ) +7O +
2 2 2 3 2 2 2
16NaHCO =====8NaCrO+2Fe O+16CO+8HO NaCO
3 2 4 2 3 2 2 2 3
解析 (4)工序③中发生的反应为铬酸钠溶液与过量的二氧化碳反应生成重铬酸钠和碳酸氢
钠沉淀,反应的离子方程式为2Na++2CrO+2CO+HO===Cr O+2NaHCO ↓。
2 2 2 3
(5)碳酸氢钠代替高温连续氧化工序中的氢氧化钠发生的主要反应为高温下 Fe(CrO ) 与氧气
2 2
和碳酸氢钠反应生成铬酸钠、氧化铁、二氧化碳和水,反应的化学方程式为 4Fe(CrO ) +
2 2
7O +16NaHCO =====8NaCrO +2Fe O +16CO +8HO;若将碳酸氢钠换为碳酸钠也能发
2 3 2 4 2 3 2 2
生类似的反应。
4.[2021·湖南,17(5)(6)节选]Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,
2 3 3
铈(Ce)主要以CePO 形式存在,还含有SiO 、Al O 、Fe O 、CaF 等物质。以独居石为原料
4 2 2 3 2 3 2
制备Ce (CO)·nHO的工艺流程如下:
2 3 3 2回答下列问题:
(5)“沉铈”过程中,生成Ce (CO)·nHO的离子方程式为__________________________。
2 3 3 2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电
4 2 3 6 12 6 4
极材料LiFePO ,同时生成CO和HO,该反应的化学方程式为_______________________
4 2
________________________________________________________________________。
答案 (5)6HCO+2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑ (6)6FePO +3LiCO +
2 2 3 3 2 2 4 2 3
C H O=====9CO↑+6HO↑+6LiFePO
6 12 6 2 4
解析 (5)用碳酸氢铵“沉铈”,则结合原子守恒、电荷守恒可知,生成 Ce (CO)·nHO的
2 3 3 2
离子方程式为6HCO+2Ce3++(n-3)H O===Ce (CO)·nHO+3CO↑。
2 2 3 3 2 2
(6)由在高温条件下,LiCO 、葡萄糖(C H O)和FePO 可制备电极材料LiFePO ,同时生成
2 3 6 12 6 4 4
CO和HO可知,该反应中Fe价态降低,C价态部分降低、部分升高,结合得失电子守恒、
2
原子守恒可知该反应的化学方程式为6FePO +3LiCO +C H O=====9CO↑+6HO↑+
4 2 3 6 12 6 2
6LiFePO 。
4
1.高锰酸钾(KMnO)是一种常用氧化剂,主要用于化工、防腐及制药工业等。以软锰矿(主
4
要成分为MnO )为原料生产高锰酸钾的工艺流程图如下:
2
“平炉”中发生反应的化学方程式为_____________________________________________。
答案 2MnO +4KOH+O===2KMnO +2HO
2 2 2 4 2
解析 根据流程图可知,在“平炉”中MnO 、KOH、O 在加热时会反应生成KMnO ,根
2 2 2 4
据原子守恒、得失电子守恒可得发生反应的化学方程式为2MnO +O +4KOH===2KMnO
2 2 2 4
+2HO。
2
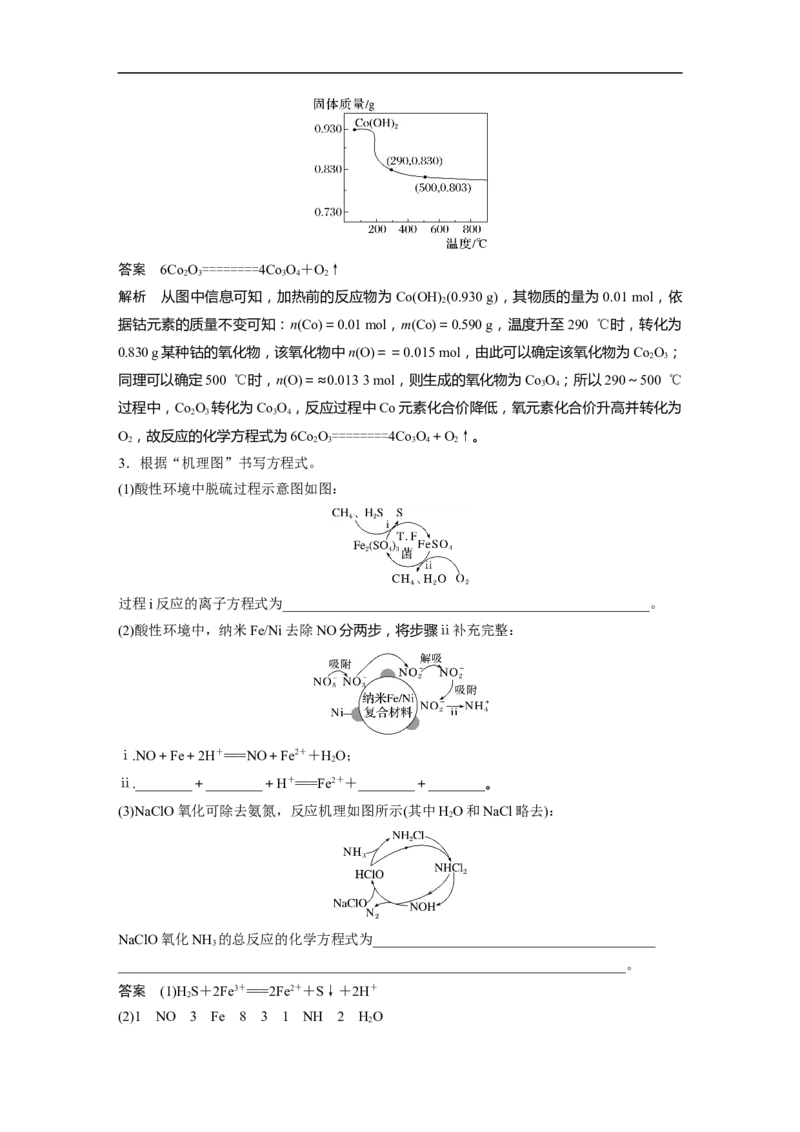
2.在空气中加热Co(OH) ,使其转化为钴的氧化物。加热过程中,固体质量与温度的关系
2
如下图所示。290~500 ℃,发生反应的化学方程式为________________________________。答案 6Co O========4Co O+O↑
2 3 3 4 2
解析 从图中信息可知,加热前的反应物为Co(OH) (0.930 g),其物质的量为0.01 mol,依
2
据钴元素的质量不变可知:n(Co)=0.01 mol,m(Co)=0.590 g,温度升至290 ℃时,转化为
0.830 g某种钴的氧化物,该氧化物中n(O)==0.015 mol,由此可以确定该氧化物为Co O;
2 3
同理可以确定500 ℃时,n(O)=≈0.013 3 mol,则生成的氧化物为Co O;所以290~500 ℃
3 4
过程中,Co O 转化为Co O ,反应过程中Co元素化合价降低,氧元素化合价升高并转化为
2 3 3 4
O,故反应的化学方程式为6Co O========4Co O+O↑。
2 2 3 3 4 2
3.根据“机理图”书写方程式。
(1)酸性环境中脱硫过程示意图如图:
过程i反应的离子方程式为____________________________________________________。
(2)酸性环境中,纳米Fe/Ni去除NO分两步,将步骤ⅱ补充完整:
ⅰ.NO+Fe+2H+===NO+Fe2++HO;
2
ⅱ.________+________+H+===Fe2++________+________。
(3)NaClO氧化可除去氨氮,反应机理如图所示(其中HO和NaCl略去):
2
NaClO氧化NH 的总反应的化学方程式为________________________________________
3
________________________________________________________________________。
答案 (1)H S+2Fe3+===2Fe2++S↓+2H+
2
(2)1 NO 3 Fe 8 3 1 NH 2 HO
2(3)2NH +3NaClO===N+3HO+3NaCl
3 2 2