文档内容
2025届高三化学一轮专题复习讲义(04)
专题一 基本概念
1-4 新情境下化学方程式的书写(1课时)
【复习目标】
1.理解实际生活或生产中涉及的化学情境,能写出对应的化学或者离子方程式。
2.掌握化学物质在具体反应中的变化及其变化规律。
【重点突破】
1.能根据新情境书写化学方程式或者离子方程式。
2.掌握书写新情境方程式书写的方法和步骤。
【真题再现】
题型一 新情境化学方程式的书写
例1.历年江苏高考题组合I
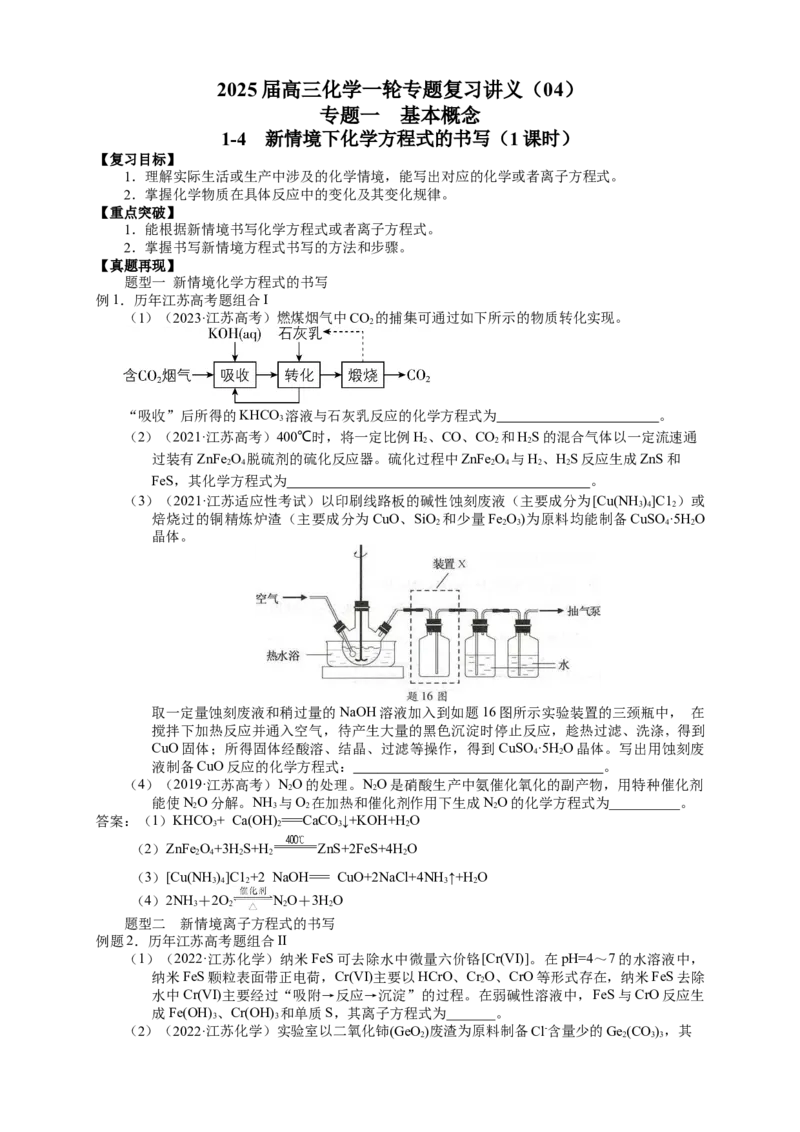
(1)(2023·江苏高考)燃煤烟气中CO 的捕集可通过如下所示的物质转化实现。
2
“吸收”后所得的KHCO 溶液与石灰乳反应的化学方程式为 。
3
(2)(2021·江苏高考)400℃时,将一定比例H、CO、CO 和HS的混合气体以一定流速通
2 2 2
过装有ZnFe O 脱硫剂的硫化反应器。硫化过程中ZnFe O 与H、HS反应生成ZnS和
2 4 2 4 2 2
FeS,其化学方程式为 。
(3)(2021·江苏适应性考试)以印刷线路板的碱性蚀刻废液(主要成分为[Cu(NH )]C1 )或
3 4 2
焙烧过的铜精炼炉渣(主要成分为CuO、SiO 和少量Fe O)为原料均能制备CuSO ·5HO
2 2 3 4 2
晶体。
取一定量蚀刻废液和稍过量的NaOH溶液加入到如题16图所示实验装置的三颈瓶中, 在
搅拌下加热反应并通入空气,待产生大量的黑色沉淀时停止反应,趁热过滤、洗涤, 得到
CuO固体;所得固体经酸溶、结晶、过滤等操作,得到 CuSO ·5HO晶体。写出用蚀刻废
4 2
液制备CuO反应的化学方程式: 。
(4)(2019·江苏高考)NO的处理。NO是硝酸生产中氨催化氧化的副产物,用特种催化剂
2 2
能使NO分解。NH 与O 在加热和催化剂作用下生成NO的化学方程式为__________。
2 3 2 2
答案:(1)KHCO + Ca(OH) ===CaCO ↓+KOH+H O
3 2 3 2
(2)ZnFe O+3H S+H ZnS+2FeS+4H O
2 4 2 2 2
(3)[Cu(NH )]C1 +2 NaOH=== CuO+2NaCl+4NH ↑+H O
3 4 2 3 2
(4)2NH +2O NO+3HO
3 2 2 2
题型二 新情境离子方程式的书写
例题2.历年江苏高考题组合II
(1)(2022·江苏化学)纳米FeS可去除水中微量六价铬[Cr(VI)]。在pH=4~7的水溶液中,
纳米FeS颗粒表面带正电荷,Cr(VI)主要以HCrO、Cr O、CrO等形式存在,纳米FeS去除
2
水中Cr(VI)主要经过“吸附→反应→沉淀”的过程。在弱碱性溶液中,FeS与CrO反应生
成Fe(OH) 、Cr(OH) 和单质S,其离子方程式为_______。
3 3
(2)(2022·江苏化学)实验室以二氧化铈(GeO )废渣为原料制备Cl-含量少的Ge(CO),其
2 2 3 3部分实验过程如下:
“酸浸”时GeO 与HO 反应生成Ge3+并放出O,该反应的离子方程式为 。
2 2 2 2
(3)(2021·江苏化学)将一定量软锰矿粉与NaSO 、HSO 溶液中的一种配成悬浊液,加入
2 3 2 4
到三颈瓶中(图1),70℃下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液
漏斗中的溶液是___;MnO 转化为Mn2+的离子方程式为 。
2
(4)(2021.江苏适应性考试)向酸性废水中加入适量 Fe (SO ) 溶液,废水中的氨氮转化为
2 4 3
NH Fe (SO )(OH) 沉淀,该反应的离子方程式为 。在 pH=9 的水
4 3 4 2 6
溶液中CrO2-与HS-反应的离子方程式为 。
4
(5)(2020·江苏化学)将FeSO 溶液与氨水−NH HCO 混合溶液反应,生成FeCO 沉淀,该
4 4 3 3
反应的离子方程式为 。NaClO溶液可由低温下将Cl 缓慢通入NaOH溶
2
液中而制得,制备 NaClO的离子方程式为 。
答案:(1)
(2)2CeO+H O+6H+===2Ce3++O ↑+4H O
2 2 2 2 2
(3) ①HSO 溶液 ② MnO +SO +2H+===Mn2++SO +H O
2 4 2 2
(4)NH ++3Fe3++2SO2-+6H O===NH Fe (SO )(OH) ↓+6H+
4 4 2 4 3 4 2 6
2CrO2-+3HS-+5H O===2Cr(OH) ↓+3S↓+7OH-
4 2 3
(5)Fe2++HCO+ NH ·H O===FeCO↓+ NH + + H O
3 2 3 4 2
或Fe2+ + HCO ─ + NH ===FeCO↓+NH+ Cl+2OH-===Cl-+ClO-+H O
3 3 3 4 2 2
【知能整合】
题型三 新情境非氧化还原反应离子方程式的书写
例4.历年江苏高考题组合III
(1)(2022·江苏高考) “Fe—HCO -—HO”“热循环制氢和甲酸”的原理为:在密闭容器中,
3 2
铁粉与吸收CO 制得的NaHCO 溶液反应,生成H、HCOONa和Fe O;Fe O 再经生物柴
2 3 2 3 4 3 4
油副产品转化为Fe。实验中发现,在300℃时,密闭容器中NaHCO 溶液与铁粉反应,反
3
应初期有FeCO 生成并放出H,该反应的离子方程式为 。
3 2
(2)(2020·江苏高考)氨水吸收SO 。向氨水中通入少量SO ,主要反应的离子方程式:
2 2
________________________。
(3)(2019·江苏高考)将氨水和NH HCO 溶液混合,可制得(NH )CO 溶液,其离子方程式:
4 3 4 2 3
。
答案:(1)(2)2NH +H O+SO ====SO+2NH 或 2 NH ·H O+SO===SO+2NH+HO
3 2 2 3 2 2 2
(3)HCO+ NH ·H O===NH+CO+H O 或 HCO+ NH ·H O===NH+CO+H O
3 2 2 3 2 2
【体系再构】
【随堂反馈】
基础训练
1.按要求完成下列方程式。
(1)已知在酸性介质中FeSO 能将+6价铬还原成+3价铬。写出Cr O与FeSO 溶液在酸性条
4 2 4
件下反应的离子方程式:________________________________。
(2)用NaClO—NaOH溶液氧化AgNO ,制得高纯度的纳米级Ag O 。写出该反应的离子方
3 2 2
程式:_______________________________________________________。
(3)KMnO 氧化废水中Mn2+生成MnO 的离子方程式为__________________________。
4 2
(4)温度高于200 ℃时,硝酸铝完全分解成氧化铝和两种气体(其体积比为4∶1),该反应的
化学方程式:______________________________________________________
(5)利用钴渣[含Co(OH) 、Fe(OH) 等]制备钴氧化物的工艺流程如下:
3 3
Co(OH) 溶解还原反应的离子方程式为____________________________________。
3
2.按要求书写方程式:
(1)已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。在一氧化
还原反应的体系中,共有KCl、Cl、HSO 、HO、KMnO 、MnSO 、KSO 七种物质。
2 2 4 2 4 4 2 4
①写出一个包含上述七种物质的氧化还原反应方程式,并配平。
______________________________________________________________________。
②在反应后的溶液中加入NaBiO(不溶于冷水),溶液又变为紫红色,BiO反应后变为无
3
色的Bi3+。写出该实验中涉及反应的离子方程式_____________________________。
(2)KMnO 的氧化性随pH的减小而增大,在酸性介质中还原产物是Mn2+;在中性或碱性介
4
质中还原产物主要是MnO 。三氯乙烯(C HCl )是地下水有机污染物的主要成分,研究显示
2 2 3
在地下水中加入KMnO 溶液可将其中的三氯乙烯除去,氧化产物只有CO ,写出反应的
4 2
化学方程式_________________________________________。
(3)已知:①MnO+e-→MnO(绿色)(强碱性条件)
②MnO+8H++5e-→Mn2+(无色)+4HO(强酸性条件)
2
将KMnO 溶液滴入NaOH溶液中微热,得到透明的绿色溶液,写出反应的离子方程式
4
_____________________________________________________________。
3.从炼钢粉尘(主要含FeO、FeO 和ZnO)中提取锌的流程如下:
3 4 2 3
“盐浸”过程ZnO转化为 ,并有少量Fe2+和Fe3+浸出。下列说法错误的是
A.“盐浸”过程若浸液pH下降,需补充NH
3
B.“滤渣”的主要成分为Fe(OH)
3C.“沉锌”过程发生反应
D.应合理控制(NH )S用量,以便滤液循环使用
4 2
拓展训练
4 .向所得Fe(OH) 沉淀中加入NaNO 溶液,可制得纳米Fe O,同时产生NO。该反应的离子方程
2 2 3 4
式:____________________________________________________。
5.尿素[CO(NH)]还原法。NO和NO 以物质的量之比1∶1与CO(NH) 反应生成无毒气体的化学
2 2 2 2 2
方程式:______________________________________。
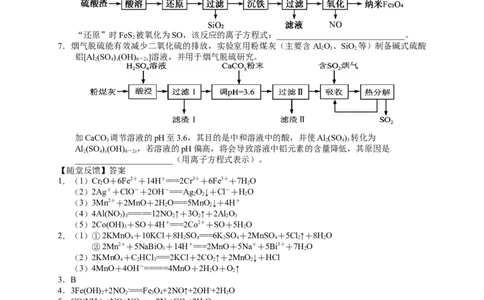
6.利用硫酸渣(主要含Fe O、SiO)制备纳米Fe O 的工艺流程如图:
2 3 2 3 4
“还原”时FeS 被氧化为SO,该反应的离子方程式:______________________________。
2
7.烟气脱硫能有效减少二氧化硫的排放,实验室用粉煤灰(主要含Al O 、SiO 等)制备碱式硫酸
2 3 2
铝[Al(SO )(OH) ]溶液,并用于烟气脱硫研究。
2 4 x 6-2x
加CaCO 调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al (SO ) 转化为
3 2 4 3
Al (SO )(OH) ,若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是
2 4 x 6-2x
_______________________(用离子方程式表示)。
【随堂反馈】答案
1.(1)Cr O+6Fe2++14H+===2Cr3++6Fe3++7HO
2 2
(2)2Ag++ClO-+2OH-===Ag O↓+Cl-+HO
2 2 2
(3)3Mn2++2MnO+2HO===5MnO↓+4H+
2 2
(4)4Al(NO )=====12NO ↑+3O↑+2Al O
3 3 2 2 2 3
(5)2Co(OH) +SO+4H+===2Co2++SO+5HO
3 2
2.(1)①2KMnO +10KCl+8HSO ===6K SO +2MnSO +5Cl↑+8HO
4 2 4 2 4 4 2 2
②2Mn2++5NaBiO+14H+===2MnO+5Na++5Bi3++7HO
3 2
(2)2KMnO +C HCl ===2KCl+2CO↑+2MnO ↓+HCl
4 2 3 2 2
(3)4MnO+4OH-=====4MnO+2HO+O↑
2 2
3.B
4.3Fe(OH) +2NO-===Fe O+2NO↑+2OH-+2H O
2 2 3 4 2
5.CO(NH)+NO+NO ===2N +CO +2H O
2 2 2 2 2 2
6.14Fe3++FeS +8H O===15Fe2++2SO+16H+
2 2
7.3CaCO +2Al3++3SO+3HO===2Al(OH) ↓+3CaSO+3CO↑
3 2 3 4 2
【课后作业】
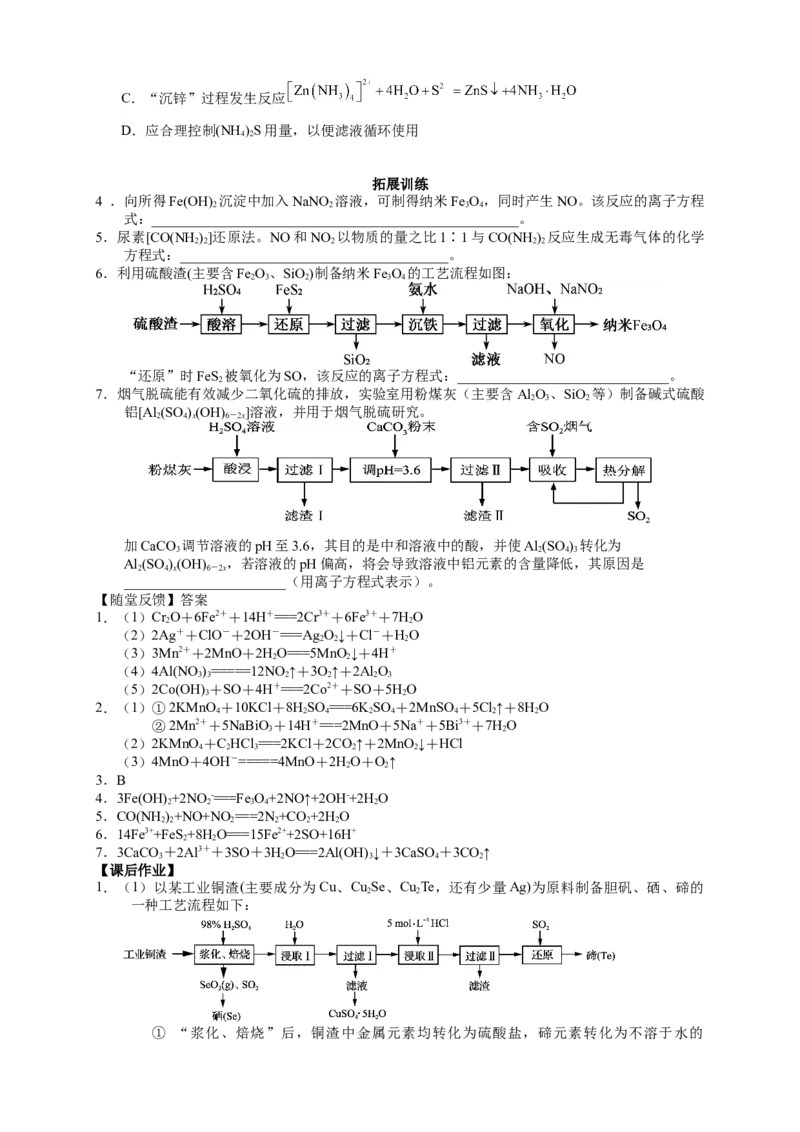
1.(1)以某工业铜渣(主要成分为Cu、Cu Se、Cu Te,还有少量Ag)为原料制备胆矾、硒、碲的
2 2
一种工艺流程如下:
① “浆化、焙烧”后,铜渣中金属元素均转化为硫酸盐,碲元素转化为不溶于水的TeO 。Cu Se与浓硫酸反应的化学方程式为_______________________________。
2 2
② “浸取Ⅱ”后,TeO 转化为TeCl,则“还原”过程反应的离子方程式为____________。
2
(2)利用软锰矿( 主要成分为MnO ,含铁的化合物等杂质)和闪锌矿(主要成分ZnS)制得硫酸
2
锰的流程如下:
①“酸浸”时,为了缩短浸取时间,常加入少量 FeSO 溶液,FeSO 的作用可能是
4 4
; MnO 、 ZnS 及 硫 酸 反 应 转 变 为 两 种 硫 酸 盐 的 化 学 方 程 式 为
2
。
②在强酸性条件下加入MnO 氧化Fe2+ 的离子方程式为 。
2
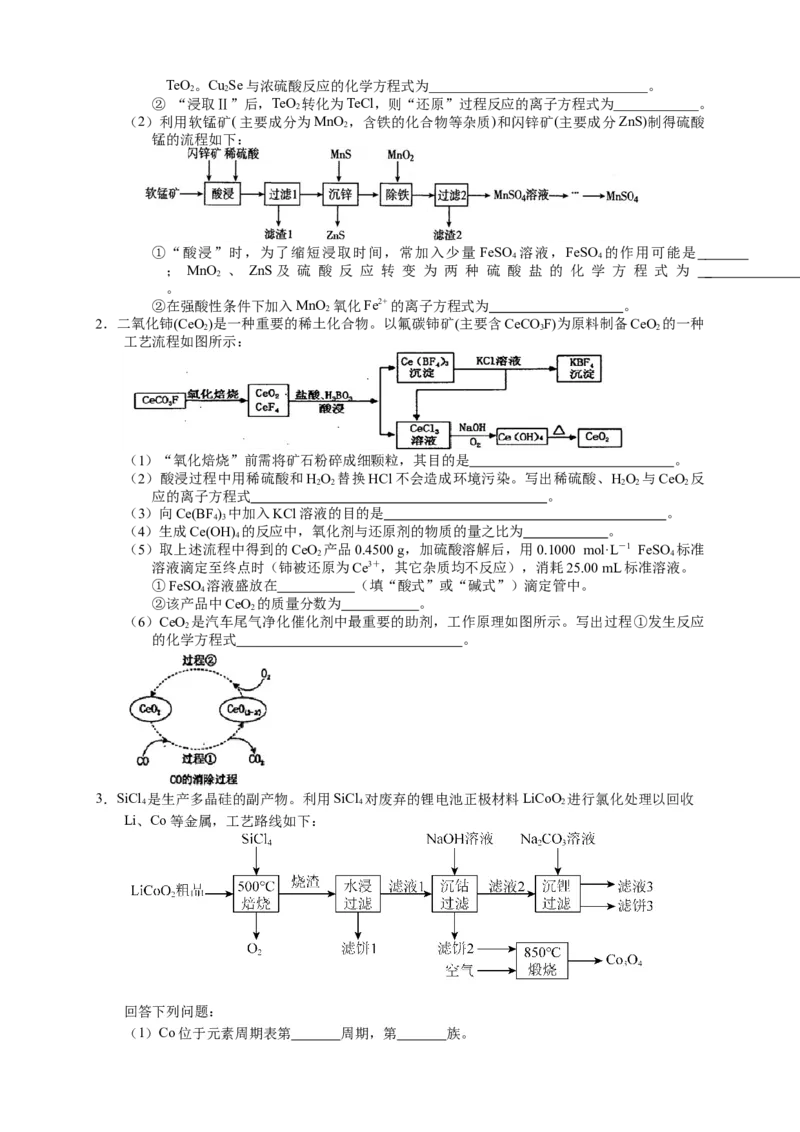
2.二氧化铈(CeO)是一种重要的稀土化合物。以氟碳铈矿(主要含CeCO F)为原料制备CeO 的一种
2 3 2
工艺流程如图所示:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是 。
(2)酸浸过程中用稀硫酸和HO 替换HCl不会造成环境污染。写出稀硫酸、HO 与CeO 反
2 2 2 2 2
应的离子方程式 。
(3)向Ce(BF ) 中加入KCl溶液的目的是 。
4 3
(4)生成Ce(OH) 的反应中,氧化剂与还原剂的物质的量之比为 。
4
(5)取上述流程中得到的CeO 产品0.4500 g,加硫酸溶解后,用0.1000 mol·L-1 FeSO 标准
2 4
溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不反应),消耗25.00 mL标准溶液。
①FeSO 溶液盛放在 (填“酸式”或“碱式”)滴定管中。
4
②该产品中CeO 的质量分数为 。
2
(6)CeO 是汽车尾气净化催化剂中最重要的助剂,工作原理如图所示。写出过程①发生反应
2
的化学方程式 。
3.SiCl 是生产多晶硅的副产物。利用SiCl 对废弃的锂电池正极材料LiCoO 进行氯化处理以回收
4 4 2
Li、Co等金属,工艺路线如下:
回答下列问题:
(1)Co位于元素周期表第 周期,第 族。(2)烧渣是LiCl、CoCl 和SiO 的混合物,“500℃焙烧”后剩余的SiCl 应先除去,否则水浸
2 2 4
时会产生大量烟雾,用化学方程式表示其原因 。
4.闭环循环有利于提高资源利用率和实现绿色化学的目标。利用氨法浸取可实现废弃物铜包钢的
有效分离,同时得到的CuCl可用于催化、医药、冶金等重要领域。工艺流程如下:
已知:室温下的K (CuCl)=10-6.8。
sp
回答下列问题:
(1)首次浸取所用深蓝色溶液①是由铜毛丝、足量液氨、空气和盐酸反应得到,该溶液主要
成分为 (填化学式)。
(2)滤渣的主要成分为 (填化学式)。
(3)浸取工序的产物为[Cu(NH )]Cl,该工序发生反应的化学方程式为 。浸取后滤液
3 2
的一半经氧化工序可得深蓝色溶液①,氧化工序发生反应的离子方程式为 。
(4)浸取工序宜在30~40℃之间进行,当环境温度较低时,浸取液再生后不需额外加热即可
进行浸取的原因是 。
(5)补全中和工序中主反应的离子方程式[Cu(NH )]++2H++Cl-==== + 。
3 2
【课后作业】答案
1.(1)①Cu Se + 6HSO ===== 2CuSO + SeO↑+ 4SO ↑ + 6HO
2 2 4 4 2 2 2
②TeCl+ 2SO + 4HO===Te + 2SO+ 6Cl-+ 8H+
2 2
(2)①催化剂 4MnO +ZnS+4H SO =4MnSO + ZnSO+4H O
2 2 4 4 4 2
②MnO +2Fe2++4H+=Mn2++2Fe3++2H O
2 2
2.(1)增大固体与气体的接触面积,增大反应速率,提高原料利用率
(2)HO + 2CeO + 6H+ = 2Ce3+ + 4H O + O↑
2 2 2 2 2
(3)避免三价铈以Ce(BF ) 沉淀的形式损失或除去BF-或提高CeCl 的产率
4 3 4 3
(4)1∶4
(5)①酸式 ②95.56%
(6)xCO + CeO = CeO + xCO
2 (2-x) 2
3.(1)4 Ⅷ (2)
4.(1)
(2)Fe
(3)
(4)盐酸和液氨反应放热
(5)CuCl↓ NH