文档内容
章末综合检测(七)
(时间:45分钟 分值:100分)
一、选择题(本题包括10小题,每小题6分,共60分)
1.下列食品添加剂中,其使用目的与反应速率有关的是( )
A.抗氧化剂 B.调味剂
C.着色剂 D.增稠剂
解析:选A。相对于食品,抗氧化剂可以更快地被氧气氧化,从而降低了包装袋中氧气的
浓度,减缓食品被氧化的速率。
2.在可逆反应中,改变下列条件一定能加快反应速率的是( )
A.增大反应物的量 B.升高温度
C.增大压强 D.分离出生成物
解析:选B。A项,若反应物为固体,则增大反应物的量,反应速率不变;C项,增大压强,
若参加反应的气体的浓度不变,则反应速率不变,如在恒容条件下充入惰性气体;D项,分离
出生成物,反应速率可能减小,也可能不变。
3.(2019·吉林模拟)在氧化钕(Nd O)等稀土催化剂的作用下可发生反应:4CO+
2 3
2NO
2
===N
2
+4CO
2
,若该反应的反应速率分别用 v(CO)、 v(NO
2
)、 v(N
2
)、 v(CO
2
)表示,则下列关
系正确的是( )
A.v(CO)= v(NO
2
) B.v(NO
2
)= v(CO
2
)
C.v(N
2
)= v(CO
2
) D.v(N
2
)= v(CO)
解析:选A。根据反应速率之比等于化学方程式中的化学计量数之比,可得 v(CO)=
v(NO
2
),2v(NO
2
)= v(CO
2
),4v(N
2
)= v(CO
2
),4v(N
2
)= v(CO),故A项正确,B、C、D三项均错误。
4.在已处于化学平衡状态的体系中,若下列物理量发生变化,则一定能表明平衡发生移
动的是( )
A.反应混合物的浓度 B.反应的平衡常数
C.正、逆反应速率 D.反应体系的压强
解析:选B。当反应前后气体分子数之和相等时,增大压强、增大反应混合物的浓度,正、
逆反应速率均增大,但平衡不移动,A、C、D三项均错误;B项正确。
5.下列叙述中,不能用平衡移动原理解释的是( )
A.黄绿色的氯水光照后颜色变浅
B.500 ℃左右比常温下更有利于合成氨
C.用纯碱溶液洗涤油污时加热效果更好
D.红棕色的NO ,加压后颜色先变深后变浅
2
解析:选B。合成氨是放热反应,升高温度是为了加快反应速率。
6.(2019·哈尔滨三中调研)下列说法中不正确的是( )A.SiO(s)+2C(s)===Si(s)+2CO(g)只能在高温下自发进行,则该反应的ΔH>0
2
B.3C(s)+CaO(s)===CaC (s)+CO(g)在常温下不能自发进行,说明该反应的ΔH>0
2
C.BaSO(s)+4C(s)===BaS(s)+4CO(g)在室温下不能自发进行,说明该反应的ΔH<0
4
D.常温下,2NO(g)+O(g)===2NO(g)能够自发进行,则该反应的ΔH<0
2 2
解析:选C。C项,由ΔG=ΔH-TΔS>0,因为该反应的ΔS>0,所以-TΔS<0,所以ΔH>0。
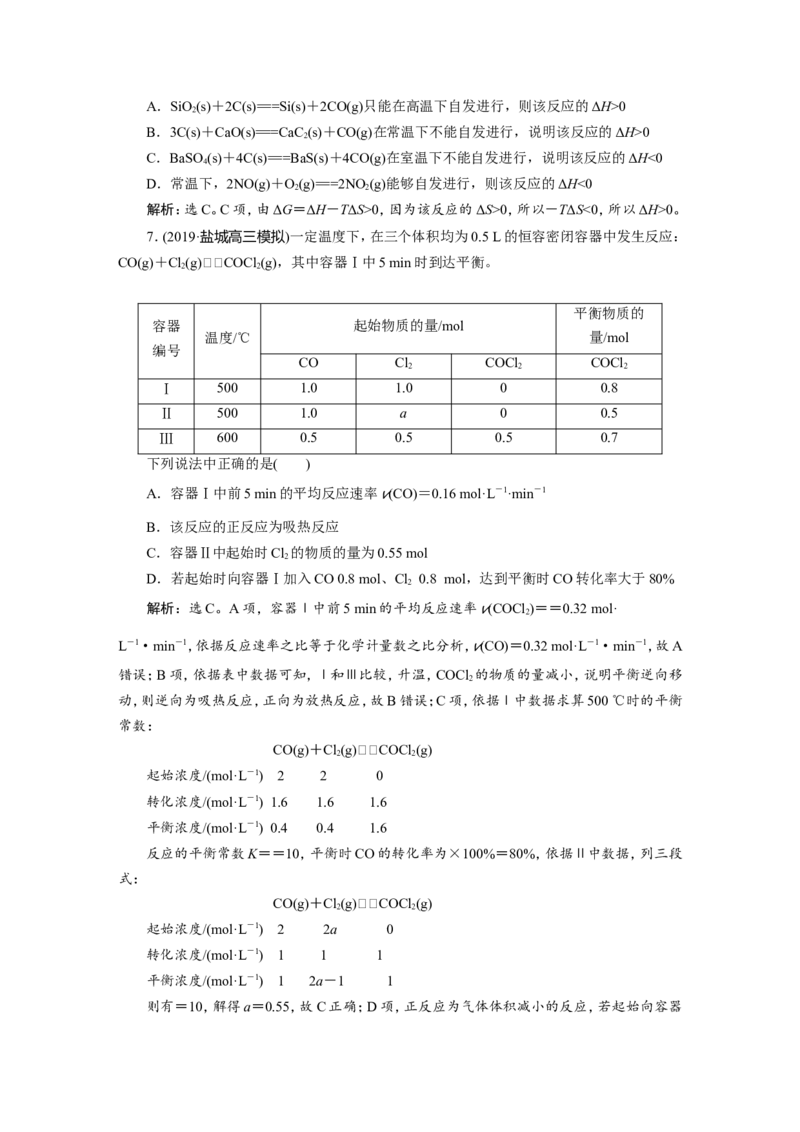
7.(2019·盐城高三模拟)一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:
CO(g)+Cl(g)COCl (g),其中容器Ⅰ中5 min时到达平衡。
2 2
平衡物质的
容器 起始物质的量/mol
温度/℃ 量/mol
编号
CO Cl COCl COCl
2 2 2
Ⅰ 500 1.0 1.0 0 0.8
Ⅱ 500 1.0 a 0 0.5
Ⅲ 600 0.5 0.5 0.5 0.7
下列说法中正确的是( )
A.容器Ⅰ中前5 min的平均反应速率 v(CO)=0.16 mol·L-1·min-1
B.该反应的正反应为吸热反应
C.容器Ⅱ中起始时Cl 的物质的量为0.55 mol
2
D.若起始时向容器Ⅰ加入CO 0.8 mol、Cl 0.8 mol,达到平衡时CO转化率大于80%
2
解析:选C。A项,容器Ⅰ中前5 min的平均反应速率 v(COCl
2
)==0.32 mol·
L-1·min-1,依据反应速率之比等于化学计量数之比分析, v(CO)=0.32 mol·L-1·min-1,故A
错误;B项,依据表中数据可知,Ⅰ和Ⅲ比较,升温,COCl 的物质的量减小,说明平衡逆向移
2
动,则逆向为吸热反应,正向为放热反应,故B错误;C项,依据Ⅰ中数据求算500 ℃时的平衡
常数:
CO(g)+Cl(g)COCl (g)
2 2
起始浓度/(mol·L-1) 2 2 0
转化浓度/(mol·L-1) 1.6 1.6 1.6
平衡浓度/(mol·L-1) 0.4 0.4 1.6
反应的平衡常数K==10,平衡时CO的转化率为×100%=80%,依据Ⅱ中数据,列三段
式:
CO(g)+Cl(g)COCl (g)
2 2
起始浓度/(mol·L-1) 2 2a 0
转化浓度/(mol·L-1) 1 1 1
平衡浓度/(mol·L-1) 1 2a-1 1
则有=10,解得a=0.55,故C正确;D项,正反应为气体体积减小的反应,若起始向容器Ⅰ中加入0.8 mol CO和0.8 mol Cl ,与容器Ⅰ相比相当于减压,平衡逆向移动,CO平衡转化
2
率降低,小于80%,故D错误。
8.汽车尾气中NO产生的反应为N(g)+O(g)2NO(g)。
2 2
一定条件下,等物质的量的N(g)和O(g)在恒容密闭容器中反
2 2
应,如图曲线a表示该反应在温度T下N 的浓度随时间的变化,
2
曲线b表示该反应在某一起始反应条件改变时N 的浓度随时
2
间的变化。下列叙述正确的是( )
A.温度T下,该反应的平衡常数K=
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的ΔH<0
解析:选A。A.由曲线a可知,达到平衡时c(N )=c mol·L-1,则生成的c(NO)=2(c-c)
2 1 0 1
mol·L-1,故K==。B.反应物和生成物都是气体,当容器保持恒容时,混合气体的密度始终保
持不变。C.催化剂的加入只能改变反应速率而不可能使平衡发生移动,故加入催化剂后达到
平衡时,c(N )仍为 c mol·L-1。D.若曲线b对应的条件改变是温度,根据达到平衡时曲线b
2 1
对应的时间短,则对应温度高,即升高温度时c(N )减小,平衡正向移动,正反应为吸热反应,
2
ΔH>0。
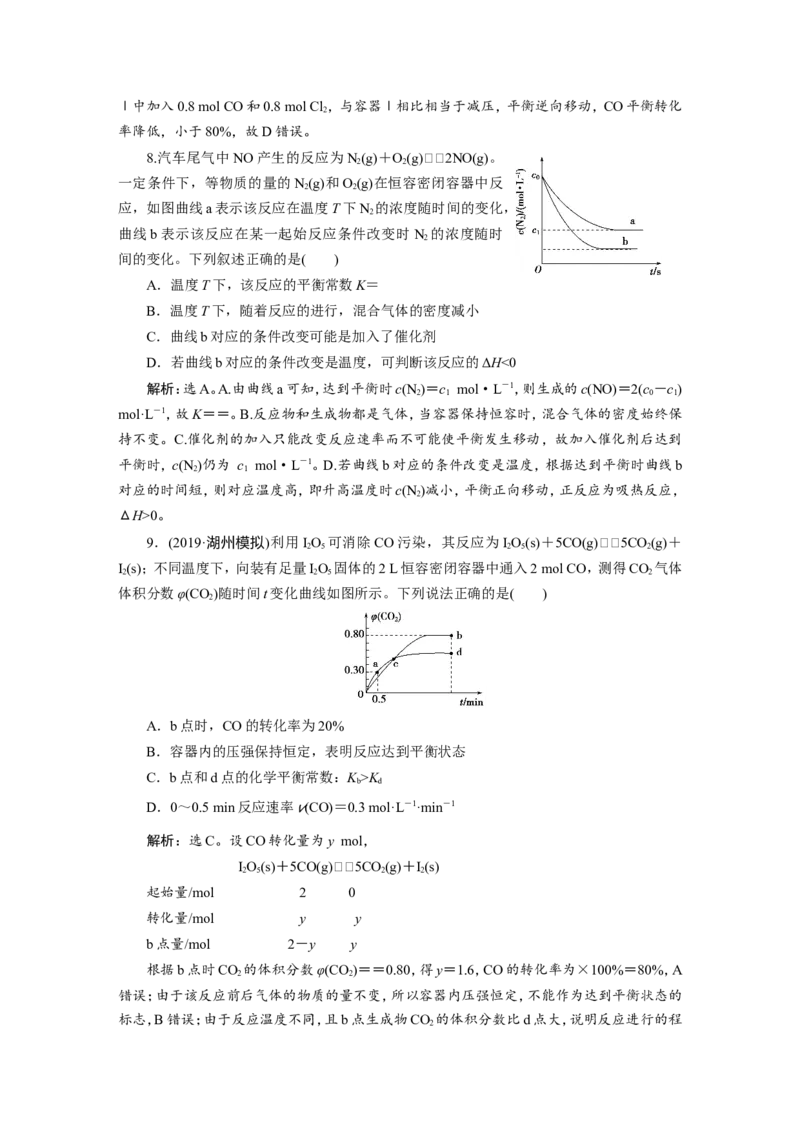
9.(2019·湖州模拟)利用IO 可消除CO污染,其反应为IO(s)+5CO(g)5CO(g)+
2 5 2 5 2
I(s);不同温度下,向装有足量IO 固体的2 L恒容密闭容器中通入2 mol CO,测得CO 气体
2 2 5 2
体积分数φ(CO)随时间t变化曲线如图所示。下列说法正确的是( )
2
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:K >K
b d
D.0~0.5 min反应速率 v(CO)=0.3 mol·L-1·min-1
解析:选C。设CO转化量为y mol,
IO(s)+5CO(g)5CO(g)+I(s)
2 5 2 2
起始量/mol 2 0
转化量/mol y y
b点量/mol 2-y y
根据b点时CO 的体积分数φ(CO)==0.80,得y=1.6,CO的转化率为×100%=80%,A
2 2
错误;由于该反应前后气体的物质的量不变,所以容器内压强恒定,不能作为达到平衡状态的
标志,B错误;由于反应温度不同,且b点生成物CO 的体积分数比d点大,说明反应进行的程
2度大,则化学平衡常数:K >K ,C正确;0~0.5 min,设CO转化量为x mol,
b d
IO(s)+5CO(g)5CO(g)+I(s)
2 5 2 2
起始量/mol 2 0
转化量/mol x x
a点量/mol 2-x x
根据a点时CO
2
的体积分数φ(CO
2
)==0.30,得x=0.6,则0~0.5 min反应速率 v(CO)=
=0.6 mol·L-1·min-1,D错误。
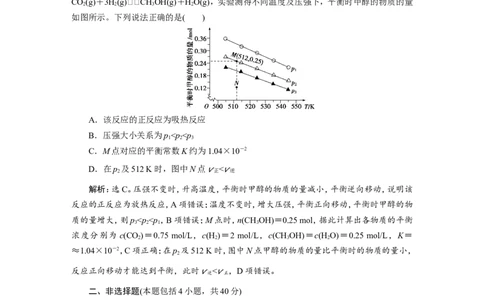
10.(2019·南昌调研)在1.0 L恒容密闭容器中投入 1 mol CO 和2.75 mol H 发生反应
2 2
CO(g)+3H(g)CHOH(g)+HO(g),实验测得不同温度及压强下,平衡时甲醇的物质的量
2 2 3 2
如图所示。下列说法正确的是( )
A.该反应的正反应为吸热反应
B.压强大小关系为p”
“=”或“<”)。
(2)反应方程式中的x=________,30 min时改变的反应条件是______________________。
(3)20~30 min时反应的平衡常数________30~40 min时反应的平衡常数(填“>”“=”或“<”)。
(4)该反应的正反应为________反应(填“放热”或“吸热”)。
(5)反应过程中B的转化率最大的时间段是________min。
解析:(1)0~20 min, A从2.0 mol·L-1减小到1.0 mol·L-1,故其反应速率为=0.05 mol·L-
1·min-1;8 min时未达到平衡,反应向正反应方向进行, v(正)>v(逆)。
(2)30 min时条件改变的瞬间,A、C浓度同等倍数减小,正、逆反应速率减小且相等,平衡
不移动,则改变的条件是扩大体积,减小压强,该反应前后气体的体积不变,故x=1。
(3)20~30 min和30~40 min两时间段内温度不变,平衡常数不变。
(4)40 min时改变条件后,C的浓度减小,A的浓度增大,说明平衡向逆反应方向移动。从
题图可知,条件改变后正、逆反应速率都增大,增大生成物的浓度、增大压强、加催化剂都不符
合题意,则改变的条件只有升高温度。升高温度,平衡向逆反应方向移动,则正反应为放热反
应。
(5)20~30 min、30~40 min两个阶段虽然条件不同,但平衡并未发生移动,40~54 min阶
段平衡向逆反应方向移动,B转化率减小,故20~40 min时间段内B的转化率最大。
答案:(1)0.05 mol·L-1·min-1 >
(2)1 扩大容器体积,减小压强
(3)= (4)放热 (5)20~40
13.(10分)(2019·襄阳调研)用天然气与CO 反应可制备合成气(CO和H 的混合气体),在
2 2
10 L 密闭容器中通入 1 mol CH 与 1 mol CO ,在一定条件下发生反应 CH(g)+
4 2 4
CO(g)2CO(g)+2H(g),测得CH 的平衡转化率与温度及压强的关系如图所示。
2 2 4
(1)1 100 ℃、p 下,气体混合后反应经过10 min至x点所对应的平衡,用CO的变化量表
2
示反应速率 v(CO)=________。
(2)由图可知,压强p 1 ________p 2 (填“大于”或“小于”);压强为p 2 时,在y点 v正
________v逆 (填“大于”“小于”或“等于”);y点对应的反应的平衡常数K=________。
解析:(1)x点对应的CH 的平衡转化率为80%,反应消耗CH、CO 的物质的量均为0.8
4 4 2
mol,生成CO、H
2
的物质的量均为1.6 mol, v(CO)==0.016 mol·L-1·min-1。(2)该反应是一个
气体分子数增大的反应,减小压强,平衡正向移动,CH 的平衡转化率增大,相同温度下p 时
4 1
CH 的平衡转化率大于p,故pv逆 ;平衡常数只与温度有关,y点对应的反应的平衡常数与x点对应
的反应的平衡常数相等。x点对应的平衡常数K==1.638 4。
答案:(1)0.016 mol·L-1·min-1 (2)小于 大于 1.638 4
14.(12分)(2019·皖南八校第一次联考)化学反应原理在科研和生产中有广泛应用。CO可
用于合成甲醇,一定温度下,向体积为2 L的密闭容器中加入CO和H ,发生反应CO(g)+
2
2H(g)CHOH(g),达到平衡后测得各组分的浓度如下:
2 3
物质 CO H CHOH
2 3
浓度/(mol·L-1) 0.9 1.0 0.6
(1)反应达到平衡时,CO的转化率为________。
(2)该反应的平衡常数K=________。
(3)恒温恒容条件下,可以说明反应已达到平衡状态的是________(填字母)。
A. v正 (CO)=2v逆 (H 2 )
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CHOH、CO、H 的浓度都不再发生变化
3 2
(4)若将容器体积压缩到1 L,则达到新平衡时c(H )的取值范围是 。
2
(5)若保持容器体积不变,再充入0.6 mol CO和0.4 mol CH 3 OH,此时 v正 ________v逆 (填
“>”“<”或“=”)。
解析: CO(g)+2H(g)CHOH(g)
2 3
起始浓度/(mol·L-1) 1.5 2.2 0
转化浓度/(mol·L-1) 0.6 1.2 0.6
平衡浓度/(mol·L-1) 0.9 1.0 0.6
(1)反应达到平衡时,CO的转化率为×100%=40%。(2)该反应的平衡常数K===。(3)根
据 化 学 反 应 速 率 之 比 等 于 化 学 计 量 数 之 比 , 有
2v正 (CO)= v正 (H 2 ),若2v正 (CO)= v逆 (H 2 ),则正、逆反应速率相等,反应达到平衡状态,A项错
误;反应在恒容条件下进行,反应物和生成物都为气体,故气体的总质量不变,容器的体积不
变,密度始终保持不变,所以混合气体的密度不变不能作为反应达到平衡的标志,B项错误;
根据“变量不变达平衡”,该反应的正反应为气体体积减小的反应,混合气体的平均相对分子
质量是变量,若不变了,证明反应已达平衡状态,C项正确;CHOH、CO、H 的浓度都不再发生
3 2
变化,说明反应已达平衡状态,D项正确。(4)将容器体积压缩为1 L,若平衡不移动,则各物质
浓度应变为原来的2倍,但压强增大,平衡向气体体积减小的方向移动,故氢气的平衡浓度小
于 2.0 mol·L - 1 , 所 以 氢 气 的 平 衡 浓 度 的 取 值 范 围 是 1.0 mol·
L-1