文档内容
第三篇 化学反应与能量
专项 19 盖斯定律
通过大量实验证明,不管化学反应是一步完成或分几步完成,其反应热是相同的。换句话说,化学反
应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。这就是盖斯定律。盖斯定律的应用价
值在于可以根据已准确测定的反应热来求知实验难测或根本无法测定的反应热,可以利用已知的反应热计
算未知的反应热。该类试题主要以生产、生活、科技和能源等社会热点问题为背景,将热化学方程式的书
写与盖斯定律的计算融合在一起进行考查,较好地考查了学生对知识的灵活应用和运算能力。解答该类题
目不仅要清楚书写热化学方程式的要求和注意事项,理解盖斯定律的含义,还要合理设计反应途径,正确
加减热化学方程式。
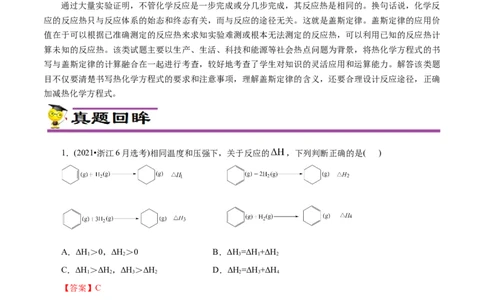
1.(2021•浙江6月选考)相同温度和压强下,关于反应的 ,下列判断正确的是( )
A.ΔH>0,ΔH>0 B.ΔH=ΔH+ΔH
1 2 3 1 2
C.ΔH>ΔH,ΔH>ΔH D.ΔH=ΔH+ΔH
1 2 3 2 2 3 4
【答案】C
【解析】一般的烯烃与氢气发生的加成反应为放热反应,但是,由于苯环结构的特殊性决定了苯环结
构的稳定性,苯与氢气发生加成反应生成1,3-环己二烯时,破坏了苯环结构的稳定性,因此该反应为吸
热反应。A项,环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放热反应,因此,ΔH<0,ΔH<
1 2
0,A不正确;B项,苯分子中没有碳碳双键,其中的碳碳键是介于单键和双键之间的特殊的共价键,因此,
其与氢气完全加成的反应热不等于环己烯、1,3-环己二烯分别与氢气发生的加成反应的反应热之和,即
ΔH≠ΔH+ΔH,B不正确;C项,环己烯、1,3-环己二烯分别与氢气发生的加成反应均为放反应,ΔH<
3 1 2 1
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司0,ΔH<0,由于1mol 1,3-环己二烯与氢气完全加成后消耗的氢气是等量环己烯的2倍,故其放出的热量
2
更多,其ΔH>ΔH;苯与氢气发生加成反应生成1,3-环己二烯的反应为吸热反应(ΔH >0),根据盖斯定
1 2 4
律可知,苯与氢气完全加成的反应热ΔH=ΔH+ΔH,因此ΔH>ΔH,C正确;D项,根据盖斯定律可知,
3 4 2 3 2
苯与氢气完全加成的反应热ΔH=ΔH+ΔH,因此ΔH=ΔH-ΔH,D不正确。故选C。
3 4 2 2 3 4
2.(2020•浙江7月选考)关于下列 的判断正确的是( )
CO(aq)+H+(aq)===HCO(aq) ΔH
1
CO(aq)+HO(l)HCO(aq)+OH−(aq) ΔH
2 2
OH−(aq)+H+(aq)===HO(l) ΔH
2 3
OH−(aq)+CHCOOH(aq)===CHCOO−(aq)+HO(l) ΔH
3 3 2 4
A.ΔH<0 ΔH<0 B.ΔH<ΔH C.ΔH<0 ΔH>0 D.ΔH>ΔH
1 2 1 2 3 4 3 4
【答案】B
【解析】碳酸氢根的电离属于吸热过程,则CO(aq)+H+(aq)=HCO- (aq)为放热反应,所以△H<0;
3 1
CO(aq)+HO(l) HCO - (aq)+OHˉ(aq)为碳酸根的水解离子方程式,CO的水解反应为吸热反应,所以
2 3
△H>0;OHˉ(aq)+H+(aq)=H O(l)表示强酸和强碱的中和反应,为放热反应,所以△H<0;醋酸与强碱的中
2 2 3
和反应为放热反应,所以△H<0;但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应
4
过程放出的热量小于强酸和强碱反应放出的热量,则△H> H;综上所述,只有△H< H 正确,故选
4 3 1 2
B。 △ △
3.(2019新课标Ⅱ卷节选)环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。
回答下列问题:
已知: (g)= (g)+H(g) ΔH=100.3 kJ·mol −1 ①
2 1
H(g)+ I (g)=2HI(g) ΔH=﹣11.0 kJ·mol −1 ②
2 2 2
对于反应: (g)+ I (g)= (g)+2HI(g) ③ ΔH=___________kJ·mol −1。
2 3
【答案】89.3
【解析】根据盖斯定律可得:反应③=①+②,可得反应③的ΔH= ΔH +ΔH =89.3KJ/mol;
3 1 2
4.(2019•新课标Ⅲ卷节选)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也
随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
Deacon直接氧化法可按下列催化过程进行:
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司CuCl (s)=CuCl(s)+ Cl(g) ΔH=83 kJ·mol-1
2 2 1
CuCl(s)+ O(g)=CuO(s)+ Cl(g) ΔH=-20 kJ·mol-1
2 2 2
CuO(s)+2HCl(g)=CuCl (s)+HO(g) ΔH=-121 kJ·mol-1
2 2 3
则4HCl(g)+O (g)=2Cl (g)+2HO(g)的ΔH=_________ kJ·mol-1。
2 2 2
【答案】﹣116
【解析】根据盖斯定律知, (反应 I+反应 II+反应 III)×2 得 4HCl(g)+O (g)=2Cl (g)+2HO(g)
2 2 2
∆H=(∆H+∆H+∆H)×2=-116kJ∙mol-1;
1 2 3
5.(2019• 北京卷节选)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
甲烷水蒸气催化重整是制高纯氢的方法之一。
①反应器中初始反应的生成物为H 和CO,其物质的量之比为4∶1,甲烷和水蒸气反应的方程式是
2 2
______________。
②已知反应器中还存在如下反应:
i.CH (g)+HO(g)=CO(g)+3H (g) ΔH
4 2 2 1
ii.CO(g)+H O(g)=CO(g)+H(g) ΔH
2 2 2 2
iii.CH (g)=C(s)+2H (g) ΔH ……
4 2 3
iii为积炭反应,利用ΔH 和ΔH 计算ΔH 时,还需要利用__________反应的ΔH。
1 2 3
【答案】① CH + 2H O= 4H + CO ② C(s)+CO(g)=2CO(g)
4 2 2 2 2
【解析】①由于生成物为H 和CO,其物质的量之比为4:1,反应物是甲烷和水蒸气,因而反应方程
2 2
式为 CH + 2H O= 4H + CO ;②ⅰ-ⅱ 可得 CH(g)+CO (g)=2CO(g)+2H(g),设为ⅳ,用ⅳ-ⅲ 可得 C(s)
4 2 2 2 4 2 2
+CO (g)=2CO(g),因为还需利用C(s)+CO(g)=2CO(g)反应的焓变;
2 2
6.(2019•天津卷节选)多晶硅是制作光伏电池的关键材料。回答下列问题:
Ⅰ.硅粉与HCl在300℃时反应生成1molSiHCl 气体和H,放出225kJ热量,该反应的热化学方程式
3 2
为________________________。
Ⅱ.将SiCl 氢化为SiHCl 有三种方法,对应的反应依次为:
4 3
①SiCl (g)+ H(g) SiHCl (g)+ HCl (g) ΔH>0
4 2 3 1
②3SiCl (g)+2H(g)+ Si(s) 4SiHCl (g) ΔH<0
4 2 3 2
3
原创精品资源学科网独家享有版权,侵权必究!
3
学科网(北京)股份有限公司③2SiCl (g)+H(g)+ Si(s) + HCl (g) 3SiHCl (g) ΔH
4 2 3 3
(4)反应③的ΔH=______(用ΔH,ΔH 表示)。
3 1 2
【答案】Ⅰ. Si(s)+3HCl(g) SiHCl (g)+H(g)
3 2
Ⅱ.(4)ΔH-ΔH
2 1
【解析】I.参加反应的物质是固态的 Si、气态的HCl,生成的是气态的SiHCl 和氢气,反应条件是
3
300℃,配平后发现SiHCl 的化学计量数恰好是1mol,由此可顺利写出该条件下的热化学方程式:Si(s)
3
+3HCl(g) SiHCl (g)+H(g) ∆H=-225kJ·mol-1;
3 2
II.(4)将反应①反向,并与反应②直接相加可得反应③,所以∆H=∆H-∆H ,因∆H<0、∆H>0,所以
3 2 1 2 1
∆H 必小于0,即反应③正反应为放热反应。
3
1.运用盖斯定律的技巧——“三调一加”
一调:根据目标热化学方程式,调整已知热化学方程式中反应物和生成物的左右位置,改写已知的热
化学方程式。
二调:根据改写的热化学方程式调整相应ΔH的符号。
三调:调整中间物质的化学计量数。
一加:将调整好的热化学方程式及其ΔH相加。
4
原创精品资源学科网独家享有版权,侵权必究!
4
学科网(北京)股份有限公司2.运用盖斯定律的三个注意事项
(1)热化学方程式乘以某一个数时,反应热的数值必须也乘上该数。
(2)热化学方程式相加减时,物质之间相加减,反应热也必须相加减。
(3)将一个热化学方程式颠倒时,ΔH的“+”“-”随之改变,但数值不变。
1.(2022·浙江省绍兴市选考二模)在一定温度压强下,依据图示关系,下列说法不正确的是( )
A.C(石墨)+ CO (g) =2CO(g) ΔH=ΔH-ΔH
2 1 2
B.1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g) ,前者放热多
2 2
C.ΔH=ΔH-ΔH
5 1 3
D.化学反应的△H,只与反应体系的始态和终态有关,与反应途径无关
【答案】B
5
原创精品资源学科网独家享有版权,侵权必究!
5
学科网(北京)股份有限公司【解析】A项,由题干信息可知,反应I:C(石墨)+ (g)=CO(g) ΔH 反应II:CO(g)+
1
(g)=CO (g) ΔH,则反应I-反应II得C(石墨)+ CO (g) =2CO(g),根据盖斯定律可知ΔH=ΔH-ΔH,A正确;
2 2 2 1 2
B项,由题干信息可知,C(石墨)= C(金刚石) ΔH<0,即1molC(石墨)具有的总能量低于1molC(金刚石),
5
则1mol C(石墨)和1mol C(金刚石)分别与足量O 反应全部转化为CO(g),后者放热多,B错误;C项,由
2 2
题干信息可知,反应I:C(石墨)+ (g)=CO(g) ΔH,反应III:C(金刚石)+ (g)=CO(g) 则反应I-反应
1
III得C(石墨)= C(金刚石),根据盖斯定律可知,ΔH=ΔH-ΔH,C正确;D项,根据盖斯定律可知,化学
5 1 3
反应的△H,只与反应体系的始态和终态有关,与反应途径无关,D正确;故选B。
2.(2022·江苏省启东中学高三模拟)“世上无难事,九天可揽月”,我国的航空航天事业取得了举世嘱
目的成就。碳酰肼类化合物[Mn(L) ]( ClO ) 是种优良的含能材料,可作为火箭推进剂的组分,其相关反应
3 4 2
的能量变化如图所示,已知△H= —299kJ/mol,则△H (kJ/mol )为( )
2 1
A.-1563 B.-1389 C.-1344 D.-1160
【答案】A
【解析】由盖斯定律可知,△H=2 H + H — H =2×(—299kJ/mol)+(—1018kJ/mol)—(+87kJ/mol)=
1 2 3 4
—1563kJ/mol,故选A。 △ △ △
3.(2022·浙江省宁波市鄞州中学模拟预测)下列关于如图所示转化关系(X代表卤素)的说法正确的是(
)
A.ΔH 越小,HX的熔沸点越高
1
6
原创精品资源学科网独家享有版权,侵权必究!
6
学科网(北京)股份有限公司B.ΔH+ΔH +ΔH =0
1 2 3
C.按照Cl、Br、I的顺序,ΔH 依次减小
2
D.过程Ⅲ的能量变化形式与高温煅烧石灰石的能量变化形式相同
【答案】C
【解析】A项,ΔH 越小,放热越多,HX能量越低,HX就越稳定,熔沸点不一定越高,故A错误;
1
B项,根据盖斯定律,ΔH=ΔH +ΔH ,故B错误;C项,原子半径越小,键能越大,按照Cl、Br、I的顺
1 2 3
序,ΔH 依次减小,故C正确;D项,过程Ⅲ形成化学键放热,高温煅烧石灰石吸热,能量变化形式不相
2
同,故D错误;故选C。
4.(2022·浙江省金丽衢十二校第二次联考)CHCOOH和氨水反应的能量循环体系如图所示,下列说法
3
正确的是( )
A.△H+ H+ H= H B.△H+ H> H+ H
1 2 3 4 1 4 2 3
C.△H 4 <△H 1 -△H 2 △ D.△H 3 <△0 △ △
【答案】C△ △
【解析】由图可知① ;②
;③ ;④
。A项,由以上得②+③+④=①,即△H+ H+ H= H,故A错误;B项,
2 3 4 1
△ △ △
由△H+ H+ H= H 得△H+ H= H+ H+2 H,中和反应是放热反应,故△H<0,所以
2 3 4 1 1 4 2 3 4 4
△H+ H△< H△+ H△,故B错误△;C项△,由△△H+△ H+ H= H 得△H= H- H- H<0,弱电解质的电离
1 4 2 3 2 3 4 1 4 1 2 3
是吸热△过程△,所以△△H>0,所以△H< H- H,△故C正△确;△D项,弱电△解质△的电离△是吸热过程,所以
3 4 1 2
△H>0,故D错误;故选C。 △ △
3
5.(2022·辽宁省沈阳市高三模拟)MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
7
原创精品资源学科网独家享有版权,侵权必究!
7
学科网(北京)股份有限公司已知:离子电荷相同时,半径越小,离子键越强。下列说法不正确的是( )
A.ΔH(MgCO )>ΔH(CaCO)>0
1 3 1 3
B.ΔH(MgCO )=ΔH (CaCO)>0
2 3 2 3
C.ΔH(CaCO)-ΔH (MgCO )=ΔH (CaO)-ΔH (MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO ,ΔH+ΔH >ΔH
3 3 1 2 3
【答案】C
【解析】根据盖斯定律可得ΔH=ΔH+ΔH +ΔH ,又易知Ca2+半径大于Mg2+半径,所以CaCO 的离子键
1 2 3 3
强度弱于MgCO ,CaO的离子键强度弱于MgO。A项,ΔH 表示断裂CO2-和M2+的离子键所吸收的能量,
3 1 3
离子键强度越大,吸收的能量越大,因而ΔH(MgCO )>ΔH(CaCO)>0,A项正确;B项,ΔH 表示断裂
1 3 1 3 2
CO2-中共价键形成O2-和CO 吸收的能量,与M2+无关,因而ΔH(MgCO )=ΔH (CaCO)>0,B项正确;C
3 2 2 3 2 3
项,由上可知ΔH(CaCO)-ΔH (MgCO )<0,而ΔH 表示形成MO离子键所放出的能量,ΔH 为负值,CaO
1 3 1 3 3 3
的离子键强度弱于MgO,因而ΔH(CaO)>ΔH(MgO),ΔH(CaO)-ΔH (MgO)>0,C项错误;D项,
3 3 3 3
ΔH+ΔH >0,ΔH<0,故ΔH+ΔH >ΔH,D项正确。故选C。
1 2 3 1 2 3
6.(2022·浙江省杭州二中、温州中学、金华一中高三选考模拟预测)已知ROH(R= Na、K)固体溶于水
放热,有关过程能量变化如图
下列说法正确的是( )
A.反应①ΔH<0,ΔS<0 B.△H(NaOH)>△H(KOH)
1 4 4
C.△H(NaOH)>△H(KOH) D.△H = H + H + H+ H
6 6 4 1 2 5 6
【答案】B △ △ △ △
【解析】A项,由于液体的混乱度大于固体,反应①ΔS>0,A错误;B项,△H 表示ROH破坏离子
4
键的过程,应为钠离子半径小于钾离子,破坏离子键氢氧化钾吸收的能量要多,则△H(NaOH)>
4
8
原创精品资源学科网独家享有版权,侵权必究!
8
学科网(北京)股份有限公司△H(KOH),B正确;C项,△H 表示氢氧根离子从气态离子转化为溶液中离子的热量变化,
4 6
△H(NaOH)= H(KOH),C错误;D项,由盖斯定律可知△H = H + H - H - H,D错误;答
6 6 4 1 2 5 6
案选B。 △ △ △ △ △
7.盖斯定律表明,在一定条件下,化学反应的反应热只与反应体系的始态和终态有关,而与反应的
途径无关。物质A在一定条件下可发生如图所示一系列转化,则下列关系错误的是( )
A.A→F的 B.
C.C→F的 D.
【答案】B
【解析】A项,根据题图可知,F→A的 ,则A→F的 ,故A正确;B项,循环一周
后,反应热之和为0,由图可知, ,故B错误;C项,F→C的
,则C→F的 ,所以C→F的 ,故C正确;
D项,A→D的 ,D→A的 ,二者的绝对值相等,符号相反,故D
正确;故选B。
8.(2022·浙江省镇海中学高三选考适应性测试)物质 、 与 的能量存在如图所示的
相互关系。已知:人为规定H(g)的能量为0kJ/mol。下列有关说法错误的是( )
2
9
原创精品资源学科网独家享有版权,侵权必究!
9
学科网(北京)股份有限公司A.物质 是图示三种物质中最稳定的
B.过程①属于吸热反应
C.由图可推知,发生消去反应①或②时,环戊烷断键吸收的能量高于环戊烯断键吸收的能量
D.物质变化过程中所放出或吸收的热量的多少与路径无关
【答案】C
【解析】A项,物质的能量越低越稳定,由图可知, 能量最低,所以最稳定,A项正确;B项,
过程①,生成物能量高于反应物,所以属于吸热反应,B项正确;C项,过程①对应环戊烯消去反应,生
成一个碳碳双键和氢气,吸收的能量为101kJ/mol,过程②对应环戊烷消去反应生成一个碳碳双键和氢气,
吸收的能量为110 kJ/mol,当物质的量相同时,环戊烷吸收的能量高,但题干并没有明确环戊烷和环戊烯
的物质的量,所以C项错误;D项,物质变化过程中所放出或吸收的热量的多少与路径无关,只与反应物
的状态和反应时的温度压强有关,所以D项正确;故选C。
9.目前世界各国都规划了碳达峰、碳中和的时间节点,以CO 为碳源,将其转化为能源物质。选择
2
性加氢合成CHOH,合成过程中发生下列反应:
3
反应i:CO(g)+H(g) CO(g)+HO(g) ∆H=-akJ‧mol-1
2 2 2 1
反应ii:CO(g)+2H(g) CHOH(g) ∆H
2 3 2
反应iii:CO(g)+3H(g) CHOH(g)+H O(g) ∆H=-bkJ‧mol-1
2 2 3 2 3
根据盖斯定律,∆H=___________kJ‧mol-1(用含a,b的代数式表示)。
2
【答案】(1)a-b
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司【解析】(1)根据盖斯定律,反应iii-反应i可得反应ii,∆H=∆H-∆H=(a-b) kJ‧mol-1。
2 3 1
10.我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO 利用的研究热点
4 2 2
之一、该重整反应体系主要涉及以下反应:
(a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
(b)CO (g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
(c)CH(g) C(s)+2H(g) ∆H
4 2 3
(d)2CO(g) CO(g)+C(s) ∆H
2 4
(e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
【答案】∆H+∆H-∆H 或∆H-∆H
2 3 5 3 4
【解析】按盖斯定律,反应a=反应b+反应c-反应e=反应c-反应d,则有∆H=∆H+∆H-∆H=∆H-
1 2 3 5 3
∆H。
4
11.CH—CO 催化重整不仅可以得到合成气CO和H,还对温室气体的减排具有重要意义。该重整反
4 2 2
应体系主要涉及以下反应:
Ⅰ.CH (g)+CO (g) 2CO(g)+2H(g) H
4 2 2 1
Ⅱ.CH
4
(g) C(s)+2H
2
(g) H
2
=+75.0k△J/mol
Ⅲ.CO
2
(g)+H
2
(g) CO(g)+△H
2
O(g) H
3
=+41.0kJ/mol
Ⅳ.CO(g)+H
2
(g) C(s)+H
2
O(g) H△4 =-131.0kJ/mol
根据盖斯定律,反应Ⅰ的△H
1
=___k△J/mol。
【答案】(1)+247.0
【解析】根据盖斯定律,Ⅱ+Ⅲ-Ⅳ=Ⅰ,△H=75.0 kJ/mol +41.0 kJ/mol -(-131.0 kJ/mol)=+247.0
1
kJ/mol。
12. CO 的资源化利用能有效减少CO 排放缓解能源危机。用CO、H 为原料合成甲醇(CHOH)过程
2 2 2 2 3
主要涉及以下反应:
a)CO(g)+3H(g) CHOH(g)+H O(g) H
2 2 3 2 1
b)CO
2
g)+H
2
(g) CO(g)+H
2
O(g) H
2
=+△41.2kJ/mol
△
c) CO(g)+H(g) CHOH(g) H=-45.1kJ/mol
2 3 3
△
根据盖斯定律,反应a的△H=___________。
1
【答案】-49.0kJ/mol
11
原创精品资源学科网独家享有版权,侵权必究!
11
学科网(北京)股份有限公司【解析】已知:b)COg)+H (g) CO(g)+HO(g) H=+41.2kJ/mol;c) CO(g)+H(g)
2 2 2 2 2
△
CHOH(g) H=-45.1kJ/mol;根据盖斯定律,由b)+ c) 2得反应a)CO(g)+3H(g) CHOH(g)+H O(g)
3 3 2 2 3 2
H= H+ △ H 2=-49.0kJ/mol。 ⇌
1 2 3
△ 1△3.甲醛△在木材加工,医药等方面有重要用涂。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程
涉及的主要反应如下:
反应I:CHOH(g) HCHO(g)+H(g) H=+85.2kJ·mol-1
3 2 1
△
应II:CHOH(g)+ O(g) HCHO(g)+HO(g) H
3 2 2 2
△
反应III:2H(g)+O(g) 2HO(g) H=-483.6kJ·mol-1
2 2 2 3
计算反应II的反应热△H 2 =____。 △
【答案】-156.6kJ·mol-1
【解析】根据盖斯定律,反应 反应III得反应II,CHOH(g)+ O(g) HCHO(g)+HO(g)
3 2 2
= 。
14.NO 和NO 是氮的两种重要氧化物。已知下列反应在298K时的反应焓变:
2 2 4
①N(g)+O(g)=2NO(g) ΔH = +180.5 kJ·mol-1
2 2 1
②2NO(g)+O (g) 2NO (g) ΔH = -112 kJ·mol-1
2 2 2
③N(g)+2O(g)=NO(g) ΔH = +10.7 kJ·mol-1
2 2 2 4 3
写出NO(g)转化为NO (g) 的热化学方程式:_______。
2 4 2
【答案】NO(g) 2NO (g) ΔH = +57.8 kJ·mol-1
2 4 2
【解析】①N(g)+O(g)=2NO(g) ΔH = +180.5 kJ·mol-1;②2NO(g)+O (g) 2NO (g) ΔH = -112
2 2 1 2 2 2
kJ·mol-1; ③N(g)+2O(g)=NO(g) ΔH = +10.7 kJ·mol-1; 利用盖斯定律,将①+②-③得NO(g)转化为
2 2 2 4 3 2 4
NO (g)的ΔH=ΔH +ΔH -ΔH = +57.8 kJ·mol-1,则热化学方程式:NO(g) 2NO (g) ΔH = +57.8 kJ·mol-1。
2 1 2 3 2 4 2
⇌
12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司13
原创精品资源学科网独家享有版权,侵权必究!
13
学科网(北京)股份有限公司